باب 01 کیمیائی تعاملات اور مساواتیں
روزمرہ زندگی کی درج ذیل صورتوں پر غور کریں اور سوچیں کہ کیا ہوتا ہے جب -
- دودھ گرمیوں میں کمرے کے درجہ حرارت پر چھوڑ دیا جائے۔
- لوہے کا توا/پین/کیل مرطوب ماحول میں کھلا چھوڑ دیا جائے۔
- انگور خمیر ہو جائیں۔
- کھانا پکایا جائے۔
- کھانا ہمارے جسم میں ہضم ہو جائے۔
- ہم سانس لیتے ہیں۔
مذکورہ بالا تمام صورتوں میں، ابتدائی مادے کی نوعیت اور شناخت کسی حد تک بدل گئی ہے۔ ہم نے اپنی پچھلی جماعتوں میں مادے کی طبیعی اور کیمیائی تبدیلیوں کے بارے میں پہلے ہی سیکھا ہے۔ جب بھی کوئی کیمیائی تبدیلی رونما ہوتی ہے، ہم کہہ سکتے ہیں کہ ایک کیمیائی تعامل وقوع پذیر ہوا ہے۔
شاید آپ سوچ رہے ہوں گے کہ دراصل کیمیائی تعامل سے کیا مراد ہے؟ ہمیں کیسے پتہ چلتا ہے کہ کوئی کیمیائی تعامل رونما ہوا ہے؟ آئیے ان سوالات کے جوابات تلاش کرنے کے لیے کچھ سرگرمیاں انجام دیتے ہیں۔
سرگرمی 1.1
احتیاط: اس سرگرمی کے لیے استاد کی مدد درکار ہے۔ بہتر ہوگا کہ طلباء مناسب چشمے پہنیں۔
- تقریباً 3-4 سینٹی میٹر لمبی میگنیشیم کی پٹی کو سینڈ پیپر سے رگڑ کر صاف کریں۔
- اسے چمٹے سے پکڑیں۔ اسے اسپرٹ لیمپ یا برنر سے جلا کر بننے والی راکھ کو واچ گلاس میں جمع کریں جیسا کہ شکل 1.1 میں دکھایا گیا ہے۔ میگنیشیم پٹی کو جلائیں اور اسے اپنی آنکھوں سے جتنا ممکن ہو دور رکھیں۔
- آپ کیا مشاہدہ کرتے ہیں؟
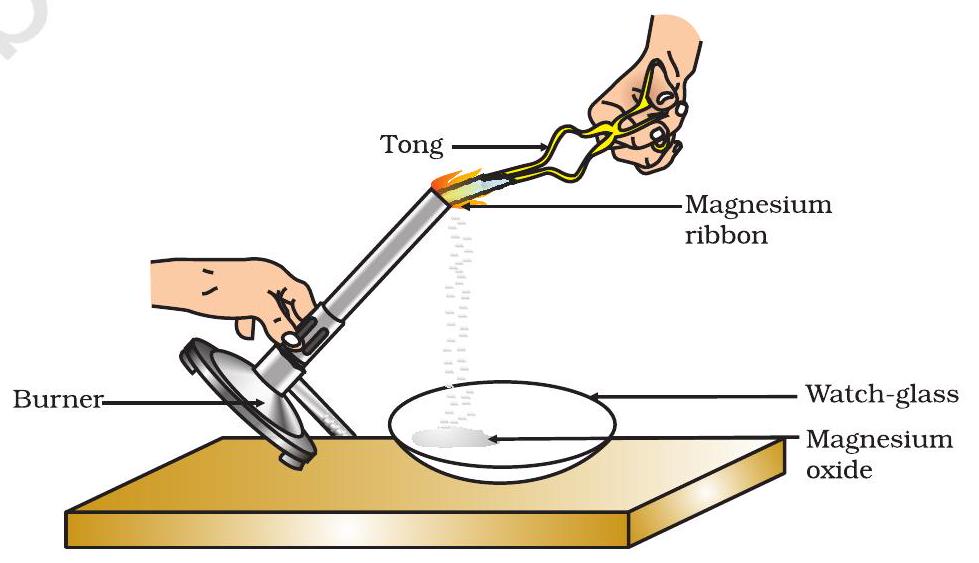
شکل 1.1
ہوا میں میگنیشیم پٹی جلانا اور واچ گلاس میں میگنیشیم آکسائیڈ جمع کرنا
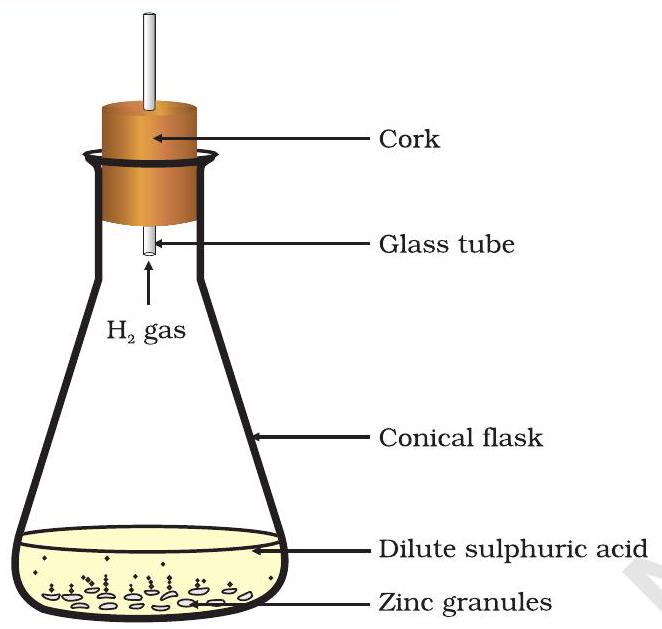
شکل 1.2 زنک پر لگ بھگ گندھک کے تیزاب کے عمل سے ہائیڈروجن گیس کی تشکیل
آپ نے ضرور مشاہدہ کیا ہوگا کہ میگنیشیم پٹی چمکدار سفید شعلے کے ساتھ جلتی ہے اور سفید پاؤڈر میں تبدیل ہو جاتی ہے۔ یہ پاؤڈر میگنیشیم آکسائیڈ ہے۔ یہ میگنیشیم اور ہوا میں موجود آکسیجن کے درمیان تعامل کی وجہ سے بنتا ہے۔
سرگرمی 1.2
- لیڈ نائٹریٹ کا محلول ایک ٹیسٹ ٹیوب میں لیں۔
- اس میں پوٹاشیم آئوڈائیڈ کا محلول شامل کریں۔
- آپ کیا مشاہدہ کرتے ہیں؟
سرگرمی 1.3
- کونیکل فلاسک یا ٹیسٹ ٹیوب میں کچھ زنک کے دانے لیں۔
- اس میں لگ بھگ ہائیڈروکلورک ایسڈ یا گندھک کا تیزاب شامل کریں (شکل 1.2)۔
احتیاط: تیزاب کو احتیاط سے ہینڈل کریں۔
- کیا آپ زنک کے دانوں کے اردگرد کچھ ہوتا ہوا محسوس کرتے ہیں؟
- کونیکل فلاسک یا ٹیسٹ ٹیوب کو چھوئیں۔ کیا اس کے درجہ حرارت میں کوئی تبدیلی آئی ہے؟
مندرجہ بالا تینوں سرگرمیوں سے، ہم کہہ سکتے ہیں کہ درج ذیل مشاہدات میں سے کوئی بھی ہمیں یہ طے کرنے میں مدد کرتا ہے کہ آیا کوئی کیمیائی تعامل رونما ہوا ہے –
- حالت میں تبدیلی
- رنگ میں تبدیلی
- گیس کا اخراج
- درجہ حرارت میں تبدیلی۔
جیسے ہم اپنے اردگرد ہونے والی تبدیلیوں کا مشاہدہ کرتے ہیں، ہم دیکھ سکتے ہیں کہ ہمارے اردگرد کیمیائی تعاملات کی ایک بڑی قسم وقوع پذیر ہو رہی ہے۔ ہم اس باب میں کیمیائی تعاملات کی مختلف اقسام اور ان کی علامتی نمائندگی کے بارے میں پڑھیں گے۔
1.1 کیمیائی مساواتیں
سرگرمی 1.1 کو اس طرح بیان کیا جا سکتا ہے – جب میگنیشیم کی پٹی آکسیجن میں جلائی جاتی ہے، تو یہ میگنیشیم آکسائیڈ میں تبدیل ہو جاتی ہے۔ جملے کی شکل میں کیمیائی تعامل کی یہ تفصیل کافی لمبی ہے۔ اسے مختصر شکل میں لکھا جا سکتا ہے۔ ایسا کرنے کا سب سے آسان طریقہ یہ ہے کہ اسے لفظی مساوات کی شکل میں لکھا جائے۔ مذکورہ بالا تعامل کے لیے لفظی مساوات یہ ہوگی –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
وہ مادے جو تعامل (1.1) میں کیمیائی تبدیلی سے گزرتے ہیں، میگنیشیم اور آکسیجن، تعامل کرنے والے مادے (ری ایکٹنٹس) ہیں۔ نیا مادہ میگنیشیم آکسائیڈ ہے، جو تعامل کے دوران بطور پیداوار (پروڈکٹ) بنتا ہے۔
لفظی مساوات تعامل کرنے والے مادوں سے پیداواروں کی طرف تبدیلی کو ان کے درمیان رکھے گئے تیر کے ذریعے دکھاتی ہے۔ تعامل کرنے والے مادے بائیں طرف (LHS) لکھے جاتے ہیں جن کے درمیان جمع کا نشان (+) ہوتا ہے۔ اسی طرح، پیداواریں دائیں طرف (RHS) لکھی جاتی ہیں جن کے درمیان جمع کا نشان (+) ہوتا ہے۔ تیر کا سرا پیداواروں کی طرف اشارہ کرتا ہے، اور تعامل کی سمت دکھاتا ہے۔
1.1.1 کیمیائی مساوات لکھنا
کیا کیمیائی مساواتوں کو ظاہر کرنے کا کوئی اور مختصر طریقہ ہے؟ کیمیائی مساواتیں زیادہ جامع اور مفید بنائی جا سکتی ہیں اگر ہم الفاظ کی بجائے کیمیائی فارمولے استعمال کریں۔ ایک کیمیائی مساوات ایک کیمیائی تعامل کو ظاہر کرتی ہے۔ اگر آپ میگنیشیم، آکسیجن اور میگنیشیم آکسائیڈ کے فارمولے یاد کریں، تو مذکورہ بالا لفظی مساوات کو اس طرح لکھا جا سکتا ہے -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
تیر کے بائیں طرف (LHS) اور دائیں طرف (RHS) پر ہر عنصر کے ایٹموں کی تعداد گنیں اور موازنہ کریں۔ کیا ہر عنصر کے ایٹموں کی تعداد دونوں اطراف میں یکساں ہے؟ اگر ہاں، تو مساوات متوازن ہے۔ اگر نہیں، تو مساوات غیر متوازن ہے کیونکہ دونوں اطراف میں کمیت یکساں نہیں ہے۔ ایسی کیمیائی مساوات تعامل کے لیے ایک اسکیلیٹل (ہڈیوں والی) کیمیائی مساوات ہوتی ہے۔ مساوات (1.2) ہوا میں میگنیشیم جلانے کے لیے ایک اسکیلیٹل کیمیائی مساوات ہے۔
1.1.2 متوازن کیمیائی مساواتیں
جماعت نہم میں آپ نے پڑھے گئے کمیت کے تحفظ کے قانون کو یاد کریں؛ کیمیائی تعامل میں نہ تو کمیت پیدا کی جا سکتی ہے اور نہ ہی تباہ کی جا سکتی ہے۔ یعنی، کیمیائی تعامل کی پیداواروں میں موجود عناصر کی کل کمیت، تعامل کرنے والے مادوں میں موجود عناصر کی کل کمیت کے برابر ہونی چاہیے۔
دوسرے الفاظ میں، ہر عنصر کے ایٹموں کی تعداد کیمیائی تعامل سے پہلے اور بعد میں یکساں رہتی ہے۔ لہٰذا، ہمیں ایک اسکیلیٹل کیمیائی مساوات کو متوازن کرنے کی ضرورت ہے۔ کیا کیمیائی مساوات (1.2) متوازن ہے؟ آئیے قدم بہ قدم کیمیائی مساوات کو متوازن کرنا سیکھتے ہیں۔
سرگرمی 1.3 کے لیے لفظی مساوات کو اس طرح ظاہر کیا جا سکتا ہے -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
مذکورہ بالا لفظی مساوات کو درج ذیل کیمیائی مساوات کے ذریعے ظاہر کیا جا سکتا ہے -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
آئیے تیر کے دونوں اطراف پر مختلف عناصر کے ایٹموں کی تعداد کا جائزہ لیں۔
| عنصر | تعامل کرنے والے مادوں میں ایٹموں کی تعداد (LHS) | پیداواروں میں ایٹموں کی تعداد (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
چونکہ ہر عنصر کے ایٹموں کی تعداد تیر کے دونوں اطراف میں یکساں ہے، لہٰذا مساوات (1.3) ایک متوازن کیمیائی مساوات ہے۔
آئیے درج ذیل کیمیائی مساوات کو متوازن کرنے کی کوشش کرتے ہیں -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
قدم I: کیمیائی مساوات کو متوازن کرنے کے لیے، پہلے ہر فارمولے کے گرد ڈبے بنائیں۔ مساوات کو متوازن کرتے وقت ڈبوں کے اندر کچھ بھی تبدیل نہ کریں۔
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
قدم II: غیر متوازن مساوات (1.5) میں موجود مختلف عناصر کے ایٹموں کی تعداد کی فہرست بنائیں۔
| عنصر | تعامل کرنے والے مادوں میں ایٹموں کی تعداد (LHS) | پیداواروں میں ایٹموں کی تعداد (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
قدم III: اکثر زیادہ سے زیادہ ایٹموں والے مرکب سے متوازن کرنا شروع کرنا آسان ہوتا ہے۔ یہ تعامل کرنے والا مادہ یا پیداوار ہو سکتا ہے۔ اس مرکب میں، اس عنصر کو منتخب کریں جس میں ایٹموں کی تعداد سب سے زیادہ ہو۔ ان معیارات کا استعمال کرتے ہوئے، ہم $Fe_3 O_4$ اور اس میں آکسیجن عنصر کو منتخب کرتے ہیں۔ دائیں طرف (RHS) پر چار آکسیجن ایٹم ہیں اور بائیں طرف (LHS) پر صرف ایک ہے۔
آکسیجن ایٹموں کو متوازن کرنے کے لیے -
| آکسیجن کے ایٹم |
تعامل کرنے والے مادوں میں | پیداواروں میں |
|---|---|---|
| (i) ابتدائی | 1($ \mathrm{H_2O} $ میں) | 4($ \mathrm{Fe_3O_4} $ میں) |
| (ii) متوازن کرنے کے لیے | 1 $\times$ 4 | 4 |
ایٹموں کی تعداد کو برابر کرنے کے لیے، یہ یاد رکھنا ضروری ہے کہ ہم تعامل میں شامل مرکبات یا عناصر کے فارمولوں میں تبدیلی نہیں کر سکتے۔ مثال کے طور پر، آکسیجن ایٹموں کو متوازن کرنے کے لیے ہم ‘4’ کو بطور ضریب $4 H_2 O$ رکھ سکتے ہیں نہ کہ $H_2 O_4$ یا $(H_2 O)_4$۔ اب جزوی طور پر متوازن مساوات بن جاتی ہے -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (جزوی طور پر متوازن مساوات)
قدم IV: Fe اور $H$ ایٹم ابھی بھی متوازن نہیں ہیں۔ آگے بڑھنے کے لیے ان عناصر میں سے کوئی بھی منتخب کریں۔ آئیے جزوی طور پر متوازن مساوات میں ہائیڈروجن ایٹموں کو متوازن کرتے ہیں۔
$H$ ایٹموں کی تعداد کو برابر کرنے کے لیے، دائیں طرف (RHS) پر ہائیڈروجن کے مالیکیولز کی تعداد چار بنائیں۔
| ہائیڈروجن کے ایٹم |
تعامل کرنے والے مادوں میں | پیداواروں میں |
|---|---|---|
| (i) ابتدائی | 8($ \mathrm{4H_2O} $ میں) | 2($ \mathrm{H_2} $ میں) |
| (ii) متوازن کرنے کے لیے | 8 | 2 $\times$ 4 |
مساوات یہ ہوگی -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(جزوی طور پر متوازن مساوات)
قدم V: مذکورہ بالا مساوات کا جائزہ لیں اور تیسرا عنصر اٹھائیں جو متوازن نہیں ہے۔ آپ دیکھیں گے کہ صرف ایک عنصر متوازن کرنے کے لیے باقی رہ گیا ہے، یعنی آئرن۔
| آئرن کے ایٹم | تعامل کرنے والے مادوں میں | پیداواروں میں |
|---|---|---|
| (i) ابتدائی | 1($ \mathrm{Fe} $ میں) | 3($ \mathrm{Fe_3O_4} $ میں) |
| (ii) متوازن کرنے کے لیے | 1 $\times$ 3 | 3 |
$Fe$ کو برابر کرنے کے لیے، ہم بائیں طرف (LHS) پر $Fe$ کے تین ایٹم لیتے ہیں۔
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
قدم VI: آخر میں، متوازن مساوات کی درستگی چیک کرنے کے لیے، ہم مساوات کے دونوں اطراف پر ہر عنصر کے ایٹم گنتے ہیں۔
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(متوازن مساوات)
مساوات (1.9) کے دونوں اطراف پر عناصر کے ایٹموں کی تعداد برابر ہے۔ یہ مساوات اب متوازن ہے۔ کیمیائی مساواتوں کو متوازن کرنے کا یہ طریقہ ہٹ اینڈ ٹرائل کہلاتا ہے کیونکہ ہم سب سے چھوٹے مکمل عددی ضریب کا استعمال کرتے ہوئے مساوات کو متوازن کرنے کے لیے کوششیں کرتے ہیں۔
قدم VII: طبیعی حالتوں کے علامات لکھنا مذکورہ بالا متوازن مساوات (1.9) کا احتیاط سے جائزہ لیں۔ کیا یہ مساوات ہمیں ہر تعامل کرنے والے مادے اور پیداوار کی طبیعی حالت کے بارے میں کچھ بتاتی ہے؟ اس مساوات میں ان کی طبیعی حالتوں کے بارے میں کوئی معلومات نہیں دی گئی ہے۔
کیمیائی مساوات کو زیادہ معلوماتی بنانے کے لیے، تعامل کرنے والے مادوں اور پیداواروں کی طبیعی حالتوں کا ذکر ان کے کیمیائی فارمولوں کے ساتھ کیا جاتا ہے۔ تعامل کرنے والے مادوں اور پیداواروں کی گیس، مائع، آبی اور ٹھوس حالتیں بالترتیب علامات (g)، (l)، (aq) اور (s) سے ظاہر کی جاتی ہیں۔ لفظ آبی (aq) لکھا جاتا ہے اگر تعامل کرنے والا مادہ یا پیداوار پانی میں محلول کی شکل میں موجود ہو۔
متوازن مساوات (1.9) بن جاتی ہے
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
نوٹ کریں کہ علامت $(g)$ کو $H_2 O$ کے ساتھ استعمال کیا جاتا ہے تاکہ یہ ظاہر کیا جا سکے کہ اس تعامل میں پانی بھاپ کی شکل میں استعمال ہوتا ہے۔
عام طور پر طبیعی حالتیں کیمیائی مساوات میں شامل نہیں کی جاتیں جب تک کہ ان کی وضاحت کرنا ضروری نہ ہو۔
کبھی کبھار تعامل کی شرائط، جیسے درجہ حرارت، دباؤ، عمل انگیز وغیرہ، مساوات میں تیر کے اوپر اور/یا نیچے ظاہر کی جاتی ہیں۔ مثال کے طور پر -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
ان مراحل کا استعمال کرتے ہوئے، کیا آپ متن میں پہلے دی گئی مساوات (1.2) کو متوازن کر سکتے ہیں؟
1.2 کیمیائی تعاملات کی اقسام
ہم نے جماعت نہم میں سیکھا تھا کہ کیمیائی تعامل کے دوران ایک عنصر کے ایٹم دوسرے عنصر کے ایٹموں میں تبدیل نہیں ہوتے۔ نہ ہی ایٹم مرکب سے غائب ہوتے ہیں یا کہیں اور سے ظاہر ہوتے ہیں۔ درحقیقت، کیمیائی تعاملات میں نئے مادے پیدا کرنے کے لیے ایٹموں کے درمیان بانڈز ٹوٹنے اور بننے کا عمل شامل ہوتا ہے۔ آپ باب 3 اور 4 میں ایٹموں کے درمیان بننے والے بانڈز کی اقسام کے بارے میں پڑھیں گے۔
1.2.1 اتحادی تعامل
سرگرمی 1.4
- ایک بیکر میں تھوڑی سی مقدار میں کیلشیم آکسائیڈ یا چونا لیں۔
- اس میں آہستہ آہستہ پانی شامل کریں۔
- بیکر کو چھوئیں جیسا کہ شکل 1.3 میں دکھایا گیا ہے۔
- کیا آپ درجہ حرارت میں کوئی تبدیلی محسوس کرتے ہیں؟
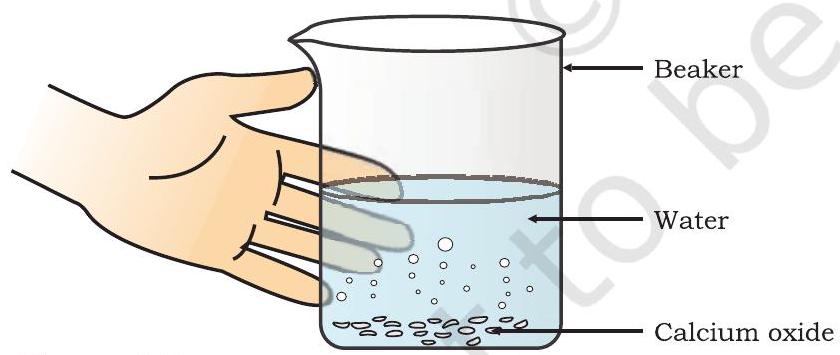
شکل 1.3 کیلشیم آکسائیڈ کے پانی کے ساتھ تعامل سے بجھا ہوا چونا بننا
کیلشیم آکسائیڈ پانی کے ساتھ زوردار تعامل کر کے بجھا ہوا چونا (کیلشیم ہائیڈروآکسائیڈ) بناتا ہے جس سے بڑی مقدار میں حرارت خارج ہوتی ہے۔
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
اس تعامل میں، کیلشیم آکسائیڈ اور پانی مل کر ایک واحد پیداوار، کیلشیم ہائیڈروآکسائیڈ بناتے ہیں۔ ایسا تعامل جس میں دو یا زیادہ تعامل کرنے والے مادوں سے ایک واحد پیداوار بنتی ہے، اتحادی تعامل کہلاتا ہے۔
کیا آپ جانتے ہیں؟
تعامل 1.13 سے بننے والے بجھے ہوئے چونے کے محلول کو دیواروں پر سفیدی کرنے کے لیے استعمال کیا جاتا ہے۔ کیلشیم ہائیڈروآکسائیڈ ہوا میں موجود کاربن ڈائی آکسائیڈ کے ساتھ آہستہ آہستہ تعامل کر کے دیواروں پر کیلشیم کاربونیٹ کی ایک پتلی تہہ بناتا ہے۔ کیلشیم کاربونیٹ سفیدی کرنے کے دو سے تین دن بعد بنتا ہے اور دیواروں کو چمکدار خاتمہ دیتا ہے۔ یہ بات دلچسپ ہے کہ سنگ مرمر کا کیمیائی فارمولا بھی $CaCO_3$ ہے۔
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
آئیے اتحادی تعاملات کی کچھ اور مثالیں زیر بحث لاتے ہیں۔
(i) کوئلہ جلنا
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ اور $O_2(g)$ سے پانی کی تشکیل
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
سادہ زبان میں ہم کہہ سکتے ہیں کہ جب دو یا زیادہ مادے (عناصر یا مرکبات) مل کر ایک واحد پیداوار بناتے ہیں، تو ایسے تعاملات اتحادی تعاملات کہلاتے ہیں۔
سرگرمی 1.4 میں، ہم نے یہ بھی مشاہدہ کیا کہ بڑی مقدار میں حرارت خارج ہوتی ہے۔ یہ تعامل کے مرکب کو گرم کر دیتا ہے۔ وہ تعاملات جن میں پیداواروں کی تشکیل کے ساتھ ساتھ حرارت خارج ہوتی ہے، حرارت زا (ایکزوتھرمک) کیمیائی تعاملات کہلاتے ہیں۔
حرارت زا تعاملات کی دیگر مثالیں ہیں -
(i) قدرتی گیس جلنا
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) کیا آپ جانتے ہیں کہ تنفس ایک حرارت زا عمل ہے؟
ہم سب جانتے ہیں کہ زندہ رہنے کے لیے ہمیں توانائی کی ضرورت ہوتی ہے۔ ہمیں یہ توانائی ہماری کھائی جانے والی خوراک سے ملتی ہے۔ ہضم کے دوران، خوراک سادہ مادوں میں ٹوٹ جاتی ہے۔ مثال کے طور پر، چاول، آلو اور روٹی میں کاربوہائیڈریٹس ہوتے ہیں۔ یہ کاربوہائیڈریٹس گلوکوز بنانے کے لیے ٹوٹتے ہیں۔ یہ گلوکوز ہمارے جسم کے خلیوں میں آکسیجن کے ساتھ مل کر توانائی فراہم کرتا ہے۔ اس تعامل کا خاص نام تنفس ہے، جس کے عمل کا آپ باب 6 میں مطالعہ کریں گے۔
$ \begin{equation*} \underset{\text{ (گلوکوز) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ توانائی } \tag{1.18} \end{equation*} $
(iii) سبزیوں کے مادے کا کمپوسٹ میں تحلیل ہونا بھی حرارت زا تعامل کی ایک مثال ہے۔
سرگرمی 1.1 میں ہونے والے تعامل کی قسم کی شناخت کریں، جہاں ایک واحد پیداوار کی تشکیل کے ساتھ ساتھ حرارت خارج ہوتی ہے۔
1.2.2 تحلیل تعامل
سرگرمی 1.5
- ایک خشک بوائلنگ ٹیوب میں تقریباً $2 g$ فیرس سلفیٹ کے کرسٹل لیں۔
- فیرس سلفیٹ کے کرسٹلز کا رنگ نوٹ کریں۔
- بوائلنگ ٹیوب کو برنر یا اسپرٹ لیمپ کی شعلے پر گرم کریں جیسا کہ شکل 1.4 میں دکھایا گیا ہے۔
- گرم کرنے کے بعد کرسٹلز کے رنگ کا مشاہدہ کریں۔
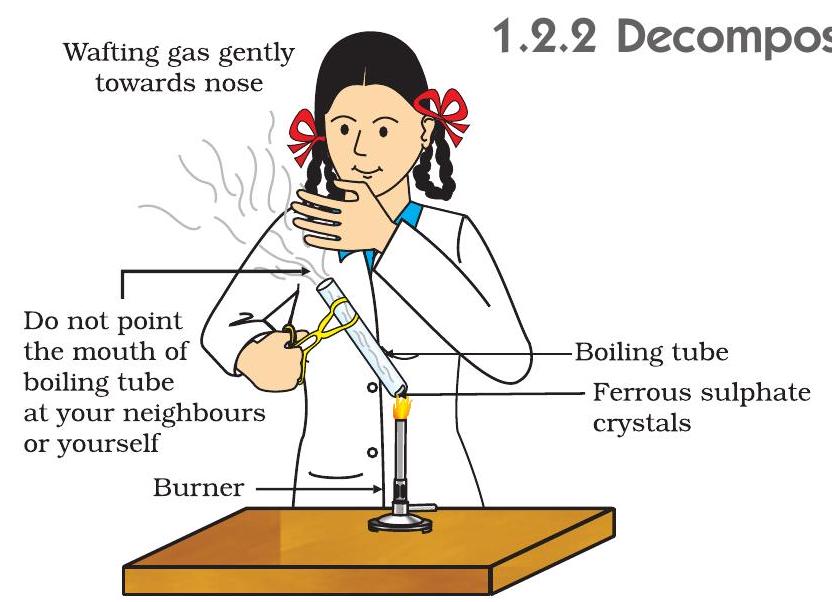
شکل 1.4 فیرس سلفیٹ کے کرسٹلز والی بوائلنگ ٹیوب کو گرم کرنے اور بو سونگھنے کا صحیح طریقہ
کیا آپ نے محسوس کیا ہے کہ فیرس سلفیٹ کے کرسٹلز کا سبز رنگ بدل گیا ہے؟ آپ گندھک جلنے کی مخصوص بو بھی محسوس کر سکتے ہیں۔
$ \underset{\text{(فیرس سلفیٹ)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (فیرک آکسائیڈ) }]{\text{ حرارت }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
اس تعامل میں آپ مشاہدہ کر سکتے ہیں کہ ایک واحد تعامل کرنے والا مادہ سادہ پیداواروں میں ٹوٹ جاتا ہے۔ یہ ایک تحلیل تعامل ہے۔ فیرس سلفیٹ کے کرسٹلز $(FeSO_4. 7 H_2 O)$ گرم کرنے پر پانی کھو دیتے ہیں اور کرسٹلز کا رنگ بدل جاتا ہے۔ پھر یہ فیرک آکسائیڈ $(Fe_2 O_3)$، سلفر ڈائی آکسائیڈ $(SO_2)$ اور سلفر ٹرائی آکسائیڈ $(SO_3)$ میں تحلیل ہو جاتا ہے۔ فیرک آکسائیڈ ایک ٹھوس ہے، جبکہ $SO_2$ اور $SO_3$ گیسیں ہیں۔
کیلشیم کاربونیٹ کا گرم کرنے پر کیلشیم آکسائیڈ اور کاربن ڈائی آکسائیڈ میں تحلیل ہونا ایک اہم تحلیل تعامل ہے جو مختلف صنعتوں میں استعمال ہوتا ہے۔ کیلشیم آکسائیڈ کو چونا یا بجھا چونا کہتے ہیں۔ اس کے بہت سے استعمال ہیں - ایک سیمنٹ کی تیاری میں ہے۔ جب تحلیل تعامل حرارت دے کر کیا جاتا ہے، تو اسے حرارتی تحلیل کہتے ہیں۔
$\underset{\text{ (Limestone) }}{CaCO_3(s)} \stackrel{\text{ Heat }}{\longrightarrow} \underset{\text{ (Quick lime) }}{CaO(s)}+{CO_2(g)} \quad (1.20)$
حرارتی تحلیل تعامل کی ایک اور مثال سرگرمی 1.6 میں دی گئی ہے۔
سرگرمی 1.6
- ایک بوائلنگ ٹیوب میں تقریباً $2 g$ لیڈ نائٹریٹ پاؤڈر لیں۔
- بوائلنگ ٹیوب کو چمٹے سے پکڑیں اور اسے شعلے پر گرم کریں، جیسا کہ شکل 1.5 میں دکھایا گیا ہے۔
- آپ کیا مشاہدہ کرتے ہیں؟ تبدیلی، اگر کوئی ہو، نوٹ کریں۔
آپ بھوری دھویں کے اخراج کا مشاہدہ کریں گے۔ یہ دھویں نائٹروجن ڈائی آکسائیڈ $(NO_2)$ کے ہیں۔ جو تعامل وقوع پذیر ہوتا ہے وہ ہے -
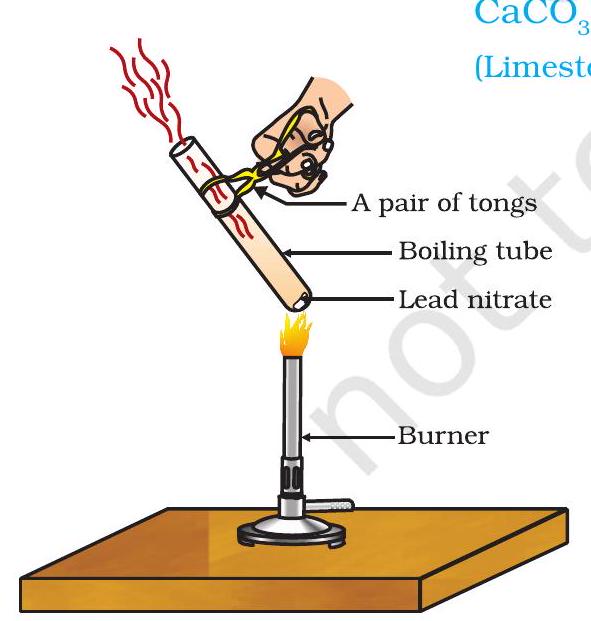
شکل 1.5 لیڈ نائٹریٹ کا گرم ہونا اور نائٹروجن ڈائی آکسائیڈ کا اخراج
$\underset{\text { (Lead nitrate) }}{2 \mathrm{~Pb}\left(\mathrm{NO}_3\right)_2(\mathrm{~s})} \xrightarrow{\text { Heat }} \underset{\text { (Lead oxide) }}{2 \mathrm{PbO}(\mathrm{s})}+\underset{\begin{array}{l}\text { (Nitrogen } \ \text { dioxide) }\end{array}}{4 \mathrm{NO}_2(\mathrm{~g})}+\underset{\text { (Oxygen) }}{\mathrm{O}_2(\mathrm{~g})} \quad (1.21)$
آئیے کچھ اور تحلیل تعاملات انجام دیتے ہیں جیسا کہ سرگرمی 1.7 اور 1.8 میں دیا گیا ہے۔
سرگرمی 1.7
- ایک پلاسٹک کا مگ لیں۔ اس کی بنیاد میں دو سوراخ کریں اور ان سوراخوں میں ربڑ کے سٹاپر لگائیں۔ ان ربڑ کے سٹاپرز میں کاربن الیکٹروڈز ڈالیں جیسا کہ شکل 1.6 میں دکھایا گیا ہے۔
- ان الیکٹروڈز کو 6 وولٹ کی بیٹری سے جوڑیں۔
- مگ کو پانی سے اس طرح بھریں کہ الیکٹروڈ ڈوب جائیں۔ پانی میں لگ بھگ گندھک کے تیزاب کی چند بوندیں شامل کریں۔
- پانی سے بھری دو ٹیسٹ ٹیوبیں لیں اور انہیں دو کاربن الیکٹروڈز پر الٹا رکھیں۔
- کرنٹ آن کریں اور آلہ کو کچھ دیر کے لیے بغیر ہلائے چھوڑ دیں۔
- آپ دونوں الیکٹروڈز پر بلبلے بنتے ہوئے دیکھیں گے۔ یہ بلبلے ٹیسٹ ٹیوبوں میں پانی کو ہٹا دیتے ہیں۔
- کیا دونوں ٹیسٹ ٹیوبوں میں جمع ہونے والی گیس کا حجم ایک جیسا ہے؟
- ایک بار جب ٹیسٹ ٹیوبیں متعلقہ گیسوں سے بھر جائیں، تو انہیں احتیاط سے ہٹا دیں۔
- ان گیسوں کو ایک ایک کر کے ٹیسٹ کرنے کے لیے ٹیسٹ ٹیوبوں کے منہ کے قریب ایک جلتی ہوئی موم بتی لائیں۔
احتیاط: یہ قدم استاد کے ذریعے احتیاط سے انجام دینا ضروری ہے۔
- ہر صورت میں کیا ہوتا ہے؟
- ہر ٹیسٹ ٹیوب میں کون سی گیس موجود ہے؟
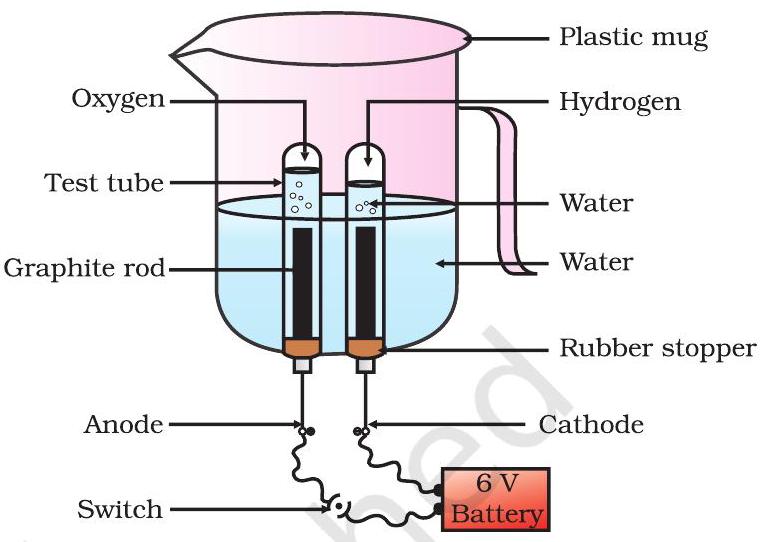
شکل 1.6 پانی کی برق پاشیدگی
سرگرمی 1.8
- ایک چائنا ڈش میں تقریباً $2 g$ سلور کلورائیڈ لیں۔
- اس کا رنگ کیا ہے؟
- اس چائنا ڈش کو کچھ دیر کے لیے دھوپ میں رکھیں (شکل 1.7)۔
- کچھ دیر بعد سلور کلورائیڈ کے رنگ کا مشاہدہ کریں۔
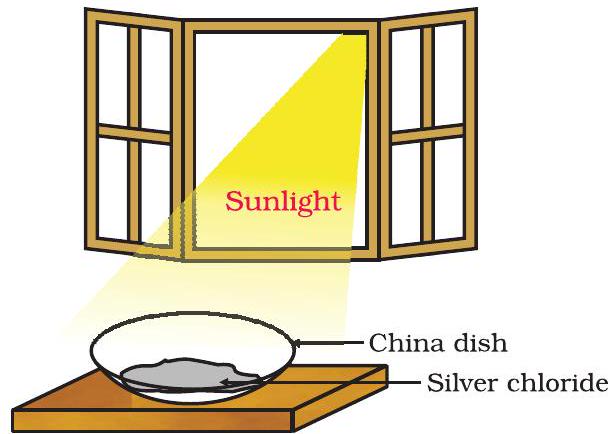
شکل 1.7 سلور کلورائیڈ دھوپ میں سرمئی ہو کر سلور دھات بناتا ہے۔
آپ دیکھیں گے کہ سفید سلور کلورائیڈ دھوپ میں سرمئی ہو جاتا ہے۔ یہ روشنی کے ذریعے سلور کلورائیڈ کے سلور اور کلورین میں تحلیل ہونے کی وجہ سے ہے۔
$ \mathrm{2 AgCl(s) \xrightarrow{\text{ دھوپ }} 2 Ag(s)+Cl_2(g)} \quad (1.22) $
سلور برومائیڈ بھی اسی طرح برتاؤ کرتا ہے۔
$\mathrm{2 AgBr(s) \xrightarrow{\text{ Sunlight }} 2 Ag(s)+Br_2(g)} \quad (1.23)$
مذکورہ بالا تعاملات سیاہ اور سفید فوٹوگرافی میں استعمال ہوتے ہیں۔ کس قسم کی توانائی ان تحلیل تعاملات کا سبب بن رہی ہے؟
ہم نے دیکھا ہے کہ تحلیل تعاملات کو تعامل کرنے والے مادوں کو توڑنے کے لیے توانائی کی ضرورت ہوتی ہے خواہ وہ حرارت، روشنی یا بجلی کی شکل میں ہو۔ وہ تعاملات جن میں توانائی جذب ہوتی ہے، حرارت گیر (اینڈوتھرمک) تعاملات کہلاتے ہیں۔
درج ذیل سرگرمی انجام دیں
ایک ٹیسٹ ٹیوب میں تقریباً $2 g$ بیریئم ہائیڈروآکسائیڈ لیں۔ اس میں $1 g$ امونیم کلورائیڈ شامل کریں اور شیشے کی سلاخ کی مدد سے مکس کریں۔ ٹیسٹ ٹیوب کی تہہ کو ا











