অধ্যায় ০১ রাসায়নিক বিক্রিয়া ও সমীকরণ
নিচের দৈনন্দিন জীবনের কিছু অবস্থা বিবেচনা কর এবং ভেবে দেখ কী ঘটে যখন -
- গ্রীষ্মকালে দুধকে ঘরের তাপমাত্রায় রাখা হয়।
- একটি লোহার তাওয়া/প্যান/পেরেক আর্দ্র বায়ুমণ্ডলে উন্মুক্ত রাখা হয়।
- আঙ্গুর গাঁজন প্রক্রিয়ার মাধ্যমে পরিবর্তিত হয়।
- খাদ্য রান্না করা হয়।
- আমাদের দেহে খাদ্য পরিপাক হয়।
- আমরা শ্বাস-প্রশ্বাস নিই।
উপরের সব অবস্থায়, প্রাথমিক পদার্থের প্রকৃতি ও পরিচয় কিছুটা পরিবর্তিত হয়েছে। আমরা আগের ক্লাসে পদার্থের ভৌত ও রাসায়নিক পরিবর্তন সম্পর্কে ইতিমধ্যেই শিখেছি। যখনই একটি রাসায়নিক পরিবর্তন ঘটে, আমরা বলতে পারি একটি রাসায়নিক বিক্রিয়া সংঘটিত হয়েছে।
তুমি সম্ভবত ভাবছ যে রাসায়নিক বিক্রিয়া বলতে আসলে কী বোঝায়? কীভাবে আমরা জানতে পারি যে একটি রাসায়নিক বিক্রিয়া সংঘটিত হয়েছে? এই প্রশ্নগুলোর উত্তর খুঁজে পেতে আসুন কিছু কার্যকলাপ সম্পাদন করি।
কার্যকলাপ ১.১
সতর্কতা: এই কার্যকলাপটির জন্য শিক্ষকের সহায়তা প্রয়োজন। শিক্ষার্থীদের উপযুক্ত চশমা পরা ভালো হবে।
- প্রায় ৩-৪ সেমি দৈর্ঘ্যের একটি ম্যাগনেসিয়াম ফিতাকে স্যান্ডপেপার দিয়ে ঘষে পরিষ্কার কর।
- একজোড়া চিমটা দিয়ে ধরে রাখ। একটি স্পিরিট ল্যাম্প বা বার্নার ব্যবহার করে জ্বালাও এবং গঠিত ছাইটিকে একটি ওয়াচ-গ্লাসে সংগ্রহ কর, যেমন চিত্র ১.১-এ দেখানো হয়েছে। ম্যাগনেসিয়াম ফিতাটি জ্বালানোর সময় তোমার চোখ থেকে যতদূর সম্ভব দূরে রাখ।
- তুমি কী লক্ষ কর?
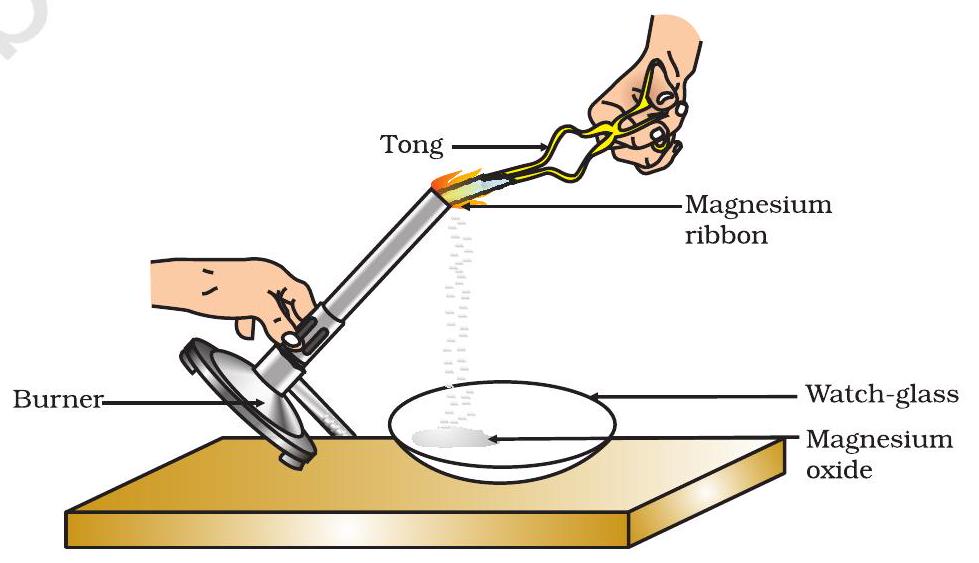
চিত্র ১.১
বায়ুতে ম্যাগনেসিয়াম ফিতার দহন এবং ওয়াচ-গ্লাসে ম্যাগনেসিয়াম অক্সাইড সংগ্রহ
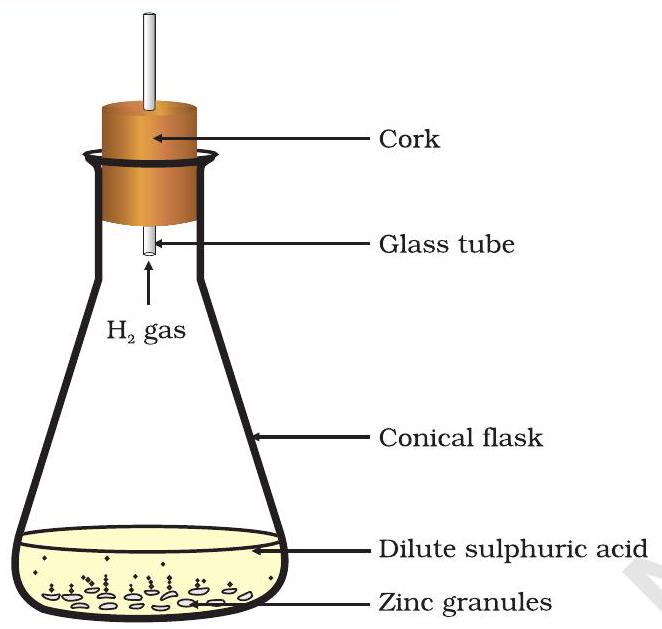
চিত্র ১.২ দস্তার উপর লঘু সালফিউরিক অ্যাসিডের ক্রিয়ায় হাইড্রোজেন গ্যাসের উৎপাদন
তুমি অবশ্যই লক্ষ্য করেছ যে ম্যাগনেসিয়াম ফিতা একটি ঝলমলে সাদা শিখা নিয়ে জ্বলে এবং একটি সাদা গুঁড়োয় পরিণত হয়। এই গুঁড়োটি হল ম্যাগনেসিয়াম অক্সাইড। এটি ম্যাগনেসিয়াম এবং বায়ুতে উপস্থিত অক্সিজেনের মধ্যে বিক্রিয়ার ফলে গঠিত হয়।
কার্যকলাপ ১.২
- একটি টেস্ট টিউবে লেড নাইট্রেট দ্রবণ নাও।
- এতে পটাসিয়াম আয়োডাইড দ্রবণ যোগ কর।
- তুমি কী লক্ষ কর?
কার্যকলাপ ১.৩
- একটি কনিক্যাল ফ্লাস্ক বা টেস্ট টিউবে কিছু দস্তার দানা নাও।
- এতে লঘু হাইড্রোক্লোরিক অ্যাসিড বা সালফিউরিক অ্যাসিড যোগ কর (চিত্র ১.২)।
সতর্কতা: অ্যাসিডটি সাবধানে ব্যবহার কর।
- দস্তার দানাগুলোর চারপাশে কিছু ঘটতে দেখছ কি?
- কনিক্যাল ফ্লাস্ক বা টেস্ট টিউবটি স্পর্শ কর। এর তাপমাত্রায় কোনো পরিবর্তন আছে কি?
উপরের তিনটি কার্যকলাপ থেকে, আমরা বলতে পারি যে নিম্নলিখিত পর্যবেক্ষণগুলোর যেকোনো একটি আমাদের একটি রাসায়নিক বিক্রিয়া সংঘটিত হয়েছে কিনা তা নির্ধারণ করতে সাহায্য করে –
- অবস্থার পরিবর্তন
- বর্ণের পরিবর্তন
- গ্যাসের বিবর্তন
- তাপমাত্রার পরিবর্তন।
আমরা আমাদের চারপাশের পরিবর্তনগুলো পর্যবেক্ষণ করলে দেখতে পাই যে আমাদের চারপাশে বিপুল বৈচিত্র্যের রাসায়নিক বিক্রিয়া ঘটছে। আমরা এই অধ্যায়ে বিভিন্ন ধরনের রাসায়নিক বিক্রিয়া এবং তাদের প্রতীকী উপস্থাপনা সম্পর্কে অধ্যয়ন করব।
১.১ রাসায়নিক সমীকরণ
কার্যকলাপ ১.১-কে এভাবে বর্ণনা করা যেতে পারে – যখন একটি ম্যাগনেসিয়াম ফিতাকে অক্সিজেনে জ্বালানো হয়, তখন তা ম্যাগনেসিয়াম অক্সাইডে রূপান্তরিত হয়। একটি রাসায়নিক বিক্রিয়ার এই বর্ণনাটি বাক্য আকারে বেশ দীর্ঘ। এটি সংক্ষিপ্ত আকারে লেখা যেতে পারে। এটি করার সবচেয়ে সহজ উপায় হল এটিকে শব্দ-সমীকরণ আকারে লেখা। উপরের বিক্রিয়ার জন্য শব্দ-সমীকরণটি হবে –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
যেসব পদার্থ বিক্রিয়ায় (১.১) রাসায়নিক পরিবর্তনের মধ্য দিয়ে যায়, অর্থাৎ ম্যাগনেসিয়াম ও অক্সিজেন, তারা বিক্রিয়ক। নতুন পদার্থটি হল ম্যাগনেসিয়াম অক্সাইড, যা বিক্রিয়ার সময় গঠিত হয়, এটি উৎপাদ।
একটি শব্দ-সমীকরণ বিক্রিয়ক থেকে উৎপাদে পরিবর্তনকে তাদের মধ্যে স্থাপিত একটি তীর চিহ্নের মাধ্যমে দেখায়। বিক্রিয়কগুলো বাম পাশে (LHS) লেখা হয় এবং তাদের মধ্যে একটি যোগ চিহ্ন (+) থাকে। একইভাবে, উৎপাদগুলো ডান পাশে (RHS) লেখা হয় এবং তাদের মধ্যেও একটি যোগ চিহ্ন (+) থাকে। তীরের মাথাটি উৎপাদের দিকে নির্দেশ করে এবং বিক্রিয়ার দিক দেখায়।
১.১.১ একটি রাসায়নিক সমীকরণ লেখা
রাসায়নিক সমীকরণ উপস্থাপনের আর কোনো সংক্ষিপ্ত উপায় আছে কি? রাসায়নিক সমীকরণগুলো আরও সংক্ষিপ্ত ও কার্যকরী করা যেতে পারে যদি আমরা শব্দের পরিবর্তে রাসায়নিক সংকেত ব্যবহার করি। একটি রাসায়নিক সমীকরণ একটি রাসায়নিক বিক্রিয়াকে উপস্থাপন করে। যদি তুমি ম্যাগনেসিয়াম, অক্সিজেন ও ম্যাগনেসিয়াম অক্সাইডের সংকেত স্মরণ কর, তবে উপরের শব্দ-সমীকরণটি এভাবে লেখা যেতে পারে -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
তীরের বাম পাশ (LHS) ও ডান পাশে (RHS) প্রতিটি মৌলের পরমাণুর সংখ্যা গণনা কর এবং তুলনা কর। উভয় পাশে প্রতিটি মৌলের পরমাণুর সংখ্যা কি একই? যদি হ্যাঁ, তবে সমীকরণটি সমতাবদ্ধ। যদি না হয়, তবে সমীকরণটি অসমতাবদ্ধ কারণ সমীকরণের উভয় পাশে ভর একই নয়। এমন একটি রাসায়নিক সমীকরণ হল একটি বিক্রিয়ার কঙ্কালসার রাসায়নিক সমীকরণ। সমীকরণ (১.২) হল বায়ুতে ম্যাগনেসিয়ামের দহনের জন্য একটি কঙ্কালসার রাসায়নিক সমীকরণ।
১.১.২ সমতাবদ্ধ রাসায়নিক সমীকরণ
তুমি নবম শ্রেণিতে যে ভর সংরক্ষণ সূত্র পড়েছ তা স্মরণ কর; একটি রাসায়নিক বিক্রিয়ায় ভর সৃষ্টি বা ধ্বংস করা যায় না। অর্থাৎ, একটি রাসায়নিক বিক্রিয়ার উৎপাদে উপস্থিত মৌলগুলোর মোট ভর বিক্রিয়কগুলিতে উপস্থিত মৌলগুলোর মোট ভরের সমান হতে হবে।
অন্য কথায়, প্রতিটি মৌলের পরমাণুর সংখ্যা একটি রাসায়নিক বিক্রিয়ার আগে ও পরে একই থাকে। তাই, আমাদের একটি কঙ্কালসার রাসায়নিক সমীকরণকে সমতাবদ্ধ করতে হবে। রাসায়নিক সমীকরণ (১.২) কি সমতাবদ্ধ? আসুন ধাপে ধাপে একটি রাসায়নিক সমীকরণ সমতাবদ্ধ করা সম্পর্কে শিখি।
কার্যকলাপ ১.৩-এর জন্য শব্দ-সমীকরণটি এভাবে উপস্থাপন করা যেতে পারে -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
উপরের শব্দ-সমীকরণটি নিম্নলিখিত রাসায়নিক সমীকরণ দ্বারা উপস্থাপন করা যেতে পারে -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
আসুন তীরের উভয় পাশে বিভিন্ন মৌলের পরমাণুর সংখ্যা পরীক্ষা করি।
| মৌল | বিক্রিয়কগুলিতে পরমাণুর সংখ্যা (LHS) | উৎপাদগুলিতে পরমাণুর সংখ্যা (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
যেহেতু প্রতিটি মৌলের পরমাণুর সংখ্যা তীরের উভয় পাশে একই, তাই সমীকরণ (১.৩) একটি সমতাবদ্ধ রাসায়নিক সমীকরণ।
আসুন নিম্নলিখিত রাসায়নিক সমীকরণটি সমতাবদ্ধ করার চেষ্টা করি -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
ধাপ I: একটি রাসায়নিক সমীকরণ সমতাবদ্ধ করতে, প্রথমে প্রতিটি সংকেতের চারপাশে বাক্স আঁক। সমীকরণ সমতাবদ্ধ করার সময় বাক্সের ভিতরের কোনো কিছু পরিবর্তন করবে না।
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
ধাপ II: অসমতাবদ্ধ সমীকরণ (১.৫)-এ উপস্থিত বিভিন্ন মৌলের পরমাণুর সংখ্যা তালিকাভুক্ত কর।
| মৌল | বিক্রিয়কগুলিতে পরমাণুর সংখ্যা (LHS) | উৎপাদগুলিতে পরমাণুর সংখ্যা (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
ধাপ III: প্রায়শই সর্বাধিক সংখ্যক পরমাণুযুক্ত যৌগ দিয়ে সমতাবদ্ধ করা শুরু করা সুবিধাজনক। এটি একটি বিক্রিয়ক বা উৎপাদ হতে পারে। সেই যৌগটিতে, যে মৌলটির সর্বাধিক সংখ্যক পরমাণু আছে তা নির্বাচন কর। এই মানদণ্ড ব্যবহার করে, আমরা $Fe_3 O_4$ এবং এতে অক্সিজেন মৌলটি নির্বাচন করি। ডান পাশে (RHS) চারটি অক্সিজেন পরমাণু আছে এবং বাম পাশে (LHS) মাত্র একটি আছে।
অক্সিজেন পরমাণুগুলো সমতাবদ্ধ করতে -
| অক্সিজেনের পরমাণু |
বিক্রিয়কগুলিতে | উৎপাদগুলিতে |
|---|---|---|
| (i) প্রাথমিক | 1($ \mathrm{H_2O} $-এ) | 4($ \mathrm{Fe_3O_4} $-এ) |
| (ii) সমতাবদ্ধ করতে | 1 $\times$ 4 | 4 |
পরমাণুর সংখ্যা সমান করতে, এটি মনে রাখতে হবে যে আমরা বিক্রিয়ায় জড়িত যৌগ বা মৌলগুলোর সংকেত পরিবর্তন করতে পারি না। উদাহরণস্বরূপ, অক্সিজেন পরমাণু সমতাবদ্ধ করতে আমরা ‘4’ গুণাঙ্ক হিসেবে $4 H_2 O$ বসাতে পারি, কিন্তু $H_2 O_4$ বা $(H_2 O)_4$ নয়। এখন আংশিকভাবে সমতাবদ্ধ সমীকরণটি হয়ে যায় -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (আংশিকভাবে সমতাবদ্ধ সমীকরণ)
ধাপ IV: Fe এবং $H$ পরমাণু এখনও সমতাবদ্ধ হয়নি। আরও এগিয়ে যেতে এই মৌলগুলোর যেকোনো একটি নির্বাচন কর। আসুন আংশিকভাবে সমতাবদ্ধ সমীকরণে হাইড্রোজেন পরমাণুগুলো সমতাবদ্ধ করি।
$H$ পরমাণুর সংখ্যা সমান করতে, ডান পাশে (RHS) হাইড্রোজেন অণুর সংখ্যাকে চার করুন।
| হাইড্রোজেনের পরমাণু |
বিক্রিয়কগুলিতে | উৎপাদগুলিতে |
|---|---|---|
| (i) প্রাথমিক | 8($ \mathrm{4H_2O} $-এ) | 2($ \mathrm{H_2} $-এ) |
| (ii) সমতাবদ্ধ করতে | 8 | 2 $\times$ 4 |
সমীকরণটি হবে -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(আংশিকভাবে সমতাবদ্ধ সমীকরণ)
ধাপ V: উপরের সমীকরণটি পরীক্ষা কর এবং তৃতীয় যে মৌলটি সমতাবদ্ধ হয়নি তা বাছাই কর। তুমি দেখবে যে কেবল একটি মৌল সমতাবদ্ধ করার জন্য বাকি আছে, সেটি হল লোহা (আয়রন)।
| লোহার পরমাণু | বিক্রিয়কগুলিতে | উৎপাদগুলিতে |
|---|---|---|
| (i) প্রাথমিক | 1($ \mathrm{Fe} $-এ) | 3($ \mathrm{Fe_3O_4} $-এ) |
| (ii) সমতাবদ্ধ করতে | 1 $\times$ 3 | 3 |
$Fe$ সমান করতে, আমরা বাম পাশে (LHS) $Fe$-এর তিনটি পরমাণু নিই।
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
ধাপ VI: শেষে, সমতাবদ্ধ সমীকরণের সঠিকতা যাচাই করতে, আমরা সমীকরণের উভয় পাশে প্রতিটি মৌলের পরমাণু গণনা করি।
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(সমতাবদ্ধ সমীকরণ)
সমীকরণ (১.৯)-এর উভয় পাশে মৌলগুলোর পরমাণুর সংখ্যা সমান। এই সমীকরণটি এখন সমতাবদ্ধ। রাসায়নিক সমীকরণ সমতাবদ্ধ করার এই পদ্ধতিকে বলা হয় হিট-অ্যান্ড-ট্রায়াল পদ্ধতি কারণ আমরা ক্ষুদ্রতম পূর্ণসংখ্যা গুণাঙ্ক ব্যবহার করে সমীকরণটি সমতাবদ্ধ করার জন্য চেষ্টা করি।
ধাপ VII: ভৌত অবস্থার প্রতীক লেখা উপরের সমতাবদ্ধ সমীকরণ (১.৯) সাবধানে পরীক্ষা কর। এই সমীকরণটি কি আমাদের প্রতিটি বিক্রিয়ক ও উৎপাদের ভৌত অবস্থা সম্পর্কে কিছু বলে? এই সমীকরণে তাদের ভৌত অবস্থা সম্পর্কে কোনো তথ্য দেওয়া হয়নি।
একটি রাসায়নিক সমীকরণকে আরও তথ্যপূর্ণ করতে, বিক্রিয়ক ও উৎপাদগুলির ভৌত অবস্থা তাদের রাসায়নিক সংকেতের পাশাপাশি উল্লেখ করা হয়। বিক্রিয়ক ও উৎপাদগুলির গ্যাসীয়, তরল, জলীয় ও কঠিন অবস্থা যথাক্রমে (g), (l), (aq) ও (s) চিহ্ন দ্বারা উপস্থাপিত হয়। জলীয় (aq) শব্দটি লেখা হয় যদি বিক্রিয়ক বা উৎপাদ জলে দ্রবণ আকারে উপস্থিত থাকে।
সমতাবদ্ধ সমীকরণ (১.৯) হয়ে যায়
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
লক্ষ্য কর যে $(g)$ প্রতীকটি $H_2 O$-এর সাথে ব্যবহার করা হয়েছে এই ইঙ্গিত দিতে যে এই বিক্রিয়ায় জল বাষ্প আকারে ব্যবহৃত হয়।
সাধারণত ভৌত অবস্থাগুলো একটি রাসায়নিক সমীকরণে অন্তর্ভুক্ত করা হয় না, যদি না সেগুলো নির্দিষ্ট করা প্রয়োজন হয়।
কখনও কখনও বিক্রিয়ার শর্ত, যেমন তাপমাত্রা, চাপ, অনুঘটক ইত্যাদি, সমীকরণের তীরের উপরে এবং/অথবা নীচে নির্দেশ করা হয়। উদাহরণস্বরূপ -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
এই ধাপগুলো ব্যবহার করে, তুমি কি আগের পাঠ্যে দেওয়া সমীকরণ (১.২) সমতাবদ্ধ করতে পার?
১.২ রাসায়নিক বিক্রিয়ার প্রকারভেদ
আমরা নবম শ্রেণিতে শিখেছি যে একটি রাসায়নিক বিক্রিয়ার সময় একটি মৌলের পরমাণু অন্য মৌলের পরমাণুতে পরিবর্তিত হয় না। আবার পরমাণু মিশ্রণ থেকে অদৃশ্যও হয় না বা অন্য কোথা থেকে আবির্ভূতও হয় না। প্রকৃতপক্ষে, রাসায়নিক বিক্রিয়ায় নতুন পদার্থ উৎপাদনের জন্য পরমাণুগুলোর মধ্যে বন্ধন ভাঙা ও গঠন জড়িত। তুমি ৩ ও ৪ নং অধ্যায়ে পরমাণুগুলোর মধ্যে গঠিত বন্ধনের প্রকার সম্পর্কে অধ্যয়ন করবে।
১.২.১ সংযোজন বিক্রিয়া
কার্যকলাপ ১.৪
- একটি বিকারকে অল্প পরিমাণ ক্যালসিয়াম অক্সাইড বা চুন নাও।
- এতে ধীরে ধীরে জল যোগ কর।
- চিত্র ১.৩-এ দেখানো মতো বিকারকটি স্পর্শ কর।
- তুমি কি তাপমাত্রায় কোনো পরিবর্তন অনুভব কর?
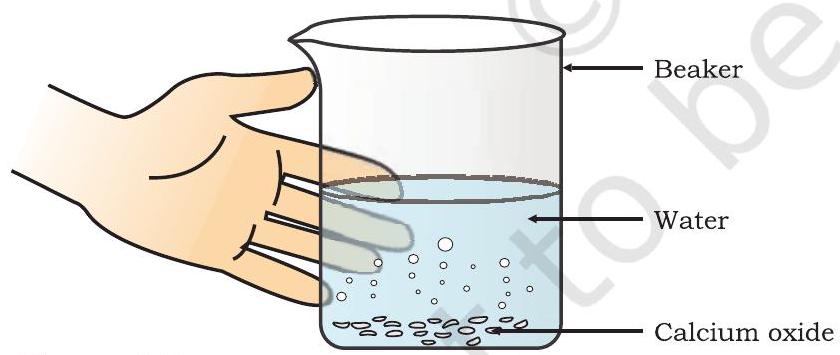
চিত্র ১.৩ ক্যালসিয়াম অক্সাইডের সাথে জলের বিক্রিয়ায় চুনের পান গঠন
ক্যালসিয়াম অক্সাইড জলের সাথে প্রবলভাবে বিক্রিয়া করে চুনের পান (ক্যালসিয়াম হাইড্রোক্সাইড) উৎপন্ন করে এবং প্রচুর পরিমাণ তাপ নির্গত করে।
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
এই বিক্রিয়ায়, ক্যালসিয়াম অক্সাইড ও জল একত্রিত হয়ে একটি একক উৎপাদ, ক্যালসিয়াম হাইড্রোক্সাইড গঠন করে। এমন একটি বিক্রিয়া যেখানে দুই বা ততোধিক বিক্রিয়ক থেকে একটি একক উৎপাদ গঠিত হয় তাকে সংযোজন বিক্রিয়া বলে।
তুমি কি জান?
বিক্রিয়া ১.১৩ দ্বারা উৎপাদিত চুনের পানির দ্রবণ দেয়াল সাদা করতে ব্যবহৃত হয়। ক্যালসিয়াম হাইড্রোক্সাইড বায়ুর কার্বন ডাই-অক্সাইডের সাথে ধীরে ধীরে বিক্রিয়া করে দেয়ালে ক্যালসিয়াম কার্বনেটের একটি পাতলা স্তর গঠন করে। ক্যালসিয়াম কার্বনেট সাদা করার দুই থেকে তিন দিন পরে গঠিত হয় এবং দেয়ালকে একটি চকচকে আভা দেয়। এটি জানা আকর্ষণীয় যে মার্বেলের রাসায়নিক সংকেতও $CaCO_3$।
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
আসুন সংযোজন বিক্রিয়ার আরও কিছু উদাহরণ আলোচনা করি।
(i) কয়লার দহন
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ ও $O_2(g)$ থেকে জল গঠন
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
সরল ভাষায় আমরা বলতে পারি যে যখন দুই বা ততোধিক পদার্থ (মৌল বা যৌগ) একত্রিত হয়ে একটি একক উৎপাদ গঠন করে, তখন সেই বিক্রিয়াগুলোকে সংযোজন বিক্রিয়া বলে।
কার্যকলাপ ১.৪-এ, আমরা আরও লক্ষ্য করেছি যে প্রচুর পরিমাণ তাপ নির্গত হয়। এটি বিক্রিয়া মিশ্রণটিকে উষ্ণ করে তোলে। যে বিক্রিয়াগুলোতে উৎপাদ গঠনের সাথে সাথে তাপ নির্গত হয় তাদের তাপউৎপাদী রাসায়নিক বিক্রিয়া বলে।
তাপউৎপাদী বিক্রিয়ার অন্যান্য উদাহরণ হল -
(i) প্রাকৃতিক গ্যাসের দহন
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) তুমি কি জান যে শ্বসন একটি তাপউৎপাদী প্রক্রিয়া?
আমরা সবাই জানি যে বেঁচে থাকার জন্য আমাদের শক্তির প্রয়োজন। আমরা যে খাবার খাই তা থেকে এই শক্তি পাই। পরিপাকের সময়, খাদ্য সরল পদার্থে ভেঙে যায়। উদাহরণস্বরূপ, ভাত, আলু ও রুটিতে কার্বোহাইড্রেট থাকে। এই কার্বোহাইড্রেটগুলো ভেঙে গ্লুকোজ গঠন করে। এই গ্লুকোজ আমাদের দেহের কোষে অক্সিজেনের সাথে মিলিত হয়ে শক্তি সরবরাহ করে। এই বিক্রিয়াটির বিশেষ নাম হল শ্বসন, যার প্রক্রিয়া তুমি ৬ নং অধ্যায়ে অধ্যয়ন করবে।
$ \begin{equation*} \underset{\text{ (গ্লুকোজ) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ শক্তি } \tag{1.18} \end{equation*} $
(iii) সবজি পদার্থের কম্পোস্টে পচনও একটি তাপউৎপাদী বিক্রিয়ার উদাহরণ।
কার্যকলাপ ১.১-এ সংঘটিত বিক্রিয়ার প্রকার চিহ্নিত কর, যেখানে একটি একক উৎপাদ গঠনের সাথে সাথে তাপ নির্গত হয়।
১.২.২ বিয়োজন বিক্রিয়া
কার্যকলাপ ১.৫
- একটি শুষ্ক বয়লিং টিউবে প্রায় $2 g$ ফেরাস সালফেট স্ফটিক নাও।
- ফেরাস সালফেট স্ফটিকের বর্ণ লক্ষ্য কর।
- একটি বার্নার বা স্পিরিট ল্যাম্পের শিখার উপর বয়লিং টিউবটি গরম কর, যেমন চিত্র ১.৪-এ দেখানো হয়েছে।
- গরম করার পর স্ফটিকগুলোর বর্ণ পর্যবেক্ষণ কর।
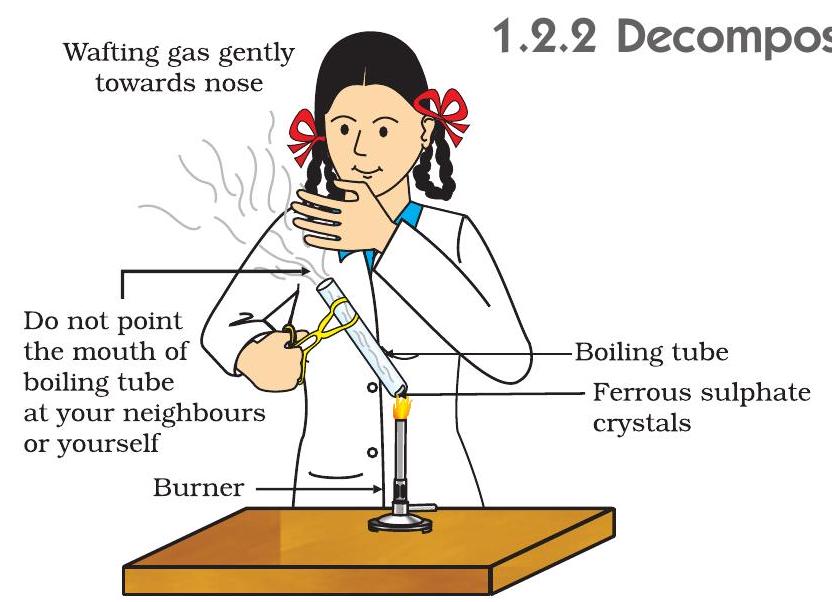
চিত্র ১.৪ ফেরাস সালফেট স্ফটিকযুক্ত বয়লিং টিউব গরম করার এবং গন্ধ শোকার সঠিক পদ্ধতি
তুমি কি লক্ষ্য করেছ যে ফেরাস সালফেট স্ফটিকের সবুজ বর্ণ পরিবর্তিত হয়েছে? তুমি জ্বলন্ত গন্ধকের বৈশিষ্ট্যপূর্ণ গন্ধও পেতে পার।
$ \underset{\text{(ফেরাস সালফেট)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (ফেরিক অক্সাইড) }]{\text{ তাপ }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
এই বিক্রিয়ায় তুমি লক্ষ্য করতে পার যে একটি একক বিক্রিয়ক ভেঙে সরল উৎপাদ দেয়। এটি একটি বিয়োজন বিক্রিয়া। ফেরাস সালফেট স্ফটিক $(FeSO_4. 7 H_2 O)$ গরম করলে জল হারায় এবং স্ফটিকগুলোর বর্ণ পরিবর্তিত হয়। তারপর এটি ফেরিক অক্সাইড $(Fe_2 O_3)$, সালফার ডাই-অক্সাইড $(SO_2)$ এবং সালফার ট্রাই-অক্সাইড $(SO_3)$-এ বিয়োজিত হয়। ফেরিক অক্সাইড একটি কঠিন, অন্যদিকে $SO_2$ ও $SO_3$ গ্যাস।
ক্যালসিয়াম কার্বনেটের তাপ প্রয়োগে ক্যালসিয়াম অক্সাইড ও কার্বন ডাই-অক্সাইডে বিয়োজন বিভিন্ন শিল্পে ব্যবহৃত একটি গুরুত্বপূর্ণ বিয়োজন বিক্রিয়া। ক্যালসিয়াম অক্সাইডকে চুন বা দ্রুত চুন বলে। এর অনেক ব্যবহার আছে - একটি হল সিমেন্ট উৎপাদনে। যখন একটি বিয়োজন বিক্রিয়া তাপ প্রয়োগে সম্পাদিত হয়, তখন তাকে তাপীয় বিয়োজন বলে।
$\underset{\text{ (Limestone) }}{CaCO_3(s)} \stackrel{\text{ Heat }}{\longrightarrow} \underset{\text{ (Quick lime) }}{CaO(s)}+{CO_2(g)} \quad (1.20)$
তাপীয় বিয়োজন বিক্রিয়ার আরেকটি উদাহরণ কার্যকলাপ ১.৬-এ দেওয়া আছে।
কার্যকলাপ ১.৬
- একটি বয়লিং টিউবে প্রায় $2 g$ লেড নাইট্রেট গুঁড়ো নাও।
- একজোড়া চিমটা দিয়ে বয়লিং টিউবটি ধরে একটি শিখার উপর গরম কর, যেমন চিত্র ১.৫-এ দেখানো হয়েছে।
- তুমি কী লক্ষ্য কর? পরিবর্তন থাকলে তা নোট কর।
তুমি বাদামি ধোঁয়ার নির্গমন লক্ষ্য করবে। এই ধোঁয়াগুলো নাইট্রোজেন ডাই-অক্সাইড $(NO_2)$-এর। যে বিক্রিয়াটি ঘটে তা হল -
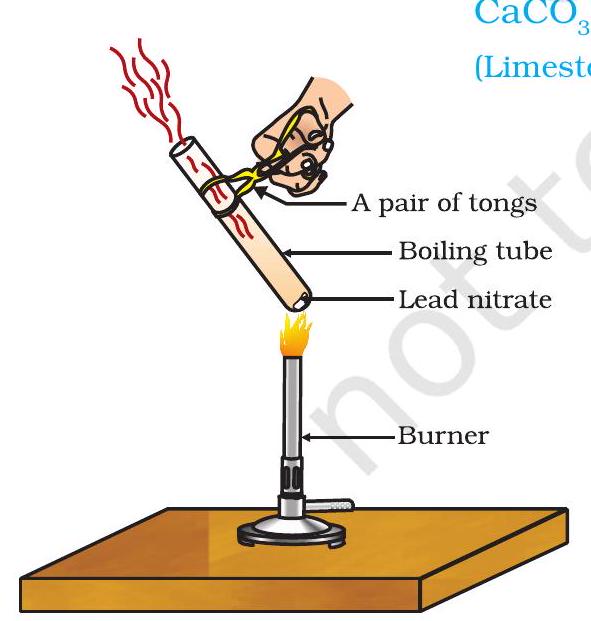
চিত্র ১.৫ লেড নাইট্রেট গরম করা এবং নাইট্রোজেন ডাই-অক্সাইডের নির্গমন
$\underset{\text { (Lead nitrate) }}{2 \mathrm{~Pb}\left(\mathrm{NO}_3\right)_2(\mathrm{~s})} \xrightarrow{\text { Heat }} \underset{\text { (Lead oxide) }}{2 \mathrm{PbO}(\mathrm{s})}+\underset{\begin{array}{l}\text { (Nitrogen } \ \text { dioxide) }\end{array}}{4 \mathrm{NO}_2(\mathrm{~g})}+\underset{\text { (Oxygen) }}{\mathrm{O}_2(\mathrm{~g})} \quad (1.21)$
আসুন কার্যকলাপ ১.৭ ও ১.৮-এ দেওয়া মতো আরও কিছু বিয়োজন বিক্রিয়া সম্পাদন করি।
কার্যকলাপ ১.৭
- একটি প্লাস্টিকের মগ নাও। এর তলদেশে দুটি ছিদ্র কর এবং এই ছিদ্রগুলিতে রাবার স্টপার লাগাও। চিত্র ১.৬-এ দেখানো মতো এই রাবার স্টপারগুলিতে কার্বন ইলেক্ট্রোড বসাও।
- এই ইলেক্ট্রোডগুলো একটি ৬ ভোল্টের ব্যাটারির সাথে সংযুক্ত কর।
- মগটিকে জল দিয়ে এমনভাবে পূর্ণ কর যাতে ইলেক্ট্রোডগুলো নিমজ্জিত থাকে। জলে কয়েক ফোঁটা লঘু সালফিউরিক অ্যাসিড যোগ কর।
- জলপূর্ণ দুটি টেস্ট টিউব নাও এবং সেগুলো দুটি কার্বন ইলেক্ট্রোডের উপর উল্টো করে রাখ।
- বিদ্যুৎ চালু কর এবং যন্ত্রপাতিটিকে কিছু সময়ের জন্য অপরিবর্তিত রাখ।
- তুমি উভয় ইলেক্ট্রোডে বুদবুদ গঠন লক্ষ্য করবে। এই বুদবুদগুলো টেস্ট টিউবগুলির জলকে স্থানচ্যুত করে।
- উভয় টেস্ট টিউবে সংগ্রহিত গ্যাসের আয়তন কি একই?
- একবার টেস্ট টিউবগুলো সংশ্লিষ্ট গ্যাসে পূর্ণ হলে, সেগুলো সাবধানে সরিয়ে নাও।
- একটি জ্বলন্ত মোমবাতি টেস্ট টিউবগুলোর মুখের কাছে এনে এই গ্যাসগুলো একে একে পরীক্ষা কর।
সতর্কতা: এই ধাপটি অবশ্যই শিক্ষক দ্বারা সাবধানে সম্পাদন করতে হবে।
- প্রতিটি ক্ষেত্রে কী ঘটে?
- প্রতিটি টেস্ট টিউবে কোন গ্যাস উপস্থিত?
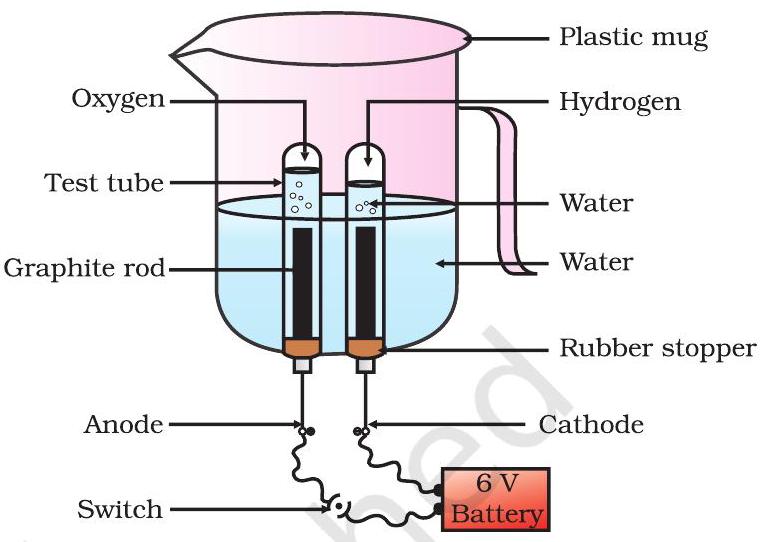
চিত্র ১.৬ জলের তড়িৎ-বিশ্লেষণ
কার্যকলাপ ১.৮
- একটি চায়না ডিশে প্রায় $2 g$ সিলভার ক্লোরাইড নাও।
- এর বর্ণ কী?
- এই চায়না ডিশটিকে কিছু সময়ের জন্য সূর্যালোকে রাখ (চিত্র ১.৭)।
- কিছু সময় পর সিলভার ক্লোরাইডের বর্ণ পর্যবেক্ষণ কর।
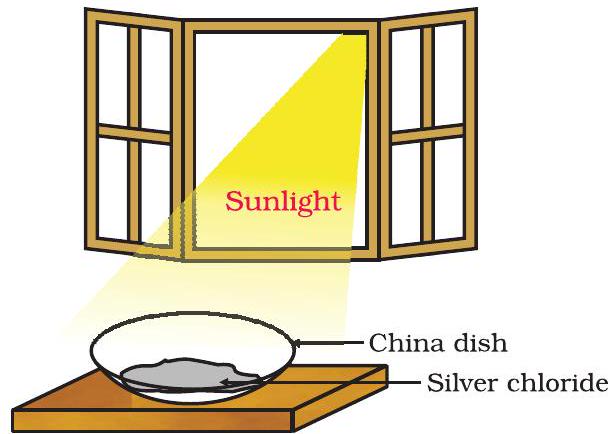
চিত্র ১.৭ সূর্যালোকে সিলভার ক্লোরাইড ধূসর হয়ে সিলভার ধাতু গঠন করে।
তুমি দেখবে যে সাদা সিলভার ক্লোরাইড সূর্যালোকে ধূসর হয়ে যায়। এটি আলোর দ্বারা সিলভার ক্লোরাইডের সিলভার ও ক্লোরিনে বিয়োজনের কারণে ঘটে।
$ \mathrm{2 AgCl(s) \xrightarrow{\text{ সূর্যালোক }} 2 Ag(s)+Cl_2(g)} \quad (1.22) $
সিলভার ব্রোমাইডও একইভাবে আচরণ করে।
$\mathrm{2 AgBr(s) \xrightarrow{\text{ Sunlight }} 2 Ag(s)+Br_2(g)} \quad (1.23)$
উপরের বিক্রিয়াগুলো সাদাকালো ফটোগ্রাফিতে ব্যবহৃত হয়। কোন ধরনের শক্তি এই বিয়োজন বিক্রিয়াগুলো ঘটাচ্ছে?
আমরা দেখেছি যে বিয়োজন বিক্রিয়াগুলোর জন্য বিক্রিয়কগুলো ভাঙতে তাপ, আলো বা বিদ্যুতের আকারে শক্তির প্রয়োজন হয়। যে বিক্রিয়াগুলোতে শক্তি শোষিত হয় সেগুলোকে তাপহারী বিক্রিয়া বলে।
নিচের কার্যকলাপটি সম্পাদন কর
একটি টেস্ট টিউবে প্রায় $2 g$ বেরিয়াম হাইড্রোক্সাইড নাও। $1 g$ অ্যামোনিয়াম ক্লোরাইড যোগ কর এবং একটি কাঁচের রড দিয়ে মিশাও। তোমার তালু দিয়ে টেস্ট টিউবের তলদেশ স্পর্শ কর। তুমি কী অনুভব কর? এটি একটি তাপউৎপাদী নাকি তাপহারী বিক্রিয়া?
১.২.৩ অপসারণ বিক্রিয়া
কার্যকলাপ ১.৯
- তিনটি লোহার পেরেক নাও এবং স্যান্ড পেপার দিয়ে ঘষে পরিষ্কার কর।
- (A) ও (B) চিহ্নিত দুটি টেস্ট টিউব নাও। প্রতিটি টেস্ট টিউবে প্রায় $10 mL$ কপার সালফেট দ্রবণ নাও।
- দুটি লোহার পেরেক একটি সুতো দিয়ে বেঁধে টেস্ট টিউব B-এর কপার সালফেট দ্রবণে প্রায় ২০ মিনিটের জন্য সাবধানে নিমজ্জিত কর [চিত্র ১.৮ (ক)]। তুলনা করার জন্য একটি লোহার পেরেক আলাদা রাখ।
- ২০ মিনিট পর, কপার সালফেট দ্রবণ থেকে লোহার পেরেকগুলো বের কর।
- টেস্ট টিউব (A) ও (B)-তে কপার সালফেট দ্রবণের নীল বর্ণের তীব্রতা তুলনা কর [চিত্র ১.৮ (খ)]।
- এছাড়াও, কপার সালফেট দ্রবণে ডোবানো লোহার পেরেকগুলোর বর্ণ আলাদা রাখা পেরেকটির সাথে তুলনা কর [চিত্র ১.৮ (খ)]।
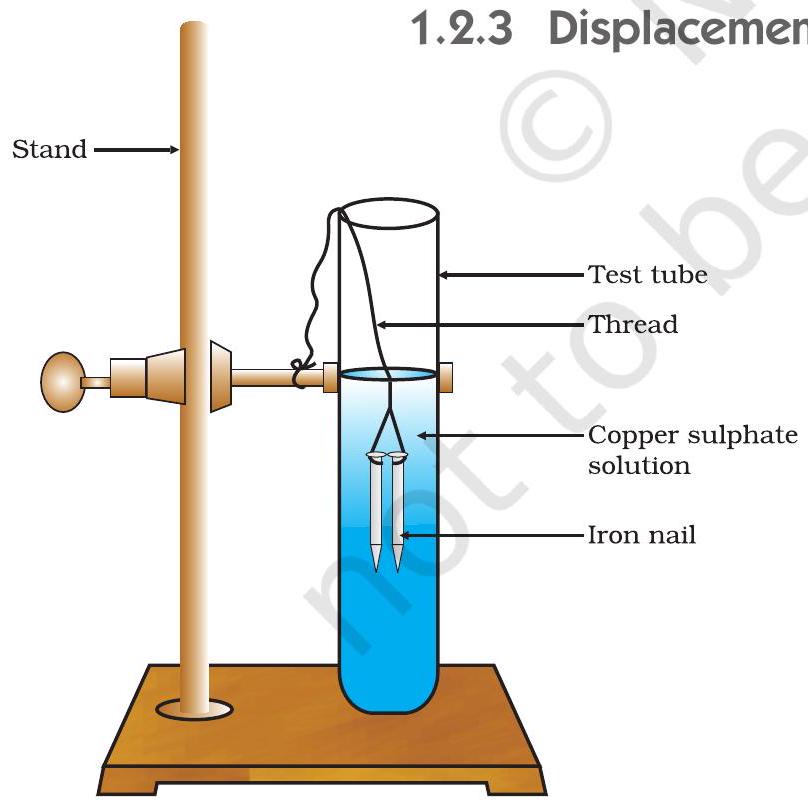
চিত্র ১.৮ (ক) কপার সালফেট দ্রবণে ডোবানো লোহার পেরেক
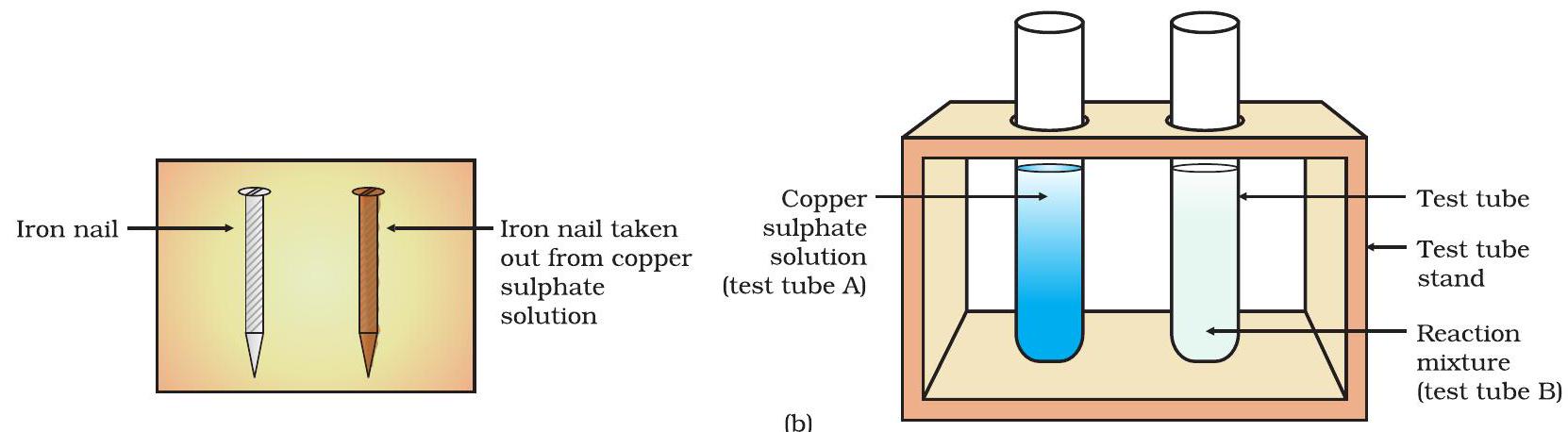
চিত্র ১.৮ (খ) পরীক্ষার আগে ও পরে লোহার পেরেক ও কপার সালফেট দ্রবণের তুলনা
লোহার পেরেকটি বাদামি বর্ণের হয়ে যায় এবং কপার সালফেট দ্রবণের নীল বর্ণ ম্লান হয়ে যায় কেন?
এই কার্যকলাপে নিম্নলিখিত রাসায়নিক বিক্রিয়া ঘটে -
$\mathrm{Fe(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Iron sulphate}}{\mathrm{FeSO_4(aq)}}+ \mathrm{Cu(s)} \quad (1.24)$
এই বিক্রিয়ায়, লোহা অন্য একটি মৌল, তামা (কপার), কপার সালফেট দ্রবণ থেকে অপসারিত বা সরিয়ে দিয়েছে। এই বিক্রিয়াটিকে অপসারণ বিক্রিয়া বলে।
অপসারণ বিক্রিয়ার অন্যান্য উদাহরণ হল
$\mathrm{Zn(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Zinc sulphate}}{\mathrm{PbCl_2(aq)}}+ \mathrm{Cu(s)}\quad (1.25)$
$\mathrm{Pb(s)}+\underset{\text{(Copper chloride)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Lead sulphate}}{\mathrm{FeSO_4(aq)}}+ \mathrm{Cu(s)}\quad (1.26)$
দস্তা ও সীসা তামার চেয়ে বেশি সক্রিয় মৌল। তারা তাদের যৌগ থেকে তামাকে অপসারিত করে।
১.২.৪ দ্বি-অপসারণ বিক্রিয়া
কার্যকলাপ ১.১০
- একটি টেস্ট টিউবে প্রায় $3 mL$ সোডিয়াম সালফেট দ্রবণ নাও।
- অন্য একটি টেস্ট টিউবে প্রায় $3 mL$ বেরিয়াম ক্লোরাইড দ্রবণ নাও।
- দুটি দ্রবণ মিশাও (চিত্র ১.৯)।
- তুমি কী লক্ষ্য কর?
তুমি লক্ষ্য করবে যে একটি সাদা পদার্থ, যা জলে অদ্রবণীয়, গঠিত হয়। এই অদ্রবণীয় পদার্থটিকে অধঃক্ষেপ বলে। যে কোনো বিক্রিয়া যা একটি অধঃক্ষেপ উৎপন্ন করে তাকে অধঃক্ষেপণ বিক্রিয়া বলা যেতে পারে।
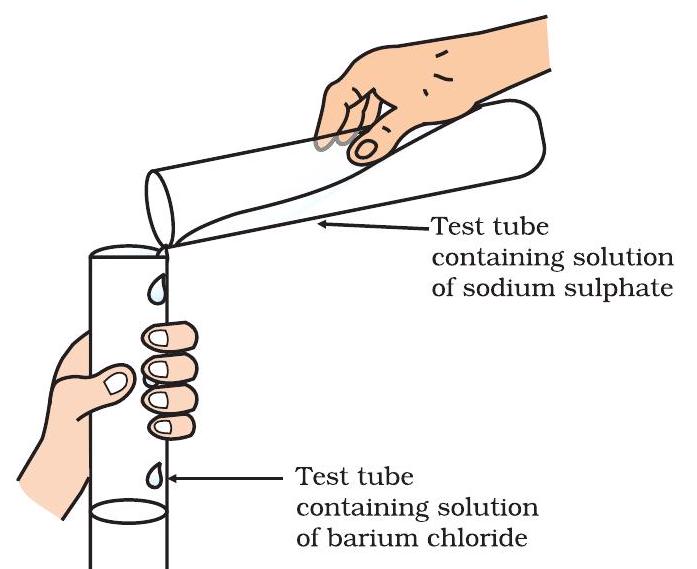
চিত্র ১.৯ বেরিয়াম সালফেট ও সোডিয়াম ক্লোরাইড গঠন
$ \underset{\text{(Sodium sulphate)}}{\mathrm{Na_2SO_4(aq)}}+\underset{\text{(Barium chloride)}}{\mathrm{BaCl_2(aq)}} \rightarrow \underset{\text{(Barium sulphate)}}{\mathrm{BaSO_4(s)}}+ \underset{\text{(Sodium chloride)}}{\mathrm{2NaCl(aq)}} \quad (1.27)$
এর কারণ কী? $BaSO_4$-এর সাদা অধঃক্ষেপটি $SO_4^{2-}$ ও $Ba^{2+}$-এর বিক্রিয়ায় গঠিত হয়। গঠিত অন্য উৎপাদটি হল সোডিয়াম ক্লোরাইড যা দ্রবণে থেকে যায়। এমন বিক্রিয়াগুল











