ਅਧਿਆਇ 01 ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਅਤੇ ਸਮੀਕਰਨ
ਰੋਜ਼ਾਨਾ ਜ਼ਿੰਦਗੀ ਦੀਆਂ ਹੇਠ ਲਿਖੀਆਂ ਸਥਿਤੀਆਂ ਬਾਰੇ ਸੋਚੋ ਅਤੇ ਵਿਚਾਰ ਕਰੋ ਕਿ ਕੀ ਹੁੰਦਾ ਹੈ ਜਦ -
- ਦੁੱਧ ਗਰਮੀਆਂ ਵਿੱਚ ਕਮਰੇ ਦੇ ਤਾਪਮਾਨ ‘ਤੇ ਛੱਡ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ।
- ਇੱਕ ਲੋਹੇ ਦਾ ਤਵਾ/ਪੈਨ/ਕੀਲਾ ਨਮੀ ਵਾਲੇ ਵਾਤਾਵਰਣ ਵਿੱਚ ਖੁੱਲ੍ਹਾ ਛੱਡ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ।
- ਅੰਗੂਰ ਖਮੀਰ ਹੋ ਜਾਂਦੇ ਹਨ।
- ਭੋਜਨ ਪਕਾਇਆ ਜਾਂਦਾ ਹੈ।
- ਭੋਜਨ ਸਾਡੇ ਸਰੀਰ ਵਿੱਚ ਪਚ ਜਾਂਦਾ ਹੈ।
- ਅਸੀਂ ਸਾਹ ਲੈਂਦੇ ਹਾਂ।
ਉੱਪਰ ਦਿੱਤੀਆਂ ਸਾਰੀਆਂ ਸਥਿਤੀਆਂ ਵਿੱਚ, ਸ਼ੁਰੂਆਤੀ ਪਦਾਰਥ ਦੀ ਪ੍ਰਕਿਰਤੀ ਅਤੇ ਪਛਾਣ ਕੁਝ ਹੱਦ ਤੱਕ ਬਦਲ ਗਈ ਹੈ। ਅਸੀਂ ਪਹਿਲਾਂ ਹੀ ਆਪਣੀਆਂ ਪਿਛਲੀਆਂ ਕਲਾਸਾਂ ਵਿੱਚ ਪਦਾਰਥ ਦੇ ਭੌਤਿਕ ਅਤੇ ਰਸਾਇਣਕ ਪਰਿਵਰਤਨਾਂ ਬਾਰੇ ਸਿੱਖ ਚੁੱਕੇ ਹਾਂ। ਜਦੋਂ ਵੀ ਇੱਕ ਰਸਾਇਣਕ ਪਰਿਵਰਤਨ ਹੁੰਦਾ ਹੈ, ਅਸੀਂ ਕਹਿ ਸਕਦੇ ਹਾਂ ਕਿ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਹੋਈ ਹੈ।
ਤੁਸੀਂ ਸ਼ਾਇਦ ਇਹ ਸੋਚ ਰਹੇ ਹੋਵੋਗੇ ਕਿ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਦਾ ਅਸਲ ਵਿੱਚ ਕੀ ਮਤਲਬ ਹੈ। ਅਸੀਂ ਕਿਵੇਂ ਜਾਣ ਸਕਦੇ ਹਾਂ ਕਿ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਹੋਈ ਹੈ? ਆਓ ਇਨ੍ਹਾਂ ਸਵਾਲਾਂ ਦਾ ਜਵਾਬ ਲੱਭਣ ਲਈ ਕੁਝ ਗਤੀਵਿਧੀਆਂ ਕਰੀਏ।
ਗਤੀਵਿਧੀ 1.1
ਸਾਵਧਾਨੀ: ਇਸ ਗਤੀਵਿਧੀ ਲਈ ਅਧਿਆਪਕ ਦੀ ਸਹਾਇਤਾ ਦੀ ਲੋੜ ਹੈ। ਇਹ ਬਿਹਤਰ ਹੋਵੇਗਾ ਜੇ ਵਿਦਿਆਰਥੀ ਢੁਕਵੇਂ ਐਨਕ ਪਹਿਨਣ।
- ਇੱਕ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਲਗਭਗ 3-4 ਸੈਂਟੀਮੀਟਰ ਲੰਬਾ ਸੈਂਡਪੇਪਰ ਨਾਲ ਰਗੜ ਕੇ ਸਾਫ਼ ਕਰੋ।
- ਇਸਨੂੰ ਚਿਮਟੀ ਨਾਲ ਫੜੋ। ਇਸਨੂੰ ਸਪਿਰਿਟ ਲੈਂਪ ਜਾਂ ਬਰਨਰ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਜਲਾਓ ਅਤੇ ਬਣੇ ਰਾਖ ਨੂੰ ਫਿੱਗ. 1.1 ਵਿੱਚ ਦਿਖਾਏ ਅਨੁਸਾਰ ਇੱਕ ਵਾਚ-ਗਲਾਸ ਵਿੱਚ ਇਕੱਠਾ ਕਰੋ। ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਜਲਾਉਂਦੇ ਸਮੇਂ ਇਸਨੂੰ ਆਪਣੀਆਂ ਅੱਖਾਂ ਤੋਂ ਜਿੰਨਾ ਦੂਰ ਸੰਭਵ ਹੋ ਸਕੇ ਰੱਖੋ।
- ਤੁਸੀਂ ਕੀ ਦੇਖਦੇ ਹੋ?
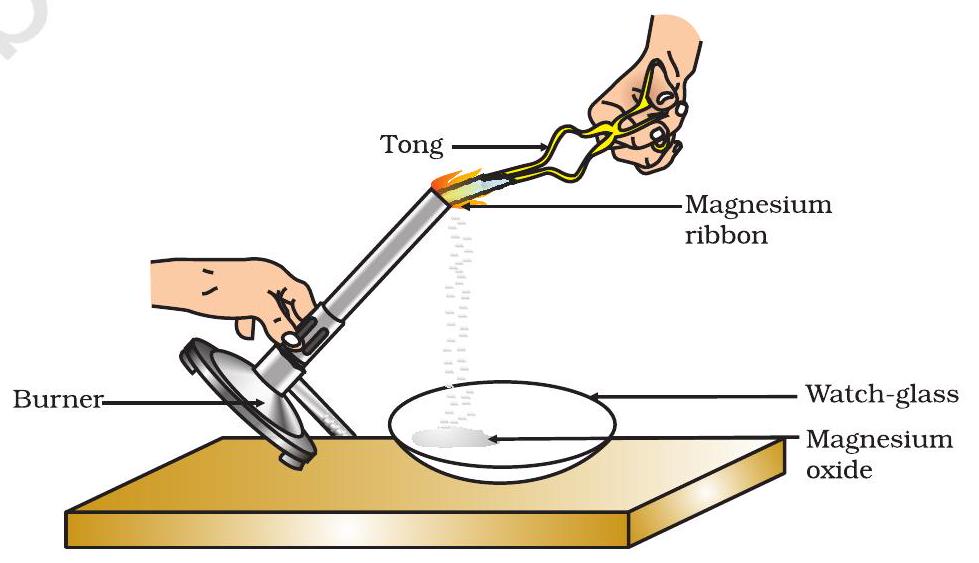
ਚਿੱਤਰ 1.1
ਹਵਾ ਵਿੱਚ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਦਾ ਜਲਣਾ ਅਤੇ ਵਾਚ-ਗਲਾਸ ਵਿੱਚ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਦਾ ਇਕੱਠਾ ਕਰਨਾ
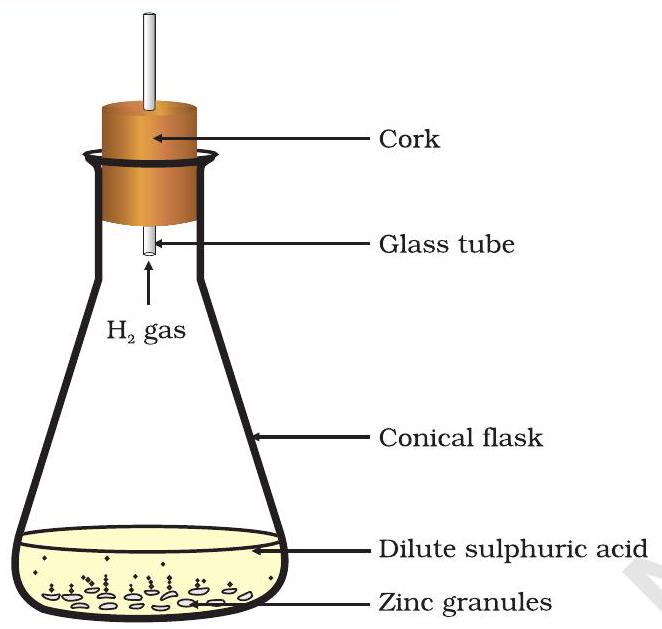
ਚਿੱਤਰ 1.2 ਜ਼ਿੰਕ ‘ਤੇ ਪਤਲੇ ਸਲਫਿਊਰਿਕ ਐਸਿਡ ਦੀ ਕਿਰਿਆ ਦੁਆਰਾ ਹਾਈਡ੍ਰੋਜਨ ਗੈਸ ਦਾ ਬਣਨਾ
ਤੁਸੀਂ ਜ਼ਰੂਰ ਦੇਖਿਆ ਹੋਵੇਗਾ ਕਿ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਇੱਕ ਚਮਕਦਾਰ ਚਿੱਟੀ ਲਾਟ ਨਾਲ ਜਲਦੀ ਹੈ ਅਤੇ ਇੱਕ ਚਿੱਟੇ ਪਾਊਡਰ ਵਿੱਚ ਬਦਲ ਜਾਂਦੀ ਹੈ। ਇਹ ਪਾਊਡਰ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਹੈ। ਇਹ ਹਵਾ ਵਿੱਚ ਮੌਜੂਦ ਮੈਗਨੀਸ਼ੀਅਮ ਅਤੇ ਆਕਸੀਜਨ ਦੇ ਵਿਚਕਾਰ ਪ੍ਰਤੀਕਿਰਿਆ ਕਾਰਨ ਬਣਦਾ ਹੈ।
ਗਤੀਵਿਧੀ 1.2
- ਇੱਕ ਟੈਸਟ ਟਿਊਬ ਵਿੱਚ ਲੈਡ ਨਾਈਟ੍ਰੇਟ ਦਾ ਘੋਲ ਲਓ।
- ਇਸ ਵਿੱਚ ਪੋਟਾਸ਼ੀਅਮ ਆਇਓਡਾਈਡ ਦਾ ਘੋਲ ਮਿਲਾਓ।
- ਤੁਸੀਂ ਕੀ ਦੇਖਦੇ ਹੋ?
ਗਤੀਵਿਧੀ 1.3
- ਇੱਕ ਸ਼ੰਕੂਦਾਰ ਫਲਾਸਕ ਜਾਂ ਟੈਸਟ ਟਿਊਬ ਵਿੱਚ ਕੁਝ ਜ਼ਿੰਕ ਦੇ ਦਾਣੇ ਲਓ।
- ਇਸ ਵਿੱਚ ਪਤਲਾ ਹਾਈਡ੍ਰੋਕਲੋਰਿਕ ਐਸਿਡ ਜਾਂ ਸਲਫਿਊਰਿਕ ਐਸਿਡ ਮਿਲਾਓ (ਫਿੱਗ. 1.2)।
ਸਾਵਧਾਨੀ: ਐਸਿਡ ਨੂੰ ਸਾਵਧਾਨੀ ਨਾਲ ਹੈਂਡਲ ਕਰੋ।
- ਕੀ ਤੁਸੀਂ ਜ਼ਿੰਕ ਦੇ ਦਾਣਿਆਂ ਦੇ ਆਸ-ਪਾਸ ਕੁਝ ਹੋਣ ਦਾ ਨਿਰੀਖਣ ਕਰਦੇ ਹੋ?
- ਸ਼ੰਕੂਦਾਰ ਫਲਾਸਕ ਜਾਂ ਟੈਸਟ ਟਿਊਬ ਨੂੰ ਛੂਹੋ। ਕੀ ਇਸਦੇ ਤਾਪਮਾਨ ਵਿੱਚ ਕੋਈ ਬਦਲਾਅ ਆਇਆ ਹੈ?
ਉੱਪਰ ਦਿੱਤੀਆਂ ਤਿੰਨ ਗਤੀਵਿਧੀਆਂ ਤੋਂ, ਅਸੀਂ ਕਹਿ ਸਕਦੇ ਹਾਂ ਕਿ ਹੇਠ ਲਿਖੀਆਂ ਨਿਰੀਖਣਾਂ ਵਿੱਚੋਂ ਕੋਈ ਵੀ ਸਾਡੀ ਮਦਦ ਕਰਦੀ ਹੈ ਇਹ ਨਿਰਧਾਰਤ ਕਰਨ ਲਈ ਕਿ ਕੀ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਹੋਈ ਹੈ -
- ਅਵਸਥਾ ਵਿੱਚ ਬਦਲਾਅ
- ਰੰਗ ਵਿੱਚ ਬਦਲਾਅ
- ਗੈਸ ਦਾ ਨਿਕਾਸ
- ਤਾਪਮਾਨ ਵਿੱਚ ਬਦਲਾਅ।
ਜਿਵੇਂ ਅਸੀਂ ਆਪਣੇ ਆਸ-ਪਾਸ ਹੋਣ ਵਾਲੇ ਬਦਲਾਵਾਂ ਦਾ ਨਿਰੀਖਣ ਕਰਦੇ ਹਾਂ, ਅਸੀਂ ਦੇਖ ਸਕਦੇ ਹਾਂ ਕਿ ਸਾਡੇ ਆਸ-ਪਾਸ ਬਹੁਤ ਸਾਰੀਆਂ ਕਿਸਮਾਂ ਦੀਆਂ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਹੋ ਰਹੀਆਂ ਹਨ। ਅਸੀਂ ਇਸ ਅਧਿਆਇ ਵਿੱਚ ਵੱਖ-ਵੱਖ ਕਿਸਮਾਂ ਦੀਆਂ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਅਤੇ ਉਹਨਾਂ ਦੇ ਪ੍ਰਤੀਕ ਚਿੰਨ੍ਹਾਂ ਬਾਰੇ ਅਧਿਐਨ ਕਰਾਂਗੇ।
1.1 ਰਸਾਇਣਕ ਸਮੀਕਰਨ
ਗਤੀਵਿਧੀ 1.1 ਨੂੰ ਇਸ ਤਰ੍ਹਾਂ ਵਰਣਨ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ - ਜਦੋਂ ਇੱਕ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਆਕਸੀਜਨ ਵਿੱਚ ਜਲਾਇਆ ਜਾਂਦਾ ਹੈ, ਤਾਂ ਇਹ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਵਿੱਚ ਬਦਲ ਜਾਂਦੀ ਹੈ। ਇੱਕ ਵਾਕ ਦੇ ਰੂਪ ਵਿੱਚ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਦਾ ਇਹ ਵਰਣਨ ਕਾਫ਼ੀ ਲੰਬਾ ਹੈ। ਇਸਨੂੰ ਇੱਕ ਛੋਟੇ ਰੂਪ ਵਿੱਚ ਲਿਖਿਆ ਜਾ ਸਕਦਾ ਹੈ। ਇਸ ਨੂੰ ਕਰਨ ਦਾ ਸਭ ਤੋਂ ਸੌਖਾ ਤਰੀਕਾ ਇਸਨੂੰ ਇੱਕ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਦੇ ਰੂਪ ਵਿੱਚ ਲਿਖਣਾ ਹੈ। ਉੱਪਰ ਦਿੱਤੀ ਪ੍ਰਤੀਕਿਰਿਆ ਲਈ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਹੋਵੇਗਾ -
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
ਉਹ ਪਦਾਰਥ ਜੋ ਪ੍ਰਤੀਕਿਰਿਆ (1.1) ਵਿੱਚ ਰਸਾਇਣਕ ਪਰਿਵਰਤਨ ਦੇ ਅਧੀਨ ਹੁੰਦੇ ਹਨ, ਮੈਗਨੀਸ਼ੀਅਮ ਅਤੇ ਆਕਸੀਜਨ, ਪ੍ਰਤੀਕਿਰਿਅਕ ਹਨ। ਨਵਾਂ ਪਦਾਰਥ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਹੈ, ਜੋ ਪ੍ਰਤੀਕਿਰਿਆ ਦੇ ਦੌਰਾਨ, ਇੱਕ ਉਤਪਾਦ ਵਜੋਂ ਬਣਦਾ ਹੈ।
ਇੱਕ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਤੋਂ ਉਤਪਾਦਾਂ ਵਿੱਚ ਤੀਰ ਦੁਆਰਾ ਪਰਿਵਰਤਨ ਦਰਸਾਉਂਦਾ ਹੈ ਜੋ ਉਹਨਾਂ ਦੇ ਵਿਚਕਾਰ ਰੱਖਿਆ ਜਾਂਦਾ ਹੈ। ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਨੂੰ ਖੱਬੇ ਪਾਸੇ (LHS) ਲਿਖਿਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਉਹਨਾਂ ਦੇ ਵਿਚਕਾਰ ਇੱਕ ਜੋੜ ਚਿੰਨ੍ਹ (+) ਹੁੰਦਾ ਹੈ। ਇਸੇ ਤਰ੍ਹਾਂ, ਉਤਪਾਦਾਂ ਨੂੰ ਸੱਜੇ ਪਾਸੇ (RHS) ਲਿਖਿਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਉਹਨਾਂ ਦੇ ਵਿਚਕਾਰ ਇੱਕ ਜੋੜ ਚਿੰਨ੍ਹ (+) ਹੁੰਦਾ ਹੈ। ਤੀਰ ਦਾ ਸਿਰਾ ਉਤਪਾਦਾਂ ਵੱਲ ਇਸ਼ਾਰਾ ਕਰਦਾ ਹੈ, ਅਤੇ ਪ੍ਰਤੀਕਿਰਿਆ ਦੀ ਦਿਸ਼ਾ ਦਰਸਾਉਂਦਾ ਹੈ।
1.1.1 ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਲਿਖਣਾ
ਕੀ ਰਸਾਇਣਕ ਸਮੀਕਰਨਾਂ ਨੂੰ ਦਰਸਾਉਣ ਲਈ ਕੋਈ ਹੋਰ ਛੋਟਾ ਤਰੀਕਾ ਹੈ? ਰਸਾਇਣਕ ਸਮੀਕਰਨਾਂ ਨੂੰ ਹੋਰ ਸੰਖੇਪ ਅਤੇ ਉਪਯੋਗੀ ਬਣਾਇਆ ਜਾ ਸਕਦਾ ਹੈ ਜੇਕਰ ਅਸੀਂ ਸ਼ਬਦਾਂ ਦੀ ਬਜਾਏ ਰਸਾਇਣਕ ਸੂਤਰਾਂ ਦੀ ਵਰਤੋਂ ਕਰੀਏ। ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਨੂੰ ਦਰਸਾਉਂਦਾ ਹੈ। ਜੇਕਰ ਤੁਸੀਂ ਮੈਗਨੀਸ਼ੀਅਮ, ਆਕਸੀਜਨ ਅਤੇ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਦੇ ਸੂਤਰ ਯਾਦ ਕਰਦੇ ਹੋ, ਤਾਂ ਉੱਪਰ ਦਿੱਤਾ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਇਸ ਤਰ੍ਹਾਂ ਲਿਖਿਆ ਜਾ ਸਕਦਾ ਹੈ -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
ਤੀਰ ਦੇ LHS ਅਤੇ RHS ‘ਤੇ ਹਰੇਕ ਤੱਤ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਕਰੋ ਅਤੇ ਤੁਲਨਾ ਕਰੋ। ਕੀ ਹਰੇਕ ਤੱਤ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਇੱਕੋ ਜਿਹੀ ਹੈ? ਜੇਕਰ ਹਾਂ, ਤਾਂ ਸਮੀਕਰਨ ਸੰਤੁਲਿਤ ਹੈ। ਜੇਕਰ ਨਹੀਂ, ਤਾਂ ਸਮੀਕਰਨ ਅਸੰਤੁਲਿਤ ਹੈ ਕਿਉਂਕਿ ਪੁੰਜ ਸਮੀਕਰਨ ਦੇ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਇੱਕੋ ਜਿਹਾ ਨਹੀਂ ਹੈ। ਅਜਿਹਾ ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਇੱਕ ਪ੍ਰਤੀਕਿਰਿਆ ਲਈ ਇੱਕ ਕੰਕਾਲੀ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਹੈ। ਸਮੀਕਰਨ (1.2) ਹਵਾ ਵਿੱਚ ਮੈਗਨੀਸ਼ੀਅਮ ਦੇ ਜਲਣ ਲਈ ਇੱਕ ਕੰਕਾਲੀ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਹੈ।
1.1.2 ਸੰਤੁਲਿਤ ਰਸਾਇਣਕ ਸਮੀਕਰਨ
ਕਲਾਸ IX ਵਿੱਚ ਤੁਸੀਂ ਪੁੰਜ ਦੇ ਸੁਰੱਖਿਅਣ ਦੇ ਨਿਯਮ ਬਾਰੇ ਪੜ੍ਹਿਆ ਸੀ; ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਪੁੰਜ ਨਾ ਤਾਂ ਬਣਾਇਆ ਜਾ ਸਕਦਾ ਹੈ ਅਤੇ ਨਾ ਹੀ ਨਸ਼ਟ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ। ਭਾਵ, ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਦੇ ਉਤਪਾਦਾਂ ਵਿੱਚ ਮੌਜੂਦ ਤੱਤਾਂ ਦਾ ਕੁੱਲ ਪੁੰਜ ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ ਮੌਜੂਦ ਤੱਤਾਂ ਦੇ ਕੁੱਲ ਪੁੰਜ ਦੇ ਬਰਾਬਰ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ।
ਦੂਜੇ ਸ਼ਬਦਾਂ ਵਿੱਚ, ਹਰੇਕ ਤੱਤ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ, ਇੱਕ ਰਸਾਇਣਕ ਪ੍ਰਤੀਕਿਰਿਆ ਤੋਂ ਪਹਿਲਾਂ ਅਤੇ ਬਾਅਦ ਵਿੱਚ, ਇੱਕੋ ਜਿਹੀ ਰਹਿੰਦੀ ਹੈ। ਇਸ ਲਈ, ਸਾਨੂੰ ਇੱਕ ਕੰਕਾਲੀ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਦੀ ਲੋੜ ਹੈ। ਕੀ ਰਸਾਇਣਕ ਸਮੀਕਰਨ (1.2) ਸੰਤੁਲਿਤ ਹੈ? ਆਓ ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਨੂੰ ਕਦਮ-ਦਰ-ਕਦਮ ਸੰਤੁਲਿਤ ਕਰਨ ਬਾਰੇ ਸਿੱਖੀਏ।
ਗਤੀਵਿਧੀ 1.3 ਲਈ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਨੂੰ ਇਸ ਤਰ੍ਹਾਂ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
ਉੱਪਰ ਦਿੱਤੇ ਸ਼ਬਦ-ਸਮੀਕਰਨ ਨੂੰ ਹੇਠ ਲਿਖੇ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਦੁਆਰਾ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
ਆਓ ਤੀਰ ਦੇ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਵੱਖ-ਵੱਖ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਦੀ ਜਾਂਚ ਕਰੀਏ।
| ਤੱਤ | ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ (LHS) | ਉਤਪਾਦਾਂ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
ਕਿਉਂਕਿ ਹਰੇਕ ਤੱਤ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਤੀਰ ਦੇ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਇੱਕੋ ਜਿਹੀ ਹੈ, ਸਮੀਕਰਨ (1.3) ਇੱਕ ਸੰਤੁਲਿਤ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਹੈ।
ਆਓ ਹੇਠ ਲਿਖੇ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਦੀ ਕੋਸ਼ਿਸ਼ ਕਰੀਏ -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
ਕਦਮ I: ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ, ਪਹਿਲਾਂ ਹਰੇਕ ਸੂਤਰ ਦੇ ਦੁਆਲੇ ਬਕਸੇ ਖਿੱਚੋ। ਸਮੀਕਰਨ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਦੇ ਸਮੇਂ ਬਕਸਿਆਂ ਦੇ ਅੰਦਰ ਕੁਝ ਵੀ ਨਾ ਬਦਲੋ।
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
ਕਦਮ II: ਅਸੰਤੁਲਿਤ ਸਮੀਕਰਨ (1.5) ਵਿੱਚ ਮੌਜੂਦ ਵੱਖ-ਵੱਖ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਸੂਚੀ ਬਣਾਓ।
| ਤੱਤ | ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ (LHS) | ਉਤਪਾਦਾਂ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
ਕਦਮ III: ਅਕਸਰ ਸੰਤੁਲਿਤ ਕਰਨਾ ਉਸ ਸੰਯੋਜਨ ਨਾਲ ਸ਼ੁਰੂ ਕਰਨਾ ਸੁਵਿਧਾਜਨਕ ਹੁੰਦਾ ਹੈ ਜਿਸ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਅਧਿਕਤਮ ਗਿਣਤੀ ਹੁੰਦੀ ਹੈ। ਇਹ ਇੱਕ ਪ੍ਰਤੀਕਿਰਿਅਕ ਜਾਂ ਉਤਪਾਦ ਹੋ ਸਕਦਾ ਹੈ। ਉਸ ਸੰਯੋਜਨ ਵਿੱਚ, ਉਸ ਤੱਤ ਨੂੰ ਚੁਣੋ ਜਿਸ ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਦੀ ਅਧਿਕਤਮ ਗਿਣਤੀ ਹੈ। ਇਹਨਾਂ ਮਾਪਦੰਡਾਂ ਦੀ ਵਰਤੋਂ ਕਰਦੇ ਹੋਏ, ਅਸੀਂ $Fe_3 O_4$ ਅਤੇ ਇਸ ਵਿੱਚ ਆਕਸੀਜਨ ਤੱਤ ਨੂੰ ਚੁਣਦੇ ਹਾਂ। RHS ‘ਤੇ ਚਾਰ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਹਨ ਅਤੇ LHS ‘ਤੇ ਸਿਰਫ਼ ਇੱਕ ਹੈ।
ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ -
| ਆਕਸੀਜਨ ਦੇ ਪਰਮਾਣੂ |
ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ | ਉਤਪਾਦਾਂ ਵਿੱਚ |
|---|---|---|
| (i) ਸ਼ੁਰੂਆਤੀ | 1($ \mathrm{H_2O} $ ਵਿੱਚ) | 4($ \mathrm{Fe_3O_4} $ ਵਿੱਚ) |
| (ii) ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ | 1 $\times$ 4 | 4 |
ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਨੂੰ ਬਰਾਬਰ ਕਰਨ ਲਈ, ਇਹ ਯਾਦ ਰੱਖਣਾ ਚਾਹੀਦਾ ਹੈ ਕਿ ਅਸੀਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਵਿੱਚ ਸ਼ਾਮਲ ਸੰਯੋਜਨਾਂ ਜਾਂ ਤੱਤਾਂ ਦੇ ਸੂਤਰਾਂ ਨੂੰ ਨਹੀਂ ਬਦਲ ਸਕਦੇ। ਉਦਾਹਰਨ ਲਈ, ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ ਅਸੀਂ ਗੁਣਾਂਕ ‘4’ $4 H_2 O$ ਵਜੋਂ ਰੱਖ ਸਕਦੇ ਹਾਂ ਨਾ ਕਿ $H_2 O_4$ ਜਾਂ $(H_2 O)_4$ ਵਜੋਂ। ਹੁਣ ਅੰਸ਼ਕ ਰੂਪ ਵਿੱਚ ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ ਬਣ ਜਾਂਦਾ ਹੈ -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (ਅੰਸ਼ਕ ਰੂਪ ਵਿੱਚ ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ)
ਕਦਮ IV: Fe ਅਤੇ $H$ ਪਰਮਾਣੂ ਅਜੇ ਵੀ ਸੰਤੁਲਿਤ ਨਹੀਂ ਹਨ। ਅੱਗੇ ਵਧਣ ਲਈ ਇਹਨਾਂ ਤੱਤਾਂ ਵਿੱਚੋਂ ਕਿਸੇ ਇੱਕ ਨੂੰ ਚੁਣੋ। ਆਓ ਅੰਸ਼ਕ ਰੂਪ ਵਿੱਚ ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ ਵਿੱਚ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰੀਏ।
$H$ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਨੂੰ ਬਰਾਬਰ ਕਰਨ ਲਈ, RHS ‘ਤੇ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਅਣੂਆਂ ਦੀ ਗਿਣਤੀ ਨੂੰ ਚਾਰ ਬਣਾਓ।
| ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਪਰਮਾਣੂ |
ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ | ਉਤਪਾਦਾਂ ਵਿੱਚ |
|---|---|---|
| (i) ਸ਼ੁਰੂਆਤੀ | 8($ \mathrm{4H_2O} $ ਵਿੱਚ) | 2($ \mathrm{H_2} $ ਵਿੱਚ) |
| (ii) ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ | 8 | 2 $\times$ 4 |
ਸਮੀਕਰਨ ਹੋਵੇਗੀ -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(ਅੰਸ਼ਕ ਰੂਪ ਵਿੱਚ ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ)
ਕਦਮ V: ਉੱਪਰ ਦਿੱਤੇ ਸਮੀਕਰਨ ਦੀ ਜਾਂਚ ਕਰੋ ਅਤੇ ਤੀਜੇ ਤੱਤ ਨੂੰ ਚੁਣੋ ਜੋ ਸੰਤੁਲਿਤ ਨਹੀਂ ਹੈ। ਤੁਸੀਂ ਦੇਖੋਗੇ ਕਿ ਸਿਰਫ਼ ਇੱਕ ਤੱਤ ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ ਬਾਕੀ ਰਹਿ ਗਿਆ ਹੈ, ਭਾਵ, ਲੋਹਾ।
| ਲੋਹੇ ਦੇ ਪਰਮਾਣੂ | ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਵਿੱਚ | ਉਤਪਾਦਾਂ ਵਿੱਚ |
|---|---|---|
| (i) ਸ਼ੁਰੂਆਤੀ | 1($ \mathrm{Fe} $ ਵਿੱਚ) | 3($ \mathrm{Fe_3O_4} $ ਵਿੱਚ) |
| (ii) ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ | 1 $\times$ 3 | 3 |
$Fe$ ਨੂੰ ਬਰਾਬਰ ਕਰਨ ਲਈ, ਅਸੀਂ LHS ‘ਤੇ $Fe$ ਦੇ ਤਿੰਨ ਪਰਮਾਣੂ ਲੈਂਦੇ ਹਾਂ।
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
ਕਦਮ VI: ਅੰਤ ਵਿੱਚ, ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ ਦੀ ਸ਼ੁੱਧਤਾ ਦੀ ਜਾਂਚ ਕਰਨ ਲਈ, ਅਸੀਂ ਸਮੀਕਰਨ ਦੇ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਹਰੇਕ ਤੱਤ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਕਰਦੇ ਹਾਂ।
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ)
ਸਮੀਕਰਨ (1.9) ਦੇ ਦੋਵੇਂ ਪਾਸਿਆਂ ‘ਤੇ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਬਰਾਬਰ ਹੈ। ਇਹ ਸਮੀਕਰਨ ਹੁਣ ਸੰਤੁਲਿਤ ਹੈ। ਰਸਾਇਣਕ ਸਮੀਕਰਨਾਂ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਦੀ ਇਸ ਵਿਧੀ ਨੂੰ ਹਿੱਟ-ਐਂਡ-ਟ੍ਰਾਇਲ ਵਿਧੀ ਕਿਹਾ ਜਾਂਦਾ ਹੈ ਕਿਉਂਕਿ ਅਸੀਂ ਸਭ ਤੋਂ ਛੋਟੇ ਪੂਰਨ ਅੰਕ ਗੁਣਾਂਕ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਸਮੀਕਰਨ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨ ਲਈ ਕੋਸ਼ਿਸ਼ਾਂ ਕਰਦੇ ਹਾਂ।
ਕਦਮ VII: ਭੌਤਿਕ ਅਵਸਥਾਵਾਂ ਦੇ ਪ੍ਰਤੀਕ ਲਿਖਣਾ ਉੱਪਰ ਦਿੱਤੇ ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ (1.9) ਦੀ ਧਿਆਨ ਨਾਲ ਜਾਂਚ ਕਰੋ। ਕੀ ਇਹ ਸਮੀਕਰਨ ਸਾਨੂੰ ਹਰੇਕ ਪ੍ਰਤੀਕਿਰਿਅਕ ਅਤੇ ਉਤਪਾਦ ਦੀ ਭੌਤਿਕ ਅਵਸਥਾ ਬਾਰੇ ਕੁਝ ਦੱਸਦੀ ਹੈ? ਇਸ ਸਮੀਕਰਨ ਵਿੱਚ ਉਹਨਾਂ ਦੀਆਂ ਭੌਤਿਕ ਅਵਸਥਾਵਾਂ ਬਾਰੇ ਕੋਈ ਜਾਣਕਾਰੀ ਨਹੀਂ ਦਿੱਤੀ ਗਈ ਹੈ।
ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਨੂੰ ਹੋਰ ਜਾਣਕਾਰੀ ਪੂਰਣ ਬਣਾਉਣ ਲਈ, ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਅਤੇ ਉਤਪਾਦਾਂ ਦੀਆਂ ਭੌਤਿਕ ਅਵਸਥਾਵਾਂ ਨੂੰ ਉਹਨਾਂ ਦੇ ਰਸਾਇਣਕ ਸੂਤਰਾਂ ਦੇ ਨਾਲ ਦਰਸਾਇਆ ਜਾਂਦਾ ਹੈ। ਪ੍ਰਤੀਕਿਰਿਅਕਾਂ ਅਤੇ ਉਤਪਾਦਾਂ ਦੀਆਂ ਗੈਸੀ, ਤਰਲ, ਜਲੀ ਅਤੇ ਠੋਸ ਅਵਸਥਾਵਾਂ ਨੂੰ ਕ੍ਰਮਵਾਰ (g), (l), (aq) ਅਤੇ (s) ਨੋਟੇਸ਼ਨਾਂ ਦੁਆਰਾ ਦਰਸਾਇਆ ਜਾਂਦਾ ਹੈ। ਸ਼ਬਦ ਜਲੀ (aq) ਲਿਖਿਆ ਜਾਂਦਾ ਹੈ ਜੇਕਰ ਪ੍ਰਤੀਕਿਰਿਅਕ ਜਾਂ ਉਤਪਾਦ ਪਾਣੀ ਵਿੱਚ ਇੱਕ ਘੋਲ ਦੇ ਰੂਪ ਵਿੱਚ ਮੌਜੂਦ ਹੈ।
ਸੰਤੁਲਿਤ ਸਮੀਕਰਨ (1.9) ਬਣ ਜਾਂਦੀ ਹੈ
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
ਨੋਟ ਕਰੋ ਕਿ ਪ੍ਰਤੀਕ $(g)$ ਨੂੰ $H_2 O$ ਨਾਲ ਵਰਤਿਆ ਜਾਂਦਾ ਹੈ ਤਾਂ ਜੋ ਇਹ ਦਰਸਾਇਆ ਜਾ ਸਕੇ ਕਿ ਇਸ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਪਾਣੀ ਦੀ ਵਰਤੋਂ ਭਾਫ ਦੇ ਰੂਪ ਵਿੱਚ ਕੀਤੀ ਜਾਂਦੀ ਹੈ।
ਆਮ ਤੌਰ ‘ਤੇ ਭੌਤਿਕ ਅਵਸਥਾਵਾਂ ਨੂੰ ਇੱਕ ਰਸਾਇਣਕ ਸਮੀਕਰਨ ਵਿੱਚ ਸ਼ਾਮਲ ਨਹੀਂ ਕੀਤਾ ਜਾਂਦਾ ਜਦੋਂ ਤੱਕ ਉਹਨਾਂ ਨੂੰ ਨਿਰਧਾਰਤ ਕਰਨਾ ਜ਼ਰੂਰੀ ਨਾ ਹੋਵੇ।
ਕਈ ਵਾਰ ਪ੍ਰਤੀਕਿਰਿਆ ਦੀਆਂ ਸ਼ਰਤਾਂ, ਜਿਵੇਂ ਕਿ ਤਾਪਮਾਨ, ਦਬਾਅ, ਉਤਪ੍ਰੇਰਕ, ਆਦਿ, ਸਮੀਕਰ











