अध्याय 01 रासायनिक अभिक्रियाएँ एवं समीकरण
दैनिक जीवन की निम्नलिखित परिस्थितियों पर विचार कीजिए और सोचिए कि क्या होता है जब -
- दूध को गर्मियों में कमरे के तापमान पर छोड़ दिया जाता है।
- एक लोहे की तवा/कड़ाही/कील को आर्द्र वातावरण में खुला छोड़ दिया जाता है।
- अंगूर किण्वित हो जाते हैं।
- भोजन पकाया जाता है।
- भोजन हमारे शरीर में पचता है।
- हम श्वसन करते हैं।
उपरोक्त सभी परिस्थितियों में, प्रारंभिक पदार्थ की प्रकृति और पहचान कुछ हद तक बदल गई है। हमने पहले ही अपनी पिछली कक्षाओं में पदार्थ के भौतिक और रासायनिक परिवर्तनों के बारे में सीखा है। जब भी कोई रासायनिक परिवर्तन होता है, हम कह सकते हैं कि एक रासायनिक अभिक्रिया हुई है।
आप शायद यह सोच रहे होंगे कि वास्तव में रासायनिक अभिक्रिया से क्या तात्पर्य है? हमें कैसे पता चलता है कि कोई रासायनिक अभिक्रिया हुई है? आइए इन प्रश्नों का उत्तर जानने के लिए कुछ क्रियाकलाप करें।
क्रियाकलाप 1.1
सावधानी: इस क्रियाकलाप के लिए शिक्षक की सहायता आवश्यक है। यह बेहतर होगा यदि छात्र उपयुक्त चश्मा पहनें।
- मैग्नीशियम की एक पट्टी (लगभग 3-4 सेमी लंबी) को सैंडपेपर से रगड़कर साफ करें।
- इसे चिमटे से पकड़ें। स्पिरिट लैंप या बर्नर का उपयोग करके इसे जलाएं और बनी राख को वॉच-ग्लास में एकत्र करें जैसा कि चित्र 1.1 में दिखाया गया है। मैग्नीशियम पट्टी को अपनी आँखों से जितना संभव हो उतना दूर रखकर जलाएं।
- आप क्या देखते हैं?
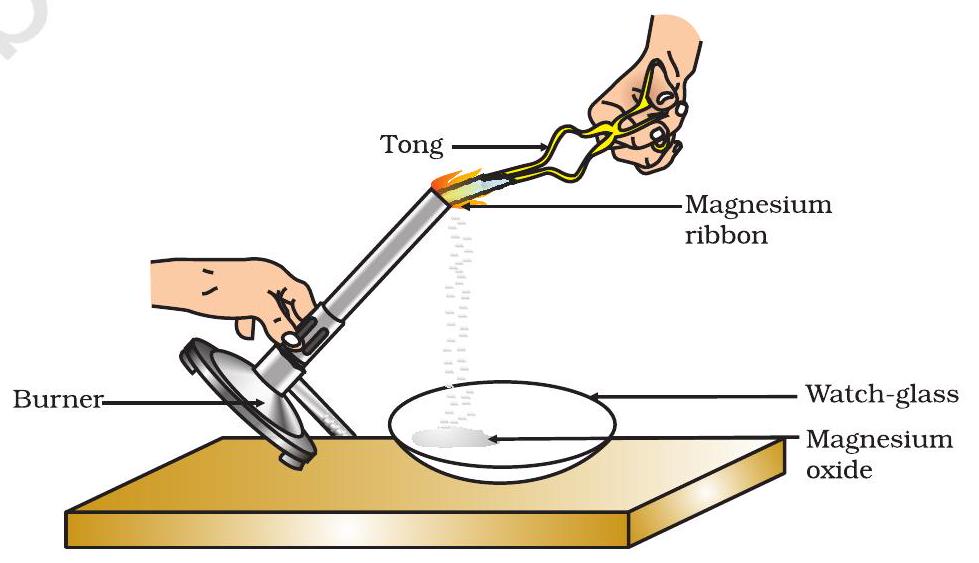
चित्र 1.1
वायु में मैग्नीशियम पट्टी का जलना और वॉच-ग्लास में मैग्नीशियम ऑक्साइड का एकत्रीकरण
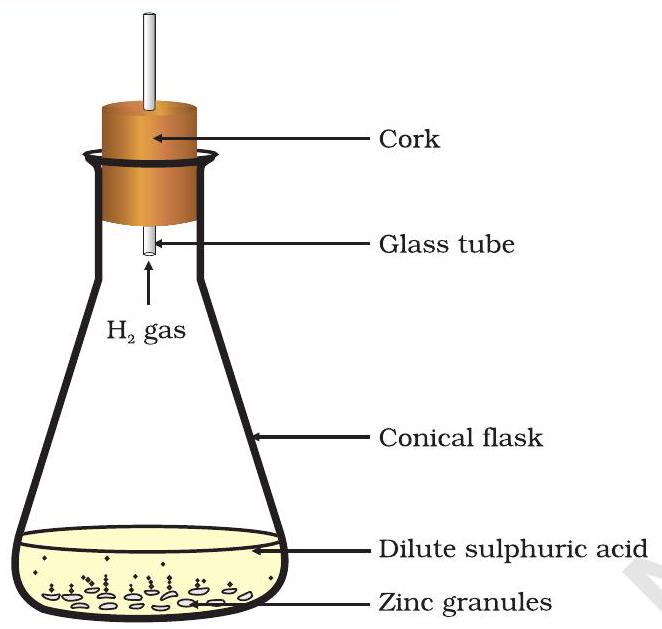
चित्र 1.2 जिंक पर तनु सल्फ्यूरिक अम्ल की क्रिया से हाइड्रोजन गैस का निर्माण
आपने अवश्य देखा होगा कि मैग्नीशियम पट्टी चमकदार सफेद लौ के साथ जलती है और एक सफेद पाउडर में बदल जाती है। यह पाउडर मैग्नीशियम ऑक्साइड है। यह मैग्नीशियम और वायु में उपस्थित ऑक्सीजन के बीच अभिक्रिया के कारण बनता है।
क्रियाकलाप 1.2
- एक परखनली में लेड नाइट्रेट विलयन लें।
- इसमें पोटैशियम आयोडाइड विलयन मिलाएं।
- आप क्या देखते हैं?
क्रियाकलाप 1.3
- एक शंक्वाकार फ्लास्क या परखनली में कुछ जिंक के दाने लें।
- इसमें तनु हाइड्रोक्लोरिक अम्ल या सल्फ्यूरिक अम्ल मिलाएं (चित्र 1.2)।
सावधानी: अम्ल को सावधानी से संभालें।
- क्या आप जिंक के दानों के आसपास कुछ होता हुआ देखते हैं?
- शंक्वाकार फ्लास्क या परखनली को छुएं। क्या इसके तापमान में कोई परिवर्तन है?
उपरोक्त तीनों क्रियाकलापों से, हम कह सकते हैं कि निम्नलिखित में से कोई भी प्रेक्षण हमें यह निर्धारित करने में मदद करता है कि कोई रासायनिक अभिक्रिया हुई है या नहीं –
- अवस्था में परिवर्तन
- रंग में परिवर्तन
- गैस का निकलना
- तापमान में परिवर्तन।
जैसे हम अपने आसपास होने वाले परिवर्तनों का अवलोकन करते हैं, हम देख सकते हैं कि हमारे आसपास विभिन्न प्रकार की रासायनिक अभिक्रियाएँ हो रही हैं। इस अध्याय में हम विभिन्न प्रकार की रासायनिक अभिक्रियाओं और उनके प्रतीकात्मक निरूपण के बारे में अध्ययन करेंगे।
1.1 रासायनिक समीकरण
क्रियाकलाप 1.1 को इस प्रकार वर्णित किया जा सकता है – जब मैग्नीशियम की एक पट्टी को ऑक्सीजन में जलाया जाता है, तो यह मैग्नीशियम ऑक्साइड में परिवर्तित हो जाती है। वाक्य रूप में रासायनिक अभिक्रिया का यह वर्णन काफी लंबा है। इसे छोटे रूप में लिखा जा सकता है। ऐसा करने का सबसे सरल तरीका इसे शब्द-समीकरण के रूप में लिखना है। उपरोक्त अभिक्रिया के लिए शब्द-समीकरण होगा –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
वे पदार्थ जो अभिक्रिया (1.1) में रासायनिक परिवर्तन से गुजरते हैं, मैग्नीशियम और ऑक्सीजन, अभिकारक हैं। नया पदार्थ मैग्नीशियम ऑक्साइड है, जो अभिक्रिया के दौरान उत्पाद के रूप में बनता है।
एक शब्द-समीकरण अभिकारकों से उत्पादों में परिवर्तन को उनके बीच रखे गए तीर के माध्यम से दर्शाता है। अभिकारकों को बाईं ओर (LHS) लिखा जाता है और उनके बीच धन चिह्न (+) लगाया जाता है। इसी प्रकार, उत्पादों को दाईं ओर (RHS) लिखा जाता है और उनके बीच धन चिह्न (+) लगाया जाता है। तीर का सिरा उत्पादों की ओर इशारा करता है, और अभिक्रिया की दिशा दर्शाता है।
1.1.1 रासायनिक समीकरण लिखना
क्या रासायनिक समीकरणों को निरूपित करने का कोई अन्य छोटा तरीका है? रासायनिक समीकरणों को और अधिक संक्षिप्त और उपयोगी बनाया जा सकता है यदि हम शब्दों के स्थान पर रासायनिक सूत्रों का उपयोग करें। एक रासायनिक समीकरण एक रासायनिक अभिक्रिया को निरूपित करता है। यदि आप मैग्नीशियम, ऑक्सीजन और मैग्नीशियम ऑक्साइड के सूत्र याद करते हैं, तो उपरोक्त शब्द-समीकरण को इस प्रकार लिखा जा सकता है -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
तत्वों के परमाणुओं की संख्या की तीर के बाईं ओर (LHS) और दाईं ओर (RHS) गिनती करें और तुलना करें। क्या प्रत्येक तत्व के परमाणुओं की संख्या दोनों ओर समान है? यदि हाँ, तो समीकरण संतुलित है। यदि नहीं, तो समीकरण असंतुलित है क्योंकि द्रव्यमान समीकरण के दोनों ओर समान नहीं है। ऐसा रासायनिक समीकरण एक अभिक्रिया के लिए कंकालीय रासायनिक समीकरण होता है। समीकरण (1.2) वायु में मैग्नीशियम के जलने के लिए एक कंकालीय रासायनिक समीकरण है।
1.1.2 संतुलित रासायनिक समीकरण
कक्षा IX में आपने द्रव्यमान संरक्षण के नियम का अध्ययन किया था; एक रासायनिक अभिक्रिया में न तो द्रव्यमान उत्पन्न किया जा सकता है और न ही नष्ट किया जा सकता है। अर्थात, एक रासायनिक अभिक्रिया के उत्पादों में उपस्थित तत्वों का कुल द्रव्यमान, अभिकारकों में उपस्थित तत्वों के कुल द्रव्यमान के बराबर होना चाहिए।
दूसरे शब्दों में, प्रत्येक तत्व के परमाणुओं की संख्या, रासायनिक अभिक्रिया से पहले और बाद में, समान रहती है। अतः, हमें एक कंकालीय रासायनिक समीकरण को संतुलित करने की आवश्यकता है। क्या रासायनिक समीकरण (1.2) संतुलित है? आइए एक रासायनिक समीकरण को चरणबद्ध तरीके से संतुलित करना सीखें।
क्रियाकलाप 1.3 के लिए शब्द-समीकरण को इस प्रकार निरूपित किया जा सकता है -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
उपरोक्त शब्द-समीकरण को निम्नलिखित रासायनिक समीकरण द्वारा निरूपित किया जा सकता है -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
आइए तीर के दोनों ओर विभिन्न तत्वों के परमाणुओं की संख्या की जाँच करें।
| तत्व | अभिकारकों में परमाणुओं की संख्या (LHS) | उत्पादों में परमाणुओं की संख्या (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
चूँकि प्रत्येक तत्व के परमाणुओं की संख्या तीर के दोनों ओर समान है, समीकरण (1.3) एक संतुलित रासायनिक समीकरण है।
आइए निम्नलिखित रासायनिक समीकरण को संतुलित करने का प्रयास करें -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
चरण I: एक रासायनिक समीकरण को संतुलित करने के लिए, सबसे पहले प्रत्येक सूत्र के चारों ओर बॉक्स बनाएं। समीकरण को संतुलित करते समय बॉक्स के अंदर कुछ भी न बदलें।
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
चरण II: असंतुलित समीकरण (1.5) में उपस्थित विभिन्न तत्वों के परमाणुओं की संख्या सूचीबद्ध करें।
| तत्व | अभिकारकों में परमाणुओं की संख्या (LHS) | उत्पादों में परमाणुओं की संख्या (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
चरण III: अधिकतम परमाणुओं वाले यौगिक से संतुलन शुरू करना अक्सर सुविधाजनक होता है। यह एक अभिकारक या उत्पाद हो सकता है। उस यौगिक में, उस तत्व का चयन करें जिसमें परमाणुओं की संख्या अधिकतम है। इन मानदंडों का उपयोग करते हुए, हम $Fe_3 O_4$ और उसमें ऑक्सीजन तत्व का चयन करते हैं। RHS पर चार ऑक्सीजन परमाणु हैं और LHS पर केवल एक है।
ऑक्सीजन परमाणुओं को संतुलित करने के लिए -
| ऑक्सीजन के परमाणु |
अभिकारकों में | उत्पादों में |
|---|---|---|
| (i) प्रारंभिक | 1($ \mathrm{H_2O} $ में) | 4($ \mathrm{Fe_3O_4} $ में) |
| (ii) संतुलित करने के लिए | 1 $\times$ 4 | 4 |
परमाणुओं की संख्या को बराबर करने के लिए, यह याद रखना चाहिए कि हम अभिक्रिया में शामिल यौगिकों या तत्वों के सूत्रों को नहीं बदल सकते। उदाहरण के लिए, ऑक्सीजन परमाणुओं को संतुलित करने के लिए हम गुणांक ‘4’ को $4 H_2 O$ के रूप में रख सकते हैं न कि $H_2 O_4$ या $(H_2 O)_4$ के रूप में। अब आंशिक रूप से संतुलित समीकरण बन जाता है -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (आंशिक रूप से संतुलित समीकरण)
चरण IV: Fe और $H$ परमाणु अभी भी संतुलित नहीं हैं। आगे बढ़ने के लिए इनमें से किसी भी तत्व को चुनें। आइए आंशिक रूप से संतुलित समीकरण में हाइड्रोजन परमाणुओं को संतुलित करें।
$H$ परमाणुओं की संख्या को बराबर करने के लिए, RHS पर हाइड्रोजन के अणुओं की संख्या चार बनाएं।
| हाइड्रोजन के परमाणु |
अभिकारकों में | उत्पादों में |
|---|---|---|
| (i) प्रारंभिक | 8($ \mathrm{4H_2O} $ में) | 2($ \mathrm{H_2} $ में) |
| (ii) संतुलित करने के लिए | 8 | 2 $\times$ 4 |
समीकरण होगा -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(आंशिक रूप से संतुलित समीकरण)
चरण V: उपरोक्त समीकरण की जाँच करें और तीसरे तत्व को चुनें जो संतुलित नहीं है। आप पाएंगे कि केवल एक तत्व संतुलित करने के लिए शेष है, वह है, आयरन।
| आयरन के परमाणु | अभिकारकों में | उत्पादों में |
|---|---|---|
| (i) प्रारंभिक | 1($ \mathrm{Fe} $ में) | 3($ \mathrm{Fe_3O_4} $ में) |
| (ii) संतुलित करने के लिए | 1 $\times$ 3 | 3 |
$Fe$ को बराबर करने के लिए, हम LHS पर $Fe$ के तीन परमाणु लेते हैं।
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
चरण VI: अंत में, संतुलित समीकरण की शुद्धता की जाँच करने के लिए, हम समीकरण के दोनों ओर प्रत्येक तत्व के परमाणुओं की गिनती करते हैं।
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(संतुलित समीकरण)
समीकरण (1.9) के दोनों ओर तत्वों के परमाणुओं की संख्या बराबर है। यह समीकरण अब संतुलित है। रासायनिक समीकरणों को संतुलित करने की इस विधि को हिट-एंड-ट्रायल विधि कहा जाता है क्योंकि हम सबसे छोटे पूर्णांक गुणांक का उपयोग करके समीकरण को संतुलित करने के लिए प्रयास करते हैं।
चरण VII: भौतिक अवस्थाओं के प्रतीक लिखना उपरोक्त संतुलित समीकरण (1.9) का ध्यानपूर्वक परीक्षण करें। क्या यह समीकरण हमें प्रत्येक अभिकारक और उत्पाद की भौतिक अवस्था के बारे में कुछ बताता है? इस समीकरण में उनकी भौतिक अवस्थाओं के बारे में कोई जानकारी नहीं दी गई है।
एक रासायनिक समीकरण को और अधिक सूचनापूर्ण बनाने के लिए, अभिकारकों और उत्पादों की भौतिक अवस्थाओं को उनके रासायनिक सूत्रों के साथ उल्लेखित किया जाता है। अभिकारकों और उत्पादों की गैसीय, द्रव, जलीय और ठोस अवस्थाओं को क्रमशः संकेतों (g), (l), (aq) और (s) द्वारा निरूपित किया जाता है। शब्द जलीय (aq) लिखा जाता है यदि अभिकारक या उत्पाद जल में विलयन के रूप में उपस्थित है।
संतुलित समीकरण (1.9) बन जाता है
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
ध्यान दें कि प्रतीक $(g)$ का उपयोग $H_2 O$ के साथ किया जाता है यह दर्शाने के लिए कि इस अभिक्रिया में जल का उपयोग भाप के रूप में किया जाता है।
आमतौर पर भौतिक अवस्थाओं को रासायनिक समीकरण में तब तक शामिल नहीं किया जाता जब तक कि उन्हें निर्दिष्ट करना आवश्यक न हो।
कभी-कभी अभिक्रिया की परिस्थितियाँ, जैसे तापमान, दाब, उत्प्रेरक, आदि, समीकरण में तीर के ऊपर और/या नीचे दर्शाई जाती हैं। उदाहरण के लिए -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
इन चरणों का उपयोग करके, क्या आप पाठ में पहले दिए गए समीकरण (1.2) को संतुलित कर सकते हैं?
1.2 रासायनिक अभिक्रियाओं के प्रकार
हमने कक्षा IX में सीखा था कि एक रासायनिक अभिक्रिया के दौरान एक तत्व के परमाणु दूसरे तत्व के परमाणुओं में नहीं बदलते। न ही परमाणु मिश्रण से गायब होते हैं या कहीं और से प्रकट होते हैं। वास्तव में, रासायनिक अभिक्रियाओं में नए पदार्थ उत्पन्न करने के लिए परमाणुओं के बीच बंधनों के टूटने और बनने की प्रक्रिया शामिल होती है। आप अध्याय 3 और 4 में परमाणुओं के बीच बने बंधनों के प्रकारों के बारे में अध्ययन करेंगे।
1.2.1 संयोजन अभिक्रिया
क्रियाकलाप 1.4
- एक बीकर में कैल्शियम ऑक्साइड या बिना बुझा चूना (क्विक लाइम) की थोड़ी मात्रा लें।
- इसमें धीरे-धीरे पानी मिलाएं।
- चित्र 1.3 में दिखाए अनुसार बीकर को छुएं।
- क्या आपको तापमान में कोई परिवर्तन महसूस होता है?
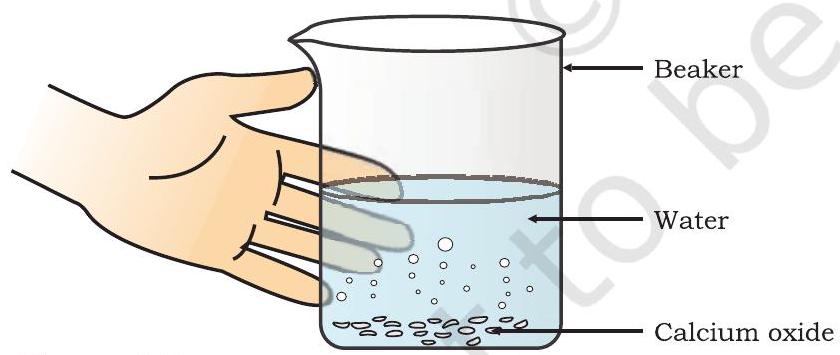
चित्र 1.3 कैल्शियम ऑक्साइड के जल के साथ अभिक्रिया से बुझा हुआ चूना (स्लेक्ड लाइम) बनना
कैल्शियम ऑक्साइड जल के साथ तीव्रता से अभिक्रिया करके बुझा हुआ चूना (कैल्शियम हाइड्रॉक्साइड) उत्पन्न करता है और बड़ी मात्रा में ऊष्मा मुक्त करता है।
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
इस अभिक्रिया में, कैल्शियम ऑक्साइड और जल मिलकर एक ही उत्पाद, कैल्शियम हाइड्रॉक्साइड बनाते हैं। ऐसी अभिक्रिया जिसमें दो या दो से अधिक अभिकारकों से एक ही उत्पाद बनता है, संयोजन अभिक्रिया कहलाती है।
क्या आप जानते हैं?
अभिक्रिया 1.13 द्वारा उत्पन्न बुझे हुए चूने के विलयन का उपयोग दीवारों पर सफेदी करने के लिए किया जाता है। कैल्शियम हाइड्रॉक्साइड वायु में उपस्थित कार्बन डाइऑक्साइड के साथ धीरे-धीरे अभिक्रिया करके दीवारों पर कैल्शियम कार्बोनेट की एक पतली परत बनाता है। कैल्शियम कार्बोनेट सफेदी करने के दो से तीन दिन बाद बनता है और दीवारों को चमकदार खत्म करता है। यह जानना दिलचस्प है कि संगमरमर का रासायनिक सूत्र भी $CaCO_3$ है।
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
आइए संयोजन अभिक्रियाओं के कुछ और उदाहरणों पर चर्चा करें।
(i) कोयले का जलना
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ और $O_2(g)$ से जल का निर्माण
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
सरल भाषा में हम कह सकते हैं कि जब दो या दो से अधिक पदार्थ (तत्व या यौगिक) मिलकर एक ही उत्पाद बनाते हैं, तो अभिक्रियाओं को संयोजन अभिक्रियाएँ कहा जाता है।
क्रियाकलाप 1.4 में, हमने यह भी देखा कि बड़ी मात्रा में ऊष्मा निकलती है। इससे अभिक्रिया मिश्रण गर्म हो जाता है। वे अभिक्रियाएँ जिनमें उत्पादों के निर्माण के साथ-साथ ऊष्मा भी मुक्त होती है, ऊष्माक्षेपी रासायनिक अभिक्रियाएँ कहलाती हैं।
ऊष्माक्षेपी अभिक्रियाओं के अन्य उदाहरण हैं -
(i) प्राकृतिक गैस का जलना
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) क्या आप जानते हैं कि श्वसन एक ऊष्माक्षेपी प्रक्रिया है?
हम सभी जानते हैं कि हमें जीवित रहने के लिए ऊर्जा की आवश्यकता होती है। हमें यह ऊर्जा हमारे द्वारा खाए जाने वाले भोजन से मिलती है। पाचन के दौरान, भोजन सरल पदार्थों में टूट जाता है। उदाहरण के लिए, चावल, आलू और रोटी में कार्बोहाइड्रेट होते हैं। इन कार्बोहाइड्रेटों को ग्लूकोज बनाने के लिए तोड़ा जाता है। यह ग्लूकोज हमारे शरीर की कोशिकाओं में ऑक्सीजन के साथ मिलकर ऊर्जा प्रदान करता है। इस अभिक्रिया का विशेष नाम श्वसन है, जिसकी प्रक्रिया का आप अध्याय 6 में अध्ययन करेंगे।
$ \begin{equation*} \underset{\text{ (ग्लूकोज) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ ऊर्जा } \tag{1.18} \end{equation*} $
(iii) सब्जियों के पदार्थ का कम्पोस्ट में अपघटन भी एक ऊष्माक्षेपी अभिक्रिया का उदाहरण है।
क्रियाकलाप 1.1 में होने वाली अभिक्रिया का प्रकार पहचानें, जहाँ एक ही उत्पाद के निर्माण के साथ-साथ ऊष्मा भी निकलती है।
1.2.2 अपघटन अभिक्रिया
क्रियाकलाप 1.5
- एक सूखी उबलने वाली परखनली में लगभग $2 g$ फेरस सल्फेट क्रिस्टल लें।
- फेरस सल्फेट क्रिस्टल के रंग पर ध्यान दें।
- चित्र 1.4 में दिखाए अनुसार बर्नर या स्पिरिट लैंप की लौ पर उबलने वाली परखनली को गर्म करें।
- गर्म करने के बाद क्रिस्टल के रंग का अवलोकन करें।
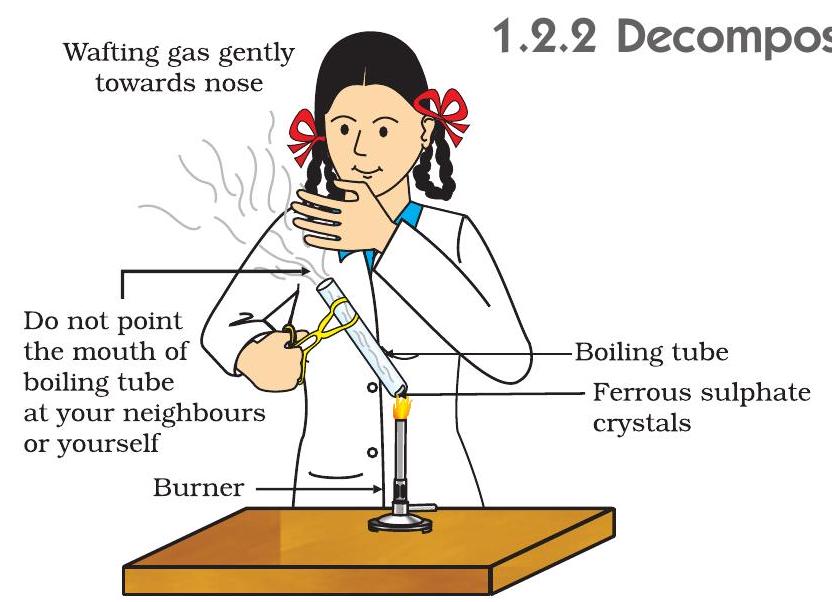
चित्र 1.4 फेरस सल्फेट के क्रिस्टल युक्त उबलने वाली परखनली को गर्म करने और गंध सूंघने का सही तरीका
क्या आपने देखा है कि फेरस सल्फेट क्रिस्टल का हरा रंग बदल गया है? आप जलती हुई सल्फर की विशिष्ट गंध भी सूंघ सकते हैं।
$ \underset{\text{(फेरस सल्फेट)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (फेरिक ऑक्साइड) }]{\text{ ऊष्मा }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
इस अभिक्रिया में आप देख सकते हैं कि एक ही अभिकारक टूटकर सरल उत्पाद देता है। यह एक अपघटन अभिक्रिया है। फेरस सल्फेट क्रिस्टल $(FeSO_4. 7 H_2 O)$ गर्म करने पर जल खो देते हैं और क्रिस्टल का रंग बदल जाता है। फिर यह फेरिक ऑक्साइड $(Fe_2 O_3)$, सल्फर डाइऑक्साइड $(SO_2)$ और सल्फर ट्राइऑक्साइड $(SO_3)$ में अपघटित हो जाता है। फेरिक ऑक्साइड एक ठोस है, जबकि $SO_2$ और $SO_3$ गैसें हैं।
गर्म करने पर कैल्शियम कार्बोनेट का कैल्शियम ऑक्साइड और कार्बन डाइऑक्साइड में अपघटन विभिन्न उद्योगों में उपयोग की जाने वाली एक महत्वपूर्ण अपघटन अभिक्रिया है। कैल्शियम ऑक्साइड को चूना या बिना बुझा चूना (क्विक लाइम) कहा जाता है। इसके कई उपयोग हैं - एक सीमेंट के निर्माण में है। जब अपघटन अभिक्रिया गर्म करके की जाती है, तो इसे ऊष्मीय अपघटन कहा जाता है।
$\underset{\text{ (Limestone) }}{CaCO_3(s)} \stackrel{\text{ Heat }}{\longrightarrow} \underset{\text{ (Quick lime) }}{CaO(s)}+{CO_2(g)} \quad (1.20)$
ऊष्मीय अपघटन अभिक्रिया का एक अन्य उदाहरण क्रियाकलाप 1.6 में दिया गया है।
क्रियाकलाप 1.6
- एक उबलने वाली परखनली में लगभग $2 g$ लेड नाइट्रेट पाउडर लें।
- चिमटे से उबलने वाली परखनली को पकड़ें और चित्र 1.5 में दिखाए अनुसार लौ पर गर्म करें।
- आप क्या देखते हैं? यदि कोई परिवर्तन हो तो उसे नोट करें।
आप भूरे रंग के धुएं के उत्सर्जन का अवलोकन करेंगे। ये धुएं नाइट











