অধ্যায় 01 ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ
দৈনন্দিন জীৱনৰ তলত দিয়া পৰিস্থিতিবোৰ বিবেচনা কৰা আৰু ভাবা কি হয় যেতিয়া -
- গৰমকালত গাখীৰ কোঠাৰ উষ্ণতাত ৰখা হয়।
- এটা লোৰ তৱা/পাতিল/কেঁকুৰা আৰ্দ্ৰ বায়ুমণ্ডলত উন্মুক্তভাৱে ৰখা হয়।
- আঙুৰ গাঁজন হয়।
- খাদ্য ৰান্ধি হয়।
- আমাৰ শৰীৰত খাদ্য জীৰ্ণ হয়।
- আমি উশাহ-নিশাহ লওঁ।
ওপৰৰ সকলো পৰিস্থিতিত, আৰম্ভণিৰ পদাৰ্থৰ প্ৰকৃতি আৰু সত্তা কিছু পৰিমাণে সলনি হৈছে। আমি ইতিমধ্যে আমাৰ আগৰ শ্ৰেণীবোৰত পদাৰ্থৰ ভৌতিক আৰু ৰাসায়নিক পৰিৱৰ্তনৰ বিষয়ে শিকিছো। যেতিয়াই ৰাসায়নিক পৰিৱৰ্তন ঘটে, তেতিয়া আমি ক’ব পাৰো যে এটা ৰাসায়নিক বিক্ৰিয়া সংঘটিত হৈছে।
তুমি কিজানি ভাবি আছা যে ৰাসায়নিক বিক্ৰিয়া বুলি ক’লে সঁচাকৈয়ে কি বুজায়। ৰাসায়নিক বিক্ৰিয়া সংঘটিত হৈছে বুলি আমি কেনেকৈ জানিব পাৰো? এই প্ৰশ্নবোৰৰ উত্তৰ বিচাৰিবলৈ আহা আমি কেইটামান কাৰ্যকলাপ কৰো।
কাৰ্যকলাপ 1.1
সতৰ্কতা: এই কাৰ্যকলাপটোৰ বাবে শিক্ষকৰ সহায়ৰ প্ৰয়োজন। ছাত্ৰ-ছাত্ৰীয়ে উপযুক্ত চকুৰ চচমা পিন্ধিলে ভাল হয়।
- এডাল মেগনেছিয়াম ফিতাৰ প্ৰায় ৩-৪ চে.মি. দীঘল অংশ বালি কাগৰেৰে ঘঁহি পৰিষ্কাৰ কৰা।
- এযোৰ চিমটাৰে ধৰি লোৱা। এটা স্পিৰিট লেম্প বা বাৰ্ণাৰ ব্যৱহাৰ কৰি জ্বলোৱা আৰু চিত্ৰ 1.1 ত দেখুওৱাৰ দৰে হোৱা ছাইখন এটা ৱাচ-গ্লাছত সংগ্ৰহ কৰা। মেগনেছিয়াম ফিতাডাল জ্বলাওঁতে ইয়াক তোমাৰ চকুৰ পৰা যিমান দূৰে পাৰি সিমান দূৰত ৰাখিবা।
- তুমি কি লক্ষ্য কৰিলা?
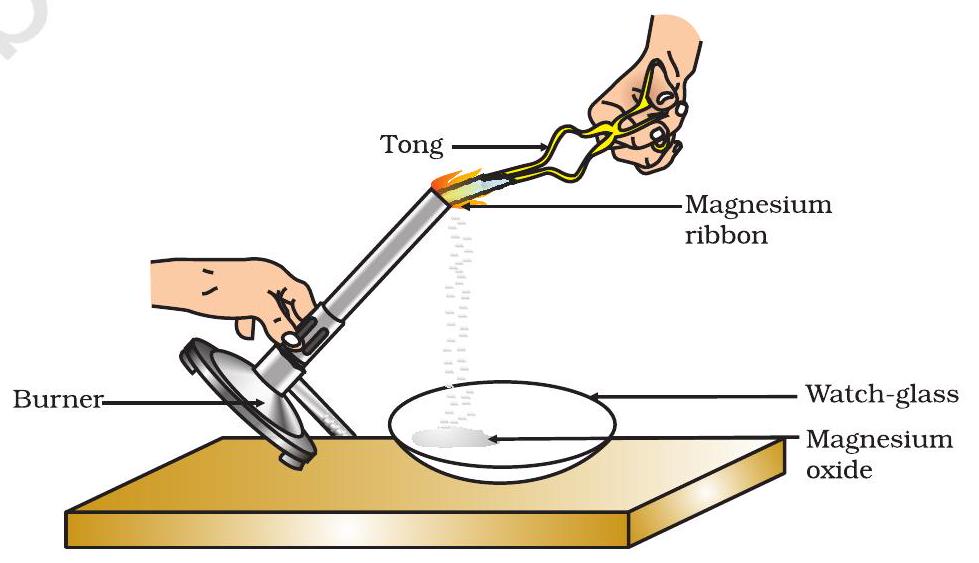
চিত্ৰ 1.1
বায়ুত মেগনেছিয়াম ফিতা জ্বলোৱা আৰু ৱাচ-গ্লাছত মেগনেছিয়াম অক্সাইড সংগ্ৰহ কৰা
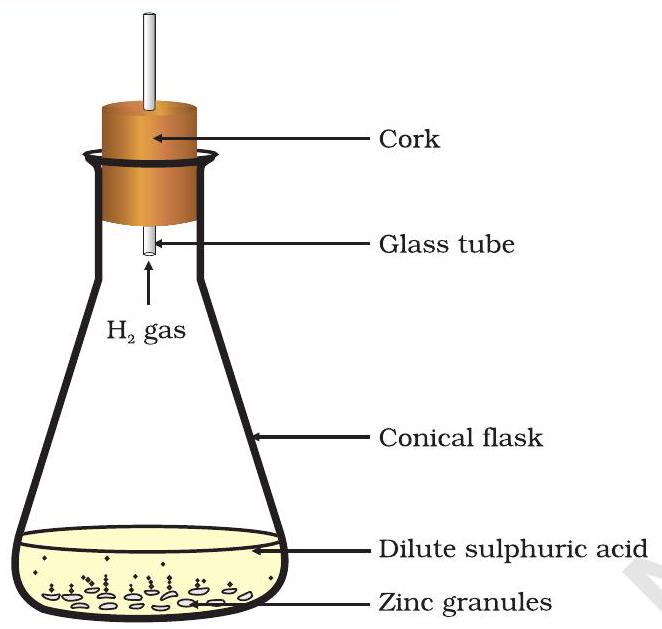
চিত্ৰ 1.2 জিংকৰ ওপৰত তনু গন্ধকৰ এছিডৰ ক্ৰিয়াৰ দ্বাৰা হাইড্ৰ’জেন গেছৰ গঠন
তুমি নিশ্চয় লক্ষ্য কৰিছা যে মেগনেছিয়াম ফিতাডাল উজ্জ্বল বগা জুইৰ শিখাৰে জ্বলে আৰু বগা গুড়িলৈ ৰূপান্তৰিত হয়। এই গুড়িটো হৈছে মেগনেছিয়াম অক্সাইড। ই মেগনেছিয়াম আৰু বায়ুত থকা অক্সিজেনৰ মাজৰ বিক্ৰিয়াৰ ফলত গঠিত হয়।
কাৰ্যকলাপ 1.2
- এটা টেষ্ট টিউবত লেড নাইট্ৰেট দ্ৰৱ লোৱা।
- ইয়াত পটেছিয়াম আয়’ডাইড দ্ৰৱ যোগ কৰা।
- তুমি কি লক্ষ্য কৰিলা?
কাৰ্যকলাপ 1.3
- এটা কনিকেল ফ্লাস্ক বা টেষ্ট টিউবত কেইটামান জিংকৰ দানা লোৱা।
- ইয়াত তনু হাইড্ৰ’ক্ল’ৰিক এছিড বা গন্ধকৰ এছিড যোগ কৰা (চিত্ৰ 1.2)।
সতৰ্কতা: এছিডটো সাৱধানেৰে হাতলোৱা।
- জিংকৰ দানাবোৰৰ চাৰিওফালে কিবা ঘটিছে নেকি লক্ষ্য কৰিলানে?
- কনিকেল ফ্লাস্ক বা টেষ্ট টিউবটো চুই চোৱা। ইয়াৰ উষ্ণতাত কিবা পৰিৱৰ্তন হৈছেনে?
ওপৰৰ তিনিটা কাৰ্যকলাপৰ পৰা, আমি ক’ব পাৰো যে তলত দিয়া যিকোনো পৰ্যবেক্ষণে আমাক ৰাসায়নিক বিক্ৰিয়া সংঘটিত হৈছে নে নাই নিৰ্ধাৰণ কৰাত সহায় কৰে –
- অৱস্থাৰ পৰিৱৰ্তন
- ৰঙৰ পৰিৱৰ্তন
- গেছৰ উৎপন্ন হোৱা
- উষ্ণতাৰ পৰিৱৰ্তন।
আমি আমাৰ চাৰিওফালৰ পৰিৱৰ্তনবোৰ লক্ষ্য কৰোঁতে দেখিবলৈ পাওঁ যে আমাৰ চাৰিওফালে বহু ধৰণৰ ৰাসায়নিক বিক্ৰিয়া সংঘটিত হৈ আছে। আমি এই অধ্যায়ত বিভিন্ন প্ৰকাৰৰ ৰাসায়নিক বিক্ৰিয়া আৰু সেইবোৰৰ প্ৰতীকী উপস্থাপনৰ বিষয়ে অধ্যয়ন কৰিম।
1.1 ৰাসায়নিক সমীকৰণ
কাৰ্যকলাপ 1.1 ক এনেদৰে বৰ্ণনা কৰিব পাৰি – যেতিয়া মেগনেছিয়াম ফিতাডাল অক্সিজেনত জ্বলোৱা হয়, ই মেগনেছিয়াম অক্সাইডলৈ ৰূপান্তৰিত হয়। বাক্যৰ ৰূপত ৰাসায়নিক বিক্ৰিয়াৰ এই বৰ্ণনা বহু দীঘল। ইয়াক চুটি ৰূপত লিখিব পাৰি। ইয়াৰ সবাতোকৈ সহজ উপায় হৈছে ইয়াক শব্দ-সমীকৰণৰ ৰূপত লিখা। ওপৰৰ বিক্ৰিয়াটোৰ বাবে শব্দ-সমীকৰণটো হ’ব –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
বিক্ৰিয়া (1.1) ত ৰাসায়নিক পৰিৱৰ্তনৰ সন্মুখীন হোৱা পদাৰ্থবোৰ, মেগনেছিয়াম আৰু অক্সিজেন, হৈছে বিক্ৰিয়ক। নতুন পদাৰ্থটো হৈছে মেগনেছিয়াম অক্সাইড, যি বিক্ৰিয়াৰ সময়ত গঠিত হৈছে, উৎপাদ হিচাপে।
এটা শব্দ-সমীকৰণে বিক্ৰিয়কৰ পৰা উৎপাদলৈ হোৱা পৰিৱৰ্তন তেওঁলোকৰ মাজত থকা এটা তীৰ চিহ্নৰ দ্বাৰা দেখুৱায়। বিক্ৰিয়কবোৰ বাওঁফালে (LHS) লিখা হয় আৰু তেওঁলোকৰ মাজত এটা যোগ চিহ্ন (+) থাকে। একেদৰে, উৎপাদবোৰ সোঁফালে (RHS) লিখা হয় আৰু তেওঁলোকৰ মাজত এটা যোগ চিহ্ন (+) থাকে। তীৰৰ মূৰটোৱে উৎপাদৰ ফালে আঙুলিয়াই দিয়ে, আৰু বিক্ৰিয়াৰ দিশ দেখুৱায়।
1.1.1 ৰাসায়নিক সমীকৰণ লিখা
ৰাসায়নিক সমীকৰণবোৰ উপস্থাপন কৰাৰ আন কোনো চুটি উপায় আছে নেকি? ৰাসায়নিক সমীকৰণবোৰ অধিক সংক্ষিপ্ত আৰু উপযোগী কৰিব পাৰি যদি আমি শব্দৰ সলনি ৰাসায়নিক সংকেত ব্যৱহাৰ কৰো। ৰাসায়নিক সমীকৰণ এটাই ৰাসায়নিক বিক্ৰিয়া এটা প্ৰতিনিধিত্ব কৰে। যদি তুমি মেগনেছিয়াম, অক্সিজেন আৰু মেগনেছিয়াম অক্সাইডৰ সংকেতবোৰ মনত পেলোৱা, তেন্তে ওপৰৰ শব্দ-সমীকৰণটো এনেদৰে লিখিব পাৰি -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
তীৰৰ বাওঁফাল (LHS) আৰু সোঁফাল (RHS) ত থকা প্ৰতিটো মৌলৰ পৰমাণুৰ সংখ্যা গণনা কৰা আৰু তুলনা কৰা। প্ৰতিটো মৌলৰ পৰমাণুৰ সংখ্যা দুয়োফালে একে নেকি? যদি হয়, তেন্তে সমীকৰণটো সমতুল্য। যদি নহয়, তেন্তে সমীকৰণটো অসমতুল্য কাৰণ ভৰ দুয়োফালে একে নহয়। এনে ৰাসায়নিক সমীকৰণটো হৈছে বিক্ৰিয়া এটাৰ বাবে কংকাল ৰাসায়নিক সমীকৰণ। সমীকৰণ (1.2) হৈছে বায়ুত মেগনেছিয়াম জ্বলোৱাৰ বাবে কংকাল ৰাসায়নিক সমীকৰণ।
1.1.2 সমতুল্য ৰাসায়নিক সমীকৰণ
তুমি নৱম শ্ৰেণীত অধ্যয়ন কৰা ভৰ সংৰক্ষণৰ সূত্ৰটো মনত পেলোৱা; ৰাসায়নিক বিক্ৰিয়া এটাত ভৰ সৃষ্টি বা ধ্বংস কৰিব নোৱাৰি। অৰ্থাৎ, ৰাসায়নিক বিক্ৰিয়া এটাৰ উৎপাদবোৰত উপস্থিত মৌলবোৰৰ মুঠ ভৰ বিক্ৰিয়কবোৰত উপস্থিত মৌলবোৰৰ মুঠ ভৰৰ সমান হ’ব লাগিব।
অন্য কথাত, প্ৰতিটো মৌলৰ পৰমাণুৰ সংখ্যা ৰাসায়নিক বিক্ৰিয়াৰ আগতে আৰু পিছতে একে থাকে। গতিকে, আমি এটা কংকাল ৰাসায়নিক সমীকৰণ সমতুল্য কৰিব লাগিব। ৰাসায়নিক সমীকৰণ (1.2) টো সমতুল্য নেকি? আহা আমি ৰাসায়নিক সমীকৰণ এটা সমতুল্য কৰাটো ক্ৰমে ক্ৰমে শিকো।
কাৰ্যকলাপ 1.3 ৰ বাবে শব্দ-সমীকৰণটো এনেদৰে উপস্থাপন কৰিব পাৰি -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
ওপৰৰ শব্দ-সমীকৰণটো তলত দিয়া ৰাসায়নিক সমীকৰণৰ দ্বাৰা উপস্থাপন কৰিব পাৰি -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
আহা আমি তীৰৰ দুয়োফালে থকা বিভিন্ন মৌলৰ পৰমাণুৰ সংখ্যা পৰীক্ষা কৰো।
| মৌল | বিক্ৰিয়কত পৰমাণুৰ সংখ্যা (LHS) | উৎপাদত পৰমাণুৰ সংখ্যা (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
প্ৰতিটো মৌলৰ পৰমাণুৰ সংখ্যা তীৰৰ দুয়োফালে একে হোৱা হেতুকে, সমীকৰণ (1.3) হৈছে এটা সমতুল্য ৰাসায়নিক সমীকৰণ।
আহা আমি তলত দিয়া ৰাসায়নিক সমীকৰণটো সমতুল্য কৰিবলৈ চেষ্টা কৰো -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
পদক্ষেপ I: ৰাসায়নিক সমীকৰণ এটা সমতুল্য কৰিবলৈ, প্ৰথমে প্ৰতিটো সংকেতৰ চাৰিওফালে বাকচ আঁকা। সমীকৰণ সমতুল্য কৰোঁতে বাকচবোৰৰ ভিতৰৰ কিবা সলনি নকৰিবা।
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
পদক্ষেপ II: অসমতুল্য সমীকৰণ (1.5) ত উপস্থিত বিভিন্ন মৌলৰ পৰমাণুৰ সংখ্যা তালিকাভুক্ত কৰা।
| মৌল | বিক্ৰিয়কত পৰমাণুৰ সংখ্যা (LHS) | উৎপাদত পৰমাণুৰ সংখ্যা (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
পদক্ষেপ III: সৰ্বাধিক সংখ্যক পৰমাণু থকা যৌগটোৰে সমতুল্য কৰাটো আৰম্ভ কৰাটো সদায় সুবিধাজনক। ই বিক্ৰিয়ক বা উৎপাদ হ’ব পাৰে। সেই যৌগটোত, সৰ্বাধিক সংখ্যক পৰমাণু থকা মৌলটো বাছনি কৰা। এই নিকষ ব্যৱহাৰ কৰি, আমি $Fe_3 O_4$ আৰু ইয়াত থকা অক্সিজেন মৌলটো বাছনি কৰো। সোঁফালে (RHS) চাৰিটা অক্সিজেন পৰমাণু আছে আৰু কেৱল বাওঁফালে (LHS) এটা আছে।
অক্সিজেন পৰমাণুবোৰ সমতুল্য কৰিবলৈ -
| অক্সিজেনৰ পৰমাণু |
বিক্ৰিয়কত | উৎপাদত |
|---|---|---|
| (i) আৰম্ভণি | 1($ \mathrm{H_2O} $ ত) | 4($ \mathrm{Fe_3O_4} $ ত) |
| (ii) সমতুল্য কৰিবলৈ | 1 $\times$ 4 | 4 |
পৰমাণুৰ সংখ্যা সমান কৰিবলৈ, ইয়াক মনত ৰাখিব লাগিব যে আমি বিক্ৰিয়াত জড়িত যৌগ বা মৌলবোৰৰ সংকেত সলনি কৰিব নোৱাৰো। উদাহৰণস্বৰূপে, অক্সিজেন পৰমাণুবোৰ সমতুল্য কৰিবলৈ আমি ‘4’ গুণাংক $4 H_2 O$ হিচাপে দিব পাৰো কিন্তু $H_2 O_4$ বা $(H_2 O)_4$ হিচাপে নহয়। এতিয়া আংশিকভাৱে সমতুল্য হোৱা সমীকৰণটো হৈছে -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (আংশিকভাৱে সমতুল্য সমীকৰণ)
পদক্ষেপ IV: Fe আৰু $H$ পৰমাণুবোৰ এতিয়াও সমতুল্য হোৱা নাই। আগবাঢ়িবলৈ এই মৌলবোৰৰ যিকোনো এটা বাছনি কৰা। আহা আমি আংশিকভাৱে সমতুল্য হোৱা সমীকৰণটোত হাইড্ৰ’জেন পৰমাণুবোৰ সমতুল্য কৰো।
$H$ পৰমাণুবোৰৰ সংখ্যা সমান কৰিবলৈ, সোঁফালে (RHS) হাইড্ৰ’জেনৰ অণুৰ সংখ্যা চাৰিটা কৰক।
| হাইড্ৰ’জেনৰ পৰমাণু |
বিক্ৰিয়কত | উৎপাদত |
|---|---|---|
| (i) আৰম্ভণি | 8($ \mathrm{4H_2O} $ ত) | 2($ \mathrm{H_2} $ ত) |
| (ii) সমতুল্য কৰিবলৈ | 8 | 2 $\times$ 4 |
সমীকৰণটো হ’ব -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(আংশিকভাৱে সমতুল্য সমীকৰণ)
পদক্ষেপ V: ওপৰৰ সমীকৰণটো পৰীক্ষা কৰা আৰু তৃতীয়টো মৌল বাছনি কৰা যিটো সমতুল্য হোৱা নাই। তুমি দেখিবা যে কেৱল এটা মৌল সমতুল্য কৰিবলৈ বাকী আছে, সেয়া হৈছে লো (আইৰন)।
| লোৰ পৰমাণু | বিক্ৰিয়কত | উৎপাদত |
|---|---|---|
| (i) আৰম্ভণি | 1($ \mathrm{Fe} $ ত) | 3($ \mathrm{Fe_3O_4} $ ত) |
| (ii) সমতুল্য কৰিবলৈ | 1 $\times$ 3 | 3 |
$Fe$ সমান কৰিবলৈ, আমি বাওঁফালে (LHS) $Fe$ ৰ তিনিটা পৰমাণু লওঁ।
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
পদক্ষেপ VI: শেষত, সমতুল্য হোৱা সমীকৰণটোৰ শুদ্ধতা পৰীক্ষা কৰিবলৈ, আমি সমীকৰণটোৰ দুয়োফালে থকা প্ৰতিটো মৌলৰ পৰমাণু গণনা কৰো।
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(সমতুল্য সমীকৰণ)
সমীকৰণ (1.9) ৰ দুয়োফালে থকা মৌলবোৰৰ পৰমাণুৰ সংখ্যা সমান। এই সমীকৰণটো এতিয়া সমতুল্য। ৰাসায়নিক সমীকৰণ সমতুল্য কৰাৰ এই পদ্ধতিক হিট-এণ্ড-ট্ৰায়েল পদ্ধতি বোলা হয় কাৰণ আমি সৰুতম পূৰ্ণ সংখ্যা গুণাংক ব্যৱহাৰ কৰি সমীকৰণ সমতুল্য কৰিবলৈ চেষ্টা কৰো।
পদক্ষেপ VII: ভৌতিক অৱস্থাৰ চিহ্ন লিখা ওপৰৰ সমতুল্য সমীকৰণ (1.9) টো সাৱধানে পৰীক্ষা কৰা। এই সমীকৰণটোৱে প্ৰতিটো বিক্ৰিয়ক আৰু উৎপাদৰ ভৌতিক অৱস্থাৰ বিষয়ে আমাক কিবা কয় নেকি? এই সমীকৰণত তেওঁলোকৰ ভৌতিক অৱস্থাৰ বিষয়ে কোনো তথ্য দিয়া হোৱা নাই।
ৰাসায়নিক সমীকৰণ এটাক অধিক তথ্যপূৰ্ণ কৰিবলৈ, বিক্ৰিয়ক আৰু উৎপাদবোৰৰ ভৌতিক অৱস্থাসমূহ তেওঁলোকৰ ৰাসায়নিক সংকেতৰ সৈতে উল্লেখ কৰা হয়। বিক্ৰিয়ক আৰু উৎপাদবোৰৰ গেছীয়, তৰল, জলীয় আৰু কঠিন অৱস্থাবোৰ ক্ৰমে (g), (l), (aq) আৰু (s) চিহ্নৰ দ্বাৰা প্ৰতিনিধিত্ব কৰা হয়। জলীয় (aq) শব্দটো লিখা হয় যদি বিক্ৰিয়ক বা উৎপাদটো পানীত দ্ৰৱ ৰূপত উপস্থিত থাকে।
সমতুল্য সমীকৰণ (1.9) হৈছে
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
মনত ৰাখিবা যে চিহ্ন $(g)$ ক $H_2 O$ ৰ সৈতে ব্যৱহাৰ কৰা হয় ইংগিত দিবলৈ যে এই বিক্ৰিয়াত পানী বাষ্প ৰূপত ব্যৱহাৰ কৰা হয়।
সাধাৰণতে ভৌতিক অৱস্থাবোৰ ৰাসায়নিক সমীকৰণত অন্তৰ্ভুক্ত নকৰা হয় যদি সেয়া নিৰ্দিষ্ট কৰাটো আৱশ্যক নহয়।
কেতিয়াবা বিক্ৰিয়াৰ বাবে উষ্ণতা, চাপ, অনুঘটক আদি বিক্ৰিয়াৰ অৱস্থাবোৰ সমীকৰণটোৰ তীৰৰ ওপৰত আৰু/বা তলত সূচিত কৰা হয়। উদাহৰণস্বৰূপে -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
এই পদক্ষেপবোৰ ব্যৱহাৰ কৰি, তুমি ইতিমধ্যে পাঠত দিয়া সমীকৰণ (1.2) টো সমতুল্য কৰিব পাৰিবানে?
1.2 ৰাসায়নিক বিক্ৰিয়াৰ প্ৰকাৰসমূহ
আমি নৱম শ্ৰেণীত শিকিছিলো যে ৰাসায়নিক বিক্ৰিয়া এটাৰ সময়ত এটা মৌলৰ পৰমাণুবোৰ আন এটা মৌললৈ ৰূপান্তৰিত নহয়। পৰমাণুবোৰ মিশ্ৰণৰ পৰা নোহোৱাও নহয় বা আন ঠাইৰ পৰা ওলাইও নাহে। প্ৰকৃততে, ৰাসায়নিক বিক্ৰিয়াবোৰত নতুন পদাৰ্থ উৎপন্ন কৰিবলৈ পৰমাণুবোৰৰ মাজৰ বান্ধ ভাঙি নতুন বান্ধ গঠন কৰা জড়িত থাকে। তুমি তৃতীয় আৰু চতুৰ্থ অধ্যায়ত পৰমাণুবোৰৰ মাজত গঠিত বান্ধৰ প্ৰকাৰৰ বিষয়ে অধ্যয়ন কৰিবা।
1.2.1 সংযোজন বিক্ৰিয়া
কাৰ্যকলাপ 1.4
- এটা বিকাৰত অলপ পৰিমাণৰ কেলছিয়াম অক্সাইড বা চূণ লোৱা।
- ইয়াত লাহে লাহে পানী যোগ কৰা।
- চিত্ৰ 1.3 ত দেখুওৱাৰ দৰে বিকাৰটো চুই চোৱা।
- উষ্ণতাত কিবা পৰিৱৰ্তন অনুভৱ কৰিলানে?
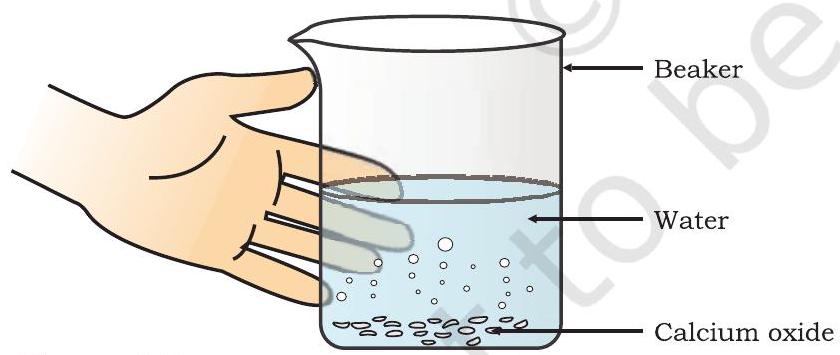
চিত্ৰ 1.3 কেলছিয়াম অক্সাইডৰ পানীৰ সৈতে বিক্ৰিয়াৰ দ্বাৰা শিল চূণৰ গঠন
কেলছিয়াম অক্সাইডে পানীৰ সৈতে সক্ৰিয়ভাৱে বিক্ৰিয়া কৰি শিল চূণ (কেলছিয়াম হাইড্ৰ’ক্সাইড) উৎপন্ন কৰে আৰু বহু পৰিমাণৰ তাপ মুক্ত কৰে।
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
এই বিক্ৰিয়াত, কেলছিয়াম অক্সাইড আৰু পানী সংযোজিত হৈ এটা একক উৎপাদ, কেলছিয়াম হাইড্ৰ’ক্সাইড গঠন কৰে। এনে বিক্ৰিয়া য’ত দুটা বা ততোধিক বিক্ৰিয়কৰ পৰা এটা একক উৎপাদ গঠিত হয় তাক সংযোজন বিক্ৰিয়া বুলি জনা যায়।
তুমি জানানে?
বিক্ৰিয়া 1.13 ৰ দ্বাৰা উৎপন্ন হোৱা শিল চূণৰ দ্ৰৱটো বেৰ বগা কৰিবলৈ ব্যৱহাৰ কৰা হয়। কেলছিয়াম হাইড্ৰ’ক্সাইডে বায়ুৰ কাৰ্বন-ডাই-অক্সাইডৰ সৈতে লাহে লাহে বিক্ৰিয়া কৰি বেৰবোৰত কেলছিয়াম কাৰ্বনেটৰ এটা পাতল স্তৰ গঠন কৰে। কেলছিয়াম কাৰ্বনেট বগা কৰাৰ দুৰ্গা দিনৰ পিছত গঠিত হয় আৰু বেৰবোৰক উজ্জ্বল ৰূপ দিয়ে। ই মনোযোগ দিবলগীয়া যে মাৰ্বলৰ ৰাসায়নিক সংকেতো $CaCO_3$।
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
আহা আমি সংযোজন বিক্ৰিয়াৰ আৰু কেইটামান উদাহৰণ আলোচনা কৰো।
(i) কয়লা জ্বলোৱা
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ আৰু $O_2(g)$ ৰ পৰা পানীৰ গঠন
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
সৰল ভাষাত আমি ক’ব পাৰো যে যেতিয়া দুটা বা ততোধিক পদাৰ্থ (মৌল বা যৌগ) সংযোজিত হৈ এটা একক উৎপাদ গঠন কৰে, তেতিয়া বিক্ৰিয়াবোৰক সংযোজন বিক্ৰিয়া বোলা হয়।
কাৰ্যকলাপ 1.4 ত, আমি ইয়াও লক্ষ্য কৰিছিলো যে বহু পৰিমাণৰ তাপ উৎপন্ন হয়। ইয়ে বিক্ৰিয়া মিশ্ৰণটো গৰম কৰি তোলে। যি বিক্ৰিয়াত উৎপাদ গঠনৰ সৈতে তাপ মুক্ত হয় তাক তাপমোচী ৰাসায়নিক বিক্ৰিয়া বোলা হয়।
তাপমোচী বিক্ৰিয়াৰ অন্যান্য উদাহৰণ হৈছে -
(i) প্ৰাকৃতিক গেছ জ্বলোৱা
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) তুমি জানানে যে উশাহ-নিশাহ এটা তাপমোচী প্ৰক্ৰিয়া?
আমি সকলোৱে জানো যে জীয়াই থাকিবলৈ আমাক শক্তিৰ প্ৰয়োজন। আমি খোৱা খাদ্যৰ পৰা এই শক্তি পাওঁ। জীৰ্ণ হোৱাৰ সময়ত, খাদ্য সৰল পদাৰ্থলৈ ভাঙি যায়। উদাহৰণস্বৰূপে, ভাত, আলু আৰু পাউৰুটিৰ কাৰ্বহাইড্ৰেট থাকে। এই কাৰ্বহাইড্ৰেটবোৰ ভাঙি গ্লুক’জ গঠন কৰে। এই গ্লুক’জে আমাৰ শৰীৰৰ কোষবোৰত অক্সিজেনৰ সৈতে সংযোজিত হৈ শক্তি প্ৰদান কৰে। এই বিক্ৰিয়াৰ বিশেষ নাম হৈছে উশাহ-নিশাহ, যাৰ প্ৰক্ৰিয়া তুমি ষষ্ঠ অধ্যায়ত অধ্যয়ন কৰিবা।
$ \begin{equation*} \underset{\text{ (গ্লুক’জ) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ শক্তি } \tag{1.18} \end{equation*} $
(iii) উদ্ভিদজ পদাৰ্থৰ কম্প’ষ্টলৈ পচনো তাপমোচী বিক্ৰিয়াৰ এটা উদাহৰণ।
কাৰ্যকলাপ 1.1 ত সংঘটিত হোৱা বিক্ৰিয়াৰ প্ৰকাৰ চিনাক্ত কৰা, য’ত এটা একক উৎপাদ গঠনৰ সৈতে তাপ ওলাই যায়।
1.2.2 বিযোজন বিক্ৰিয়া
কাৰ্যকলাপ 1.5
- এটা শুকান বয়লিং টিউবত প্ৰায় $2 g$ ফেৰাছ চালফেট ক্ৰিষ্টেল লোৱা।
- ফেৰাছ চালফেট ক্ৰিষ্টেলবোৰৰ ৰঙটো লক্ষ্য কৰা।
- চিত্ৰ 1.4 ত দেখুওৱাৰ দৰে বাৰ্ণাৰ বা স্পিৰিট লেম্পৰ জুইৰ ওপৰত বয়লিং টিউবটো তপতাওৱা।
- তপতালেৰে পিছত ক্ৰিষ্টেলবোৰৰ ৰঙ লক্ষ্য কৰা।
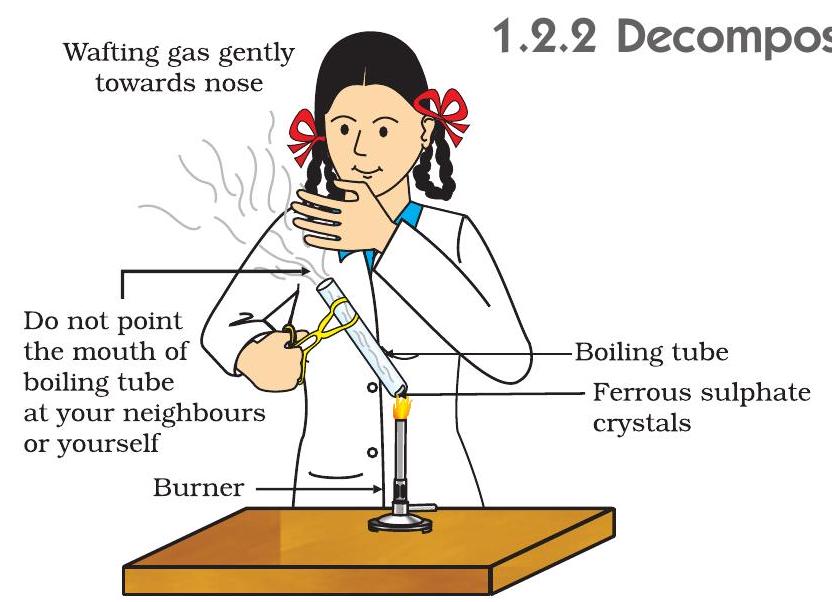
চিত্ৰ 1.4 ফেৰাছ চালফেট ক্ৰিষ্টেল থকা বয়লিং টিউব তপতোৱাৰ আৰু গোন্ধ লোৱাৰ শুদ্ধ উপায়
তুমি লক্ষ্য কৰিছানে যে ফেৰাছ চালফেট ক্ৰিষ্টেলবোৰৰ সেউজীয়া ৰঙটো সলনি হৈছে? তুমি গন্ধক জ্বলোৱাৰ বৈশিষ্ট্যপূৰ্ণ গোন্ধও ল’ব পাৰা।
$ \underset{\text{(ফেৰাছ চালফেট)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (ফেৰিক অক্সাইড) }]{\text{ তাপ }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
এই বিক্ৰিয়াত তুমি লক্ষ্য কৰিব পাৰা যে এটা একক বিক্ৰিয়ক ভাঙি সৰল উৎপাদ দিয়ে। ই এটা বিযোজন বিক্ৰিয়া। ফেৰাছ চালফেট ক্ৰিষ্টেল $(FeSO_4. 7 H_2 O)$ তপতালে পানী হেৰুৱায় আৰু ক্ৰিষ্টেলবোৰৰ ৰঙ সলনি হয়। ইয়াৰ পিছত ই ফেৰিক অক্সাইড $(Fe_2 O_3)$, গন্ধক-ডাই-অক্সাইড $(SO_2)$ আৰু গন্ধক-ট্ৰাই-অক্সাইড $(SO_3)$ লৈ বিযোজিত হয়। ফেৰিক অক্সাইড এটা কঠিন পদাৰ্থ, আনহাতে $SO_2$ আৰু $SO_3$ গেছ।
তপতালে কেলছিয়াম কাৰ্বনেটৰ কেলছিয়াম অক্সাইড আৰু কাৰ্বন-ডাই-অক্সাইডলৈ বিযোজন বিভিন্ন উদ্যোগত ব্যৱহাৰ কৰা এটা গুৰুত্বপূৰ্ণ বিযোজন বিক্ৰিয়া। কেলছিয়াম অক্সাইডক চূণ বা শিল চূণ বোলা হয়। ইয়াৰ বহু ব্যৱহাৰ আছে - এটা হৈছে চিমেণ্টৰ উৎপাদন। যেতিয়া বিযোজন বিক্ৰিয়া এটা তপতাই কৰা হয়, তেতিয়া ইয়াক তাপীয় বিযোজন বোলা হয়।
$\underset{\text{ (Limestone) }}{CaCO_3(s)} \stackrel{\text{ Heat }}{\longrightarrow} \underset{\text{ (Quick lime) }}{CaO(s)}+{CO_2(g)} \quad (1.20)$
তাপীয় বিযোজন বিক্ৰিয়াৰ আন এটা উদাহৰণ কাৰ্যকলাপ 1.6 ত দিয়া হৈছে।
কাৰ্যকলাপ 1.6
- এটা বয়লিং টিউবত প্ৰায় $2 g$ লেড নাইট্ৰেট গুড়ি লোৱা।
- এযোৰ চিমটাৰে বয়লিং টিউবটো ধৰি লোৱা আৰু চিত্ৰ 1.5 ত দেখুওৱাৰ দৰে জুইৰ ওপৰত তপতাওৱা।
- তুমি কি লক্ষ্য কৰিলা? পৰিৱৰ্তনটো, যদি থাকে, টোকা কৰি ৰাখা।
তুমি মটীয়া ধোৱাৰ উৎপাদন লক্ষ্য কৰিবা। এই ধোৱাবোৰ নাইট্ৰ’জেন-ডাই-অক্সাইড $(NO_2)$ ৰ। সংঘটিত হোৱা বিক্ৰিয়াটো হৈছে -
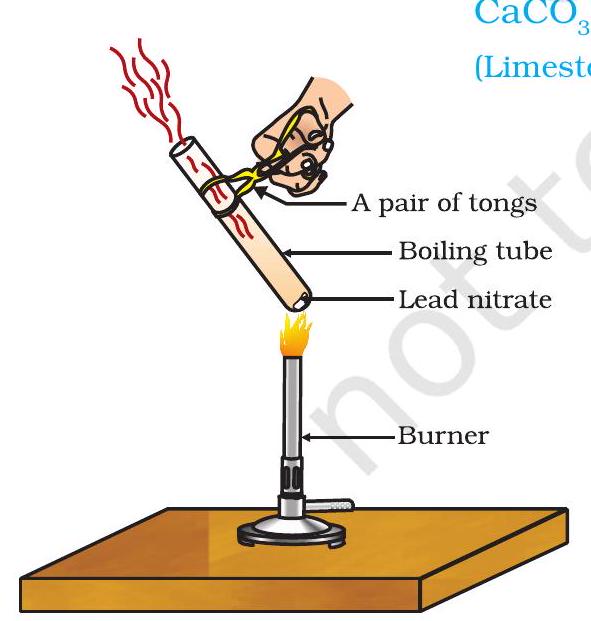
চিত্ৰ 1.5 লেড নাইট্ৰেট তপতোৱা আৰু নাইট্ৰ’জেন-ডাই-অক্সাইডৰ উৎপাদন
$\underset{\text { (Lead nitrate) }}{2 \mathrm{~Pb}\left(\mathrm{NO}_3\right)_2(\mathrm{~s})} \xrightarrow{\text { Heat }} \underset{\text { (Lead oxide) }}{2 \mathrm{PbO}(\mathrm{s})}+\underset{\begin{array}{l}\text { (Nitrogen } \ \text { dioxide) }\end{array}}{4 \mathrm{NO}_2(\mathrm{~g})}+\underset{\text { (Oxygen) }}{\mathrm{O}_2(\mathrm{~g})} \quad (1.21)$
আহা আমি কাৰ্যকলাপ 1.7 আৰু 1.8 ত দিয়াৰ দৰে আৰু কেইটামান বিযোজন বিক্ৰিয়া কৰো।
কাৰ্যকলাপ 1.7
- এটা প্লাষ্টিকৰ মগ লোৱা। ইয়াৰ তলিত দুটা খোলা কৰা আৰু এই খোলাবোৰত ৰবৰ ষ্টপাৰ ফিট কৰা। চিত্ৰ 1.6 ত দেখুওৱাৰ দৰে এই ৰবৰ ষ্টপাৰবোৰত কাৰ্বন ইলেক্ট্ৰ’ড সুমুৱাই দিয়া।
- এই ইলেক্ট্ৰ’ডবোৰ 6 ভ’ল্টৰ বেটাৰী এটাৰ সৈতে সংযোগ কৰা।
- মগটো পানীৰে ভৰোৱা যাতে ইলেক্ট্ৰ’ডবোৰ ডুব যায়। পানীত কেইটোপাল তনু গন্ধকৰ এছিড যোগ কৰা।
- পানীৰে ভৰোৱা দুটা টেষ্ট টিউব লোৱা আৰু দুয়োটা কাৰ্বন ইলেক্ট্ৰ’ডৰ ওপৰত ওলোটাকৈ ৰাখা।
- বিদ্যুৎ প্ৰৱাহ চালু কৰা আৰু যন্ত্ৰটো কিছু সময়ৰ বাবে অক্ষুণ্ণ ৰাখা।
- তুমি দুয়োটা ইলেক্ট্ৰ’ডত বুদবুদৰ গঠন লক্ষ্য কৰিবা। এই বুদবুদবোৰে টেষ্ট টিউববোৰৰ পানী ঠেলি আঁতৰাই দিয়ে।
- দুয়োটা টেষ্ট টিউ











