પ્રકરણ 01 રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો
નીચેની રોજિંદા જીવનની પરિસ્થિતિઓ ધ્યાનમાં લો અને વિચારો કે શું થાય છે જ્યારે -
- દૂધ ઉનાળામાં રૂમના તાપમાને છોડી દેવામાં આવે.
- લોખંડની તવા/કડાઈ/કીલી ભેજવાળા વાતાવરણમાં ખુલ્લી મૂકવામાં આવે.
- દ્રાક્ષ ફરમેન્ટ થાય.
- ખોરાક રાંધવામાં આવે.
- ખોરાક આપણા શરીરમાં પાચન પામે.
- આપણે શ્વસન કરીએ.
ઉપરોક્ત તમામ પરિસ્થિતિઓમાં, પ્રારંભિક પદાર્થની પ્રકૃતિ અને ઓળખ કંઈક અંશે બદલાઈ ગઈ છે. આપણે આપણી પહેલાની ધોરણોમાં પદાર્થના ભૌતિક અને રાસાયણિક ફેરફારો વિશે પહેલેથી જ શીખી ચૂક્યા છીએ. જ્યારે પણ રાસાયણિક ફેરફાર થાય છે, ત્યારે આપણે કહી શકીએ કે રાસાયણિક પ્રક્રિયા થઈ છે.
તમને કદાચ આશ્ચર્ય થતું હશે કે રાસાયણિક પ્રક્રિયા થવાથી ખરેખર શું અર્થ થાય છે? રાસાયણિક પ્રક્રિયા થઈ છે તે આપણે કેવી રીતે જાણી શકીએ? ચાલો આ પ્રશ્નોનો જવાબ શોધવા માટે કેટલીક પ્રવૃત્તિઓ કરીએ.
પ્રવૃત્તિ 1.1
ચેતવણી: આ પ્રવૃત્તિ માટે શિક્ષકની સહાયતા જરૂરી છે. વિદ્યાર્થીઓએ યોગ્ય આંખના ચશ્મા પહેરવા એ વધુ સારું રહેશે.
- મેગ્નેશિયમની લગભગ 3-4 સેમી લાંબી પટ્ટીને સેન્ડપેપરથી ઘસીને સાફ કરો.
- તેને ચીપિયા વડે પકડો. સ્પિરિટ લેમ્પ અથવા બર્નરનો ઉપયોગ કરીને તેને સળગાવો અને આકૃતિ 1.1 માં બતાવ્યા પ્રમાણે બનેલી રાખને વોચ-ગ્લાસમાં એકઠી કરો. મેગ્નેશિયમ પટ્ટીને તમારી આંખોથી શક્ય તેટલા દૂર રાખીને સળગાવો.
- તમે શું અવલોકન કરો છો?
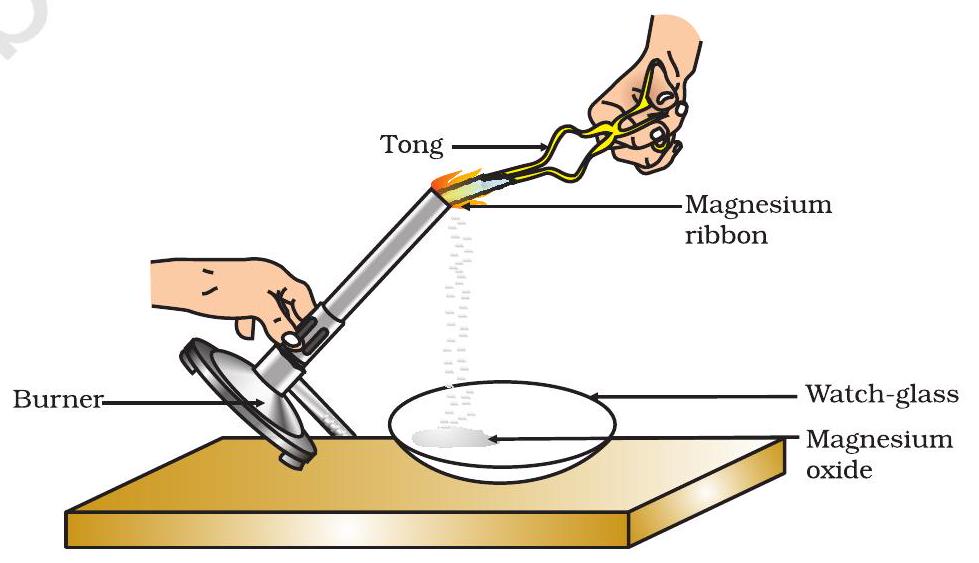
આકૃતિ 1.1
હવામાં મેગ્નેશિયમ પટ્ટીનું બળવું અને વોચ-ગ્લાસમાં મેગ્નેશિયમ ઑક્સાઇડનું એકત્રીકરણ
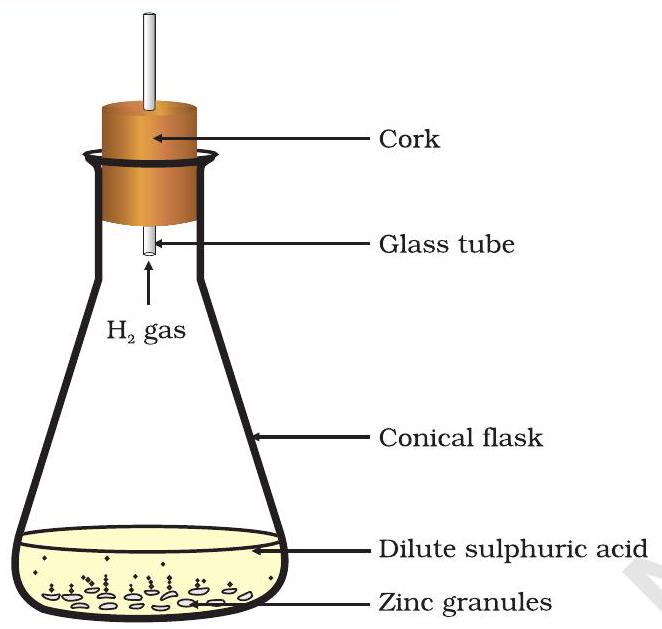
આકૃતિ 1.2 ઝિંક પર સલ્ફ્યુરિક એસિડની મંદ ક્રિયા દ્વારા હાઇડ્રોજન વાયુની રચના
તમે જોયું હશે કે મેગ્નેશિયમ પટ્ટી તેજસ્વી સફેદ જ્યોત સાથે બળે છે અને સફેદ પાવડરમાં બદલાઈ જાય છે. આ પાવડર મેગ્નેશિયમ ઑક્સાઇડ છે. તે હવામાં હાજર મેગ્નેશિયમ અને ઑક્સિજન વચ્ચેની પ્રક્રિયાને કારણે રચાય છે.
પ્રવૃત્તિ 1.2
- ટેસ્ટ ટ્યુબમાં લેડ નાઇટ્રેટનું દ્રાવણ લો.
- આમાં પોટેશિયમ આયોડાઇડનું દ્રાવણ ઉમેરો.
- તમે શું અવલોકન કરો છો?
પ્રવૃત્તિ 1.3
- કોનિકલ ફ્લાસ્ક અથવા ટેસ્ટ ટ્યુબમાં થોડા ઝિંકના દાણા લો.
- આમાં મંદ હાઇડ્રોક્લોરિક એસિડ અથવા સલ્ફ્યુરિક એસિડ ઉમેરો (આકૃતિ 1.2).
ચેતવણી: એસિડની સાવચેતીથી સંભાળ લો.
- શું તમે ઝિંકના દાણાઓની આસપાસ કંઈક થતું જોઈ રહ્યા છો?
- કોનિકલ ફ્લાસ્ક અથવા ટેસ્ટ ટ્યુબને સ્પર્શ કરો. શું તેના તાપમાનમાં કોઈ ફેરફાર છે?
ઉપરોક્ત ત્રણેય પ્રવૃત્તિઓ પરથી, આપણે કહી શકીએ કે નીચેનામાંથી કોઈ પણ અવલોકન એ રાસાયણિક પ્રક્રિયા થઈ છે કે નહીં તે નક્કી કરવામાં આપણી મદદ કરે છે –
- અવસ્થામાં ફેરફાર
- રંગમાં ફેરફાર
- વાયુનું ઉત્સર્જન
- તાપમાનમાં ફેરફાર.
આપણે આપણી આસપાસ થતા ફેરફારોનું અવલોકન કરીએ ત્યારે, આપણે જોઈ શકીએ છીએ કે આપણી આસપાસ અનેક પ્રકારની રાસાયણિક પ્રક્રિયાઓ થઈ રહી છે. આ પ્રકરણમાં આપણે વિવિધ પ્રકારની રાસાયણિક પ્રક્રિયાઓ અને તેમના પ્રતીકાત્મક નિરૂપણ વિશે અભ્યાસ કરીશું.
1.1 રાસાયણિક સમીકરણો
પ્રવૃત્તિ 1.1 નું વર્ણન આ રીતે કરી શકાય – જ્યારે મેગ્નેશિયમ પટ્ટીને ઑક્સિજનમાં બાળવામાં આવે છે, ત્યારે તે મેગ્નેશિયમ ઑક્સાઇડમાં રૂપાંતરિત થાય છે. વાક્યના સ્વરૂપમાં રાસાયણિક પ્રક્રિયાનું આ વર્ણન તદ્દન લાંબું છે. તેને ટૂંકા સ્વરૂપમાં લખી શકાય છે. આ કરવાનો સૌથી સરળ રસ્તો એ છે કે તેને શબ્દ-સમીકરણના સ્વરૂપમાં લખવું. ઉપરોક્ત પ્રક્રિયા માટે શબ્દ-સમીકરણ હશે –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
પ્રક્રિયા (1.1) માં જે પદાર્થો રાસાયણિક ફેરફાર પામે છે, મેગ્નેશિયમ અને ઑક્સિજન, તે પ્રક્રિયકો છે. નવો પદાર્થ મેગ્નેશિયમ ઑક્સાઇડ છે, જે પ્રક્રિયા દરમિયાન, ઉત્પાદ તરીકે રચાય છે.
એક શબ્દ-સમીકરણ તેમની વચ્ચે મૂકેલા તીર દ્વારા પ્રક્રિયકોનું ઉત્પાદમાં રૂપાંતર દર્શાવે છે. પ્રક્રિયકો ડાબી બાજુ (LHS) પર લખવામાં આવે છે અને તેમની વચ્ચે વત્તાનું ચિહ્ન (+) હોય છે. તે જ રીતે, ઉત્પાદ જમણી બાજુ (RHS) પર લખવામાં આવે છે અને તેમની વચ્ચે વત્તાનું ચિહ્ન (+) હોય છે. તીરનું મથાળું ઉત્પાદ તરફ નિર્દેશ કરે છે, અને પ્રક્રિયાની દિશા દર્શાવે છે.
1.1.1 રાસાયણિક સમીકરણ લખવું
શું રાસાયણિક સમીકરણોને રજૂ કરવા માટે કોઈ અન્ય ટૂંકો માર્ગ છે? જો આપણે શબ્દોને બદલે રાસાયણિક સૂત્રોનો ઉપયોગ કરીએ તો રાસાયણિક સમીકરણો વધુ સંક્ષિપ્ત અને ઉપયોગી બની શકે છે. રાસાયણિક સમીકરણ એ રાસાયણિક પ્રક્રિયાનું પ્રતિનિધિત્વ કરે છે. જો તમને મેગ્નેશિયમ, ઑક્સિજન અને મેગ્નેશિયમ ઑક્સાઇડના સૂત્રો યાદ હોય, તો ઉપરોક્ત શબ્દ-સમીકરણ આ રીતે લખી શકાય છે -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
તીરની ડાબી બાજુ (LHS) અને જમણી બાજુ (RHS) પર દરેક તત્વના અણુઓની સંખ્યા ગણો અને તુલના કરો. શું દરેક તત્વના અણુઓની સંખ્યા બંને બાજુએ સમાન છે? જો હા, તો સમીકરણ સંતુલિત છે. જો ના, તો સમીકરણ અસંતુલિત છે કારણ કે સમીકરણની બંને બાજુએ દળ સમાન નથી. આવું રાસાયણિક સમીકરણ એ પ્રક્રિયા માટેનું કંકાલ રાસાયણિક સમીકરણ છે. સમીકરણ (1.2) હવામાં મેગ્નેશિયમના બળવા માટેનું કંકાલ રાસાયણિક સમીકરણ છે.
1.1.2 સંતુલિત રાસાયણિક સમીકરણો
તમે ધોરણ IX માં અભ્યાસ કરેલા દળના સંરક્ષણના નિયમને યાદ કરો; રાસાયણિક પ્રક્રિયામાં દળ ન તો સર્જી શકાય છે અને ન તો નાશ પામી શકે છે. એટલે કે, રાસાયણિક પ્રક્રિયાના ઉત્પાદમાં હાજર તત્વોનું કુલ દળ પ્રક્રિયકોમાં હાજર તત્વોના કુલ દળ જેટલું હોવું જોઈએ.
બીજા શબ્દોમાં કહીએ તો, દરેક તત્વના અણુઓની સંખ્યા રાસાયણિક પ્રક્રિયા પહેલા અને પછી સમાન રહે છે. તેથી, આપણે કંકાલ રાસાયણિક સમીકરણને સંતુલિત કરવાની જરૂર છે. શું રાસાયણિક સમીકરણ (1.2) સંતુલિત છે? ચાલો રાસાયણિક સમીકરણને સંતુલિત કરવા વિશે પગલું દર પગલું શીખીએ.
પ્રવૃત્તિ 1.3 માટેનું શબ્દ-સમીકરણ આ રીતે રજૂ કરી શકાય છે -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
ઉપરોક્ત શબ્દ-સમીકરણ નીચેના રાસાયણિક સમીકરણ દ્વારા રજૂ કરી શકાય છે -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
ચાલો તીરની બંને બાજુએ વિવિધ તત્વોના અણુઓની સંખ્યા તપાસીએ.
| તત્વ | પ્રક્રિયકોમાં અણુઓની સંખ્યા (LHS) | ઉત્પાદમાં અણુઓની સંખ્યા (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
દરેક તત્વના અણુઓની સંખ્યા તીરની બંને બાજુએ સમાન હોવાથી, સમીકરણ (1.3) એક સંતુલિત રાસાયણિક સમીકરણ છે.
ચાલો નીચેના રાસાયણિક સમીકરણને સંતુલિત કરવાનો પ્રયાસ કરીએ -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
પગલું I: રાસાયણિક સમીકરણને સંતુલિત કરવા માટે, પ્રથમ દરેક સૂત્રની આસપાસ બોક્સ દોરો. સમીકરણને સંતુલિત કરતી વખતે બોક્સની અંદર કંઈપણ બદલશો નહીં.
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
પગલું II: અસંતુલિત સમીકરણ (1.5) માં હાજર વિવિધ તત્વોના અણુઓની સંખ્યાની યાદી બનાવો.
| તત્વ | પ્રક્રિયકોમાં અણુઓની સંખ્યા (LHS) | ઉત્પાદમાં અણુઓની સંખ્યા (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
પગલું III: સૌથી વધુ અણુઓ ધરાવતા સંયોજન સાથે સંતુલન શરૂ કરવું ઘણીવાર સુવિધાજનક હોય છે. તે પ્રક્રિયક અથવા ઉત્પાદ હોઈ શકે છે. તે સંયોજનમાં, તે તત્વ પસંદ કરો જેમાં સૌથી વધુ અણુઓ હોય. આ માપદંડનો ઉપયોગ કરીને, આપણે $Fe_3 O_4$ અને તેમાં ઑક્સિજન તત્વ પસંદ કરીએ છીએ. જમણી બાજુએ ચાર ઑક્સિજન અણુઓ છે અને ડાબી બાજુએ ફક્ત એક જ છે.
ઑક્સિજન અણુઓને સંતુલિત કરવા માટે -
| ઑક્સિજનના અણુઓ |
પ્રક્રિયકોમાં | ઉત્પાદમાં |
|---|---|---|
| (i) પ્રારંભિક | 1($ \mathrm{H_2O} $ માં) | 4($ \mathrm{Fe_3O_4} $ માં) |
| (ii) સંતુલિત કરવા માટે | 1 $\times$ 4 | 4 |
અણુઓની સંખ્યા સમાન કરવા માટે, તે યાદ રાખવું જોઈએ કે આપણે પ્રક્રિયામાં સામેલ સંયોજનો અથવા તત્વોના સૂત્રોમાં ફેરફાર કરી શકતા નથી. ઉદાહરણ તરીકે, ઑક્સિજન અણુઓને સંતુલિત કરવા માટે આપણે ગુણાંક ‘4’ $4 H_2 O$ તરીકે મૂકી શકીએ છીએ અને $H_2 O_4$ અથવા $(H_2 O)_4$ તરીકે નહીં. હવે આંશિક રીતે સંતુલિત સમીકરણ બને છે -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (આંશિક રીતે સંતુલિત સમીકરણ)
પગલું IV: Fe અને $H$ અણુઓ હજુ પણ સંતુલિત નથી. આગળ વધવા માટે આમાંથી કોઈ પણ તત્વ પસંદ કરો. ચાલો આંશિક રીતે સંતુલિત સમીકરણમાં હાઇડ્રોજન અણુઓને સંતુલિત કરીએ.
$H$ અણુઓની સંખ્યા સમાન કરવા માટે, જમણી બાજુએ હાઇડ્રોજનના અણુઓની સંખ્યા ચાર બનાવો.
| હાઇડ્રોજનના અણુઓ |
પ્રક્રિયકોમાં | ઉત્પાદમાં |
|---|---|---|
| (i) પ્રારંભિક | 8($ \mathrm{4H_2O} $ માં) | 2($ \mathrm{H_2} $ માં) |
| (ii) સંતુલિત કરવા માટે | 8 | 2 $\times$ 4 |
સમીકરણ હશે -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(આંશિક રીતે સંતુલિત સમીકરણ)
પગલું V: ઉપરોક્ત સમીકરણની તપાસ કરો અને ત્રીજું તત્વ પસંદ કરો જે સંતુલિત નથી. તમે જોશો કે ફક્ત એક જ તત્વ સંતુલિત કરવા માટે બાકી રહ્યું છે, તે છે, આયર્ન.
| આયર્નના અણુઓ | પ્રક્રિયકોમાં | ઉત્પાદમાં |
|---|---|---|
| (i) પ્રારંભિક | 1($ \mathrm{Fe} $ માં) | 3($ \mathrm{Fe_3O_4} $ માં) |
| (ii) સંતુલિત કરવા માટે | 1 $\times$ 3 | 3 |
$Fe$ ને સમાન કરવા માટે, આપણે ડાબી બાજુએ $Fe$ ના ત્રણ અણુઓ લઈએ છીએ.
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
પગલું VI: છેલ્લે, સંતુલિત સમીકરણની શુદ્ધતા તપાસવા માટે, આપણે સમીકરણની બંને બાજુએ દરેક તત્વના અણુઓ ગણીએ છીએ.
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(સંતુલિત સમીકરણ)
સમીકરણ (1.9) ની બંને બાજુએ તત્વોના અણુઓની સંખ્યા સમાન છે. આ સમીકરણ હવે સંતુલિત છે. રાસાયણિક સમીકરણોને સંતુલિત કરવાની આ પદ્ધતિને હિટ-ઍન્ડ-ટ્રાયલ પદ્ધતિ કહેવામાં આવે છે કારણ કે આપણે સૌથી નાના પૂર્ણાંક ગુણાંકનો ઉપયોગ કરીને સમીકરણને સંતુલિત કરવા માટે પ્રયાસો કરીએ છીએ.
પગલું VII: ભૌતિક અવસ્થાઓના પ્રતીકો લખવા ઉપરોક્ત સંતુલિત સમીકરણ (1.9) ને કાળજીપૂર્વક તપાસો. શું આ સમીકરણ દરેક પ્રક્રિયક અને ઉત્પાદની ભૌતિક અવસ્થા વિશે આપણને કંઈક કહે છે? આ સમીકરણમાં તેમની ભૌતિક અવસ્થાઓ વિશે કોઈ માહિતી આપવામાં આવી નથી.
રાસાયણિક સમીકરણને વધુ માહિતીપ્રદ બનાવવા માટે, પ્રક્રિયકો અને ઉત્પાદની ભૌતિક અવસ્થાઓ તેમના રાસાયણિક સૂત્રો સાથે ઉલ્લેખિત કરવામાં આવે છે. પ્રક્રિયકો અને ઉત્પાદની વાયુ, પ્રવાહી, જલીય અને ઘન અવસ્થાઓને અનુક્રમે (g), (l), (aq) અને (s) સંકેતો દ્વારા રજૂ કરવામાં આવે છે. જો પ્રક્રિયક અથવા ઉત્પાદ પાણીમાં દ્રાવણના રૂપમાં હાજર હોય તો જલીય (aq) શબ્દ લખવામાં આવે છે.
સંતુલિત સમીકરણ (1.9) બને છે
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
નોંધ લો કે પ્રતીક $(g)$ નો ઉપયોગ $H_2 O$ સાથે થાય છે જે દર્શાવે છે કે આ પ્રક્રિયામાં પાણીનો ઉપયોગ વરાળના રૂપમાં થાય છે.
સામાન્ય રીતે ભૌતિક અવસ્થાઓ રાસાયણિક સમીકરણમાં સમાવવામાં આવતી નથી જ્યાં સુધી તેમને સ્પષ્ટ કરવું જરૂરી ન હોય.
કેટલીકવાર પ્રક્રિયાની પરિસ્થિતિઓ, જેમ કે તાપમાન, દબાણ, ઉદ્દીપક, વગેરે, સમીકરણમાં તીરની ઉપર અને/અથવા નીચે સૂચવવામાં આવે છે. ઉદાહરણ તરીકે -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
આ પગલાંઓનો ઉપયોગ કરીને, શું તમે અગાઉ લખાણમાં આપેલ સમીકરણ (1.2) ને સંતુલિત કરી શકો છો?
1.2 રાસાયણિક પ્રક્રિયાઓના પ્રકારો
આપણે ધોરણ IX માં શીખ્યા છીએ કે રાસાયણિક પ્રક્રિયા દરમિયાન એક તત્વના અણુઓ બીજા તત્વના અણુઓમાં રૂપાંતરિત થતા નથી. અને ન તો અણુઓ મિશ્રણમાંથી અદૃશ્ય થાય છે અથવા બીજે ક્યાંથી પ્રગટ થાય છે. ખરેખર, રાસાયણિક પ્રક્રિયાઓમાં નવા પદાર્થો ઉત્પન્ન કરવા માટે અણુઓ વચ્ચેના બંધ તોડવા અને બનાવવાનો સમાવેશ થાય છે. તમે પ્રકરણ 3 અને 4 માં અણુઓ વચ્ચે રચાતા બંધના પ્રકારો વિશે અભ્યાસ કરશો.
1.2.1 સંયોજન પ્રક્રિયા
પ્રવૃત્તિ 1.4
- બીકરમાં થોડી માત્રામાં કેલ્શિયમ ઑક્સાઇડ અથવા ક્વિક લાઇમ લો.
- આમાં ધીમે ધીમે પાણી ઉમેરો.
- આકૃતિ 1.3 માં બતાવ્યા પ્રમાણે બીકરને સ્પર્શ કરો.
- શું તમને તાપમાનમાં કોઈ ફેરફાર થતો લાગે છે?
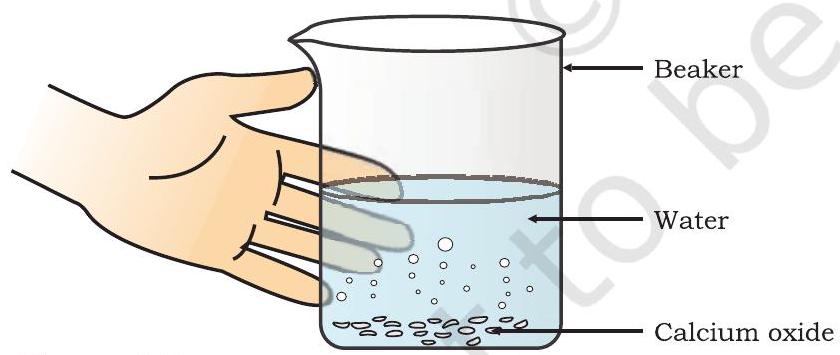
આકૃતિ 1.3 કેલ્શિયમ ઑક્સાઇડની પાણી સાથેની પ્રક્રિયા દ્વારા સ્લેક્ડ લાઇમની રચના
કેલ્શિયમ ઑક્સાઇડ પાણી સાથે જોરદાર પ્રક્રિયા કરીને સ્લેક્ડ લાઇમ (કેલ્શિયમ હાઇડ્રોક્સાઇડ) ઉત્પન્ન કરે છે અને ભારે માત્રામાં ઉષ્મા મુક્ત કરે છે.
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
આ પ્રક્રિયામાં, કેલ્શિયમ ઑક્સાઇડ અને પાણી સંયોજિત થઈને એક જ ઉત્પાદ, કેલ્શિયમ હાઇડ્રોક્સાઇડ બનાવે છે. આવી પ્રક્રિયા જેમાં બે અથવા વધુ પ્રક્રિયકોમાંથી એક જ ઉત્પાદ રચાય છે તેને સંયોજન પ્રક્રિયા તરીકે ઓળખવામાં આવે છે.
શું તમે જાણો છો?
પ્રક્રિયા 1.13 દ્વારા ઉત્પન્ન થયેલ સ્લેક્ડ લાઇમના દ્રાવણનો ઉપયોગ દિવાલો પર સફેદી કરવા માટે થાય છે. કેલ્શિયમ હાઇડ્રોક્સાઇડ હવામ











