అధ్యాయం 01 రసాయన ప్రతిచర్యలు మరియు సమీకరణాలు
ప్రతిరోజూ జరిగే కింది పరిస్థితులను పరిగణించండి మరియు ఏమి జరుగుతుందో ఆలోచించండి -
- పాలు వేసవిలో గది ఉష్ణోగ్రత వద్ద వదిలివేయబడినప్పుడు.
- ఒక ఇనుప తవా/పాన్/మేకు తేమగల వాతావరణంలో బహిర్గతంగా వదిలివేయబడినప్పుడు.
- ద్రాక్ష కిణ్వం చెందినప్పుడు.
- ఆహారం వండినప్పుడు.
- ఆహారం మన శరీరంలో జీర్ణమైనప్పుడు.
- మనం శ్వాసించినప్పుడు.
పైన పేర్కొన్న అన్ని పరిస్థితులలో, ప్రారంభ పదార్థం యొక్క స్వభావం మరియు గుర్తింపు కొంతవరకు మారిపోయాయి. మనం ఇప్పటికే మన మునుపటి తరగతులలో పదార్థం యొక్క భౌతిక మరియు రసాయన మార్పుల గురించి నేర్చుకున్నాము. ఎప్పుడైతే ఒక రసాయన మార్పు సంభవిస్తుందో, అప్పుడు ఒక రసాయన ప్రతిచర్య జరిగింది అని మనం చెప్పగలం.
రసాయన ప్రతిచర్య అంటే నిజంగా ఏమిటో మీరు ఆశ్చర్యపోతున్నారేమో. ఒక రసాయన ప్రతిచర్య జరిగిందని మనకు ఎలా తెలుస్తుంది? ఈ ప్రశ్నలకు సమాధానం కనుగొనేందుకు కొన్ని కృత్యాలను చేద్దాం.
కృత్యం 1.1
హెచ్చరిక: ఈ కృత్యానికి ఉపాధ్యాయుని సహాయం అవసరం. విద్యార్థులు తగిన కళ్లద్దాలు ధరించడం మంచిది.
- ఒక మెగ్నీషియం రిబ్బన్ సుమారు 3-4 సెం.మీ పొడవును స్మెర్గా కాగితంతో రుద్దడం ద్వారా శుభ్రం చేయండి.
- దాన్ని ఒక జత టాంగ్స్తో పట్టుకోండి. స్పిరిట్ దీపం లేదా బర్నర్ ఉపయోగించి దాన్ని కాల్చండి మరియు ఏర్పడిన బూడిదను ఫిగ్. 1.1లో చూపినట్లుగా ఒక వాచ్-గ్లాస్లో సేకరించండి. మెగ్నీషియం రిబ్బన్ను మీ కళ్ళకు వీలైనంత దూరంగా ఉంచి కాల్చండి.
- మీరు ఏమి గమనించారు?
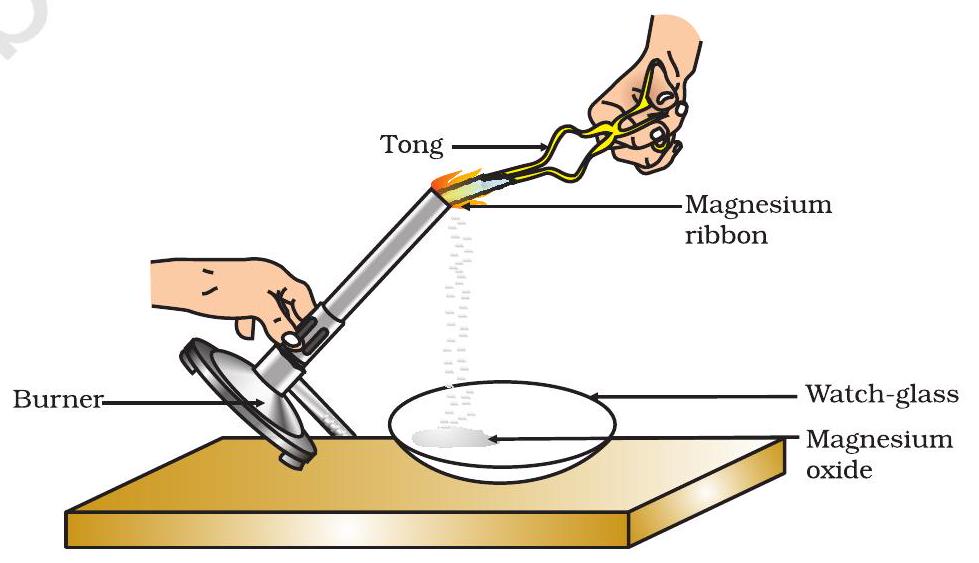
ఫిగర్ 1.1
గాలిలో మెగ్నీషియం రిబ్బన్ దహనం మరియు వాచ్-గ్లాస్లో మెగ్నీషియం ఆక్సైడ్ సేకరణ
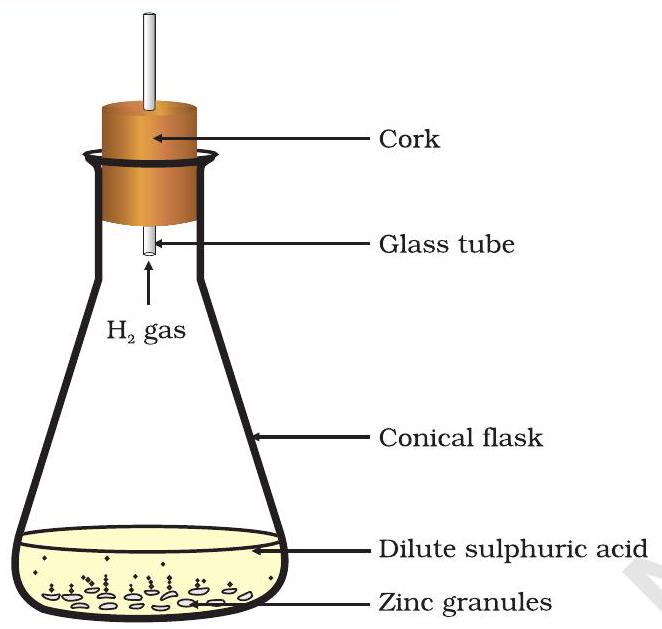
ఫిగర్ 1.2 జింక్పై సల్ఫ్యూరిక్ ఆమ్లం యొక్క చర్య ద్వారా హైడ్రోజన్ వాయువు ఏర్పడటం
మెగ్నీషియం రిబ్బన్ ఒక మెరుస్తున్న తెల్లని జ్వాలతో మండి, తెల్లటి పొడిగా మారుతుందని మీరు గమనించి ఉండాలి. ఈ పొడి మెగ్నీషియం ఆక్సైడ్. ఇది గాలిలో ఉన్న మెగ్నీషియం మరియు ఆక్సిజన్ మధ్య ప్రతిచర్య వలన ఏర్పడుతుంది.
కృత్యం 1.2
- ఒక టెస్ట్ ట్యూబ్లో లెడ్ నైట్రేట్ ద్రావణాన్ని తీసుకోండి.
- దీనికి పొటాషియం అయోడైడ్ ద్రావణాన్ని కలపండి.
- మీరు ఏమి గమనించారు?
కృత్యం 1.3
- ఒక కోనికల్ ఫ్లాస్క్ లేదా టెస్ట్ ట్యూబ్లో కొన్ని జింక్ రేణువులను తీసుకోండి.
- దీనికి సల్ఫ్యూరిక్ ఆమ్లం లేదా హైడ్రోక్లోరిక్ ఆమ్లాన్ని కలపండి (ఫిగ్. 1.2).
హెచ్చరిక: ఆమ్లాన్ని జాగ్రత్తగా నిర్వహించండి.
- జింక్ రేణువుల చుట్టూ ఏదైనా జరుగుతున్నట్లు మీరు గమనించారా?
- కోనికల్ ఫ్లాస్క్ లేదా టెస్ట్ ట్యూబ్ను తాకండి. దాని ఉష్ణోగ్రతలో ఏదైనా మార్పు ఉందా?
పై మూడు కృత్యాల నుండి, ఒక రసాయన ప్రతిచర్య జరిగిందో లేదో నిర్ణయించడంలో కింది పరిశీలనలలో ఏదైనా ఒకటి మాకు సహాయపడుతుందని మనం చెప్పగలం –
- స్థితిలో మార్పు
- రంగులో మార్పు
- వాయువు వెలువడటం
- ఉష్ణోగ్రతలో మార్పు.
మన చుట్టూ జరిగే మార్పులను మనం గమనిస్తున్నప్పుడు, మన చుట్టూ అనేక రకాల రసాయన ప్రతిచర్యలు జరుగుతున్నట్లు మనం చూడవచ్చు. ఈ అధ్యాయంలో వివిధ రకాల రసాయన ప్రతిచర్యలు మరియు వాటి ప్రతీకాత్మక ప్రాతినిధ్యం గురించి మనం అధ్యయనం చేస్తాము.
1.1 రసాయన సమీకరణాలు
కృత్యం 1.1ను ఇలా వివరించవచ్చు – మెగ్నీషియం రిబ్బన్ను ఆక్సిజన్లో కాల్చినప్పుడు, అది మెగ్నీషియం ఆక్సైడ్గా మార్చబడుతుంది. ఒక వాక్య రూపంలో రసాయన ప్రతిచర్య యొక్క ఈ వివరణ చాలా పొడవుగా ఉంటుంది. దీన్ని చిన్న రూపంలో రాయవచ్చు. దీన్ని చేయడానికి సరళమైన మార్గం దాన్ని ఒక పద-సమీకరణ రూపంలో రాయడం. పై ప్రతిచర్యకు పద-సమీకరణం ఇలా ఉంటుంది –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
ప్రతిచర్యలో (1.1) రసాయన మార్పును పొందే పదార్థాలు (మెగ్నీషియం మరియు ఆక్సిజన్) కారకాలు (రియాక్టెంట్స్). కొత్త పదార్థం మెగ్నీషియం ఆక్సైడ్, ఇది ప్రతిచర్య సమయంలో ఉత్పన్నంగా (ప్రాడక్ట్గా) ఏర్పడుతుంది.
ఒక పద-సమీకరణం కారకాల నుండి ఉత్పన్నాలకు మార్పును వాటి మధ్య ఉంచబడిన బాణం ద్వారా చూపుతుంది. కారకాలు ఎడమ వైపు (LHS) వ్రాయబడతాయి మరియు వాటి మధ్య ప్లస్ గుర్తు (+) ఉంటుంది. అదేవిధంగా, ఉత్పన్నాలు కుడి వైపు (RHS) వ్రాయబడతాయి మరియు వాటి మధ్య ప్లస్ గుర్తు (+) ఉంటుంది. బాణం యొక్క ముఖం ఉత్పన్నాల వైపు చూపుతుంది మరియు ప్రతిచర్య యొక్క దిశను చూపుతుంది.
1.1.1 రసాయన సమీకరణాన్ని రాయడం
రసాయన సమీకరణాలను సూచించడానికి మరే ఇతర చిన్న మార్గం ఉందా? పదాలకు బదులుగా రసాయన సూత్రాలను ఉపయోగిస్తే రసాయన సమీకరణాలను మరింత సంక్షిప్తంగా మరియు ఉపయోగకరంగా చేయవచ్చు. ఒక రసాయన సమీకరణం ఒక రసాయన ప్రతిచర్యను సూచిస్తుంది. మీరు మెగ్నీషియం, ఆక్సిజన్ మరియు మెగ్నీషియం ఆక్సైడ్ యొక్క సూత్రాలను గుర్తుకు తెస్తే, పై పద-సమీకరణాన్ని ఇలా రాయవచ్చు -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
LHS మరియు RHSలోని బాణం యొక్క ప్రతి మూలకం యొక్క అణువుల సంఖ్యను లెక్కించండి మరియు పోల్చండి. ప్రతి మూలకం యొక్క అణువుల సంఖ్య రెండు వైపులా ఒకేలా ఉందా? అవును అయితే, సమీకరణం సమతుల్యం చేయబడింది. లేకపోతే, సమీకరణం యొక్క రెండు వైపులా ద్రవ్యరాశి ఒకేలా లేనందున సమీకరణం సమతుల్యం చేయబడలేదు. అటువంటి రసాయన సమీకరణం ఒక ప్రతిచర్యకు అస్థిపంజర రసాయన సమీకరణం. సమీకరణం (1.2) గాలిలో మెగ్నీషియం దహనానికి అస్థిపంజర రసాయన సమీకరణం.
1.1.2 సమతుల్య రసాయన సమీకరణాలు
మీరు తరగతి IXలో చదివిన ద్రవ్యరాశి నిత్యత్వ నియమాన్ని గుర్తుకు తెచ్చుకోండి; ఒక రసాయన ప్రతిచర్యలో ద్రవ్యరాశిని సృష్టించలేము లేదా నాశనం చేయలేము. అంటే, ఒక రసాయన ప్రతిచర్య యొక్క ఉత్పన్నాలలో ఉన్న మూలకాల మొత్తం ద్రవ్యరాశి కారకాలలో ఉన్న మూలకాల మొత్తం ద్రవ్యరాశికి సమానంగా ఉండాలి.
మరో మాటలో చెప్పాలంటే, ప్రతి మూలకం యొక్క అణువుల సంఖ్య, ఒక రసాయన ప్రతిచర్యకు ముందు మరియు తర్వాత, ఒకేలా ఉంటుంది. అందువల్ల, మనం ఒక అస్థిపంజర రసాయన సమీకరణాన్ని సమతుల్యం చేయాలి. రసాయన సమీకరణం (1.2) సమతుల్యం చేయబడిందా? ఒక రసాయన సమీకరణాన్ని దశలవారీగా సమతుల్యం చేయడం గురించి తెలుసుకుందాం.
కృత్యం 1.3 కోసం పద-సమీకరణం ఇలా సూచించబడవచ్చు -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
పై పద-సమీకరణాన్ని కింది రసాయన సమీకరణం ద్వారా సూచించవచ్చు -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
బాణం యొక్క రెండు వైపులా ఉన్న వివిధ మూలకాల అణువుల సంఖ్యను పరిశీలిద్దాం.
| మూలకం | కారకాలలో అణువుల సంఖ్య (LHS) | ఉత్పన్నాలలో అణువుల సంఖ్య (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
ప్రతి మూలకం యొక్క అణువుల సంఖ్య బాణం యొక్క రెండు వైపులా ఒకేలా ఉన్నందున, సమీకరణం (1.3) ఒక సమతుల్య రసాయన సమీకరణం.
కింది రసాయన సమీకరణాన్ని సమతుల్యం చేయడానికి ప్రయత్నిద్దాం -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
దశ I: ఒక రసాయన సమీకరణాన్ని సమతుల్యం చేయడానికి, ముందుగా ప్రతి సూత్రం చుట్టూ పెట్టెలను గీయండి. సమీకరణాన్ని సమతుల్యం చేస్తున్నప్పుడు పెట్టెల లోపల ఏదీ మార్చవద్దు.
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
దశ II: అసమతుల్య సమీకరణం (1.5)లో ఉన్న వివిధ మూలకాల అణువుల సంఖ్యను జాబితా చేయండి.
| మూలకం | కారకాలలో అణువుల సంఖ్య (LHS) | ఉత్పన్నాలలో అణువుల సంఖ్య (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
దశ III: గరిష్ట సంఖ్యలో అణువులను కలిగి ఉన్న సమ్మేళనంతో సమతుల్యం చేయడం ప్రారంభించడం తరచూ సౌకర్యంగా ఉంటుంది. ఇది ఒక కారకం లేదా ఉత్పన్నం కావచ్చు. ఆ సమ్మేళనంలో, గరిష్ట సంఖ్యలో అణువులను కలిగి ఉన్న మూలకాన్ని ఎంచుకోండి. ఈ ప్రమాణాలను ఉపయోగించి, మనం $Fe_3 O_4$ మరియు దానిలోని ఆక్సిజన్ మూలకాన్ని ఎంచుకుంటాము. RHSలో నాలుగు ఆక్సిజన్ అణువులు మరియు LHSలో ఒకటి మాత్రమే ఉన్నాయి.
ఆక్సిజన్ అణువులను సమతుల్యం చేయడానికి -
| ఆక్సిజన్ యొక్క అణువులు |
కారకాలలో | ఉత్పన్నాలలో |
|---|---|---|
| (i) ప్రారంభ | 1($ \mathrm{H_2O} $ లో ) | 4($ \mathrm{Fe_3O_4} $ లో ) |
| (ii) సమతుల్యం చేయడానికి | 1 $\times$ 4 | 4 |
అణువుల సంఖ్యను సమానం చేయడానికి, ప్రతిచర్యలో పాల్గొనే సమ్మేళనాలు లేదా మూలకాల సూత్రాలను మార్చలేమని గుర్తుంచుకోవాలి. ఉదాహరణకు, ఆక్సిజన్ అణువులను సమతుల్యం చేయడానికి మనం ‘4’ గుణకాన్ని $4 H_2 O$గా ఉంచవచ్చు, కానీ $H_2 O_4$ లేదా $(H_2 O)_4$గా కాదు. ఇప్పుడు పాక్షికంగా సమతుల్యం చేయబడిన సమీకరణం ఇలా అవుతుంది -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (పాక్షికంగా సమతుల్యం చేయబడిన సమీకరణం)
దశ IV: Fe మరియు $H$ అణువులు ఇంకా సమతుల్యం చేయబడలేదు. మరింత ముందుకు సాగడానికి ఈ మూలకాలలో దేనినైనా ఎంచుకోండి. పాక్షికంగా సమతుల్యం చేయబడిన సమీకరణంలో హైడ్రోజన్ అణువులను సమతుల్యం చేద్దాం.
$H$ అణువుల సంఖ్యను సమానం చేయడానికి, RHSలో హైడ్రోజన్ అణువుల సంఖ్యను నాలుగుగా చేయండి.
| హైడ్రోజన్ యొక్క అణువులు |
కారకాలలో | ఉత్పన్నాలలో |
|---|---|---|
| (i) ప్రారంభ | 8($ \mathrm{4H_2O} $ లో ) | 2($ \mathrm{H_2} $ లో ) |
| (ii) సమతుల్యం చేయడానికి | 8 | 2 $\times$ 4 |
సమీకరణం ఇలా ఉంటుంది -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(పాక్షికంగా సమతుల్యం చేయబడిన సమీకరణం)
దశ V: పై సమీకరణాన్ని పరిశీలించండి మరియు సమతుల్యం చేయబడని మూడవ మూలకాన్ని ఎంచుకోండి. ఒక మూలకం మాత్రమే సమతుల్యం చేయడానికి మిగిలి ఉందని మీరు కనుగొంటారు, అది ఇనుము.
| ఇనుము యొక్క అణువులు | కారకాలలో | ఉత్పన్నాలలో |
|---|---|---|
| (i) ప్రారంభ | 1($ \mathrm{Fe} $ లో ) | 3($ \mathrm{Fe_3O_4} $ లో ) |
| (ii) సమతుల్యం చేయడానికి | 1 $\times$ 3 | 3 |
$Fe$ని సమానం చేయడానికి, మనం LHSలో $Fe$ యొక్క మూడు అణువులను తీసుకుంటాము.
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
దశ VI: చివరగా, సమతుల్యం చేయబడిన సమీకరణం యొక్క ఖచ్చితత్వాన్ని తనిఖీ చేయడానికి, మనం సమీకరణం యొక్క రెండు వైపులా ఉన్న ప్రతి మూలకం యొక్క అణువులను లెక్కిస్తాము.
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(సమతుల్యం చేయబడిన సమీకరణం)
సమీకరణం (1.9) యొక్క రెండు వైపులా ఉన్న మూలకాల అణువుల సంఖ్యలు సమానంగా ఉన్నాయి. ఈ సమీకరణం ఇప్పుడు సమతుల్యం చేయబడింది. రసాయన సమీకరణాలను సమతుల్యం చేయడానికి ఈ పద్ధతిని హిట్-అండ్-ట్రయల్ పద్ధతి అంటారు, ఎందుకంటే మనం చిన్న పూర్ణాంక గుణకాన్ని ఉపయోగించి సమీకరణాన్ని సమతుల్యం చేయడానికి ప్రయత్నాలు చేస్తాము.
దశ VII: భౌతిక స్థితుల గుర్తులను రాయడం పై సమతుల్యం చేయబడిన సమీకరణం (1.9)ని జాగ్రత్తగా పరిశీలించండి. ఈ సమీకరణం ప్రతి కారకం మరియు ఉత్పన్నం యొక్క భౌతిక స్థితి గురించి మాకు ఏదైనా చెబుతుందా? వాటి భౌతిక స్థితుల గురించి ఈ సమీకరణంలో ఎటువంటి సమాచారం ఇవ్వబడలేదు.
ఒక రసాయన సమీకరణాన్ని మరింత సమాచారప్రదంగా చేయడానికి, కారకాలు మరియు ఉత్పన్నాల భౌతిక స్థితులు వాటి రసాయన సూత్రాలతో పాటు పేర్కొనబడతాయి. కారకాలు మరియు ఉత్పన్నాల వాయు, ద్రవ, జలద్రావణ మరియు ఘన స్థితులు వరుసగా (g), (l), (aq) మరియు (s) సంకేతాల ద్వారా సూచించబడతాయి. కారకం లేదా ఉత్పన్నం నీటిలో ద్రావణంగా ఉంటే జలద్రావణ (aq) అనే పదం వ్రాయబడుతుంది.
సమతుల్యం చేయబడిన సమీకరణం (1.9) అవుతుంది
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
$(g)$ గుర్తు $H_2 O$తో ఉపయోగించబడిందని గమనించండి, ఈ ప్రతిచర్యలో నీరు ఆవిరి రూపంలో ఉపయోగించబడుతుందని సూచించడానికి.
సాధారణంగా భౌతిక స్థితులు రసాయన సమీకరణంలో చేర్చబడవు, వాటిని పేర్కొనడం అవసరం కానప్పుడు.
కొన్నిసార్లు ప్రతిచర్య కోసం ఉష్ణోగ్రత, పీడనం, ఉత్ప్రేరకం మొదలైన ప్రతిచర్య పరిస్థితులు సమీకరణంలో బాణం పైన మరియు/లేదా క్రింద సూచించబడతాయి. ఉదాహరణకు -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
ఈ దశలను ఉపయోగించి, మీరు ముందు వచ్చిన పాఠంలో ఇవ్వబడిన సమీకరణం (1.2)ని సమతుల్యం చేయగలరా?
1.2 రసాయన ప్రతిచర్యల రకాలు
తరగతి IXలో మనం నేర్చుకున్నట్లుగా, ఒక రసాయన ప్రతిచర్య సమయంలో ఒక మూలకం యొక్క అణువులు మరొక మూలకం యొక్క అణువులుగా మారవు. అణువులు మిశ్రమం నుండి అదృశ్యం కావు లేదా మరెక్కడనో కనిపించవు. వాస్తవానికి, రసాయన ప్రతిచర్యలు కొత్త పదార్థాలను ఉత్పత్తి చేయడానికి అణువుల మధ్య బంధాలు విచ్ఛిన్నం మరియు ఏర్పడటాన్ని కలిగి ఉంటాయి. మీరు అధ్యాయాలు 3 మరియు 4లో అణువుల మధ్య ఏర్పడే బంధాల రకాల గురించి అధ్యయనం చేస్తారు.
1.2.1 సంయోగ ప్రతిచర్య
కృత్యం 1.4
- ఒక బీకర్లో కొంచెం కాల్షియం ఆక్సైడ్ లేదా క్విక్ లైమ్ తీసుకోండి.
- దీనికి నీటిని నెమ్మదిగా కలపండి.
- ఫిగ్. 1.3లో చూపినట్లుగా బీకర్ను తాకండి.
- ఉష్ణోగ్రతలో ఏదైనా మార్పు మీరు అనుభవిస్తున్నారా?
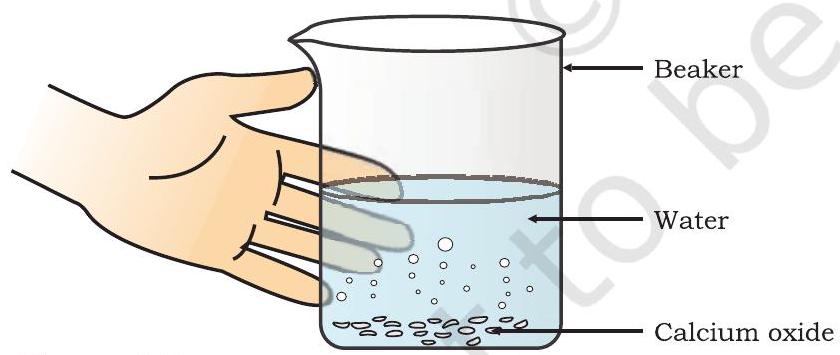
ఫిగర్ 1.3 కాల్షియం ఆక్సైడ్ మరియు నీటి ప్రతిచర్య ద్వారా స్లేక్డ్ లైమ్ ఏర్పడటం
కాల్షియం ఆక్సైడ్ నీటితో తీవ్రంగా చర్య జరిపి స్లేక్డ్ లైమ్ (కాల్షియం హైడ్రాక్సైడ్) ఉత్పత్తి చేస్తుంది, ఇది ఎక్కువ మొత్తంలో వేడిని విడుదల చేస్తుంది.
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
ఈ ప్రతిచర్యలో, కాల్షియం ఆక్సైడ్ మరియు నీరు కలిసి ఒకే ఉత్పన్నం, కాల్షియం హైడ్రాక్సైడ్ను ఏర్పరుస్తాయి. రెండు లేదా అంతకంటే ఎక్కువ కారకాల నుండి ఒకే ఉత్పన్నం ఏర్పడే అటువంటి ప్రతిచర్యను సంయోగ ప్రతిచర్య అంటారు.
మీకు తెలుసా?
ప్రతిచర్య 1.13 ద్వారా ఉత్పత్తి చేయబడిన స్లేక్డ్ లైమ్ ద్రావణం గోడలకు తెల్లని రంగు వేయడానికి ఉపయోగించబడుతుంది. కాల్షియం హైడ్రాక్సైడ్ గాలిలోని కార్బన్ డయాక్సైడ్తో నెమ్మదిగా చర్య జరిపి గోడలపై కాల్షియం కార్బోనేట్ యొక్క సన్నని పొరను ఏర్పరుస్తుంది. కాల్షియం కార్బోనేట్ తెల్లని రంగు వేసిన రెండు నుండి మూడు రోజుల తర్వాత ఏర్పడుతుంది మరియు గోడలకు మెరిసే పూతను ఇస్తుంది. పాలరాయి యొక్క రసాయన సూత్రం కూడా $CaCO_3$ అని తెలుసుకోవడం ఆసక్తికరంగా ఉంటుంది.
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
సంయోగ ప్రతిచర్యల యొక్క మరికొన్ని ఉదాహరణలను చర్చిద్దాం.
(i) బొగ్గు దహనం
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ మరియు $O_2(g)$ నుండి నీటి ఏర్పడటం
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$











