ಅಧ್ಯಾಯ 01 ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳು ಮತ್ತು ಸಮೀಕರಣಗಳು
ಕೆಳಗಿನ ದೈನಂದಿನ ಜೀವನದ ಪರಿಸ್ಥಿತಿಗಳನ್ನು ಪರಿಗಣಿಸಿ ಮತ್ತು ಏನಾಗುತ್ತದೆ ಎಂದು ಯೋಚಿಸಿ -
- ಹಾಲನ್ನು ಬೇಸಿಗೆಯಲ್ಲಿ ಕೋಣೆಯ ತಾಪಮಾನದಲ್ಲಿ ಬಿಟ್ಟರೆ.
- ಕಬ್ಬಿಣದ ತವಾ/ಪಾತ್ರೆ/ಆಣಿಯನ್ನು ಆರ್ದ್ರ ವಾತಾವರಣದಲ್ಲಿ ಬಿಟ್ಟರೆ.
- ದ್ರಾಕ್ಷಿ ಹುದುಗಿದಾಗ.
- ಆಹಾರವನ್ನು ಬೇಯಿಸಿದಾಗ.
- ಆಹಾರವು ನಮ್ಮ ದೇಹದಲ್ಲಿ ಜೀರ್ಣವಾದಾಗ.
- ನಾವು ಉಸಿರಾಡಿದಾಗ.
ಮೇಲಿನ ಎಲ್ಲಾ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಆರಂಭಿಕ ವಸ್ತುವಿನ ಸ್ವರೂಪ ಮತ್ತು ಗುರುತು ಸ್ವಲ್ಪಮಟ್ಟಿಗೆ ಬದಲಾಗಿದೆ. ನಮ್ಮ ಹಿಂದಿನ ತರಗತಿಗಳಲ್ಲಿ ನಾವು ಈಗಾಗಲೇ ವಸ್ತುವಿನ ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ಬದಲಾವಣೆಗಳ ಬಗ್ಗೆ ಕಲಿತಿದ್ದೇವೆ. ಯಾವಾಗಲೂ ರಾಸಾಯನಿಕ ಬದಲಾವಣೆ ಸಂಭವಿಸಿದಾಗ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ ನಡೆದಿದೆ ಎಂದು ನಾವು ಹೇಳಬಹುದು.
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ ಎಂದರೆ ನಿಜವಾಗಿ ಏನು ಎಂಬುದರ ಬಗ್ಗೆ ನೀವು ಬಹುಶಃ ಯೋಚಿಸುತ್ತಿರಬಹುದು. ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ ನಡೆದಿದೆ ಎಂದು ನಮಗೆ ಹೇಗೆ ತಿಳಿಯುತ್ತದೆ? ಈ ಪ್ರಶ್ನೆಗಳಿಗೆ ಉತ್ತರ ಕಂಡುಹಿಡಿಯಲು ಕೆಲವು ಚಟುವಟಿಕೆಗಳನ್ನು ಮಾಡೋಣ.
ಚಟುವಟಿಕೆ 1.1
ಎಚ್ಚರಿಕೆ: ಈ ಚಟುವಟಿಕೆಗೆ ಶಿಕ್ಷಕರ ಸಹಾಯ ಅಗತ್ಯವಿದೆ. ವಿದ್ಯಾರ್ಥಿಗಳು ಸೂಕ್ತ ಕನ್ನಡಕಗಳನ್ನು ಧರಿಸಿದರೆ ಉತ್ತಮ.
- ಸುಮಾರು 3-4 ಸೆಂ.ಮೀ. ಉದ್ದದ ಮೆಗ್ನೀಸಿಯಂ ಪಟ್ಟಿಯನ್ನು ಸ್ಯಾಂಡ್ಪೇಪರ್ನಿಂದ ಉಜ್ಜಿ ಸ್ವಚ್ಛಗೊಳಿಸಿ.
- ಒಂದು ಚಿಮುಟದಿಂದ ಅದನ್ನು ಹಿಡಿದುಕೊಳ್ಳಿ. ಸ್ಪಿರಿಟ್ ದೀಪ ಅಥವಾ ಬರ್ನರ್ ಬಳಸಿ ಅದನ್ನು ಸುಡಿ ಮತ್ತು ಉಂಟಾದ ಬೂದಿಯನ್ನು ವಾಚ್-ಗ್ಲಾಸ್ನಲ್ಲಿ ಸಂಗ್ರಹಿಸಿ (ಚಿತ್ರ 1.1 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ). ಮೆಗ್ನೀಸಿಯಂ ಪಟ್ಟಿಯನ್ನು ನಿಮ್ಮ ಕಣ್ಣುಗಳಿಂದ ಸಾಧ್ಯವಾದಷ್ಟು ದೂರವಾಗಿ ಇರಿಸಿ ಸುಡಿ.
- ನೀವು ಏನು ಗಮನಿಸುತ್ತೀರಿ?
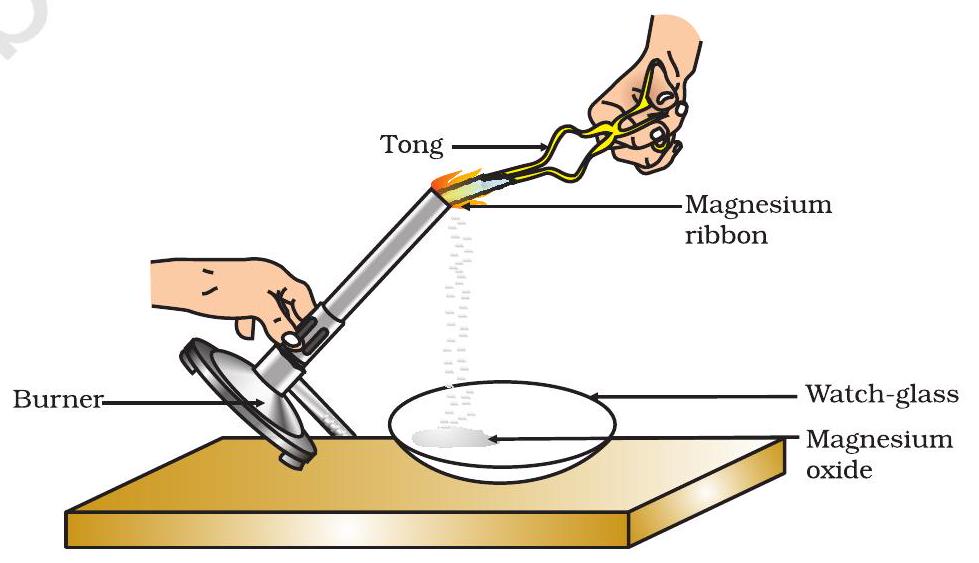
ಚಿತ್ರ 1.1
ಗಾಳಿಯಲ್ಲಿ ಮೆಗ್ನೀಸಿಯಂ ಪಟ್ಟಿಯನ್ನು ಸುಡುವುದು ಮತ್ತು ವಾಚ್-ಗ್ಲಾಸ್ನಲ್ಲಿ ಮೆಗ್ನೀಸಿಯಂ ಆಕ್ಸೈಡ್ ಸಂಗ್ರಹಿಸುವುದು
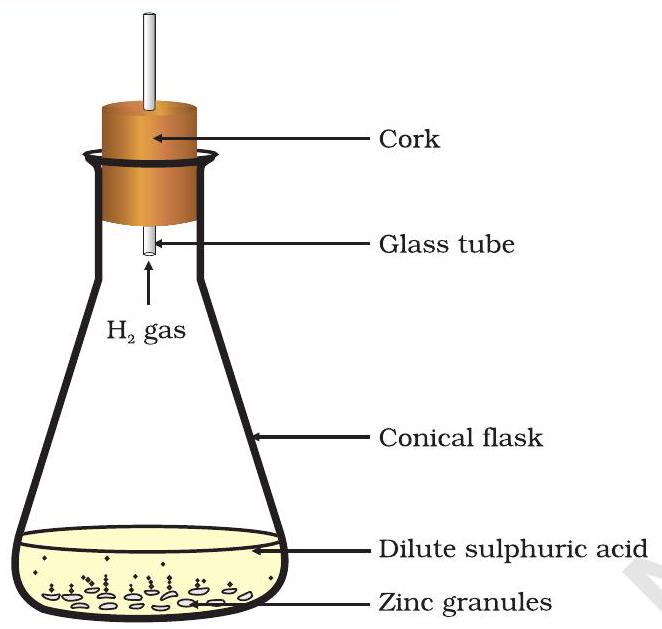
ಚಿತ್ರ 1.2 ಸತುವಿನ ಮೇಲೆ ದುರ್ಬಲ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದ ಕ್ರಿಯೆಯಿಂದ ಹೈಡ್ರೋಜನ್ ಅನಿಲದ ರಚನೆ
ಮೆಗ್ನೀಸಿಯಂ ಪಟ್ಟಿಯು ಪ್ರಕಾಶಮಾನವಾದ ಬಿಳಿ ಜ್ವಾಲೆಯೊಂದಿಗೆ ಸುಡುತ್ತದೆ ಮತ್ತು ಬಿಳಿ ಪುಡಿಯಾಗಿ ಬದಲಾಗುತ್ತದೆ ಎಂದು ನೀವು ಗಮನಿಸಿರಬೇಕು. ಈ ಪುಡಿಯು ಮೆಗ್ನೀಸಿಯಂ ಆಕ್ಸೈಡ್ ಆಗಿದೆ. ಇದು ಗಾಳಿಯಲ್ಲಿ ಇರುವ ಮೆಗ್ನೀಸಿಯಂ ಮತ್ತು ಆಮ್ಲಜನಕದ ನಡುವಿನ ಕ್ರಿಯೆಯಿಂದ ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
ಚಟುವಟಿಕೆ 1.2
- ಒಂದು ಟೆಸ್ಟ್ ಟ್ಯೂಬ್ನಲ್ಲಿ ಲೆಡ್ ನೈಟ್ರೇಟ್ ದ್ರಾವಣ ತೆಗೆದುಕೊಳ್ಳಿ.
- ಇದಕ್ಕೆ ಪೊಟ್ಯಾಸಿಯಂ ಅಯೊಡೈಡ್ ದ್ರಾವಣ ಸೇರಿಸಿ.
- ನೀವು ಏನು ಗಮನಿಸುತ್ತೀರಿ?
ಚಟುವಟಿಕೆ 1.3
- ಒಂದು ಕೋನೀಯ ಫ್ಲಾಸ್ಕ್ ಅಥವಾ ಟೆಸ್ಟ್ ಟ್ಯೂಬ್ನಲ್ಲಿ ಕೆಲವು ಸತು ಕಣಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ.
- ಇದಕ್ಕೆ ದುರ್ಬಲ ಹೈಡ್ರೋಕ್ಲೋರಿಕ್ ಆಮ್ಲ ಅಥವಾ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲ ಸೇರಿಸಿ (ಚಿತ್ರ 1.2).
ಎಚ್ಚರಿಕೆ: ಆಮ್ಲವನ್ನು ಜಾಗರೂಕತೆಯಿಂದ ನಿಭಾಯಿಸಿ.
- ಸತು ಕಣಗಳ ಸುತ್ತಲೂ ಏನಾದರೂ ನಡೆಯುತ್ತಿದೆಯೇ ಎಂದು ನೀವು ಗಮನಿಸುತ್ತೀರಾ?
- ಕೋನೀಯ ಫ್ಲಾಸ್ಕ್ ಅಥವಾ ಟೆಸ್ಟ್ ಟ್ಯೂಬ್ ಅನ್ನು ಮುಟ್ಟಿ. ಅದರ ತಾಪಮಾನದಲ್ಲಿ ಯಾವುದೇ ಬದಲಾವಣೆ ಇದೆಯೇ?
ಮೇಲಿನ ಮೂರು ಚಟುವಟಿಕೆಗಳಿಂದ, ಈ ಕೆಳಗಿನ ಯಾವುದೇ ಅವಲೋಕನಗಳು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ ನಡೆದಿದೆಯೇ ಎಂದು ನಿರ್ಧರಿಸಲು ನಮಗೆ ಸಹಾಯ ಮಾಡುತ್ತದೆ ಎಂದು ನಾವು ಹೇಳಬಹುದು –
- ಸ್ಥಿತಿಯಲ್ಲಿ ಬದಲಾವಣೆ
- ಬಣ್ಣದಲ್ಲಿ ಬದಲಾವಣೆ
- ಅನಿಲದ ವಿಕಸನ
- ತಾಪಮಾನದಲ್ಲಿ ಬದಲಾವಣೆ.
ನಮ್ಮ ಸುತ್ತಲೂ ನಡೆಯುವ ಬದಲಾವಣೆಗಳನ್ನು ನಾವು ಗಮನಿಸಿದಂತೆ, ನಮ್ಮ ಸುತ್ತಲೂ ನಡೆಯುತ್ತಿರುವ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ವೈವಿಧ್ಯಮಯ ಸಮೂಹವಿದೆ ಎಂದು ನಾವು ನೋಡಬಹುದು. ಈ ಅಧ್ಯಾಯದಲ್ಲಿ ವಿವಿಧ ರೀತಿಯ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳು ಮತ್ತು ಅವುಗಳ ಸಂಕೇತಾತ್ಮಕ ನಿರೂಪಣೆಯ ಬಗ್ಗೆ ನಾವು ಅಧ್ಯಯನ ಮಾಡುತ್ತೇವೆ.
1.1 ರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳು
ಚಟುವಟಿಕೆ 1.1 ಅನ್ನು ಈ ರೀತಿ ವಿವರಿಸಬಹುದು – ಮೆಗ್ನೀಸಿಯಂ ಪಟ್ಟಿಯನ್ನು ಆಮ್ಲಜನಕದಲ್ಲಿ ಸುಡುವಾಗ, ಅದು ಮೆಗ್ನೀಸಿಯಂ ಆಕ್ಸೈಡ್ ಆಗಿ ಪರಿವರ್ತನೆಗೊಳ್ಳುತ್ತದೆ. ವಾಕ್ಯ ರೂಪದಲ್ಲಿ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಈ ವಿವರಣೆ ಸಾಕಷ್ಟು ಉದ್ದವಾಗಿದೆ. ಇದನ್ನು ಸಂಕ್ಷಿಪ್ತ ರೂಪದಲ್ಲಿ ಬರೆಯಬಹುದು. ಇದನ್ನು ಮಾಡಲು ಸರಳವಾದ ಮಾರ್ಗವೆಂದರೆ ಅದನ್ನು ಪದ-ಸಮೀಕರಣದ ರೂಪದಲ್ಲಿ ಬರೆಯುವುದು. ಮೇಲಿನ ಕ್ರಿಯೆಗೆ ಪದ-ಸಮೀಕರಣವು ಹೀಗಿರುತ್ತದೆ –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
ಕ್ರಿಯೆಯಲ್ಲಿ (1.1) ರಾಸಾಯನಿಕ ಬದಲಾವಣೆಗೆ ಒಳಗಾಗುವ ವಸ್ತುಗಳು (ಮೆಗ್ನೀಸಿಯಂ ಮತ್ತು ಆಮ್ಲಜನಕ) ಕ್ರಿಯಾಜನಕಗಳು. ಹೊಸ ವಸ್ತುವು ಮೆಗ್ನೀಸಿಯಂ ಆಕ್ಸೈಡ್, ಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ ರೂಪುಗೊಂಡು, ಉತ್ಪನ್ನವಾಗಿದೆ.
ಪದ-ಸಮೀಕರಣವು ಕ್ರಿಯಾಜನಕಗಳಿಂದ ಉತ್ಪನ್ನಗಳಿಗೆ ಬದಲಾವಣೆಯನ್ನು ಅವುಗಳ ನಡುವೆ ಇರಿಸಲಾದ ಬಾಣದ ಮೂಲಕ ತೋರಿಸುತ್ತದೆ. ಕ್ರಿಯಾಜನಕಗಳನ್ನು ಎಡಭಾಗದಲ್ಲಿ (LHS) ಬರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಅವುಗಳ ನಡುವೆ ಜೊತೆಗೆ (+) ಚಿಹ್ನೆ ಇರುತ್ತದೆ. ಅದೇ ರೀತಿ, ಉತ್ಪನ್ನಗಳನ್ನು ಬಲಭಾಗದಲ್ಲಿ (RHS) ಬರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಅವುಗಳ ನಡುವೆ ಜೊತೆಗೆ (+) ಚಿಹ್ನೆ ಇರುತ್ತದೆ. ಬಾಣದ ತಲೆಯು ಉತ್ಪನ್ನಗಳ ಕಡೆಗೆ ತೋರಿಸುತ್ತದೆ ಮತ್ತು ಕ್ರಿಯೆಯ ದಿಕ್ಕನ್ನು ತೋರಿಸುತ್ತದೆ.
1.1.1 ರಾಸಾಯನಿಕ ಸಮೀಕರಣ ಬರೆಯುವುದು
ರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳನ್ನು ಪ್ರತಿನಿಧಿಸಲು ಬೇರೆ ಯಾವುದೇ ಸಂಕ್ಷಿಪ್ತ ಮಾರ್ಗವಿದೆಯೇ? ನಾವು ಪದಗಳ ಬದಲು ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳನ್ನು ಬಳಸಿದರೆ ರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳನ್ನು ಹೆಚ್ಚು ಸಂಕ್ಷಿಪ್ತ ಮತ್ತು ಉಪಯುಕ್ತವಾಗಿ ಮಾಡಬಹುದು. ರಾಸಾಯನಿಕ ಸಮೀಕರಣವು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತದೆ. ನೀವು ಮೆಗ್ನೀಸಿಯಂ, ಆಮ್ಲಜನಕ ಮತ್ತು ಮೆಗ್ನೀಸಿಯಂ ಆಕ್ಸೈಡ್ನ ಸೂತ್ರಗಳನ್ನು ನೆನಪಿಸಿಕೊಂಡರೆ, ಮೇಲಿನ ಪದ-ಸಮೀಕರಣವನ್ನು ಈ ರೀತಿ ಬರೆಯಬಹುದು -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
ಬಾಣದ ಎಡಭಾಗ (LHS) ಮತ್ತು ಬಲಭಾಗದಲ್ಲಿ (RHS) ಪ್ರತಿ ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಎಣಿಸಿ ಮತ್ತು ಹೋಲಿಕೆ ಮಾಡಿ. ಪ್ರತಿ ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ ಎರಡೂ ಬದಿಗಳಲ್ಲಿ ಒಂದೇ ಆಗಿದೆಯೇ? ಹೌದು ಎಂದಾದರೆ, ಸಮೀಕರಣವು ಸಮತೋಲಿತವಾಗಿದೆ. ಇಲ್ಲವಾದರೆ, ಸಮೀಕರಣದ ಎರಡೂ ಬದಿಗಳಲ್ಲಿ ದ್ರವ್ಯರಾಶಿ ಒಂದೇ ಆಗಿಲ್ಲದ ಕಾರಣ ಸಮೀಕರಣವು ಸಮತೋಲಿತವಾಗಿಲ್ಲ. ಅಂತಹ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವು ಕ್ರಿಯೆಗೆ ಅಸ್ಥಿಪಂಜರ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವಾಗಿದೆ. ಸಮೀಕರಣ (1.2) ಗಾಳಿಯಲ್ಲಿ ಮೆಗ್ನೀಸಿಯಂ ಸುಡುವಿಕೆಗೆ ಅಸ್ಥಿಪಂಜರ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವಾಗಿದೆ.
1.1.2 ಸಮತೋಲಿತ ರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳು
ನೀವು IX ನೇ ತರಗತಿಯಲ್ಲಿ ಅಧ್ಯಯನ ಮಾಡಿದ ದ್ರವ್ಯರಾಶಿಯ ಸಂರಕ್ಷಣಾ ನಿಯಮವನ್ನು ನೆನಪಿಸಿಕೊಳ್ಳಿ; ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯಲ್ಲಿ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಸೃಷ್ಟಿಸಲಾಗುವುದಿಲ್ಲ ಅಥವಾ ನಾಶಪಡಿಸಲಾಗುವುದಿಲ್ಲ. ಅಂದರೆ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಇರುವ ಮೂಲಧಾತುಗಳ ಒಟ್ಟು ದ್ರವ್ಯರಾಶಿಯು ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ ಇರುವ ಮೂಲಧಾತುಗಳ ಒಟ್ಟು ದ್ರವ್ಯರಾಶಿಗೆ ಸಮನಾಗಿರಬೇಕು.
ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಪ್ರತಿ ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗೆ ಮೊದಲು ಮತ್ತು ನಂತರ, ಒಂದೇ ಆಗಿರುತ್ತದೆ. ಆದ್ದರಿಂದ, ನಾವು ಅಸ್ಥಿಪಂಜರ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವನ್ನು ಸಮತೋಲಿಸಬೇಕಾಗುತ್ತದೆ. ರಾಸಾಯನಿಕ ಸಮೀಕರಣ (1.2) ಸಮತೋಲಿತವಾಗಿದೆಯೇ? ರಾಸಾಯನಿಕ ಸಮೀಕರಣವನ್ನು ಹಂತ ಹಂತವಾಗಿ ಸಮತೋಲಿಸುವುದನ್ನು ಕಲಿಯೋಣ.
ಚಟುವಟಿಕೆ 1.3 ಗಾಗಿ ಪದ-ಸಮೀಕರಣವನ್ನು ಈ ರೀತಿ ಪ್ರತಿನಿಧಿಸಬಹುದು -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
ಮೇಲಿನ ಪದ-ಸಮೀಕರಣವನ್ನು ಈ ಕೆಳಗಿನ ರಾಸಾಯನಿಕ ಸಮೀಕರಣದಿಂದ ಪ್ರತಿನಿಧಿಸಬಹುದು -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
ಬಾಣದ ಎರಡೂ ಬದಿಗಳಲ್ಲಿ ವಿವಿಧ ಮೂಲಧಾತುಗಳ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಪರೀಕ್ಷಿಸೋಣ.
| ಮೂಲಧಾತು | ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ (LHS) | ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
ಪ್ರತಿ ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ ಬಾಣದ ಎರಡೂ ಬದಿಗಳಲ್ಲಿ ಒಂದೇ ಆಗಿರುವುದರಿಂದ, ಸಮೀಕರಣ (1.3) ಸಮತೋಲಿತ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವಾಗಿದೆ.
ಕೆಳಗಿನ ರಾಸಾಯನಿಕ ಸಮೀಕರಣವನ್ನು ಸಮತೋಲಿಸಲು ಪ್ರಯತ್ನಿಸೋಣ -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
ಹಂತ I: ರಾಸಾಯನಿಕ ಸಮೀಕರಣವನ್ನು ಸಮತೋಲಿಸಲು, ಮೊದಲು ಪ್ರತಿ ಸೂತ್ರದ ಸುತ್ತಲೂ ಪೆಟ್ಟಿಗೆಗಳನ್ನು ಎಳೆಯಿರಿ. ಸಮೀಕರಣವನ್ನು ಸಮತೋಲಿಸುವಾಗ ಪೆಟ್ಟಿಗೆಗಳ ಒಳಗಿನ ಯಾವುದನ್ನೂ ಬದಲಾಯಿಸಬೇಡಿ.
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
ಹಂತ II: ಸಮತೋಲಿತವಲ್ಲದ ಸಮೀಕರಣದಲ್ಲಿ (1.5) ಇರುವ ವಿವಿಧ ಮೂಲಧಾತುಗಳ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಪಟ್ಟಿ ಮಾಡಿ.
| ಮೂಲಧಾತು | ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ (LHS) | ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
ಹಂತ III: ಗರಿಷ್ಠ ಸಂಖ್ಯೆಯ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಸಂಯುಕ್ತದೊಂದಿಗೆ ಸಮತೋಲಿಸಲು ಪ್ರಾರಂಭಿಸುವುದು ಸಾಮಾನ್ಯವಾಗಿ ಅನುಕೂಲಕರವಾಗಿರುತ್ತದೆ. ಅದು ಕ್ರಿಯಾಜನಕ ಅಥವಾ ಉತ್ಪನ್ನವಾಗಿರಬಹುದು. ಆ ಸಂಯುಕ್ತದಲ್ಲಿ, ಗರಿಷ್ಠ ಸಂಖ್ಯೆಯ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಮೂಲಧಾತುವನ್ನು ಆಯ್ಕೆ ಮಾಡಿ. ಈ ಮಾನದಂಡಗಳನ್ನು ಬಳಸಿ, ನಾವು $Fe_3 O_4$ ಮತ್ತು ಅದರಲ್ಲಿನ ಆಮ್ಲಜನಕ ಮೂಲಧಾತುವನ್ನು ಆಯ್ಕೆ ಮಾಡುತ್ತೇವೆ. ಬಲಭಾಗದಲ್ಲಿ (RHS) ನಾಲ್ಕು ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳಿವೆ ಮತ್ತು ಎಡಭಾಗದಲ್ಲಿ (LHS) ಕೇವಲ ಒಂದು ಮಾತ್ರ ಇದೆ.
ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳನ್ನು ಸಮತೋಲಿಸಲು -
| ಆಮ್ಲಜನಕದ ಪರಮಾಣುಗಳು |
ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ | ಉತ್ಪನ್ನಗಳಲ್ಲಿ |
|---|---|---|
| (i) ಆರಂಭಿಕ | 1($ \mathrm{H_2O} $ ನಲ್ಲಿ) | 4($ \mathrm{Fe_3O_4} $ ನಲ್ಲಿ) |
| (ii) ಸಮತೋಲಿಸಲು | 1 $\times$ 4 | 4 |
ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಸಮಾನಗೊಳಿಸಲು, ಕ್ರಿಯೆಗಳಲ್ಲಿ ಭಾಗವಹಿಸುವ ಸಂಯುಕ್ತಗಳು ಅಥವಾ ಮೂಲಧಾತುಗಳ ಸೂತ್ರಗಳನ್ನು ನಾವು ಬದಲಾಯಿಸಲು ಸಾಧ್ಯವಿಲ್ಲ ಎಂಬುದನ್ನು ನೆನಪಿನಲ್ಲಿಡಬೇಕು. ಉದಾಹರಣೆಗೆ, ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳನ್ನು ಸಮತೋಲಿಸಲು ನಾವು ಗುಣಾಂಕ ‘4’ ಅನ್ನು $4 H_2 O$ ಎಂದು ಇಡಬಹುದು ಆದರೆ $H_2 O_4$ ಅಥವಾ $(H_2 O)_4$ ಅಲ್ಲ. ಈಗ ಭಾಗಶಃ ಸಮತೋಲಿತ ಸಮೀಕರಣವು ಆಗುತ್ತದೆ -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (ಭಾಗಶಃ ಸಮತೋಲಿತ ಸಮೀಕರಣ)
ಹಂತ IV: Fe ಮತ್ತು $H$ ಪರಮಾಣುಗಳು ಇನ್ನೂ ಸಮತೋಲಿತವಾಗಿಲ್ಲ. ಮುಂದುವರಿಯಲು ಈ ಯಾವುದೇ ಮೂಲಧಾತುಗಳನ್ನು ಆಯ್ಕೆ ಮಾಡಿ. ಭಾಗಶಃ ಸಮತೋಲಿತ ಸಮೀಕರಣದಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಸಮತೋಲಿಸೋಣ.
$H$ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಸಮಾನಗೊಳಿಸಲು, ಬಲಭಾಗದಲ್ಲಿ (RHS) ಹೈಡ್ರೋಜನ್ ಅಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ನಾಲ್ಕು ಮಾಡಿ.
| ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳು |
ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ | ಉತ್ಪನ್ನಗಳಲ್ಲಿ |
|---|---|---|
| (i) ಆರಂಭಿಕ | 8($ \mathrm{4H_2O} $ ನಲ್ಲಿ) | 2($ \mathrm{H_2} $ ನಲ್ಲಿ) |
| (ii) ಸಮತೋಲಿಸಲು | 8 | 2 $\times$ 4 |
ಸಮೀಕರಣವು ಹೀಗಿರುತ್ತದೆ -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(ಭಾಗಶಃ ಸಮತೋಲಿತ ಸಮೀಕರಣ)
ಹಂತ V: ಮೇಲಿನ ಸಮೀಕರಣವನ್ನು ಪರೀಕ್ಷಿಸಿ ಮತ್ತು ಸಮತೋಲಿತವಾಗಿಲ್ಲದ ಮೂರನೇ ಮೂಲಧಾತುವನ್ನು ಆಯ್ಕೆ ಮಾಡಿ. ಕೇವಲ ಒಂದು ಮೂಲಧಾತು ಮಾತ್ರ ಸಮತೋಲಿಸಲು ಉಳಿದಿದೆ ಎಂದು ನೀವು ಕಾಣುತ್ತೀರಿ, ಅದು ಕಬ್ಬಿಣ.
| ಕಬ್ಬಿಣದ ಪರಮಾಣುಗಳು | ಕ್ರಿಯಾಜನಕಗಳಲ್ಲಿ | ಉತ್ಪನ್ನಗಳಲ್ಲಿ |
|---|---|---|
| (i) ಆರಂಭಿಕ | 1($ \mathrm{Fe} $ ನಲ್ಲಿ) | 3($ \mathrm{Fe_3O_4} $ ನಲ್ಲಿ) |
| (ii) ಸಮತೋಲಿಸಲು | 1 $\times$ 3 | 3 |
$Fe$ ಅನ್ನು ಸಮಾನಗೊಳಿಸಲು, ನಾವು ಎಡಭಾಗದಲ್ಲಿ (LHS) $Fe$ ನ ಮೂರು ಪರಮಾಣುಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತೇವೆ.
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
ಹಂತ VI: ಅಂತಿಮವಾಗಿ, ಸಮತೋಲಿತ ಸಮೀಕರಣದ ಸರಿಯಾದತೆಯನ್ನು ಪರಿಶೀಲಿಸಲು, ನಾವು ಸಮೀಕರಣದ ಎರಡೂ ಬದಿಗಳಲ್ಲಿ ಪ್ರತಿ ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳನ್ನು ಎಣಿಸುತ್ತೇವೆ.
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(ಸಮತೋಲಿತ ಸಮೀಕರಣ)
ಸಮೀಕರಣ (1.9) ನ ಎರಡೂ ಬದಿಗಳ ಮೂಲಧಾತುಗಳ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ ಸಮಾನವಾಗಿದೆ. ಈ ಸಮೀಕರಣವು ಈಗ ಸಮತೋಲಿತವಾಗಿದೆ. ರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳನ್ನು ಸಮತೋಲಿಸುವ ಈ ವಿಧಾನವನ್ನು ಹಿಟ್-ಆಂಡ್-ಟ್ರಯಲ್ ವಿಧಾನ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಏಕೆಂದರೆ ನಾವು ಚಿಕ್ಕ ಪೂರ್ಣಾಂಕ ಗುಣಾಂಕವನ್ನು ಬಳಸಿಕೊಂಡು ಸಮೀಕರಣವನ್ನು ಸಮತೋಲಿಸಲು ಪ್ರಯತ್ನಗಳನ್ನು ಮಾಡುತ್ತೇವೆ.
ಹಂತ VII: ಭೌತಿಕ ಸ್ಥಿತಿಗಳ ಸಂಕೇತಗಳನ್ನು ಬರೆಯುವುದು ಮೇಲಿನ ಸಮತೋಲಿತ ಸಮೀಕರಣ (1.9) ಅನ್ನು ಎಚ್ಚರಿಕೆಯಿಂದ ಪರೀಕ್ಷಿಸಿ. ಈ ಸಮೀಕರಣವು ಪ್ರತಿ ಕ್ರಿಯಾಜನಕ ಮತ್ತು ಉತ್ಪನ್ನದ ಭೌತಿಕ ಸ್ಥಿತಿಯ ಬಗ್ಗೆ ನಮಗೆ ಏನಾದರೂ ತಿಳಿಸುತ್ತದೆಯೇ? ಅವುಗಳ ಭೌತಿಕ ಸ್ಥಿತಿಗಳ ಬಗ್ಗೆ ಈ ಸಮೀಕರಣದಲ್ಲಿ ಯಾವುದೇ ಮಾಹಿತಿ ನೀಡಿಲ್ಲ.
ರಾಸಾಯನಿಕ ಸಮೀಕರಣವನ್ನು ಹೆಚ್ಚು ಮಾಹಿತಿಪೂರ್ಣಗೊಳಿಸಲು, ಕ್ರಿಯಾಜನಕಗಳು ಮತ್ತು ಉತ್ಪನ್ನಗಳ ಭೌತಿಕ ಸ್ಥಿತಿಗಳನ್ನು ಅವುಗಳ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳ ಜೊತೆಗೆ ಉಲ್ಲೇಖಿಸಲಾಗುತ್ತದೆ. ಕ್ರಿಯಾಜನಕಗಳು ಮತ್ತು ಉತ್ಪನ್ನಗಳ ಅನಿಲ, ದ್ರವ, ಜಲೀಯ ಮತ್ತು ಘನ ಸ್ಥಿತಿಗಳನ್ನು ಕ್ರಮವಾಗಿ (g), (l), (aq) ಮತ್ತು (s) ಸಂಕೇತಗಳಿಂದ ಪ್ರತಿನಿಧಿಸಲಾಗುತ್ತದೆ. ಕ್ರಿಯಾಜನಕ ಅಥವಾ ಉತ್ಪನ್ನವು ನೀರಿನಲ್ಲಿ ದ್ರಾವಣವಾಗಿ ಇದ್ದರೆ ಜಲೀಯ (aq) ಎಂದು ಬರೆಯಲಾಗುತ್ತದೆ.
ಸಮತೋಲಿತ ಸಮೀಕರಣ (1.9) ಆಗುತ್ತದೆ
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
$(g)$ ಸಂಕೇತವನ್ನು $H_2 O$ ಜೊತೆಗೆ ಬಳಸಲಾಗಿದೆ ಎಂಬುದನ್ನು ಗಮನಿಸಿ, ಈ ಕ್ರಿಯೆಯಲ್ಲಿ ನೀರನ್ನು ಉಗಿಯ ರೂಪದಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ ಎಂದು ಸೂಚಿಸಲು.
ಸಾಮಾನ್ಯವಾಗಿ ಅವುಗಳನ್ನು ನಿರ್ದಿಷ್ಟಪಡಿಸುವುದು ಅಗತ್ಯವಿಲ್ಲದ ಹೊರತು ಭೌತಿಕ ಸ್ಥಿತಿಗಳನ್ನು ರಾಸಾಯನಿಕ ಸಮೀಕರಣದಲ್ಲಿ ಸೇರಿಸಲಾಗುವುದಿಲ್ಲ.
ಕೆಲವೊಮ್ಮೆ ಕ್ರಿಯೆಯ ಪರಿಸ್ಥಿತಿಗಳು, ಉದಾಹರಣೆಗೆ ತಾಪಮಾನ, ಒತ್ತಡ, ಉತ್ಪ್ರೇರಕ, ಇತ್ಯಾದಿ, ಸಮೀಕರಣದಲ್ಲಿ ಬಾಣದ ಮೇಲೆ ಮತ್ತು/ಅಥವಾ ಕೆಳಗೆ ಸೂಚಿಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
ಈ ಹಂತಗಳನ್ನು ಬಳಸಿಕೊಂಡು, ನೀವು ಹಿಂದಿನ ಪಠ್ಯದಲ್ಲಿ ನೀಡಲಾದ ಸಮೀಕರಣ (1.2) ಅನ್ನು ಸಮತೋಲಿಸಬಹುದೇ?
1.2 ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ವಿಧಗಳು
IX ನೇ ತರಗತಿಯಲ್ಲಿ ನಾವು ಕಲಿತಿದ್ದೇವೆ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ ಒಂದು ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳು ಇನ್ನೊಂದು ಮೂಲಧಾತುವಿನ ಪರಮಾಣುಗಳಾಗಿ ಬದಲಾಗುವುದಿಲ್ಲ. ಅಥವಾ ಮಿಶ್ರಣದಿಂದ ಪರಮಾಣುಗಳು ಕಣ್ಮರೆಯಾಗುವುದಿಲ್ಲ ಅಥವಾ ಬೇರೆಡೆಯಿಂದ ಕಾಣಿಸಿಕೊಳ್ಳುವುದಿಲ್ಲ. ವಾಸ್ತವವಾಗಿ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳು ಹೊಸ ವಸ್ತುಗಳನ್ನು ಉತ್ಪಾದಿಸಲು ಪರಮಾಣುಗಳ ನಡುವಿನ ಬಂಧಗಳನ್ನು ಮುರಿಯುವುದು ಮತ್ತು ರಚಿಸುವುದನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. ಪರಮಾಣುಗಳ ನಡುವೆ ರೂಪುಗೊಂಡ ಬಂಧಗಳ ವಿಧಗಳ ಬಗ್ಗೆ ನೀವು ಅಧ್ಯಾಯ 3 ಮತ್ತು 4 ರಲ್ಲಿ ಅಧ್ಯಯನ ಮಾಡುತ್ತೀರಿ.
1.2.1 ಸಂಯೋಜನಾ ಕ್ರಿಯೆ
ಚಟುವಟಿಕೆ 1.4
- ಒಂದು ಬೀಕರ್ನಲ್ಲಿ ಸ್ವಲ್ಪ ಪ್ರಮಾಣದ ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡ್ ಅಥವಾ ಸುಣ್ಣವನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ.
- ಇದಕ್ಕೆ ನಿಧಾನವಾಗಿ ನೀರು ಸೇರಿಸಿ.
- ಚಿತ್ರ 1.3 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ಬೀಕರ್ ಅನ್ನು ಮುಟ್ಟಿ.
- ತಾಪಮಾನದಲ್ಲಿ ಯಾವುದೇ ಬದಲಾವಣೆಯನ್ನು ನೀವು ಅನುಭವಿಸುತ್ತೀರಾ?
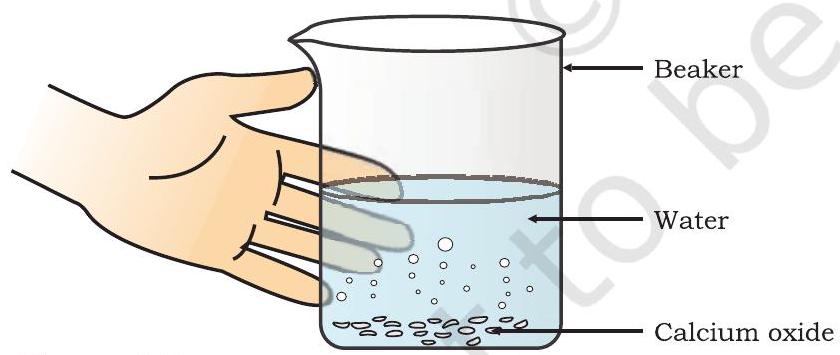
ಚಿತ್ರ 1.3 ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡ್ ಮತ್ತು ನೀರಿನ ಕ್ರಿಯೆಯಿಂದ ಸುಣ್ಣದ ನೀರಿನ ರಚನೆ
ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡ್ ನೀರಿನೊಂದಿಗೆ ತೀವ್ರವಾಗಿ ಕ್ರಿಯೆ ನಡೆಸಿ ಸುಣ್ಣದ ನೀರು (ಕ್ಯಾಲ್ಸಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್) ಉತ್ಪಾದಿಸುತ್ತದೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದ ಉಷ್ಣವನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ.
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
ಈ ಕ್ರಿಯೆಯಲ್ಲಿ, ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡ್ ಮತ್ತು ನೀರು ಸಂಯೋಜನೆ ಹೊಂದಿ ಒಂದೇ ಉತ್ಪನ್ನವಾದ ಕ್ಯಾಲ್ಸಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ. ಎರಡು ಅಥವಾ ಹೆಚ್ಚಿನ ಕ್ರಿಯಾಜನಕಗಳಿಂದ ಒಂದೇ ಉತ್ಪನ್ನ ರೂಪುಗೊಳ್ಳುವ ಅಂತಹ ಕ್ರಿಯೆಯನ್ನು ಸಂಯೋಜನಾ ಕ್ರಿಯೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ನಿಮಗೆ ತಿಳಿದಿದೆಯೇ?
ಕ್ರಿಯೆ 1.13 ರಿಂದ ಉತ್ಪತ್ತಿಯಾದ ಸುಣ್ಣದ ನೀರಿನ ದ್ರಾವಣವನ್ನು ಗೋಡೆಗಳಿಗೆ ಸುಣ್ಣ ಬಳಿಯಲು ಬಳಸಲಾಗುತ್ತದೆ. ಕ್ಯಾಲ್ಸಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ ಗಾಳಿಯಲ್ಲಿನ ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ನೊಂದಿಗೆ ನಿಧಾನವಾಗಿ ಕ್ರಿಯೆ ನಡೆಸಿ ಗೋಡೆಗಳ ಮೇಲೆ ಕ್ಯಾಲ್ಸಿಯಂ ಕಾರ್ಬೋನೇಟ್ನ ತೆಳುವಾದ ಪದರವನ್ನು ರೂಪಿಸುತ್ತದೆ. ಕ್ಯಾಲ್ಸಿಯಂ ಕಾರ್ಬೋನೇಟ್ ಸುಣ್ಣ ಬಳಿದ ಎರಡರಿಂದ ಮೂರು ದಿನಗಳ ನಂತರ ರೂಪುಗೊಳ್ಳುತ್ತದೆ ಮತ್ತು ಗೋಡೆಗಳಿಗೆ ಹೊಳಪು ನೀಡುತ್ತದೆ. ಅಮೃತಶಿಲೆಗೆ ರಾಸಾಯನಿಕ ಸೂತ್ರವೂ $CaCO_3$ ಎಂಬುದು ಕುತೂಹಲಕಾರಿಯಾಗಿದೆ.
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
ಸಂಯೋಜನಾ ಕ್ರಿಯೆಗಳ ಇನ್ನೂ ಕೆಲವು ಉದಾಹರಣೆಗಳನ್ನು ಚರ್ಚಿಸೋಣ.
(i) ಕಲ್ಲಿದ್ದಲು ಸುಡುವುದು
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ ಮತ್ತು $O_2(g)$ ನಿಂದ ನೀರಿನ ರಚನೆ
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
ಸರಳ ಭಾಷೆಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಎರಡು ಅಥವಾ ಹೆಚ್ಚಿನ ವಸ್ತುಗಳು (ಮೂಲಧಾತುಗಳು ಅಥವಾ ಸಂಯುಕ್ತಗಳು) ಸಂಯೋಜನೆ ಹೊಂದಿ ಒಂದೇ ಉತ್ಪನ್ನವನ್ನು ರೂಪಿಸಿದಾಗ, ಆ ಕ್ರಿಯೆಗಳನ್ನು ಸಂಯೋಜನಾ ಕ್ರಿಯೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಚಟುವಟಿಕೆ 1.4 ರಲ್ಲಿ, ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದ ಉಷ್ಣವು ಬಿಡುಗಡ











