प्रकरण 01 रासायनिक अभिक्रिया व समीकरणे
दैनंदिन जीवनातील खालील परिस्थितींचा विचार करा आणि विचार करा की जेव्हा -
- उन्हाळ्यात दूध खोलीच्या तपमानावर ठेवले जाते.
- लोखंडी तवा/पॅन/खिळा आर्द्र वातावरणात उघडा ठेवला जातो.
- द्राक्षे किण्वित होतात.
- अन्न शिजवले जाते.
- आपल्या शरीरात अन्न पचते.
- आपण श्वासोच्छ्वास करतो.
वरील सर्व परिस्थितींमध्ये, सुरुवातीच्या पदार्थाचे स्वरूप आणि ओळख काही अंशी बदललेली असते. आपण आपल्या मागील वर्गांमध्ये द्रव्याचे भौतिक आणि रासायनिक बदलांबद्दल आधीच शिकलो आहोत. जेव्हा जेव्हा रासायनिक बदल घडतो, तेव्हा आपण असे म्हणू शकतो की एक रासायनिक अभिक्रिया घडली आहे.
तुम्ही कदाचित हे विचार करत असाल की रासायनिक अभिक्रिया म्हणजे नेमके काय? रासायनिक अभिक्रिया घडली आहे हे आपल्याला कसे कळते? या प्रश्नांची उत्तरे शोधण्यासाठी आपण काही क्रियाकलाप करूया.
क्रियाकलाप 1.1
सावधानता: या क्रियाकलापासाठी शिक्षकांची मदत आवश्यक आहे. विद्यार्थ्यांनी योग्य चष्मा घातले तर चांगले.
- सुमारे 3-4 सेमी लांबीची मॅग्नेशियमची पट्टी सँडपेपरने घासून स्वच्छ करा.
- ती चिमट्याने धरा. स्पिरिट लॅम्प किंवा बर्नर वापरून ती जाळा आणि तयार झालेली राख फिग. 1.1 मध्ये दाखवल्याप्रमाणे वॉच-ग्लासमध्ये गोळा करा. मॅग्नेशियम पट्टी जाळताना ती आपल्या डोळ्यांपासून शक्य तितकी दूर ठेवा.
- तुम्ही काय पाहता?
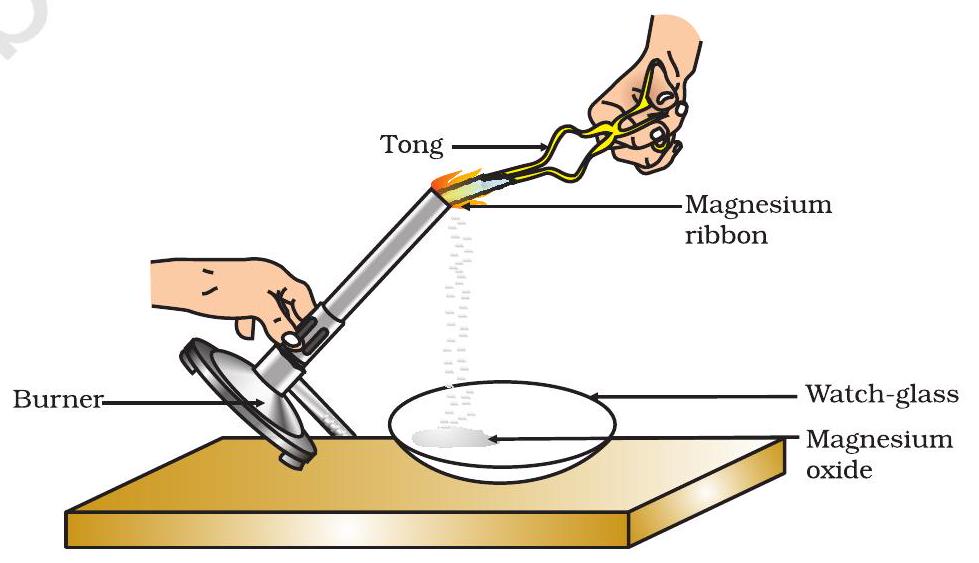
आकृती 1.1
हवेत मॅग्नेशियम पट्टी जाळणे आणि वॉच-ग्लासमध्ये मॅग्नेशियम ऑक्साईड गोळा करणे
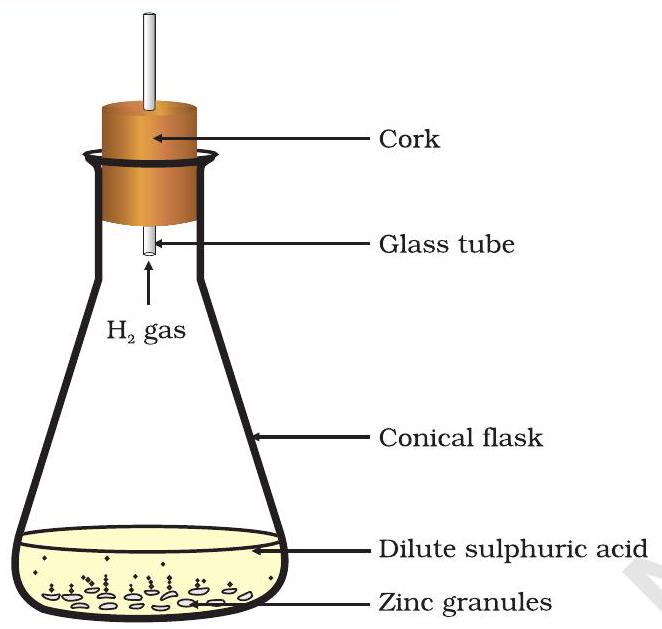
आकृती 1.2 झिंकवर सौम्य सल्फ्यूरिक आम्लाच्या क्रियेने हायड्रोजन वायू तयार होणे
तुम्ही नक्कीच पाहिले असेल की मॅग्नेशियम पट्टी तेजस्वी पांढऱ्या ज्योतीसह जळते आणि पांढऱ्या पावडरमध्ये बदलते. ही पूड मॅग्नेशियम ऑक्साईड आहे. हे मॅग्नेशियम आणि हवेमध्ये असलेल्या ऑक्सिजन यांच्यातील अभिक्रियेमुळे तयार होते.
क्रियाकलाप 1.2
- एका चाचणी नलिकेत लेड नायट्रेट द्रावण घ्या.
- यात पोटॅशियम आयोडाइड द्रावण घाला.
- तुम्ही काय पाहता?
क्रियाकलाप 1.3
- शंकूच्या आकाराच्या फ्लास्क किंवा चाचणी नलिकेत काही झिंकचे कण घ्या.
- यात सौम्य हायड्रोक्लोरिक आम्ल किंवा सल्फ्यूरिक आम्ल घाला (आकृती 1.2).
सावधानता: आम्ल काळजीपूर्वक हाताळा.
- झिंकच्या कणांभोवती काही घडताना तुम्ही पाहता का?
- शंकूच्या आकाराच्या फ्लास्क किंवा चाचणी नलिकेला स्पर्श करा. त्याच्या तापमानात काही बदल आहे का?
वरील तीनही क्रियाकलापांवरून, आपण असे म्हणू शकतो की खालीलपैकी कोणतेही निरीक्षण रासायनिक अभिक्रिया घडली आहे की नाही हे ठरवण्यास मदत करते –
- अवस्थेतील बदल
- रंगात बदल
- वायूचे उत्सर्जन
- तापमानात बदल.
आपण आपल्या भोवती होणाऱ्या बदलांचे निरीक्षण करतो, तेव्हा आपल्याला दिसते की आपल्या भोवती विविध प्रकारच्या रासायनिक अभिक्रिया घडत आहेत. या प्रकरणात आपण विविध प्रकारच्या रासायनिक अभिक्रिया आणि त्यांचे प्रतीकात्मक निरूपण याबद्दल अभ्यास करू.
1.1 रासायनिक समीकरणे
क्रियाकलाप 1.1 चे वर्णन असे केले जाऊ शकते – जेव्हा मॅग्नेशियम पट्टी ऑक्सिजनमध्ये जाळली जाते, तेव्हा ती मॅग्नेशियम ऑक्साईडमध्ये रूपांतरित होते. वाक्यरूपातील रासायनिक अभिक्रियेचे हे वर्णन बरेच लांब आहे. ते लहान स्वरूपात लिहिता येते. हे करण्याचा सर्वात सोपा मार्ग म्हणजे ते शब्द-समीकरणाच्या रूपात लिहिणे. वरील अभिक्रियेसाठी शब्द-समीकरण असे असेल –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
अभिक्रिया (1.1) मध्ये रासायनिक बदल घडवून आणणारे पदार्थ, मॅग्नेशियम आणि ऑक्सिजन, हे अभिक्रियाकारक आहेत. नवीन पदार्थ म्हणजे मॅग्नेशियम ऑक्साईड, जो अभिक्रियेदरम्यान उत्पादन म्हणून तयार होतो.
शब्द-समीकरण अभिक्रियाकारकांपासून उत्पादनांकडे त्यांच्यामध्ये ठेवलेल्या बाणाद्वारे होणारा बदल दर्शवते. अभिक्रियाकारक डाव्या बाजूला (LHS) लिहिलेले असतात आणि त्यांच्यामध्ये अधिक चिन्ह (+) असते. त्याचप्रमाणे, उत्पादने उजव्या बाजूला (RHS) लिहिली जातात आणि त्यांच्यामध्ये अधिक चिन्ह (+) असते. बाणाचे टोक उत्पादनांकडे निर्देशित करते आणि अभिक्रियेची दिशा दर्शवते.
1.1.1 रासायनिक समीकरण लिहिणे
रासायनिक समीकरणे दर्शवण्याचा आणखी काही लहान मार्ग आहे का? जर आपण शब्दांऐवजी रासायनिक सूत्रे वापरली तर रासायनिक समीकरणे अधिक संक्षिप्त आणि उपयुक्त बनवता येतील. रासायनिक समीकरण ही एक रासायनिक अभिक्रिया दर्शवते. जर तुम्हाला मॅग्नेशियम, ऑक्सिजन आणि मॅग्नेशियम ऑक्साईडची सूत्रे आठवत असतील, तर वरील शब्द-समीकरण असे लिहिले जाऊ शकते -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
बाणाच्या LHS आणि RHS वर प्रत्येक मूलद्रव्याच्या अणूंची संख्या मोजा आणि तुलना करा. दोन्ही बाजूंवर प्रत्येक मूलद्रव्याच्या अणूंची संख्या सारखीच आहे का? होय असल्यास, समीकरण संतुलित आहे. नसल्यास, समीकरण असंतुलित आहे कारण द्रव्यमान समीकरणाच्या दोन्ही बाजूंवर सारखे नाही. असे रासायनिक समीकरण हे अभिक्रियेसाठी अस्थायू रासायनिक समीकरण आहे. समीकरण (1.2) हे हवेत मॅग्नेशियम जाळण्यासाठीचे अस्थायू रासायनिक समीकरण आहे.
1.1.2 संतुलित रासायनिक समीकरणे
इयत्ता IX मध्ये तुम्ही अभ्यासलेल्या द्रव्यमानाच्या संवर्धनाच्या नियमाची आठवण करा; रासायनिक अभिक्रियेत द्रव्यमान निर्माण होऊ शकत नाही किंवा नष्टही होऊ शकत नाही. म्हणजेच, रासायनिक अभिक्रियेच्या उत्पादनांमध्ये असलेल्या मूलद्रव्यांचे एकूण द्रव्यमान अभिक्रियाकारकांमध्ये असलेल्या मूलद्रव्यांच्या एकूण द्रव्यमानाइतकेच असणे आवश्यक आहे.
दुसऱ्या शब्दांत, प्रत्येक मूलद्रव्याच्या अणूंची संख्या रासायनिक अभिक्रियेपूर्वी आणि नंतर सारखीच राहते. म्हणून, आपल्याला अस्थायू रासायनिक समीकरण संतुलित करणे आवश्यक आहे. रासायनिक समीकरण (1.2) संतुलित आहे का? चला, रासायनिक समीकरण संतुलित करणे चरणबद्ध पद्धतीने शिकूया.
क्रियाकलाप 1.3 साठीचे शब्द-समीकरण असे दर्शवले जाऊ शकते -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
वरील शब्द-समीकरण खालील रासायनिक समीकरणाद्वारे दर्शवले जाऊ शकते -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
चला, बाणाच्या दोन्ही बाजूंवर विविध मूलद्रव्यांच्या अणूंची संख्या तपासूया.
| मूलद्रव्य | अभिक्रियाकारकांमधील अणूंची संख्या (LHS) | उत्पादनांमधील अणूंची संख्या (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
प्रत्येक मूलद्रव्याच्या अणूंची संख्या बाणाच्या दोन्ही बाजूंवर सारखीच असल्यामुळे, समीकरण (1.3) हे एक संतुलित रासायनिक समीकरण आहे.
चला, खालील रासायनिक समीकरण संतुलित करण्याचा प्रयत्न करूया -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
पायरी I: रासायनिक समीकरण संतुलित करण्यासाठी, प्रथम प्रत्येक सूत्राभोवती बॉक्स काढा. समीकरण संतुलित करताना बॉक्समध्ये काहीही बदल करू नका.
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
पायरी II: असंतुलित समीकरण (1.5) मध्ये असलेल्या विविध मूलद्रव्यांच्या अणूंची संख्या सूचीबद्ध करा.
| मूलद्रव्य | अभिक्रियाकारकांमधील अणूंची संख्या (LHS) | उत्पादनांमधील अणूंची संख्या (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
पायरी III: सहसा ज्या संयुगामध्ये अणूंची संख्या जास्तीत जास्त असते, त्या संयुगासह संतुलन सुरू करणे सोयीचे असते. तो एक अभिक्रियाकारक किंवा उत्पादन असू शकते. त्या संयुगात, ज्या मूलद्रव्याच्या अणूंची संख्या सर्वाधिक आहे ते मूलद्रव्य निवडा. या निकषांचा वापर करून, आपण $Fe_3 O_4$ आणि त्यातील ऑक्सिजन हे मूलद्रव्य निवडतो. RHS वर चार ऑक्सिजन अणू आहेत आणि LHS वर फक्त एक आहे.
ऑक्सिजन अणू संतुलित करण्यासाठी -
| ऑक्सिजनचे अणू |
अभिक्रियाकारकांमध्ये | उत्पादनांमध्ये |
|---|---|---|
| (i) सुरुवातीचे | 1 ($ \mathrm{H_2O} $ मध्ये) | 4 ($ \mathrm{Fe_3O_4} $ मध्ये) |
| (ii) संतुलित करण्यासाठी | 1 $\times$ 4 | 4 |
अणूंची संख्या समान करण्यासाठी, हे लक्षात ठेवले पाहिजे की आपण अभिक्रियेत सामील असलेल्या संयुगांची किंवा मूलद्रव्यांची सूत्रे बदलू शकत नाही. उदाहरणार्थ, ऑक्सिजन अणू संतुलित करण्यासाठी आपण गुणांक ‘4’ $4 H_2 O$ म्हणून ठेवू शकतो, $H_2 O_4$ किंवा $(H_2 O)_4$ म्हणून नाही. आता अंशतः संतुलित समीकरण होते -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (अंशतः संतुलित समीकरण)
पायरी IV: Fe आणि $H$ अणू अजूनही संतुलित नाहीत. पुढे जाण्यासाठी यापैकी कोणतेही मूलद्रव्य निवडा. चला, अंशतः संतुलित समीकरणातील हायड्रोजन अणू संतुलित करूया.
$H$ अणूंची संख्या समान करण्यासाठी, RHS वर हायड्रोजनच्या रेणूंची संख्या चार करा.
| हायड्रोजनचे अणू |
अभिक्रियाकारकांमध्ये | उत्पादनांमध्ये |
|---|---|---|
| (i) सुरुवातीचे | 8 ($ \mathrm{4H_2O} $ मध्ये) | 2 ($ \mathrm{H_2} $ मध्ये) |
| (ii) संतुलित करण्यासाठी | 8 | 2 $\times$ 4 |
समीकरण असे असेल -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(अंशतः संतुलित समीकरण)
पायरी V: वरील समीकरणाचे परीक्षण करा आणि तिसरे मूलद्रव्य निवडा जे संतुलित नाही. तुम्हाला आढळेल की फक्त एक मूलद्रव्य संतुलित करायचे शिल्लक आहे, ते म्हणजे लोह.
| लोहाचे अणू | अभिक्रियाकारकांमध्ये | उत्पादनांमध्ये |
|---|---|---|
| (i) सुरुवातीचे | 1 ($ \mathrm{Fe} $ मध्ये) | 3 ($ \mathrm{Fe_3O_4} $ मध्ये) |
| (ii) संतुलित करण्यासाठी | 1 $\times$ 3 | 3 |
$Fe$ समान करण्यासाठी, आपण LHS वर $Fe$ चे तीन अणू घेतो.
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
पायरी VI: शेवटी, संतुलित समीकरणाची शुद्धता तपासण्यासाठी, आपण समीकरणाच्या दोन्ही बाजूंच्या प्रत्येक मूलद्रव्याचे अणू मोजतो.
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(संतुलित समीकरण)
समीकरण (1.9) च्या दोन्ही बाजूंच्या मूलद्रव्यांच्या अणूंची संख्या समान आहे. हे समीकरण आता संतुलित आहे. रासायनिक समीकरणे संतुलित करण्याच्या या पद्धतीला हिट-अँड-ट्रायल पद्धत म्हणतात कारण आपण सर्वात लहान पूर्णांक गुणांक वापरून समीकरण संतुलित करण्यासाठी प्रयत्न करतो.
पायरी VII: भौतिक अवस्थांची चिन्हे लिहिणे वरील संतुलित समीकरण (1.9) काळजीपूर्वक तपासा. हे समीकरण आपल्याला प्रत्येक अभिक्रियाकारक आणि उत्पादनाच्या भौतिक अवस्थेबद्दल काही सांगते का? त्यांच्या भौतिक अवस्थांबद्दल या समीकरणात कोणतीही माहिती दिलेली नाही.
रासायनिक समीकरण अधिक माहितीपूर्ण बनवण्यासाठी, अभिक्रियाकारक आणि उत्पादनांच्या भौतिक अवस्था त्यांच्या रासायनिक सूत्रांसह नमूद केल्या जातात. अभिक्रियाकारक आणि उत्पादनांची वायू, द्रव, जलीय आणि घन अवस्था अनुक्रमे (g), (l), (aq) आणि (s) या संकेतांद्वारे दर्शविली जातात. जर अभिक्रियाकारक किंवा उत्पादन पाण्यात द्रावणाच्या स्वरूपात असेल तर जलीय (aq) हा शब्द लिहिला जातो.
संतुलित समीकरण (1.9) होते
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
लक्षात घ्या की $(g)$ हे चिन्ह $H_2 O$ सह वापरले जाते हे दर्शवण्यासाठी की या अभिक्रियेत पाणी वाफेच्या स्वरूपात वापरले जाते.
सहसा भौतिक अवस्था रासायनिक समीकरणात समाविष्ट केल्या जात नाहीत जोपर्यंत ते निर्दिष्ट करणे आवश्यक नाही.
काहीवेळा अभिक्रियेच्या परिस्थिती, जसे की तापमान, दाब, उत्प्रेरक इ., समीकरणातील बाणाच्या वर आणि/किंवा खाली दर्शविल्या जातात. उदाहरणार्थ -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
या चरणांचा वापर करून, तुम्ही आधी मजकुरात दिलेले समीकरण (1.2) संतुलित करू शकता का?
1.2 रासायनिक अभिक्रियांचे प्रकार
आपण इयत्ता IX मध्ये शिकलो आहोत की रासायनिक अभिक्रियेदरम्यान एका मूलद्रव्याचे अणू दुसऱ्या मूलद्रव्यात बदलत नाहीत. किंवा अणू मिश्रणातून नाहीसे होत नाहीत किंवा इतरत्र दिसत नाहीत. वास्तविक, रासायनिक अभिक्रियांमध्ये नवीन पदार्थ तयार करण्यासाठी अणूंमधील बंध तोडणे आणि बनवणे समाविष्ट असते. तुम्ही प्रकरण 3 आणि 4 मध्ये अणूंमध्ये तयार होणाऱ्या बंधांच्या प्रकारांबद्दल अभ्यास कराल.
1.2.1 संयोग अभिक्रिया
क्रियाकलाप 1.4
- बीकरमध्ये थोडे कॅल्शियम ऑक्साईड किंवा चुना घ्या.
- यात हळूहळू पाणी घाला.
- आकृती 1.3 मध्ये दाखवल्याप्रमाणे बीकरला स्पर्श करा.
- तुम्हाला तापमानात काही बदल जाणवतो का?
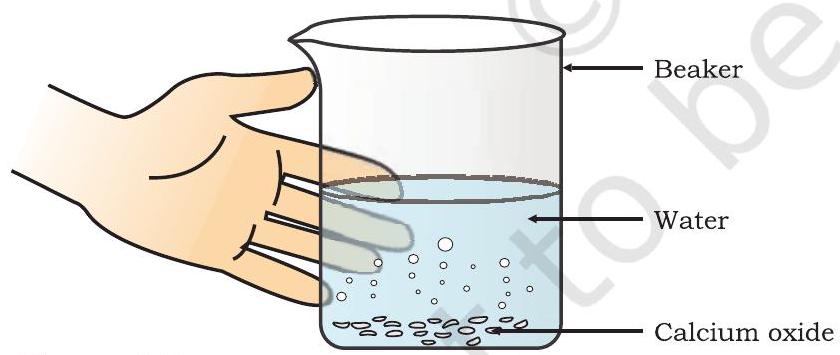
आकृती 1.3 कॅल्शियम ऑक्साईड आणि पाण्याच्या अभिक्रियेने बुजलेला चुना तयार होणे
कॅल्शियम ऑक्साईड पाण्याबरोबर जोरदार अभिक्रिया करून बुजलेला चुना (कॅल्शियम हायड्रॉक्साईड) तयार करते आणि प्रचंड प्रमाणात उष्णता सोडते.
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
या अभिक्रियेत, कॅल्शियम ऑक्साईड आणि पाणी एकत्र होऊन एकच उत्पादन, कॅल्शियम हायड्रॉक्साईड तयार करते. अशी अभिक्रिया ज्यामध्ये दोन किंवा अधिक अभिक्रियाकारकांपासून एकच उत्पादन तयार होते त्याला संयोग अभिक्रिया म्हणतात.
तुम्हाला माहिती आहे का?
अभिक्रिया 1.13 द्वारे तयार झालेल्या बुजलेल्या चुन्याचे द्रावण भिंतींवर पांढरा रंग देण्यासाठी वापरले जाते. कॅल्शियम हायड्रॉक्साईड हवेतील कार्बन डायऑक्साइडसह हळूहळू अभिक्रिया करून भिंतींवर कॅल्शियम कार्बोनेटची पातळ थर तयार करते. पांढरा रंग दिल्यानंतर दोन ते तीन दिवसांनी कॅल्शियम कार्बोनेट तयार होते आणि भिंतींना चमकदार पूर्णता देते. हे लक्षणीय आहे की संगमरवरीचे रासायनिक सूत्र देखील $CaCO_3$ आहे.
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
चला, संयोग अभिक्रियांची आणखी काही उदाहरणे चर्चा करूया.
(i) कोळशाचे ज्वलन
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ आणि $O_2(g)$ पासून पाणी तयार होणे
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
सोप्या भाषेत आपण असे म्हणू शकतो की जेव्हा दोन किंवा अधिक पदार्थ (मूलद्रव्ये किंवा संयुगे) एकत्र होऊन एकच उत्पादन तयार करतात, तेव्हा त्या अभिक्रियांना संयोग अभिक्रिया म्हणतात.
क्रियाकलाप 1.4 मध्ये, आपण हे देखील पाहिले की प्रचंड प्रमाणात उष्णता निर्माण होते. यामुळे अभिक्रिया मिश्रण उबदार होते. ज्या अभिक्रियांमध्ये उत्पादनांसोबत उष्णता सोडली जाते त्यांना उष्मादायी रासायनिक अभिक्रिया म्हणतात.
उष्मादायी अभिक्रियांची इतर उदाहरणे आहेत -
(i) नैसर्गिक वायूचे ज्वलन
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) तुम्हाला माहित आहे का की श्वसन ही एक उष्मादायी प्रक्रिया आहे?
आपण जगण्यासाठी ऊर्जेची आवश्यकता असते हे आपल्या सर्वांना माहित आहे. आपण खाणाऱ्या अन्नातून ही ऊर्जा मिळवतो. पचनादरम्यान, अन्न सोप्या पदार्थांमध्ये विघटित होते. उदाहरणार्थ, तांदूळ, बटाटे आणि भाकरीत कर्बोदके असतात. ही कर्बोदके ग्लुकोजमध्ये विघटित होतात. हे ग्लुकोज आपल्या शरीरातील पेशींमध्ये ऑक्सिजनसह एकत्र होते आणि ऊर्जा पुरवते. या अभिक्रियेचे विशेष नाव श्वसन आहे, ज्याची प्रक्रिया तुम्ही प्रकरण 6 मध्ये अभ्यासाल.
$ \begin{equation*} \underset{\text{ (ग्लुकोज) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ ऊर्जा } \tag{1.18} \end{equation*} $
(iii) वनस्पती पदार्थाचे कंपोस्टमध्ये विघटन हे देखील उष्मादायी अभिक्रियेचे उदाहरण आहे.
क्रियाकलाप 1.1 मध्ये घडणाऱ्या अभिक्रियेचा प्रकार ओळखा, जिथे एकाच उत्पादनासह उष्णता बाहेर सोडली जाते.
1.2.2 विघटन अभिक्रिया
क्रियाकलाप 1.5
- एका कोरड्या उकळत्या नलिकेत सुमारे $2 g$ फेरस सल्फेट क्रिस्टल घ्या.
- फेरस सल्फेट क्रिस्टल्सचा रंग लक्षात घ्या.
- आकृती 1.4 मध्ये दाखवल्याप्रमाणे बर्नर किंवा स्पिरिट लॅम्पच्या ज्योतीवर उकळत्या नलिकेला उष्णता द्या.
- उष्णता देल्यानंतर क्रिस्टल्सचा रंग निरीक्षण करा.
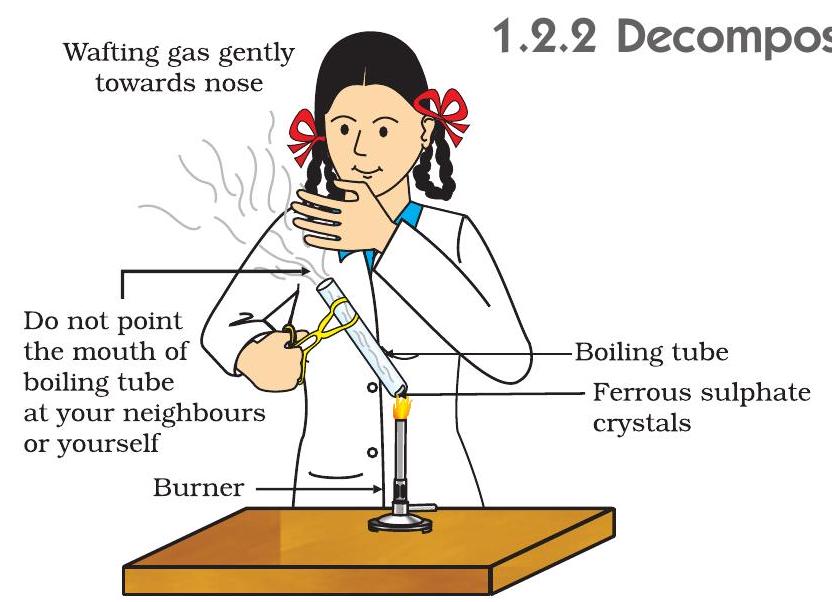
आकृती 1.4 फेरस सल्फेटचे क्रिस्टल असलेली उकळती नलिका उष्णता देण्याची आणि वास घेण्याची योग्य पद्धत
तुम्ही पाहिले आहे की फेरस सल्फेट क्रिस्टल्सचा हिरवा रंग बदलला आहे? तुम्हाला जळत्या सल्फरचा वैशिष्ट्यपूर्ण वास देखील येतो.
$ \underset{\text{(फेरस सल्फेट)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (फेरिक ऑक्साईड) }]{\text{ उष्णता }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
या अभिक्रियेत तुम्ही पाहू शकता की एकच अभिक्रियाकारक सोप्या उत्पादनांमध्ये विघटित होतो. ही एक विघटन अभिक्रिया आहे. फेरस सल्फेट क्रिस्टल्स $(FeSO_4. 7 H_2 O)$ उष्णता दिल्यावर पाणी गमावतात आणि क्रिस्टल्सचा रंग बदलतो. नंतर ते फेरिक ऑक्साईड $(Fe_2 O_3)$, सल्फर डायऑक्साइड $(SO_2)$ आणि सल्फर ट्रायऑक्साइड $(SO_3)$ मध्ये विघटित होते. फेरिक ऑक्साईड घन आहे, तर $SO_2$ आणि $SO_3$ वायू आहेत.
कॅल्शियम कार्बोनेटचे उष्णता देऊन कॅल्शियम ऑक्साईड आणि कार्बन डायऑक्साइडमध्ये विघटन ही विविध उद्योगांमध्ये वापरली जाणारी एक महत्त्वाची विघटन अभिक्रिया आहे. कॅल्शियम ऑक्साईडला चुना किंवा क्विक लाइ











