அத்தியாயம் 01 வேதியியல் வினைகள் மற்றும் சமன்பாடுகள்
பின்வரும் அன்றாட வாழ்க்கைச் சூழ்நிலைகளைக் கவனியுங்கள் மற்றும் என்ன நடக்கிறது என்று சிந்தியுங்கள் -
- பாலை கோடைகாலத்தில் அறை வெப்பநிலையில் விட்டுவைத்தால்.
- இரும்பு தவா/பான்/ஆணி ஈரப்பதமான வளிமண்டலத்தில் வெளிப்படையாக விடப்பட்டால்.
- திராட்சை புளிக்கும்.
- உணவு சமைக்கப்படுகிறது.
- உணவு நம் உடலில் செரிக்கப்படுகிறது.
- நாம் சுவாசிக்கிறோம்.
மேலே உள்ள அனைத்து சூழ்நிலைகளிலும், ஆரம்பப் பொருளின் தன்மையும் அடையாளமும் ஓரளவு மாற்றமடைந்துள்ளன. நாம் ஏற்கனவே நமது முந்தைய வகுப்புகளில் பொருளின் இயற்பியல் மற்றும் வேதியியல் மாற்றங்களைப் பற்றி கற்றுக்கொண்டோம். ஒரு வேதியியல் மாற்றம் ஏற்படும் போதெல்லாம், ஒரு வேதியியல் வினை நடந்துள்ளது என்று நாம் கூறலாம்.
ஒரு வேதியியல் வினை என்பது உண்மையில் என்ன என்பதைப் பற்றி நீங்கள் யோசித்துக் கொண்டிருக்கலாம். ஒரு வேதியியல் வினை நடந்துள்ளது என்பதை நாம் எவ்வாறு அறிவோம்? இந்தக் கேள்விகளுக்கான பதிலைக் கண்டறிய சில செயல்பாடுகளைச் செய்வோம்.
செயல்பாடு 1.1
எச்சரிக்கை: இந்தச் செயல்பாட்டிற்கு ஆசிரியரின் உதவி தேவை. மாணவர்கள் பொருத்தமான கண்ணாடிகளை அணிவது நல்லது.
- சுமார் 3-4 செ.மீ நீளமுள்ள மெக்னீசியம் நாடாவை மணல் தாளால் தேய்த்து சுத்தம் செய்யவும்.
- ஒரு இடுக்கி மூலம் அதைப் பிடிக்கவும். ஒரு ஆவிவிளக்கு அல்லது பர்னரைப் பயன்படுத்தி அதை எரித்து, உருவாகும் சாம்பலை படம் 1.1 இல் காட்டப்பட்டுள்ளபடி ஒரு வாட்ச்-கிளாஸில் சேகரிக்கவும். உங்கள் கண்களிலிருந்து முடிந்தவரை தொலைவில் வைத்து மெக்னீசியம் நாடாவை எரிக்கவும்.
- நீங்கள் என்ன கவனிக்கிறீர்கள்?
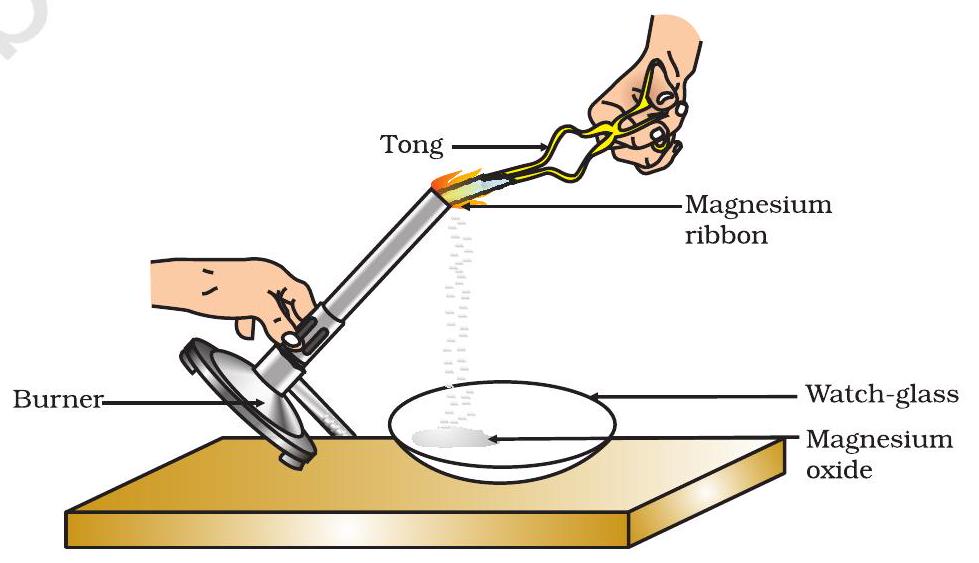
படம் 1.1
காற்றில் மெக்னீசியம் நாடாவை எரித்தல் மற்றும் வாட்ச்-கிளாஸில் மெக்னீசியம் ஆக்சைடை சேகரித்தல்
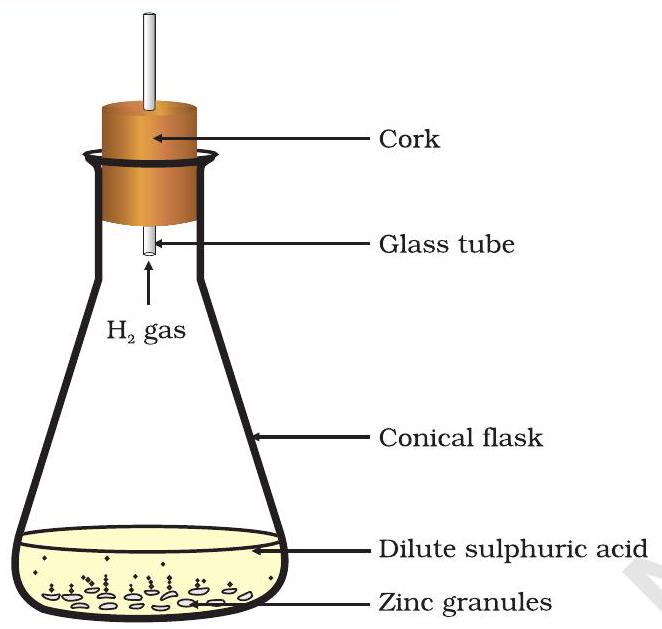
படம் 1.2 துத்தநாகத்தின் மீது நீர்த்த கந்தக அமிலத்தின் செயல்பாட்டால் ஹைட்ரஜன் வாயு உருவாதல்
மெக்னீசியம் நாடா ஒரு கண்கூசும் வெள்ளை சுடரில் எரிந்து வெள்ளைப் பொடியாக மாறுவதை நீங்கள் கவனித்திருக்க வேண்டும். இந்தப் பொடி மெக்னீசியம் ஆக்சைடு ஆகும். இது மெக்னீசியம் மற்றும் காற்றில் உள்ள ஆக்ஸிஜன் இடையேயான வினையின் காரணமாக உருவாகிறது.
செயல்பாடு 1.2
- ஒரு சோதனைக் குழாயில் லெட் நைட்ரேட் கரைசலை எடுத்துக் கொள்ளுங்கள்.
- இதில் பொட்டாசியம் அயோடைடு கரைசலைச் சேர்க்கவும்.
- நீங்கள் என்ன கவனிக்கிறீர்கள்?
செயல்பாடு 1.3
- ஒரு கூம்பு வடிவ குடுவை அல்லது சோதனைக் குழாயில் சில துத்தநாகத் துகள்களை எடுத்துக் கொள்ளுங்கள்.
- இதில் நீர்த்த ஹைட்ரோகுளோரிக் அமிலம் அல்லது கந்தக அமிலத்தைச் சேர்க்கவும் (படம் 1.2).
எச்சரிக்கை: அமிலத்தை கவனத்துடன் கையாளவும்.
- துத்தநாகத் துகள்களைச் சுற்றி ஏதாவது நடப்பதை நீங்கள் கவனிக்கிறீர்களா?
- கூம்பு வடிவ குடுவை அல்லது சோதனைக் குழாயைத் தொடவும். அதன் வெப்பநிலையில் ஏதேனும் மாற்றம் உள்ளதா?
மேலே உள்ள மூன்று செயல்பாடுகளிலிருந்து, பின்வரும் கவனிப்புகளில் ஏதேனும் ஒரு வேதியியல் வினை நடந்துள்ளதா என்பதை தீர்மானிக்க உதவுகிறது என்று நாம் கூறலாம் –
- நிலையில் மாற்றம்
- நிறத்தில் மாற்றம்
- ஒரு வாயுவின் வெளியீடு
- வெப்பநிலையில் மாற்றம்.
நம்மைச் சுற்றி ஏற்படும் மாற்றங்களை நாம் கவனிக்கும்போது, நம்மைச் சுற்றி பல்வேறு வகையான வேதியியல் வினைகள் நடைபெறுவதைக் காணலாம். இந்த அத்தியாயத்தில் பல்வேறு வகையான வேதியியல் வினைகள் மற்றும் அவற்றின் குறியீட்டு பிரதிநிதித்துவம் பற்றி நாம் படிப்போம்.
1.1 வேதியியல் சமன்பாடுகள்
செயல்பாடு 1.1 பின்வருமாறு விவரிக்கப்படலாம் – ஒரு மெக்னீசியம் நாடா ஆக்ஸிஜனில் எரிக்கப்படும் போது, அது மெக்னீசியம் ஆக்சைடாக மாற்றப்படுகிறது. ஒரு வேதியியல் வினையை வாக்கிய வடிவில் விவரிப்பது மிகவும் நீளமானது. இதை ஒரு குறுகிய வடிவத்தில் எழுதலாம். இதைச் செய்ய எளிய வழி, அதை ஒரு சொல்-சமன்பாட்டின் வடிவத்தில் எழுதுவது. மேலே உள்ள வினைக்கான சொல்-சமன்பாடு –
$ \underset{(\text{Reactants})}{\mathrm{Magnesium}+\mathrm{Oxygen}} \rightarrow \underset{(\text{Product})}{\mathrm{Magnesium Oxide}} $
வினையில் (1.1) வேதியியல் மாற்றத்திற்கு உட்படும் பொருட்கள் (1.1), மெக்னீசியம் மற்றும் ஆக்ஸிஜன், வினைபடுபொருட்கள் ஆகும். புதிய பொருள் மெக்னீசியம் ஆக்சைடு, வினையின் போது உருவாகும், ஒரு விளைபொருளாகும்.
ஒரு சொல்-சமன்பாடு வினைபடுபொருட்களிலிருந்து விளைபொருட்களுக்கு அவற்றுக்கிடையே வைக்கப்பட்டுள்ள அம்புக்குறி மூலம் மாற்றத்தைக் காட்டுகிறது. வினைபடுபொருட்கள் இடது பக்கத்தில் (LHS) அவற்றுக்கிடையே கூட்டல் குறி (+) உடன் எழுதப்பட்டுள்ளன. இதேபோல், விளைபொருட்கள் வலது பக்கத்தில் (RHS) அவற்றுக்கிடையே கூட்டல் குறி (+) உடன் எழுதப்பட்டுள்ளன. அம்புக்குறியின் முனை விளைபொருட்களை நோக்கி சுட்டிக்காட்டுகிறது, மற்றும் வினையின் திசையைக் காட்டுகிறது
1.1.1 ஒரு வேதியியல் சமன்பாட்டை எழுதுதல்
வேதியியல் சமன்பாடுகளைக் குறிக்க வேறு எந்த குறுகிய வழியும் உள்ளதா? சொற்களுக்குப் பதிலாக வேதியியல் வாய்பாடுகளைப் பயன்படுத்தினால், வேதியியல் சமன்பாடுகளை மிகவும் சுருக்கமாகவும் பயனுள்ளதாகவும் ஆக்கலாம். ஒரு வேதியியல் சமன்பாடு ஒரு வேதியியல் வினையைக் குறிக்கிறது. மெக்னீசியம், ஆக்ஸிஜன் மற்றும் மெக்னீசியம் ஆக்சைட்டின் வாய்பாடுகளை நீங்கள் நினைவுபடுத்தினால், மேலே உள்ள சொல்-சமன்பாட்டை இவ்வாறு எழுதலாம் -
$$ \begin{equation*} \mathrm{Mg}+\mathrm{O} _{2} \rightarrow \mathrm{MgO} \tag{1.2} \end{equation*} $$
LHS மற்றும் RHS ஆகியவற்றில் உள்ள ஒவ்வொரு தனிமத்தின் அணுக்களின் எண்ணிக்கையை அம்புக்குறியின் இருபுறமும் எண்ணி ஒப்பிடுங்கள். ஒவ்வொரு தனிமத்தின் அணுக்களின் எண்ணிக்கை இருபுறமும் ஒரே மாதிரியாக உள்ளதா? ஆம் என்றால், சமன்பாடு சமநிலையில் உள்ளது. இல்லையென்றால், சமன்பாட்டின் இருபுறமும் நிறை ஒரே மாதிரியாக இல்லாததால் சமன்பாடு சமநிலையற்றது. அத்தகைய வேதியியல் சமன்பாடு ஒரு வினைக்கான எலும்புக்கூட்டு வேதியியல் சமன்பாடு ஆகும். சமன்பாடு (1.2) என்பது காற்றில் மெக்னீசியம் எரிவதற்கான எலும்புக்கூட்டு வேதியியல் சமன்பாடு ஆகும்.
1.1.2 சமநிலை வேதியியல் சமன்பாடுகள்
நீங்கள் IX ஆம் வகுப்பில் படித்த நிறைப் பாதுகாப்பு விதியை நினைவுபடுத்துங்கள்; ஒரு வேதியியல் வினையில் நிறை உருவாக்கப்படவோ அழிக்கப்படவோ முடியாது. அதாவது, ஒரு வேதியியல் வினையின் விளைபொருட்களில் உள்ள தனிமங்களின் மொத்த நிறை, வினைபடுபொருட்களில் உள்ள தனிமங்களின் மொத்த நிறைக்கு சமமாக இருக்க வேண்டும்.
வேறுவிதமாகக் கூறினால், ஒவ்வொரு தனிமத்தின் அணுக்களின் எண்ணிக்கையும், ஒரு வேதியியல் வினைக்கு முன்னும் பின்னும் ஒரே மாதிரியாக இருக்கும். எனவே, ஒரு எலும்புக்கூட்டு வேதியியல் சமன்பாட்டை சமநிலைப்படுத்த வேண்டும். வேதியியல் சமன்பாடு (1.2) சமநிலையில் உள்ளதா? படிப்படியாக ஒரு வேதியியல் சமன்பாட்டை சமநிலைப்படுத்துவது பற்றி அறிந்து கொள்வோம்.
செயல்பாடு 1.3க்கான சொல்-சமன்பாடு பின்வருமாறு குறிப்பிடப்படலாம் -
$\mathrm{Zinc + Sulphuric \quad acid}\rightarrow \mathrm{Zinc \quad sulphate + Hydrogen}$
மேலே உள்ள சொல்-சமன்பாடு பின்வரும் வேதியியல் சமன்பாட்டால் குறிப்பிடப்படலாம் -
$$\mathrm{Zn}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{ZnSO} _{4}+\mathrm{H} _{2} \tag{1.3}$$
அம்புக்குறியின் இருபுறமும் உள்ள வெவ்வேறு தனிமங்களின் அணுக்களின் எண்ணிக்கையைப் பார்ப்போம்.
| தனிமம் | வினைபடுபொருட்களில் உள்ள அணுக்களின் எண்ணிக்கை (LHS) | விளைபொருட்களில் உள்ள அணுக்களின் எண்ணிக்கை (RHS) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{~S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
ஒவ்வொரு தனிமத்தின் அணுக்களின் எண்ணிக்கையும் அம்புக்குறியின் இருபுறமும் ஒரே மாதிரியாக இருப்பதால், சமன்பாடு (1.3) ஒரு சமநிலை வேதியியல் சமன்பாடு ஆகும்.
பின்வரும் வேதியியல் சமன்பாட்டை சமநிலைப்படுத்த முயற்சிப்போம் -
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.4} \end{equation*} $$
படி I: ஒரு வேதியியல் சமன்பாட்டை சமநிலைப்படுத்த, முதலில் ஒவ்வொரு வாய்பாட்டையும் சுற்றி பெட்டிகளை வரையவும். சமன்பாட்டை சமநிலைப்படுத்தும் போது பெட்டிகளுக்குள் எதையும் மாற்ற வேண்டாம்.
$$ \begin{equation*} \mathrm{Fe}+\mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+\mathrm{H} _{2} \tag{1.5} \end{equation*} $$
படி II: சமநிலையற்ற சமன்பாட்டில் (1.5) உள்ள வெவ்வேறு தனிமங்களின் அணுக்களின் எண்ணிக்கையை பட்டியலிடுங்கள்.
| தனிமம் | வினைபடுபொருட்களில் உள்ள அணுக்களின் எண்ணிக்கை (LHS) | விளைபொருட்களில் உள்ள அணுக்களின் எண்ணிக்கை (RHS) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
படி III: அதிகபட்ச அணுக்களைக் கொண்ட சேர்மத்துடன் சமநிலைப்படுத்தத் தொடங்குவது பெரும்பாலும் வசதியானது. அது ஒரு வினைபடுபொருளாகவோ அல்லது விளைபொருளாகவோ இருக்கலாம். அந்தச் சேர்மத்தில், அதிகபட்ச அணுக்களைக் கொண்ட தனிமத்தைத் தேர்ந்தெடுக்கவும். இந்த அளவுகோல்களைப் பயன்படுத்தி, நாம் $Fe_3 O_4$ மற்றும் அதில் உள்ள ஆக்ஸிஜன் தனிமத்தைத் தேர்ந்தெடுக்கிறோம். RHS இல் நான்கு ஆக்ஸிஜன் அணுக்கள் உள்ளன, LHS இல் ஒன்று மட்டுமே உள்ளன.
ஆக்ஸிஜன் அணுக்களை சமநிலைப்படுத்த -
| ஆக்ஸிஜனின் அணுக்கள் |
வினைபடுபொருட்களில் | விளைபொருட்களில் |
|---|---|---|
| (i) ஆரம்ப | 1($ \mathrm{H_2O} $ இல்) | 4($ \mathrm{Fe_3O_4} $ இல்) |
| (ii) சமநிலைப்படுத்த | 1 $\times$ 4 | 4 |
அணுக்களின் எண்ணிக்கையை சமப்படுத்த, வினையில் ஈடுபடும் சேர்மங்கள் அல்லது தனிமங்களின் வாய்பாடுகளை மாற்ற முடியாது என்பதை நினைவில் கொள்ள வேண்டும். எடுத்துக்காட்டாக, ஆக்ஸிஜன் அணுக்களை சமநிலைப்படுத்த, குணகம் ‘4’ ஐ $4 H_2 O$ என வைக்கலாம், ஆனால் $H_2 O_4$ அல்லது $(H_2 O)_4$ அல்ல. இப்போது பகுதியாக சமநிலைப்படுத்தப்பட்ட சமன்பாடு ஆகிறது -
$$ \begin{equation*}\boxed{\mathrm{Fe}}+4\boxed{\mathrm{H_2O}}\rightarrow \boxed{\mathrm{Fe_3O_4}}+\boxed{\mathrm{H_2}} \hspace{123 px} \tag {1.6} \end{equation*} $$ (பகுதியாக சமநிலைப்படுத்தப்பட்ட சமன்பாடு)
படி IV: Fe மற்றும் $H$ அணுக்கள் இன்னும் சமநிலையில் இல்லை. மேலும் தொடர இந்த தனிமங்களில் ஏதேனும் ஒன்றைத் தேர்ந்தெடுக்கவும். பகுதியாக சமநிலைப்படுத்தப்பட்ட சமன்பாட்டில் ஹைட்ரஜன் அணுக்களை சமநிலைப்படுத்துவோம்.
$H$ அணுக்களின் எண்ணிக்கையை சமப்படுத்த, ஹைட்ரஜன் மூலக்கூறுகளின் எண்ணிக்கையை RHS இல் நான்காக ஆக்கவும்.
| ஹைட்ரஜனின் அணுக்கள் |
வினைபடுபொருட்களில் | விளைபொருட்களில் |
|---|---|---|
| (i) ஆரம்ப | 8($ \mathrm{4H_2O} $ இல்) | 2($ \mathrm{H_2} $ இல்) |
| (ii) சமநிலைப்படுத்த | 8 | 2 $\times$ 4 |
சமன்பாடு இருக்கும் -
$$ \begin{equation*} \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.7} \end{equation*} $$
(பகுதியாக சமநிலைப்படுத்தப்பட்ட சமன்பாடு)
படி V: மேலே உள்ள சமன்பாட்டைப் பார்த்து, சமநிலையற்ற மூன்றாவது தனிமத்தைத் தேர்ந்தெடுக்கவும். ஒரே ஒரு தனிமம் மட்டுமே சமநிலைப்படுத்தப்பட வேண்டும் என்பதை நீங்கள் காணலாம், அதாவது, இரும்பு.
| இரும்பின் அணுக்கள் | வினைபடுபொருட்களில் | விளைபொருட்களில் |
|---|---|---|
| (i) ஆரம்ப | 1($ \mathrm{Fe} $ இல்) | 3($ \mathrm{Fe_3O_4} $ இல்) |
| (ii) சமநிலைப்படுத்த | 1 $\times$ 3 | 3 |
$Fe$ ஐ சமப்படுத்த, LHS இல் $Fe$ இன் மூன்று அணுக்களை எடுத்துக்கொள்கிறோம்.
$$ \begin{equation*} 3 \boxed{\mathrm{Fe}}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.8} \end{equation*} $$
படி VI: இறுதியாக, சமநிலைப்படுத்தப்பட்ட சமன்பாட்டின் சரியான தன்மையைச் சரிபார்க்க, சமன்பாட்டின் இருபுறமும் உள்ள ஒவ்வொரு தனிமத்தின் அணுக்களையும் எண்ணுகிறோம்.
$$ \begin{equation*} 3 \mathrm{Fe}+4 \mathrm{H} _{2} \mathrm{O} \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}+4 \mathrm{H} _{2} \tag{1.9} \end{equation*} $$
(சமநிலைப்படுத்தப்பட்ட சமன்பாடு)
சமன்பாடு (1.9) இன் இருபுறமும் உள்ள தனிமங்களின் அணுக்களின் எண்ணிக்கை சமம். இந்த சமன்பாடு இப்போது சமநிலையில் உள்ளது. வேதியியல் சமன்பாடுகளை சமநிலைப்படுத்தும் இந்த முறை, சிறிய முழு எண் குணகத்தைப் பயன்படுத்தி சமன்பாட்டை சமநிலைப்படுத்த சோதனைகளைச் செய்வதால், ஹிட்-அண்ட்-ட்ரையல் முறை என்று அழைக்கப்படுகிறது.
படி VII: இயற்பியல் நிலைகளின் குறியீடுகளை எழுதுதல் மேலே உள்ள சமநிலைப்படுத்தப்பட்ட சமன்பாடு (1.9) ஐ கவனமாகப் பாருங்கள். ஒவ்வொரு வினைபடுபொருள் மற்றும் விளைபொருளின் இயற்பியல் நிலை பற்றி இந்த சமன்பாடு நமக்கு ஏதாவது சொல்கிறதா? அவற்றின் இயற்பியல் நிலைகள் பற்றிய தகவல் இந்த சமன்பாட்டில் கொடுக்கப்படவில்லை.
ஒரு வேதியியல் சமன்பாட்டை மேலும் தகவலறிந்ததாக ஆக்க, வினைபடுபொருட்கள் மற்றும் விளைபொருட்களின் இயற்பியல் நிலைகள் அவற்றின் வேதியியல் வாய்பாடுகளுடன் குறிப்பிடப்படுகின்றன. வினைபடுபொருட்கள் மற்றும் விளைபொருட்களின் வாயு, திரவ, நீரிய மற்றும் திட நிலைகள் முறையே (g), (l), (aq) மற்றும் (s) குறியீடுகளால் குறிக்கப்படுகின்றன. வினைபடுபொருள் அல்லது விளைபொருள் நீரில் ஒரு கரைசலாக இருந்தால், நீரிய (aq) என்ற சொல் எழுதப்படுகிறது.
சமநிலைப்படுத்தப்பட்ட சமன்பாடு (1.9) ஆகிறது
$$ \begin{equation*} 3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H} _{2} \mathrm{O}(\mathrm{g}) \rightarrow \mathrm{Fe} _{3} \mathrm{O} _{4}(\mathrm{~s})+4 \mathrm{H} _{2}(\mathrm{~g}) \tag{1.10} \end{equation*} $$
$(g)$ குறியீடு $H_2 O$ உடன் பயன்படுத்தப்படுகிறது என்பதை கவனிக்கவும், இந்த வினையில் நீர் நீராவி வடிவில் பயன்படுத்தப்படுகிறது என்பதைக் குறிக்க.
பொதுவாக இயற்பியல் நிலைகள் அவற்றைக் குறிப்பிட வேண்டியதன் அவசியம் இல்லாவிட்டால், ஒரு வேதியியல் சமன்பாட்டில் சேர்க்கப்படுவதில்லை.
சில நேரங்களில் வினை நிலைமைகள், வெப்பநிலை, அழுத்தம், வினையூக்கி போன்றவை, சமன்பாட்டில் அம்புக்குறிக்கு மேலே மற்றும்/அல்லது கீழே குறிக்கப்படுகின்றன. உதாரணத்திற்கு -
$$\mathrm{CO}(\mathrm{g})+2 \mathrm{H}_2(\mathrm{~g}) \xrightarrow{340 \mathrm{~atm}} \mathrm{CH}_3 \mathrm{OH}(\mathrm{l}) \quad \tag{1.11}$$
$6 \mathrm{CO_2} (aq) +12 \mathrm{H_2 O(l)} \xrightarrow[\text{ Chlorophyll }]{\text{ Sunlight }} \underset{\text{ (Glucose) }}{\mathrm{C_6 H_{12} O_6} \text{ (aq) }}+6 \mathrm{O_2} (aq) +6 \mathrm{H_2 O}(l) \tag {1.12}$
இந்த படிகளைப் பயன்படுத்தி, முன்பு உரையில் கொடுக்கப்பட்ட சமன்பாடு (1.2) ஐ நீங்கள் சமநிலைப்படுத்த முடியுமா?
1.2 வேதியியல் வினைகளின் வகைகள்
ஒரு வேதியியல் வினையின் போது ஒரு தனிமத்தின் அணுக்கள் மற்றொரு தனிமத்தின் அணுக்களாக மாறாது என்பதை நாம் IX ஆம் வகுப்பில் கற்றுக்கொண்டோம். அணுக்கள் கலவையிலிருந்து மறைந்துவிடுவதில்லை அல்லது வேறு இடத்திலிருந்து தோன்றுவதில்லை. உண்மையில், வேதியியல் வினைகள் புதிய பொருட்களை உற்பத்தி செய்வதற்காக அணுக்களுக்கு இடையே உள்ள பிணைப்புகளை உடைப்பதையும் உருவாக்குவதையும் உள்ளடக்கியது. அத்தியாயங்கள் 3 மற்றும் 4 இல் அணுக்களுக்கு இடையே உருவாகும் பிணைப்புகளின் வகைகள் பற்றி நீங்கள் படிப்பீர்கள்.
1.2.1 சேர்மான வினை
செயல்பாடு 1.4
- ஒரு குடுவையில் சிறிது கால்சியம் ஆக்சைடு அல்லது சுண்ணாம்பை எடுத்துக் கொள்ளுங்கள்.
- இதில் மெதுவாக தண்ணீர் சேர்க்கவும்.
- படம் 1.3 இல் காட்டப்பட்டுள்ளபடி குடுவையைத் தொடவும்.
- வெப்பநிலையில் ஏதேனும் மாற்றத்தை நீங்கள் உணர்கிறீர்களா?
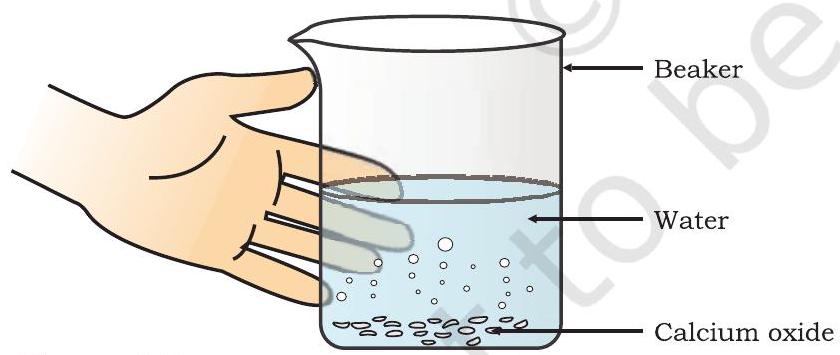
படம் 1.3 கால்சியம் ஆக்சைடு மற்றும் நீரின் வினையால் சுண்ணாம்பு உருவாதல்
கால்சியம் ஆக்சைடு தண்ணீருடன் தீவிரமாக வினைபட்டு சுண்ணாம்பு (கால்சியம் ஹைட்ராக்சைடு) உற்பத்தி செய்கிறது, அதிக அளவு வெப்பத்தை வெளியிடுகிறது.
$$ \underset{\text{ (Quick lime) }}{\mathrm{CaO(s)}}+\quad \mathrm{H_2 O(l)} \to \underset{\text{ (Slaked lime) }}{\mathrm{Ca(OH)_2(aq)}}+\text{ Heat } \tag {1.13} $$
இந்த வினையில், கால்சியம் ஆக்சைடு மற்றும் நீர் சேர்ந்து ஒரு ஒற்றை விளைபொருளான கால்சியம் ஹைட்ராக்சைடை உருவாக்குகின்றன. இரண்டு அல்லது அதற்கு மேற்பட்ட வினைபடுபொருட்களிலிருந்து ஒரு ஒற்றை விளைபொருள் உருவாகும் இத்தகைய வினை சேர்மான வினை என்று அழைக்கப்படுகிறது.
உங்களுக்குத் தெரியுமா?
வினை 1.13 மூலம் உற்பத்தி செய்யப்படும் சுண்ணாம்பின் கரைசல் சுவர்களை வெள்ளையடிக்கப் பயன்படுகிறது. கால்சியம் ஹைட்ராக்சைடு காற்றில் உள்ள கார்பன் டை ஆக்சைட்டுடன் மெதுவாக வினைபட்டு சுவர்களில் கால்சியம் கார்பனேட்டின் மெல்லிய அடுக்கை உருவாக்குகிறது. வெள்ளையடித்த இரண்டு முதல் மூன்று நாட்களுக்குப் பிறகு கால்சியம் கார்பனேட் உருவாகி சுவர்களுக்கு மினுமினுப்பான முடிவை அளிக்கிறது. பளிங்குக்கான வேதியியல் வாய்பாடும் $CaCO_3$ என்பது கவனிக்கத்தக்கது.
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$
சேர்மான வினைகளின் இன்னும் சில எடுத்துக்காட்டுகளைப் பற்றி விவாதிப்போம்.
(i) நிலக்கரியை எரித்தல்
$$ \begin{equation*} \mathrm{C}(\mathrm{s})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g}) \tag{1.15} \end{equation*} $$
(ii) $H_2(g)$ மற்றும் $O_2(g)$ இலிருந்து நீர் உருவாதல்
$$ \begin{equation*} 2 \mathrm{H} _{2}(\mathrm{~g})+\mathrm{O} _{2}(\mathrm{~g}) \rightarrow 2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$
எளிய மொழியில், இரண்டு அல்லது அதற்கு மேற்பட்ட பொருட்கள் (தனிமங்கள் அல்லது சேர்மங்கள்) சேர்ந்து ஒரு ஒற்றை விளைபொருளை உருவாக்கும் போது, அந்த வினைகள் சேர்மான வினைகள் என்று கூறலாம்.
செயல்பாடு 1.4 இல், அதிக அளவு வெப்பம் வெளியிடப்படுவதையும் நாம் கவனித்தோம். இது வினை கலவையை சூடாக்குகிறது. விளைபொருட்கள் உருவாவதுடன் வெப்பம் வெளியிடப்படும் வினைகள் வெப்பவெளியீட்டு வேதியியல் வினைகள் என்று அழைக்கப்படுகின்றன.
வெப்பவெளியீட்டு வினைகளின் பிற எடுத்துக்காட்டுகள் -
(i) இயற்கை எரிவாயுவை எரித்தல்
$$ \begin{equation*} \mathrm{CH_4(g)+2 O_2(g) \to CO_2(g)+2 H_2 O(g)} \tag{1.17} \end{equation*} $$
(ii) சுவாசிப்பு ஒரு வெப்பவெளியீட்டு செயல்முறை என்பது உங்களுக்குத் தெரியுமா?
வாழ நமக்கு ஆற்றல் தேவை என்பது நமக்குத் தெரியும். நாம் உண்ணும் உணவிலிருந்து இந்த ஆற்றலைப் பெறுகிறோம். செரிமானத்தின் போது, உணவு எளிமையான பொருட்களாக உடைக்கப்படுகிறது. எடுத்துக்காட்டாக, அரிசி, உருளைக்கிழங்கு மற்றும் ரொட்டியில் கார்போஹைட்ரேட்டுகள் உள்ளன. இந்த கார்போஹைட்ரேட்டுகள் உடைக்கப்பட்டு குளுக்கோஸ் உருவாகிறது. இந்த குளுக்கோஸ் நம் உடலின் செல்களில் உள்ள ஆக்ஸிஜனுடன் இணைந்து ஆற்றலை வழங்குகிறது. இந்த வினையின் சிறப்புப் பெயர் சுவாசிப்பு, அதன் செயல்முறையை நீங்கள் அத்தியாயம் 6 இல் படிப்பீர்கள்.
$ \begin{equation*} \underset{\text{ (குளுக்கோஸ்) }}{C_6 H_{12} O_6(aq)}+6 O_2(aq) \to 6 CO_2(aq)+6 H_2 O(l)+\text{ ஆற்றல் } \tag{1.18} \end{equation*} $
(iii) காய்கறி பொருட்களின் சிதைவு குப்பையாக மாறுவதும் வெப்பவெளியீட்டு வினைக்கு ஒரு எடுத்துக்காட்டு.
செயல்பாடு 1.1 இல் நடைபெறும் வினையின் வகையை அடையாளம் காணவும், அங்கு ஒரு ஒற்றை விளைபொருளின் உருவாக்கத்துடன் வெப்பம் வெளியிடப்படுகிறது.
1.2.2 சிதைவு வினை
செயல்பாடு 1.5
- ஒரு உலர் கொதிக்கும் குழாயில் சுமார் $2 g$ பெர்ரஸ் சல்பேட் படிகங்களை எடுத்துக் கொள்ளுங்கள்.
- பெர்ரஸ் சல்பேட் படிகங்களின் நிறத்தைக் கவனிக்கவும்.
- படம் 1.4 இல் காட்டப்பட்டுள்ளபடி ஒரு பர்னர் அல்லது ஆவிவிளக்கின் சுடரில் கொதிக்கும் குழாயை சூடாக்கவும்.
- சூடாக்கிய பிறகு படிகங்களின் நிறத்தைக் கவனிக்கவும்.
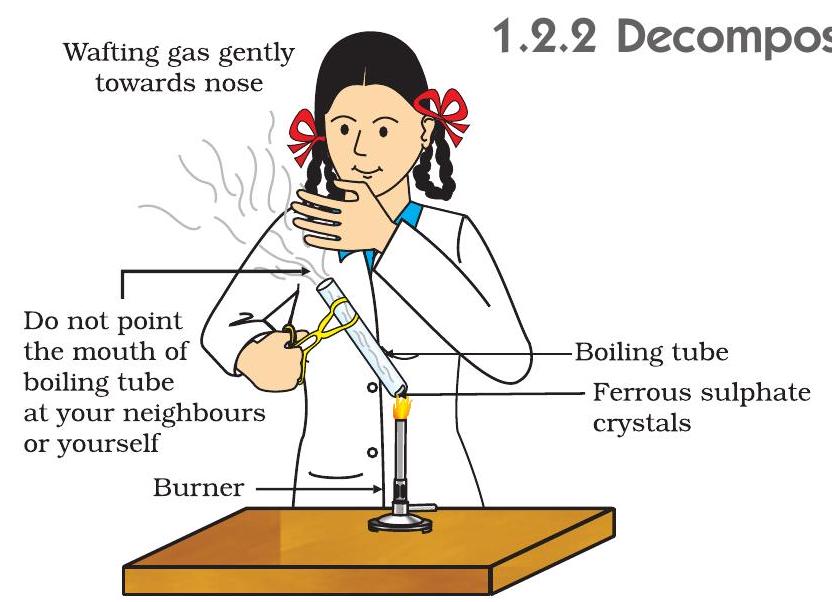
படம் 1.4 பெர்ரஸ் சல்பேட் படிகங்கள் கொண்ட கொதிக்கும் குழாயை சூடாக்குவதற்கும் மணத்தை முகர்வதற்கும் சரியான வழி
பெர்ரஸ் சல்பேட் படிகங்களின் பச்சை நிறம் மாறிவிட்டதை நீங்கள் கவனித்தீர்களா? எரியும் கந்தகத்தின் தனித்துவமான வாசனையையும் நீங்கள் முகரலாம்.
$ \underset{\text{(பெர்ரஸ் சல்பேட்)}}{\mathrm{2 FeSO_4(s)}} \xrightarrow[\text{ (பெரிக் ஆக்சைடு) }]{\text{ வெப்பம் }} \underset{\text{ Fe }}{\mathrm{Fe_2 O_3(s)+SO_2(g)+SO_3(g)}} \quad {1.19} $
இந்த வினையில், ஒரு ஒற்றை வினைபடுபொருள் எளிமையான விளைபொருட்களைக் கொடுக்க உடைந்துவிடுவதை நீங்கள் கவனிக்கலாம். இது ஒரு சிதைவு வினை. பெர்ரஸ்











