کیا ہمارے ارد گرد کی مادہ خالص ہے؟
ہم کیسے فیصلہ کرتے ہیں کہ دودھ، گھی، مکھن، نمک، مصالحے، معدنی پانی یا جوس جو ہم بازار سے خریدتے ہیں خالص ہیں؟

شکل 2.1: کچھ قابل استعمال اشیاء
کیا آپ نے کبھی ان قابل استعمال اشیاء کے پیکٹوں پر ‘خالص’ لکھا ہوا دیکھا ہے؟ عام آدمی کے لیے خالص کا مطلب ہے جس میں ملاوٹ نہ ہو۔ لیکن، ایک سائنسدان کے لیے یہ تمام چیزیں درحقیقت مختلف مادوں کے مرکب ہیں اور اس لیے خالص نہیں ہیں۔ مثال کے طور پر، دودھ درحقیقت پانی، چکنائی، پروٹین وغیرہ کا مرکب ہے۔ جب ایک سائنسدان کہتا ہے کہ کوئی چیز خالص ہے، تو اس کا مطلب ہے کہ اس مادے کے تمام تشکیل دینے والے ذرات اپنی کیمیائی نوعیت میں ایک جیسے ہیں۔ ایک خالص مادہ ایک قسم کے ذرات پر مشتمل ہوتا ہے۔ دوسرے لفظوں میں، ایک مادہ مادے کی خالص واحد شکل ہے۔
جیسا کہ ہم ارد گرد دیکھتے ہیں، ہم دیکھ سکتے ہیں کہ ہمارے ارد گرد کی زیادہ تر مادہ دو یا دو سے زیادہ خالص اجزاء کے مرکب کی شکل میں موجود ہے، مثال کے طور پر، سمندری پانی، معدنیات، مٹی، وغیرہ، سب مرکب ہیں۔
2.1 مرکب کیا ہے؟
مرکب مادے کی خالص شکل سے زیادہ ایک قسم سے بنتے ہیں۔ ہم جانتے ہیں کہ گھلے ہوئے سوڈیم کلورائیڈ کو پانی سے بخارات بننے کے جسمانی عمل کے ذریعے الگ کیا جا سکتا ہے۔ تاہم، سوڈیم کلورائیڈ خود ایک خالص مادہ ہے اور اسے اس کے کیمیائی اجزاء میں جسمانی عمل کے ذریعے الگ نہیں کیا جا سکتا۔ اسی طرح، چینی ایک ایسا مادہ ہے جس میں صرف ایک قسم کی خالص مادہ ہوتی ہے اور اس کی ترکیب ہر جگہ یکساں ہوتی ہے۔
سافٹ ڈرنک اور مٹی واحد خالص مادے نہیں ہیں۔ خالص مادہ کا ماخذ جو بھی ہو، اس میں ہمیشہ یکساں خصوصی خصوصیات ہوں گی۔
لہذا، ہم کہہ سکتے ہیں کہ ایک مرکب میں ایک سے زیادہ خالص مادہ ہوتے ہیں۔
2.1.1 مرکب کی اقسام
مرکب بنانے والے اجزاء کی نوعیت پر منحصر ہے، ہمارے پاس مختلف قسم کے مرکب ہو سکتے ہیں۔
سرگرمی 2.1
آئیے کلاس کو گروپ A، $B, C$ اور $D$ میں تقسیم کرتے ہیں۔
-
گروپ A ایک بیکر لیتا ہے جس میں $50 mL$ پانی ہو اور ایک اسپاٹولا بھر کاپر سلفیٹ پاؤڈر۔ گروپ B ایک بیکر میں $50 mL$ پانی اور دو اسپاٹولا بھر کاپر سلفیٹ پاؤڈر لیتا ہے۔
-
گروپ C اور D کاپر سلفیٹ اور پوٹاشیم پرمنگنیٹ یا عام نمک (سوڈیم کلورائیڈ) کی مختلف مقدار لے سکتے ہیں اور دیے گئے اجزاء کو ملا کر ایک مرکب بنا سکتے ہیں۔ رنگ اور ساخت میں یکسانیت پر مشاہدات رپورٹ کریں۔
-
گروپ A اور B نے ایک ایسا مرکب حاصل کیا ہے جس کی ترکیب ہر جگہ یکساں ہے۔ ایسے مرکبوں کو ہم جنس مرکب یا محلول کہتے ہیں۔ ایسے مرکبوں کی کچھ دیگر مثالیں ہیں: (i) پانی میں گھلا ہوا نمک اور (ii) پانی میں گھلی ہوئی چینی۔ دونوں گروپوں کے محلولوں کے رنگ کا موازنہ کریں۔ اگرچہ دونوں گروپوں نے کاپر سلفیٹ کا محلول حاصل کیا ہے لیکن محلولوں کے رنگ کی شدت مختلف ہے۔ یہ ظاہر کرتا ہے کہ ایک ہم جنس مرکب میں متغیر ترکیب ہو سکتی ہے۔
-
گروپ C اور D نے ایسے مرکب حاصل کیے ہیں، جو جسمانی طور پر الگ الگ حصوں پر مشتمل ہیں اور ان کی ترکیب غیر یکساں ہے۔ ایسے مرکبوں کو غیر ہم جنس مرکب کہتے ہیں۔ سوڈیم کلورائیڈ اور لوہے کے برادے، نمک اور گندھک، اور تیل اور پانی کے مرکب غیر ہم جنس مرکب کی مثالیں ہیں۔
سرگرمی 2.2
-
آئیے دوبارہ کلاس کو چار گروپوں- A, B, C اور D میں تقسیم کرتے ہیں۔
-
ہر گروپ کو درج ذیل نمونے تقسیم کریں:
-
گروپ A کو کاپر سلفیٹ کے چند کرسٹل۔
-
گروپ B کو ایک اسپاٹولا بھر کاپر سلفیٹ۔
-
گروپ $C$ کو چاک پاؤڈر یا گیہوں کا آٹا۔
-
گروپ D کو دودھ یا سیاہی کی چند بوندیں۔
-
-
ہر گروپ کو دیا گیا نمونہ پانی میں ملانا چاہیے اور شیشے کی سلاخ سے اچھی طرح ہلانا چاہیے۔ کیا مرکب میں ذرات نظر آتے ہیں؟
-
مرکب والے بیکر کے ذریعے ٹارچ سے روشنی کی کرن ڈالیں اور سامنے سے مشاہدہ کریں۔ کیا روشنی کی کرن کا راستہ نظر آیا؟
-
مرکبوں کو کچھ منٹ کے لیے بغیر ہلائے چھوڑ دیں (اور اس دوران فلٹریشن کا سامان تیار کریں)۔ کیا مرکب مستحکم ہے یا کچھ وقت بعد ذرات بیٹھنے لگتے ہیں؟
-
مرکب کو فلٹر کریں۔ کیا فلٹر پیپر پر کوئی باقیات ہیں؟
-
نتائج پر بحث کریں اور رائے قائم کریں۔
گروپ $A$ اور $B$ نے ایک محلول حاصل کیا ہے۔
گروپ $C$ نے ایک معلق حاصل کیا ہے۔
گروپ D نے ایک کولائیڈل محلول حاصل کیا ہے۔
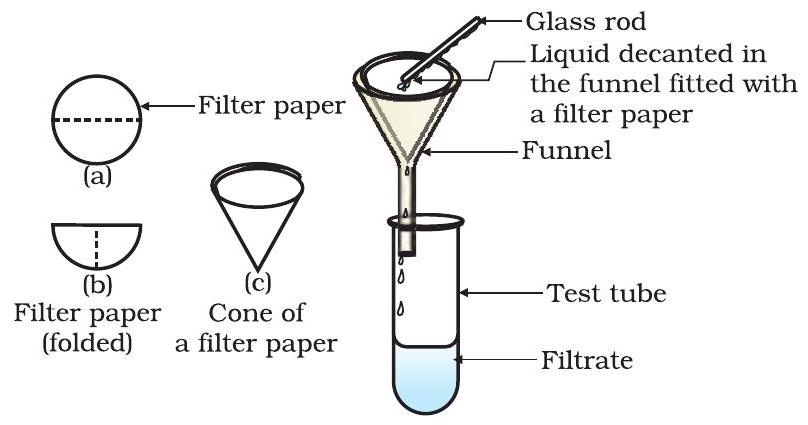
شکل 2.2: فلٹریشن
اب، ہم آئندہ حصوں میں محلول، معلق اور کولائیڈل محلول کے بارے میں سیکھیں گے۔
2.2 محلول کیا ہے؟
محلول دو یا دو سے زیادہ مادوں کا ہم جنس مرکب ہے۔ آپ اپنی روزمرہ زندگی میں مختلف قسم کے محلولوں سے واسطہ پڑتا ہے۔ لیموں پانی، سوڈا واٹر، وغیرہ، سب محلولوں کی مثالیں ہیں۔ عام طور پر ہم محلول کو ایک مائع کے طور پر سوچتے ہیں جس میں کوئی ٹھوس، مائع یا گیس گھلی ہوئی ہو۔ لیکن، ہمارے پاس ٹھوس محلول (مُصْطَلِح) اور گیس محلول (ہوا) بھی ہو سکتے ہیں۔ ایک محلول میں ذرہ کی سطح پر یکسانیت ہوتی ہے۔ مثال کے طور پر، لیموں پانی ہر جگہ ایک جیسا ذائقہ رکھتا ہے۔ یہ ظاہر کرتا ہے کہ چینی یا نمک کے ذرات محلول میں یکساں طور پر تقسیم ہیں۔
مُصْطَلِح: مُصْطَلِح دو یا دو سے زیادہ دھاتوں یا ایک دھات اور ایک غیر دھات کے مرکب ہیں اور انہیں جسمانی طریقوں سے ان کے اجزاء میں الگ نہیں کیا جا سکتا۔ لیکن پھر بھی، ایک مُصْطَلِح کو مرکب سمجھا جاتا ہے کیونکہ یہ اپنے اجزاء کی خصوصیات ظاہر کرتا ہے اور اس کی ترکیب متغیر ہو سکتی ہے۔ مثال کے طور پر، پیتل تقریباً $30 %$ زنک اور $70 %$ تانبے کا مرکب ہے۔
ایک محلول میں ایک محلل اور ایک محلول اس کے اجزاء کے طور پر ہوتے ہیں۔ محلول کا وہ جزو جو دوسرے جزو کو اس میں گھلاتا ہے (عام طور پر وہ جزو جو زیادہ مقدار میں موجود ہوتا ہے) محلل کہلاتا ہے۔ محلول کا وہ جزو جو محلل میں گھل جاتا ہے (عام طور پر کم مقدار میں موجود ہوتا ہے) محلول کہلاتا ہے۔
مثالیں:
(i) پانی میں چینی کا محلول ٹھوس میں مائع محلول ہے۔ اس محلول میں، چینی محلول ہے اور پانی محلل ہے۔
(ii) الکحل میں آیوڈین کا محلول جسے ‘ٹنکچر آف آیوڈین’ کہتے ہیں، میں آیوڈین (ٹھوس) محلول ہے اور الکحل (مائع) محلل ہے۔
(iii) ایریٹڈ ڈرنکس جیسے سوڈا واٹر، وغیرہ، گیس میں مائع محلول ہیں۔ ان میں کاربن ڈائی آکسائیڈ (گیس) محلول کے طور پر اور پانی (مائع) محلل کے طور پر ہوتا ہے۔
(iv) ہوا گیس میں گیس کا مرکب ہے۔ ہوا متعدد گیسوں کا ہم جنس مرکب ہے۔ اس کے دو اہم اجزاء ہیں: آکسیجن $(21 %)$ اور نائٹروجن (78%)۔ دیگر گیسوں کی مقدار بہت کم ہوتی ہے۔
محلول کی خصوصیات
-
محلول ایک ہم جنس مرکب ہے۔
-
محلول کے ذرات $1 nm(10^{-9}.$ میٹر $)$ قطر سے چھوٹے ہوتے ہیں۔ لہذا، وہ ننگی آنکھوں سے نہیں دیکھے جا سکتے۔
-
بہت چھوٹے ذرہ سائز کی وجہ سے، وہ محلول سے گزرنے والی روشنی کی کرن کو منتشر نہیں کرتے۔ لہذا، محلول میں روشنی کا راستہ نظر نہیں آتا۔
-
محلول کے ذرات کو فلٹریشن کے عمل کے ذریعے مرکب سے الگ نہیں کیا جا سکتا۔ محلول کے ذرات بغیر ہلائے چھوڑنے پر بیٹھتے نہیں ہیں، یعنی محلول مستحکم ہوتا ہے۔
2.2.1 محلول کی ارتکاز
سرگرمی 2.2 میں، ہم نے مشاہدہ کیا کہ گروپ A اور B نے مختلف رنگت کے محلول حاصل کیے۔ لہذا، ہم سمجھتے ہیں کہ ایک محلول میں محلول اور محلل کا نسبتی تناسب مختلف ہو سکتا ہے۔ محلول میں موجود محلول کی مقدار کے لحاظ سے، اسے ہلکا، گاڑھا یا سیر شدہ محلول کہا جا سکتا ہے۔ ہلکا اور گاڑھا تقابلی اصطلاحات ہیں۔ سرگرمی 2.2 میں، گروپ A کے ذریعے حاصل کردہ محلول گروپ B کے ذریعے حاصل کردہ محلول کے مقابلے میں ہلکا ہے۔
سرگرمی 2.3
-
دو الگ الگ بیکروں میں ہر ایک میں تقریباً $50 mL$ پانی لیں۔
-
ایک بیکر میں نمک اور دوسرے بیکر میں چینی یا بیریم کلورائیڈ مسلسل ہلاتے ہوئے ملائیں۔ جب مزید محلول نہ گھل سکے، تو بیکر کے مواد کو تقریباً $5^{\circ} C$ درجہ حرارت بڑھانے کے لیے گرم کریں۔
-
دوبارہ محلول ملانا شروع کریں۔
کیا ایک مخصوص درجہ حرارت پر پانی میں گھلنے والے نمک اور چینی یا بیریم کلورائیڈ کی مقدار ایک جیسی ہے؟
کسی بھی خاص درجہ حرارت پر، ایک محلول جس نے اتنا محلول گھلایا ہو جتنا وہ گھلانے کی صلاحیت رکھتا ہے، سیر شدہ محلول کہلاتا ہے۔ دوسرے لفظوں میں، جب کسی محلول میں ایک مخصوص درجہ حرارت پر مزید محلول نہیں گھلایا جا سکتا، تو اسے سیر شدہ محلول کہتے ہیں۔ اس درجہ حرارت پر سیر شدہ محلول میں موجود محلول کی مقدار کو اس کی حل پذیری کہتے ہیں۔
اگر محلول میں موجود محلول کی مقدار سیر ہونے کی سطح سے کم ہو، تو اسے غیر سیر شدہ محلول کہتے ہیں۔
اگر آپ ایک مخصوص درجہ حرارت پر سیر شدہ محلول لیں اور اسے آہستہ آہستہ ٹھنڈا کریں تو کیا ہوگا؟
ہم اوپر کی سرگرمی سے یہ نتیجہ اخذ کر سکتے ہیں کہ ایک دیے گئے محلل میں مختلف مادوں کی ایک ہی درجہ حرارت پر حل پذیری مختلف ہوتی ہے۔
محلول کی ارتکاز محلول کی دی گئی مقدار (بڑے پیمانے پر یا حجم) میں موجود محلول کی مقدار (بڑے پیمانے پر یا حجم) ہے۔
محلول کی ارتکاز کو ظاہر کرنے کے مختلف طریقے ہیں، لیکن یہاں ہم صرف تین طریقے سیکھیں گے۔
(i) محلول کا بڑے پیمانے پر بڑے پیمانے پر فیصد
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) محلول کا بڑے پیمانے پر حجم فیصد
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) محلول کا حجم بذریعہ حجم فیصد
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
مثال 2.1 ایک محلول میں $40 g$ عام نمک $320 g$ پانی میں ہوتا ہے۔ بڑے پیمانے پر بڑے پیمانے پر فیصد کے لحاظ سے محلول کی ارتکاز کا حساب لگائیں۔
حل:
محلول (نمک) کا بڑے پیمانے پر $\quad=40 g$
محلل (پانی) کا بڑے پیمانے پر $=320 g$
ہم جانتے ہیں،
محلول کا بڑے پیمانے پر $=$ محلول کا بڑے پیمانے پر + محلل کا بڑے پیمانے پر
$$=40 g+320 g$$
$$=360 g$$
محلول کا بڑے پیمانے پر فیصد
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
2.2.2 معلق کیا ہے؟
سرگرمی 2.2 غیر ہم جنس نظام، جیسے کہ گروپ $C$ کے ذریعے سرگرمی 2.2 میں حاصل کردہ، جس میں ٹھوس مائع میں منتشر ہوتے ہیں، معلق کہلاتے ہیں۔ معلق ایک غیر ہم جنس مرکب ہے جس میں محلول کے ذرات گھلتے نہیں ہیں بلکہ میڈیم کے بڑے حصے میں معلق رہتے ہیں۔ معلق کے ذرات ننگی آنکھ سے نظر آتے ہیں۔
معلق کی خصوصیات
-
معلق ایک غیر ہم جنس مرکب ہے۔
-
معلق کے ذرات ننگی آنکھ سے دیکھے جا سکتے ہیں۔
-
معلق کے ذرات اس سے گزرنے والی روشنی کی کرن کو منتشر کرتے ہیں اور اس کا راستہ نظر آنے لگتا ہے۔
-
جب معلق کو بغیر ہلائے چھوڑ دیا جاتا ہے تو محلول کے ذرات بیٹھ جاتے ہیں، یعنی معلق غیر مستحکم ہوتا ہے۔ انہیں فلٹریشن کے عمل کے ذریعے مرکب سے الگ کیا جا سکتا ہے۔ جب ذرات بیٹھ جاتے ہیں، تو معلق ٹوٹ جاتا ہے اور وہ اب روشنی کو منتشر نہیں کرتا۔
2.2.3 کولائیڈل محلول کیا ہے؟
سرگرمی 2.2 گروپ D کے ذریعے سرگرمی 2.2 میں حاصل کردہ مرکب کو کولائیڈ یا کولائیڈل محلول کہتے ہیں۔ کولائیڈ کے ذرات محلول میں یکساں طور پر پھیلے ہوتے ہیں۔ معلق کے مقابلے میں ذرات کے نسبتاً چھوٹے سائز کی وجہ سے، مرکب ہم جنس نظر آتا ہے۔ لیکن درحقیقت، کولائیڈل محلول ایک غیر ہم جنس مرکب ہے، مثال کے طور پر، دودھ۔
کولائیڈل ذرات کے چھوٹے سائز کی وجہ سے، ہم انہیں ننگی آنکھوں سے نہیں دیکھ سکتے۔ لیکن، یہ ذرات آسانی سے نظر آنے والی روشنی کی کرن کو منتشر کر سکتے ہیں جیسا کہ سرگرمی 2.2 میں مشاہدہ کیا گیا۔ روشنی کی کرن کے اس منتشر ہونے کو ٹنڈال اثر کہتے ہیں، اس سائنسدان کے نام پر جس نے اس اثر کو دریافت کیا۔
ٹنڈال اثر اس وقت بھی مشاہدہ کیا جا سکتا ہے جب روشنی کی ایک باریک کرن ایک چھوٹے سوراخ کے ذریعے کمرے میں داخل ہوتی ہے۔ یہ ہوا میں موجود دھول اور دھوئیں کے ذرات کے ذریعے روشنی کے منتشر ہونے کی وجہ سے ہوتا ہے۔
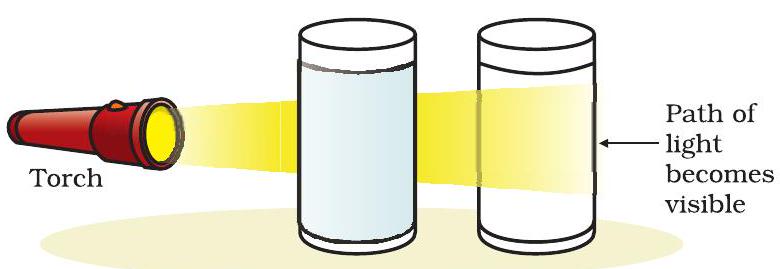
شکل 2.3: (a) کاپر سلفیٹ کا محلول ٹنڈال اثر نہیں دکھاتا، (b) پانی اور دودھ کا مرکب ٹنڈال اثر دکھاتا ہے۔
ٹنڈال اثر اس وقت مشاہدہ کیا جا سکتا ہے جب سورج کی روشنی گھنے جنگل کے چھتر کے ذریعے گزرتی ہے۔ جنگل میں دھند میں پانی کے چھوٹے چھوٹے قطرے ہوتے ہیں، جو ہوا میں منتشر کولائیڈ کے ذرات کے طور پر کام کرتے ہیں۔

شکل 2.4: ٹنڈال اثر
کولائیڈ کی خصوصیات
-
کولائیڈ ایک غیر ہم جنس مرکب ہے۔
-
کولائیڈ کے ذرات کا سائز اتنا چھوٹا ہوتا ہے کہ انہیں ننگی آنکھوں سے انفرادی طور پر نہیں دیکھا جا سکتا۔
-
کولائیڈ اتنا بڑا ہوتا ہے کہ اس سے گزرنے والی روشنی کی کرن کو منتشر کر سکے اور اس کا راستہ نظر آنے لگے۔
-
وہ بغیر ہلائے چھوڑنے پر بیٹھتے نہیں ہیں، یعنی کولائیڈ کافی مستحکم ہوتا ہے۔
-
انہیں فلٹریشن کے عمل کے ذریعے مرکب سے الگ نہیں کیا جا سکتا۔ لیکن، علیحدگی کی ایک خاص تکنیک جسے سینٹرفیوگیشن کہتے ہیں (سرگرمی 2.5 انجام دیں)، کولائیڈل ذرات کو الگ کرنے کے لیے استعمال کی جا سکتی ہے۔
کولائیڈل محلول کے اجزاء منتشر مرحلہ اور منتشر میڈیم ہیں۔ محلول نما جزو یا کولائیڈ میں منتشر ذرات منتشر مرحلہ بناتے ہیں، اور وہ جزو جس میں منتشر مرحلہ معلق ہوتا ہے منتشر میڈیم کہلاتا ہے۔ کولائیڈز کو منتشر میڈیم اور منتشر مرحلے کی حالت (ٹھوس، مائع یا گیس) کے مطابق درجہ بندی کیا جاتا ہے۔ کچھ عام مثالیں جدول 2.1 میں دی گئی ہیں۔ اس جدول سے آپ دیکھ سکتے ہیں کہ یہ روزمرہ کی زندگی میں بہت عام ہیں۔
جدول 2.1: کولائیڈز کی عام مثالیں
| منتشر مرحلہ | منتشر میڈیم | قسم | مثال |
|---|---|---|---|
| مائع | گیس | ایروسول | دھند، بادل، کہر |
| ٹھوس | گیس | ایروسول | دھواں، گاڑی کا اخراج |
| گیس | مائع | جھاگ | شیونگ کریم |
| مائع | مائع | ایملشن | دودھ، فیس کریم |
| ٹھوس | مائع | سول | میگنیشیا کا دودھ، کیچڑ |
| گیس | ٹھوس | جھاگ | جھاگ، ربڑ، اسفنج، پمائس |
| مائع | ٹھوس | جیل | جیلی، پنیر، مکھن |
| ٹھوس | ٹھوس | ٹھوس سول | رنگین قیمتی پتھر، دودھیا شیشہ |
2.3 جسمانی اور کیمیائی تبدیلیاں
پچھلے باب میں، ہم نے مادے کی کچھ جسمانی خصوصیات کے بارے میں سیکھا ہے۔ وہ خصوصیات جو مشاہدہ کی جا سکتی ہیں اور بیان کی جا سکتی ہیں جیسے رنگ، سختی، جمود، سیالیت، کثافت، پگھلنے کا نقطہ، ابلنے کا نقطہ وغیرہ جسمانی خصوصیات ہیں۔
حالات کی باہمی تبدیلی ایک جسمانی تبدیلی ہے کیونکہ یہ تبدیلیاں ترکیب میں تبدیلی کے بغیر اور مادے کی کیمیائی نوعیت میں کوئی تبدیلی کے بغیر رونما ہوتی ہیں۔ اگرچہ برف، پانی اور پانی کی بھاپ سب مختلف نظر آتے ہیں اور مختلف جسمانی خصوصیات ظاہر کرتے ہیں، وہ کیمیائی طور پر ایک جیسے ہیں۔
پانی اور کھانا پکانے کا تیل دونوں مائع ہیں لیکن ان کی کیمیائی خصوصیات مختلف ہیں۔ وہ بو اور آتش گیریت میں مختلف ہیں۔ ہم جانتے ہیں کہ تیل ہوا میں جلتا ہے جبکہ پانی آگ بجھاتا ہے۔ یہ تیل کی یہی کیمیائی خاصیت ہے جو اسے پانی سے مختلف بناتی ہے۔ جلنا ایک کیمیائی تبدیلی ہے۔ اس عمل کے دوران ایک مادہ دوسرے کے ساتھ تعامل کرتا ہے تاکہ کیمیائی ترکیب میں تبدیلی آئے۔ کیمیائی تبدیلی مادے کی کیمیائی خصوصیات میں تبدیلی لاتی ہے اور ہمیں نئے مادے ملتے ہیں۔ کیمیائی تبدیلی کو کیمیائی رد عمل بھی کہتے ہیں۔
موم بتی کے جلنے کے دوران، جسمانی اور کیمیائی دونوں تبدیلیاں رونما ہوتی ہیں۔ کیا آپ ان میں فرق کر سکتے ہیں؟
2.4 خالص مادوں کی اقسام کیا ہیں؟
ان کی کیمیائی ترکیب کی بنیاد پر، مادوں کو عناصر یا مرکبات کے طور پر درجہ بندی کیا جا سکتا ہے۔
2.4.1 عناصر
رابرٹ بوائل 1661 میں عنصر کی اصطلاح استعمال کرنے والے پہلے سائنسدان تھے۔ اینٹون لارینٹ لیوازئے (1743-94)، ایک فرانسیسی کیمیا دان، عنصر کی تجرباتی طور پر مفید تعریف قائم کرنے والے پہلے شخص تھے۔ انہوں نے عنصر کی تعریف مادے کی ایک بنیادی شکل کے طور پر کی جو کیمیائی رد عمل کے ذریعے سادہ مادوں میں توڑی نہیں جا سکتی۔
عناصر کو عام طور پر دھاتوں، غیر دھاتوں اور دھات نما میں تقسیم کیا جا سکتا ہے۔
دھاتیں عام طور پر درج ذیل میں سے کچھ یا تمام خصوصیات ظاہر کرتی ہیں:
-
ان میں چمک ہوتی ہے۔
-
ان کا رنگ چاندی جیسا سرمئی یا سنہری پیلا ہوتا ہے۔
-
وہ حرارت اور بجلی کی موصل ہوتی ہیں۔
-
وہ قابل کھنچاؤ ہوتی ہیں (تاروں میں کھینچی جا سکتی ہیں)۔
-
وہ قابل پتھرائی ہوتی ہیں (پتلی چادروں میں کوٹی جا سکتی ہیں)۔
-
وہ صوتی ہوتی ہیں (ٹکرانے پر گھنٹی جیسی آواز پیدا کرتی ہیں)۔
دھاتوں کی مثالیں سونا، چاندی، تانبا، لوہا، سوڈیم، پوٹاشیم وغیرہ ہیں۔ پارا واحد دھات ہے جو کمرے کے درجہ حرارت پر مائع ہوتی ہے۔
غیر دھاتیں عام طور پر درج ذیل میں سے کچھ یا تمام خصوصیات ظاہر کرتی ہیں:
-
وہ رنگوں کی مختلف قسمیں ظاہر کرتی ہیں۔
-
وہ حرارت اور بجلی کی خراب موصل ہوتی ہیں۔
-
وہ چمکدار، صوتی یا قابل پتھرائی نہیں ہوتیں۔
غیر دھاتوں کی مثالیں ہائیڈروجن، آکسیجن، آیوڈین، کاربن (کوئلہ، کوک)، برومین، کلورین وغیرہ ہیں۔ کچھ عناصر میں دھاتوں اور غیر دھاتوں کے درمیان درمیانی خصوصیات ہوتی ہیں، انہیں دھات نما کہتے ہیں؛ مثالیں بورون، سلیکون، جرمانیم، وغیرہ ہیں۔
-
فی الحال جانے جانے والے عناصر کی تعداد 100 سے زیادہ ہے۔ بانوے عناصر قدرتی طور پر پائے جاتے ہیں اور باقی انسان ساختہ ہیں۔
-
عناصر کی اکثریت ٹھوس ہے۔
-
کمرے کے درجہ حرارت پر گیارہ عناصر گیس کی حالت میں ہیں۔
-
کمرے کے درجہ حرارت پر دو عناصر مائع ہیں- پارا اور برومین۔
-
عناصر، گیلیم اور سیزیم کمرے کے درجہ حرارت سے تھوڑا اوپر (303 K) درجہ حرارت پر مائع بن جاتے ہیں۔
2.4.2 مرکبات
ایک مرکب دو یا دو سے زیادہ عناصر پر مشتمل مادہ ہے، جو ایک دوسرے کے ساتھ کیمیائی طور پر ایک مقررہ تناسب میں ملے ہوتے ہیں۔
جب دو یا دو سے زیادہ عناصر ملتے ہیں تو ہمیں کیا ملتا ہے؟
سرگرمی 2.4
-
کلاس کو دو گروپوں میں تقسیم کریں۔ دونوں گروپوں کو چائنا ڈش میں $5 g$ لوہے کے برادے اور $3 g$ گندھک پاؤڈر دیں۔
$ \mathrm{Group} \hspace{4px}\mathrm{I} $
-
لوہے کے برادے اور گندھک پاؤڈر کو ملا کر پیس لیں۔
$ \mathrm{Group} \hspace{4px}\mathrm{II} $
-
لوہے کے برادے اور گندھک پاؤڈر کو ملا کر پیس لیں۔ اس مرکب کو مضبوطی سے گرم کریں یہاں تک کہ سرخ گرم ہو جائے۔ شعلے سے ہٹا دیں اور مرکب کو ٹھنڈا ہونے دیں۔
$ \mathrm{Group} \hspace{4px}\mathrm{I} $ $ \mathrm{and} \hspace{4px} \mathrm{Group} \hspace{4px}\mathrm{II} $
-
حاصل کردہ مواد میں مقناطیسیت چیک کریں۔ ایک مقناطیس مواد کے قریب لائیں اور چیک کریں کہ آیا مواد مقناطیس کی طرف کھنچتا ہے۔ گروپوں کے ذریعے حاصل کردہ مواد کی ساخت اور رنگ کا موازنہ کریں۔
-
حاصل کردہ مواد کے ایک حصے میں کاربن ڈائی سلفائیڈ ملائیں۔ اچھی طرح ہلائیں اور فلٹر کریں۔
-
حاصل کردہ مواد کے دوسرے حصے میں ہلکی گندھک کا تیزاب یا ہلکی ہائیڈروکلورک ایسڈ ملائیں۔ (نوٹ: اس سرگرمی کے لیے استاد کی نگرانی ضروری ہے)۔
-
دونوں عناصر (لوہا اور گندھک) کے ساتھ الگ الگ اوپر کے تمام مراحل انجام دیں۔
اب جواب دیں
-
کیا دونوں گروپوں کے ذریعے حاصل کردہ مواد ایک جیسے نظر آتے تھے؟
-
کس گروپ نے مقناطیسی خصوصیات والا مواد حاصل کیا؟
-
کیا ہم حاصل کردہ مواد کے اجزاء کو الگ کر سکتے ہیں؟
-
ہلکی گندھک کا تیزاب یا ہلکی ہائیڈروکلورک ایسڈ ملانے پر، کیا دونوں گروپوں نے گیس حاصل کی؟ کیا دونوں صورتوں میں گیس کی بو ایک جیسی تھی یا مختلف؟
گروپ I کے ذریعے حاصل کردہ گیس ہائیڈروجن ہے، یہ بے رنگ، بے بو اور آتش گیر ہے- کلاس میں ہائیڈروجن کے لیے دہن ٹیسٹ کرنے کی سفارش نہیں کی جاتی۔ گروپ II کے ذریعے حاصل کردہ گیس ہائیڈروجن سلفائیڈ ہے۔ یہ سڑے ہوئے انڈوں کی بو والی بے رنگ گیس ہے۔
آپ نے مشاہدہ کیا ہوگا کہ دونوں گروپوں کے ذریعے حاصل کردہ مصنوعات مختلف خصوصیات ظاہر کرتی ہیں، حالانکہ شروع میں مواد ایک جیسے تھے۔ گروپ I نے ایک جسمانی تبدیلی سے متعلق سرگرمی انجام دی ہے جبکہ گروپ II کے معاملے میں، ایک کیمیائی تبدیلی (ایک کیمیائی رد عمل) ر











