আমাদের চারপাশের বস্তু কি বিশুদ্ধ?
আমরা কীভাবে বিচার করব যে আমরা বাজার থেকে যে দুধ, ঘি, মাখন, লবণ, মসলা, খনিজ জল বা রস কিনি সেগুলো বিশুদ্ধ কিনা?

চিত্র ২.১: কিছু ভোগ্যপণ্য
আপনি কি কখনও এই ভোগ্যপণ্যগুলোর প্যাকেটে ‘বিশুদ্ধ’ শব্দটি লেখা দেখেছেন? একজন সাধারণ মানুষের কাছে বিশুদ্ধ বলতে বোঝায় কোন ভেজাল নেই। কিন্তু, একজন বিজ্ঞানীর কাছে এই সমস্ত জিনিস আসলে বিভিন্ন পদার্থের মিশ্রণ এবং তাই বিশুদ্ধ নয়। উদাহরণস্বরূপ, দুধ আসলে জল, চর্বি, প্রোটিন ইত্যাদির মিশ্রণ। যখন একজন বিজ্ঞানী বলেন যে কিছু বিশুদ্ধ, এর অর্থ হল সেই পদার্থের গঠনকারী সমস্ত কণা তাদের রাসায়নিক প্রকৃতিতে একই। একটি বিশুদ্ধ পদার্থ এক ধরনের কণা নিয়ে গঠিত। অন্য কথায়, একটি পদার্থ হল বস্তুর একটি বিশুদ্ধ একক রূপ।
আমরা চারপাশে তাকালে দেখতে পাই যে আমাদের চারপাশের বেশিরভাগ বস্তু দুই বা ততোধিক বিশুদ্ধ উপাদানের মিশ্রণ হিসাবে বিদ্যমান, উদাহরণস্বরূপ, সমুদ্রের জল, খনিজ, মাটি ইত্যাদি সবই মিশ্রণ।
২.১ মিশ্রণ কী?
মিশ্রণ একাধিক ধরনের বিশুদ্ধ বস্তুর রূপ দ্বারা গঠিত। আমরা জানি যে দ্রবীভূত সোডিয়াম ক্লোরাইডকে বাষ্পীভবনের ভৌত প্রক্রিয়া দ্বারা জল থেকে আলাদা করা যেতে পারে। যাইহোক, সোডিয়াম ক্লোরাইড নিজেই একটি বিশুদ্ধ পদার্থ এবং এটিকে এর রাসায়নিক উপাদানগুলিতে ভৌত প্রক্রিয়া দ্বারা আলাদা করা যায় না। একইভাবে, চিনি হল একটি পদার্থ যা শুধুমাত্র এক ধরনের বিশুদ্ধ বস্তু ধারণ করে এবং এর গঠন সর্বত্র একই।
সফট ড্রিংক এবং মাটি একক বিশুদ্ধ পদার্থ নয়। একটি বিশুদ্ধ পদার্থের উৎস যাই হোক না কেন, এর সর্বদা একই বৈশিষ্ট্যগত ধর্ম থাকবে।
অতএব, আমরা বলতে পারি যে একটি মিশ্রণে একাধিক বিশুদ্ধ পদার্থ থাকে।
২.১.১ মিশ্রণের প্রকারভেদ
একটি মিশ্রণ গঠনকারী উপাদানগুলির প্রকৃতির উপর নির্ভর করে, আমাদের বিভিন্ন ধরনের মিশ্রণ থাকতে পারে।
ক্রিয়াকলাপ ২.১
আসুন আমরা শ্রেণীটিকে A, $B, C$ এবং $D$ দলে ভাগ করি।
-
দল A একটি বিকার নেয় যাতে $50 mL$ জল এবং এক স্প্যাচুলা পূর্ণ কপার সালফেট গুঁড়ো থাকে। দল B একটি বিকারে $50 mL$ জল এবং দুই স্প্যাচুলা পূর্ণ কপার সালফেট গুঁড়ো নেয়।
-
দল C এবং D বিভিন্ন পরিমাণে কপার সালফেট এবং পটাসিয়াম পারম্যাঙ্গানেট বা সাধারণ লবণ (সোডিয়াম ক্লোরাইড) নিতে পারে এবং প্রদত্ত উপাদানগুলিকে মিশিয়ে একটি মিশ্রণ তৈরি করতে পারে। রঙ এবং গঠনে সমরূপতার উপর পর্যবেক্ষণগুলি রিপোর্ট কর।
-
দল A এবং B একটি মিশ্রণ পেয়েছে যা সর্বত্র একটি সমান গঠন বিশিষ্ট। এই ধরনের মিশ্রণগুলিকে বলা হয় সমজাতীয় মিশ্রণ বা দ্রবণ। এই ধরনের মিশ্রণের আরও কিছু উদাহরণ হল: (i) জলে দ্রবীভূত লবণ এবং (ii) জলে দ্রবীভূত চিনি। দুটি দলের দ্রবণের রঙের তুলনা করুন। যদিও উভয় দলই কপার সালফেট দ্রবণ পেয়েছে কিন্তু দ্রবণের রঙের তীব্রতা ভিন্ন। এটি দেখায় যে একটি সমজাতীয় মিশ্রণের গঠন পরিবর্তনশীল হতে পারে।
-
দল C এবং D মিশ্রণ পেয়েছে, যাতে ভৌতভাবে স্বতন্ত্র অংশ থাকে এবং অসম গঠন বিশিষ্ট। এই ধরনের মিশ্রণগুলিকে বলা হয় বিষমজাতীয় মিশ্রণ। সোডিয়াম ক্লোরাইড এবং লোহার গুঁড়ো, লবণ এবং গন্ধক, এবং তেল ও জলের মিশ্রণ হল বিষমজাতীয় মিশ্রণের উদাহরণ।
ক্রিয়াকলাপ ২.২
-
আসুন আমরা আবার শ্রেণীটিকে চারটি দলে ভাগ করি- A, B, C এবং D।
-
প্রতিটি দলে নিম্নলিখিত নমুনাগুলি বিতরণ করুন:
-
দল A-কে কপার সালফেটের কয়েকটি স্ফটিক।
-
দল B-কে এক স্প্যাচুলা পূর্ণ কপার সালফেট।
-
দল $C$-কে চক পাউডার বা গমের আটা।
-
দল D-কে দুধ বা কালির কয়েক ফোঁটা।
-
-
প্রতিটি দলের উচিত প্রদত্ত নমুনাটি জলে যোগ করা এবং একটি কাচের রড ব্যবহার করে ভালোভাবে নাড়ানো। মিশ্রণে কণাগুলি দৃশ্যমান কি?
-
একটি টর্চ থেকে আলোর রশ্মি মিশ্রণ ধারণকারী বিকার দিয়ে পরিচালিত করুন এবং সামনে থেকে পর্যবেক্ষণ করুন। আলোর রশ্মির পথ দৃশ্যমান ছিল কি?
-
মিশ্রণগুলিকে কয়েক মিনিটের জন্য অপরিবর্তিত রেখে দিন (এবং এর মধ্যে পরিস্রাবণ যন্ত্রপাতি সেট আপ করুন)। মিশ্রণটি স্থির নাকি কিছু সময় পরে কণাগুলি জমা হতে শুরু করে?
-
মিশ্রণটি পরিস্রুত করুন। পরিস্রাবণ কাগজে কোন অবশিষ্টাংশ আছে কি?
-
ফলাফলগুলি নিয়ে আলোচনা করুন এবং একটি মতামত গঠন করুন।
দল $A$ এবং $B$ একটি দ্রবণ পেয়েছে।
দল $C$ একটি নিলম্বন পেয়েছে।
দল D একটি কোলয়েডাল দ্রবণ পেয়েছে।
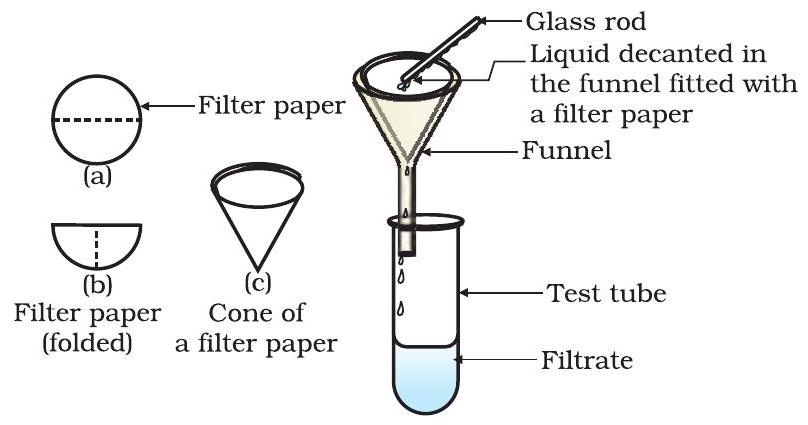
চিত্র ২.২: পরিস্রাবণ
এখন, আমরা নিম্নলিখিত বিভাগগুলিতে দ্রবণ, নিলম্বন এবং কোলয়েডাল দ্রবণ সম্পর্কে জানব।
২.২ দ্রবণ কী?
একটি দ্রবণ হল দুই বা ততোধিক পদার্থের একটি সমজাতীয় মিশ্রণ। আপনি আপনার দৈনন্দিন জীবনে বিভিন্ন ধরনের দ্রবণের সম্মুখীন হন। লেবুর শরবত, সোডা জল ইত্যাদি সবই দ্রবণের উদাহরণ। সাধারণত আমরা একটি দ্রবণকে একটি তরল হিসাবে ভাবি যাতে একটি কঠিন, তরল বা গ্যাস দ্রবীভূত থাকে। কিন্তু, আমাদের কঠিন দ্রবণ (মিশ্র ধাতু) এবং গ্যাসীয় দ্রবণ (বায়ু) ও থাকতে পারে। একটি দ্রবণে কণা স্তরে সমজাতীয়তা থাকে। উদাহরণস্বরূপ, লেবুর শরবত সর্বত্র একই স্বাদের। এটি দেখায় যে চিনি বা লবণের কণাগুলি দ্রবণে সমানভাবে বিতরণ করা হয়েছে।
মিশ্র ধাতু: মিশ্র ধাতু হল দুই বা ততোধিক ধাতু বা একটি ধাতু এবং একটি অধাতুর মিশ্রণ এবং এগুলিকে ভৌত পদ্ধতি দ্বারা তাদের উপাদানগুলিতে আলাদা করা যায় না। কিন্তু তবুও, একটি মিশ্র ধাতুকে একটি মিশ্রণ হিসাবে বিবেচনা করা হয় কারণ এটি তার উপাদানগুলির বৈশিষ্ট্য দেখায় এবং পরিবর্তনশীল গঠন থাকতে পারে। উদাহরণস্বরূপ, পিতল হল প্রায় $30 %$ দস্তা এবং $70 %$ তামার একটি মিশ্রণ।
একটি দ্রবণের উপাদান হিসাবে একটি দ্রাবক এবং একটি দ্রব থাকে। দ্রবণের যে উপাদানটি অপর উপাদানকে তাতে দ্রবীভূত করে (সাধারণত বেশি পরিমাণে উপস্থিত উপাদান) তাকে দ্রাবক বলে। দ্রবণের যে উপাদানটি দ্রাবকে দ্রবীভূত হয় (সাধারণত কম পরিমাণে উপস্থিত) তাকে দ্রব বলে।
উদাহরণ:
(i) জলে চিনির দ্রবণ হল কঠিন-তরল দ্রবণ। এই দ্রবণে, চিনি হল দ্রব এবং জল হল দ্রাবক।
(ii) অ্যালকোহলে আয়োডিনের দ্রবণ, যা ‘টিংচার অফ আয়োডিন’ নামে পরিচিত, তাতে আয়োডিন (কঠিন) দ্রব এবং অ্যালকোহল (তরল) দ্রাবক হিসাবে থাকে।
(iii) সোডা জল ইত্যাদির মতো এয়ারেটেড পানীয় হল গ্যাস-তরল দ্রবণ। এগুলিতে কার্বন ডাই অক্সাইড (গ্যাস) দ্রব এবং জল (তরল) দ্রাবক হিসাবে থাকে।
(iv) বায়ু হল গ্যাস-গ্যাস মিশ্রণ। বায়ু হল বেশ কয়েকটি গ্যাসের একটি সমজাতীয় মিশ্রণ। এর দুটি প্রধান উপাদান হল: অক্সিজেন $(21 %)$ এবং নাইট্রোজেন (৭৮%)। অন্যান্য গ্যাসগুলি খুব অল্প পরিমাণে উপস্থিত থাকে।
একটি দ্রবণের বৈশিষ্ট্য
-
একটি দ্রবণ হল একটি সমজাতীয় মিশ্রণ।
-
একটি দ্রবণের কণাগুলির ব্যাস $1 nm(10^{-9}.$ মিটারের চেয়ে ছোট। তাই, এগুলি খালি চোখে দেখা যায় না।
-
খুব ছোট কণার আকারের কারণে, এগুলি দ্রবণের মধ্য দিয়ে যাওয়া আলোর রশ্মিকে বিচ্ছুরিত করে না। তাই, একটি দ্রবণে আলোর পথ দৃশ্যমান নয়।
-
দ্রব কণাগুলিকে পরিস্রাবণ প্রক্রিয়া দ্বারা মিশ্রণ থেকে আলাদা করা যায় না। দ্রব কণাগুলি অপরিবর্তিত অবস্থায় রেখে দিলে নিচে জমা হয় না, অর্থাৎ, একটি দ্রবণ স্থির।
২.২.১ একটি দ্রবণের ঘনত্ব
ক্রিয়াকলাপ ২.২-এ, আমরা পর্যবেক্ষণ করেছি যে দল A এবং B দ্রবণের বিভিন্ন শেড পেয়েছে। সুতরাং, আমরা বুঝতে পারি যে একটি দ্রবণে দ্রব এবং দ্রাবকের আপেক্ষিক অনুপাত পরিবর্তিত হতে পারে। একটি দ্রবণে উপস্থিত দ্রবের পরিমাণের উপর নির্ভর করে, এটিকে লঘু, ঘন বা সম্পৃক্ত দ্রবণ বলা যেতে পারে। লঘু এবং ঘন হল তুলনামূলক শব্দ। ক্রিয়াকলাপ ২.২-এ, দল B দ্বারা প্রাপ্ত দ্রবণের তুলনায় দল A দ্বারা প্রাপ্ত দ্রবণটি লঘু।
ক্রিয়াকলাপ ২.৩
-
দুটি পৃথক বিকারে প্রতিটিতে প্রায় $50 mL$ জল নিন।
-
এক বিকারে লবণ এবং দ্বিতীয় বিকারে চিনি বা বেরিয়াম ক্লোরাইড যোগ করুন অবিরত নাড়ার সাথে। যখন আর দ্রব দ্রবীভূত করা যায় না, তখন বিকারটির উপাদানগুলিকে প্রায় $5^{\circ} C$ তাপমাত্রা বাড়ানোর জন্য গরম করুন।
-
আবার দ্রব যোগ করা শুরু করুন।
একটি নির্দিষ্ট তাপমাত্রায় জলে দ্রবীভূত করা যেতে পারে এমন লবণ এবং চিনি বা বেরিয়াম ক্লোরাইডের পরিমাণ কি একই?
যে কোনো নির্দিষ্ট তাপমাত্রায়, একটি দ্রবণ যা যতটা দ্রবীভূত করতে সক্ষম ততটা দ্রব দ্রবীভূত করেছে, তাকে একটি সম্পৃক্ত দ্রবণ বলা হয়। অন্য কথায়, যখন একটি নির্দিষ্ট তাপমাত্রায় একটি দ্রবণে আর দ্রব দ্রবীভূত করা যায় না, তখন তাকে সম্পৃক্ত দ্রবণ বলে। এই তাপমাত্রায় সম্পৃক্ত দ্রবণে উপস্থিত দ্রবের পরিমাণকে এর দ্রাব্যতা বলে।
যদি একটি দ্রবণে থাকা দ্রবের পরিমাণ সম্পৃক্ততার মাত্রার চেয়ে কম হয়, তবে তাকে একটি অসম্পৃক্ত দ্রবণ বলে।
আপনি যদি একটি নির্দিষ্ট তাপমাত্রায় একটি সম্পৃক্ত দ্রবণ নেন এবং ধীরে ধীরে ঠান্ডা করেন তাহলে কী হবে?
উপরের ক্রিয়াকলাপ থেকে আমরা অনুমান করতে পারি যে একটি নির্দিষ্ট দ্রাবকে বিভিন্ন পদার্থের একই তাপমাত্রায় বিভিন্ন দ্রাব্যতা রয়েছে।
একটি দ্রবণের ঘনত্ব হল একটি প্রদত্ত পরিমাণ (ভর বা আয়তন) দ্রবণে উপস্থিত দ্রবের পরিমাণ (ভর বা আয়তন)।
একটি দ্রবণের ঘনত্ব প্রকাশ করার বিভিন্ন উপায় আছে, কিন্তু এখানে আমরা শুধুমাত্র তিনটি পদ্ধতি শিখব।
(i) একটি দ্রবণের ভর দ্বারা ভর শতাংশ
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) একটি দ্রবণের আয়তন দ্বারা ভর শতাংশ
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) একটি দ্রবণের আয়তন দ্বারা আয়তন শতাংশ
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
উদাহরণ ২.১ একটি দ্রবণে $40 g$ সাধারণ লবণ $320 g$ জলে থাকে। দ্রবণের ভর দ্বারা ভর শতাংশের পরিপ্রেক্ষিতে ঘনত্ব গণনা করুন।
সমাধান:
দ্রবের ভর (লবণ) $\quad=40 g$
দ্রাবকের ভর (জল) $=320 g$
আমরা জানি,
দ্রবণের ভর $=$ দ্রবের ভর + দ্রাবকের ভর
$$=40 g+320 g$$
$$=360 g$$
দ্রবণের ভর শতাংশ
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
২.২.২ নিলম্বন কী?
ক্রিয়াকলাপ ২.২ অসমজাতীয় ব্যবস্থা, যেমন দল $C$ দ্বারা ক্রিয়াকলাপ ২.২-এ প্রাপ্ত, যাতে কঠিন পদার্থগুলি তরলে বিক্ষিপ্ত থাকে, তাদের নিলম্বন বলে। একটি নিলম্বন হল একটি বিষমজাতীয় মিশ্রণ যাতে দ্রব কণাগুলি দ্রবীভূত হয় না কিন্তু মাধ্যমের সমগ্র আয়তনে নিলম্বিত থাকে। একটি নিলম্বনের কণাগুলি খালি চোখে দৃশ্যমান।
একটি নিলম্বনের বৈশিষ্ট্য
-
নিলম্বন হল একটি বিষমজাতীয় মিশ্রণ।
-
একটি নিলম্বনের কণাগুলি খালি চোখে দেখা যায়।
-
একটি নিলম্বনের কণাগুলি এর মধ্য দিয়ে যাওয়া আলোর রশ্মিকে বিচ্ছুরিত করে এবং এর পথ দৃশ্যমান করে।
-
একটি নিলম্বনকে অপরিবর্তিত অবস্থায় রেখে দিলে দ্রব কণাগুলি নিচে জমা হয়, অর্থাৎ, একটি নিলম্বন অস্থির। এগুলিকে পরিস্রাবণ প্রক্রিয়া দ্বারা মিশ্রণ থেকে আলাদা করা যেতে পারে। যখন কণাগুলি জমা হয়, নিলম্বন ভেঙে যায় এবং এটি আর আলো বিচ্ছুরিত করে না।
২.২.৩ কোলয়েডাল দ্রবণ কী?
ক্রিয়াকলাপ ২.২ ক্রিয়াকলাপ ২.২-এ দল D দ্বারা প্রাপ্ত মিশ্রণটিকে একটি কোলয়েড বা একটি কোলয়েডাল দ্রবণ বলা হয়। একটি কোলয়েডের কণাগুলি দ্রবণ জুড়ে সমানভাবে ছড়িয়ে থাকে। একটি নিলম্বনের তুলনায় অপেক্ষাকৃত ছোট কণার আকারের কারণে, মিশ্রণটি সমজাতীয় বলে মনে হয়। কিন্তু আসলে, একটি কোলয়েডাল দ্রবণ হল একটি বিষমজাতীয় মিশ্রণ, উদাহরণস্বরূপ, দুধ।
কোলয়েডাল কণার ছোট আকারের কারণে, আমরা এগুলি খালি চোখে দেখতে পাই না। কিন্তু, এই কণাগুলি সহজেই দৃশ্যমান আলোর একটি রশ্মিকে বিচ্ছুরিত করতে পারে যেমন ক্রিয়াকলাপ ২.২-এ পর্যবেক্ষণ করা হয়েছে। আলোর একটি রশ্মির এই বিচ্ছুরণকে টিনডাল প্রভাব বলা হয় যে বিজ্ঞানীর নামানুসারে এই প্রভাব আবিষ্কার করেছিলেন।
যখন একটি সূক্ষ্ম আলোর রশ্মি একটি ছোট ছিদ্র দিয়ে একটি ঘরে প্রবেশ করে তখনও টিনডাল প্রভাব পর্যবেক্ষণ করা যেতে পারে। এটি বাতাসে ধুলো এবং ধোঁয়ার কণা দ্বারা আলোর বিচ্ছুরণের কারণে ঘটে।
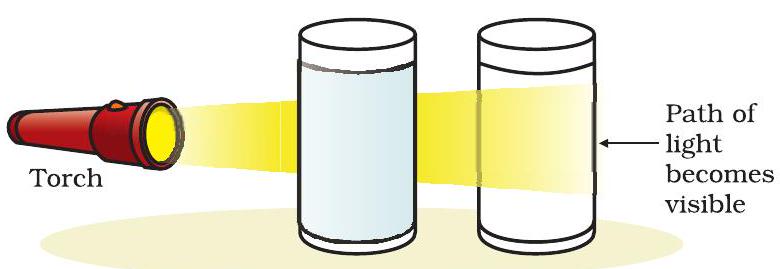
চিত্র ২.৩: (ক) কপার সালফেটের দ্রবণ টিনডাল প্রভাব দেখায় না, (খ) জল এবং দুধের মিশ্রণ টিনডাল প্রভাব দেখায়।
যখন সূর্যালোক একটি ঘন বনের চাঁদোয়ার মধ্য দিয়ে যায় তখন টিনডাল প্রভাব পর্যবেক্ষণ করা যেতে পারে। বনে কুয়াশায় জলের ক্ষুদ্র ফোঁটা থাকে, যা বাতাসে বিক্ষিপ্ত কোলয়েডের কণা হিসাবে কাজ করে।

চিত্র ২.৪: টিনডাল প্রভাব
একটি কোলয়েডের বৈশিষ্ট্য
-
একটি কোলয়েড হল একটি বিষমজাতীয় মিশ্রণ।
-
একটি কোলয়েডের কণার আকার এত ছোট যে খালি চোখে পৃথকভাবে দেখা যায় না।
-
কোলয়েডগুলি যথেষ্ট বড় যে এর মধ্য দিয়ে যাওয়া আলোর একটি রশ্মিকে বিচ্ছুরিত করে এবং এর পথ দৃশ্যমান করে।
-
এগুলি অপরিবর্তিত অবস্থায় রেখে দিলে নিচে জমা হয় না, অর্থাৎ, একটি কোলয়েড বেশ স্থির।
-
এগুলিকে পরিস্রাবণ প্রক্রিয়া দ্বারা মিশ্রণ থেকে আলাদা করা যায় না। কিন্তু, কেন্দ্রাতিগীকরণ নামক পৃথকীকরণের একটি বিশেষ কৌশল (ক্রিয়াকলাপ ২.৫ সম্পাদন করুন) ব্যবহার করে কোলয়েডাল কণাগুলিকে আলাদা করা যেতে পারে।
একটি কোলয়েডাল দ্রবণের উপাদানগুলি হল বিক্ষিপ্ত পর্যায় এবং বিসরণ মাধ্যম। একটি কোলয়েডে দ্রব-সদৃশ উপাদান বা বিক্ষিপ্ত কণাগুলি বিক্ষিপ্ত পর্যায় গঠন করে, এবং যে উপাদানে বিক্ষিপ্ত পর্যায় নিলম্বিত থাকে তাকে বিসরণ মাধ্যম বলে। বিসরণ মাধ্যম এবং বিক্ষিপ্ত পর্যায়ের অবস্থা (কঠিন, তরল বা গ্যাস) অনুসারে কোলয়েডগুলিকে শ্রেণীবদ্ধ করা হয়। কিছু সাধারণ উদাহরণ সারণী ২.১-এ দেওয়া হয়েছে। এই সারণী থেকে আপনি দেখতে পাবেন যে এগুলি খুব সাধারণ দৈনন্দিন জীবনের।
সারণী ২.১: কোলয়েডের সাধারণ উদাহরণ
| বিক্ষিপ্ত পর্যায় | বিসরণ মাধ্যম | প্রকার | উদাহরণ |
|---|---|---|---|
| তরল | গ্যাস | এরোসল | কুয়াশা, মেঘ, হালকা কুয়াশা |
| কঠিন | গ্যাস | এরোসল | ধোঁয়া, অটোমোবাইল নিষ্কাশন |
| গ্যাস | তরল | ফোম | শেভিং ক্রিম |
| তরল | তরল | ইমালশন | দুধ, ফেস ক্রিম |
| কঠিন | তরল | সোল | ম্যাগনেশিয়ার দুধ, কাদা |
| গ্যাস | কঠিন | ফোম | ফোম, রাবার, স্পঞ্জ, পামিস |
| তরল | কঠিন | জেল | জেলি, পনির, মাখন |
| কঠিন | কঠিন | কঠিন সোল | রঙিন রত্নপাথর, দুধের মতো কাচ |
২.৩ ভৌত ও রাসায়নিক পরিবর্তন
পূর্ববর্তী অধ্যায়ে, আমরা বস্তুর কয়েকটি ভৌত ধর্ম সম্পর্কে শিখেছি। যে ধর্মগুলি পর্যবেক্ষণ এবং নির্দিষ্ট করা যায় যেমন রঙ, কাঠিন্য, অনমনীয়তা, প্রবাহিততা, ঘনত্ব, গলনাঙ্ক, স্ফুটনাঙ্ক ইত্যাদি সেগুলি হল ভৌত ধর্ম।
অবস্থার পারস্পরিক রূপান্তর হল একটি ভৌত পরিবর্তন কারণ এই পরিবর্তনগুলি গঠনের কোন পরিবর্তন ছাড়াই এবং পদার্থের রাসায়নিক প্রকৃতির কোন পরিবর্তন ছাড়াই ঘটে। যদিও বরফ, জল এবং জলীয় বাষ্প সবই আলাদা দেখায় এবং বিভিন্ন ভৌত ধর্ম প্রদর্শন করে, এগুলি রাসায়নিকভাবে একই।
জল এবং রান্নার তেল উভয়ই তরল কিন্তু তাদের রাসায়নিক বৈশিষ্ট্য ভিন্ন। এগুলি গন্ধ এবং দাহ্যতায় ভিন্ন। আমরা জানি যে তেল বাতাসে জ্বলে কিন্তু জল আগুন নিভিয়ে দেয়। তেলের এই রাসায়নিক ধর্মই এটিকে জল থেকে আলাদা করে তোলে। দহন একটি রাসায়নিক পরিবর্তন। এই প্রক্রিয়ার সময় একটি পদার্থ রাসায়নিক গঠনের পরিবর্তনের জন্য অপর একটি পদার্থের সাথে বিক্রিয়া করে। রাসায়নিক পরিবর্তন বস্তুর রাসায়নিক ধর্মে পরিবর্তন আনে এবং আমরা নতুন পদার্থ পাই। একটি রাসায়নিক পরিবর্তনকে রাসায়নিক বিক্রিয়াও বলা হয়।
একটি মোমবাতি জ্বলার সময়, ভৌত এবং রাসায়নিক উভয় পরিবর্তনই ঘটে। আপনি কি এগুলোর মধ্যে পার্থক্য করতে পারেন?
২.৪ বিশুদ্ধ পদার্থের প্রকারগুলি কী কী?
তাদের রাসায়নিক গঠনের ভিত্তিতে, পদার্থগুলিকে মৌল বা যৌগ হিসাবে শ্রেণীবদ্ধ করা যেতে পারে।
২.৪.১ মৌল
রবার্ট বয়েল ১৬৬১ সালে প্রথম বিজ্ঞানী যিনি মৌল শব্দটি ব্যবহার করেছিলেন। অ্যান্টোইন লরেন্ট ল্যাভয়সিয়ার (১৭৪৩-৯৪), একজন ফরাসি রসায়নবিদ, প্রথম একজন মৌলের একটি পরীক্ষামূলকভাবে দরকারী সংজ্ঞা প্রতিষ্ঠা করেছিলেন। তিনি একটি মৌলকে বস্তুর একটি মৌলিক রূপ হিসাবে সংজ্ঞায়িত করেছিলেন যা রাসায়নিক বিক্রিয়া দ্বারা সরল পদার্থে ভাঙা যায় না।
মৌলগুলিকে সাধারণত ধাতু, অধাতু এবং ধাতুকল্পে বিভক্ত করা যায়।
ধাতুগুলি সাধারণত নিম্নলিখিত ধর্মগুলির কিছু বা সবগুলি প্রদর্শন করে:
- এদের একটি চকচকে ভাব (উজ্জ্বলতা) থাকে।
- এদের রূপালী-ধূসর বা সোনালি-হলুদ রঙ থাকে।
- এগুলি তাপ ও বিদ্যুৎ পরিবহন করে।
- এগুলি প্রসারণযোগ্য (তারের আকারে টানা যেতে পারে)।
- এগুলি নমনীয় (পাতলা চাদরে পিটিয়ে সমতল করা যেতে পারে)।
- এগুলি ধ্বনিবাহী (আঘাত করলে রিং করার মতো শব্দ করে)।
ধাতুর উদাহরণ হল সোনা, রূপা, তামা, লোহা, সোডিয়াম, পটাসিয়াম ইত্যাদি। পারদ হল একমাত্র ধাতু যা ঘরের তাপমাত্রায় তরল।
অধাতুগুলি সাধারণত নিম্নলিখিত ধর্মগুলির কিছু বা সবগুলি প্রদর্শন করে:
- এগুলি বিভিন্ন রঙ প্রদর্শন করে।
- এগুলি তাপ ও বিদ্যুতের দুর্বল পরিবাহী।
- এগুলি চকচকে, ধ্বনিবাহী বা নমনীয় নয়।
অধাতুর উদাহরণ হল হাইড্রোজেন, অক্সিজেন, আয়োডিন, কার্বন (কয়লা, কোক), ব্রোমিন, ক্লোরিন ইত্যাদি। কিছু মৌলের ধর্ম ধাতু এবং অধাতুর মধ্যবর্তী, এগুলিকে ধাতুকল্প বলে; উদাহরণ হল বোরন, সিলিকন, জার্মেনিয়াম ইত্যাদি।
- বর্তমানে পরিচিত মৌলের সংখ্যা ১০০-এর বেশি। বাহান্নটি মৌল প্রাকৃতিকভাবে ঘটে এবং বাকিগুলি মানবসৃষ্ট।
- বেশিরভাগ মৌল কঠিন।
- ঘরের তাপমাত্রায় এগারোটি মৌল গ্যাসীয় অবস্থায় থাকে।
- দুটি মৌল ঘরের তাপমাত্রায় তরল- পারদ এবং ব্রোমিন।
- গ্যালিয়াম এবং সিজিয়াম মৌলগুলি ঘরের তাপমাত্রার (৩০৩ K) সামান্য উপরে তাপমাত্রায় তরল হয়ে যায়।
২.৪.২ যৌগ
একটি যৌগ হল দুই বা ততোধিক মৌল দ্বারা গঠিত একটি পদার্থ, রাসায়নিকভাবে একে অপরের সাথে একটি নির্দিষ্ট অনুপাতে মিলিত।
দুই বা ততোধিক মৌল মিলিত হলে আমরা কী পাই?
ক্রিয়াকলাপ ২.৪
-
শ্রেণীটিকে দুটি দলে ভাগ করুন। উভয় দলকে একটি চিনামাটির বাটিতে $5 g$ লোহার গুঁড়ো এবং $3 g$ গন্ধক গুঁড়ো দিন।
$ \mathrm{Group} \hspace{4px}\mathrm{I} $
-
লোহার গুঁড়ো এবং গন্ধক গুঁড়ো মিশিয়ে পিষুন।
$ \mathrm{Group} \hspace{4px}\mathrm{II} $
-
লোহার গুঁড়ো এবং গন্ধক গুঁড়ো মিশিয়ে পিষুন। এই মিশ্রণটিকে প্রবলভাবে গরম করুন লাল গরম না হওয়া পর্যন্ত। শিখা থেকে সরান এবং মিশ্রণটিকে ঠান্ডা হতে দিন।
$ \mathrm{Group} \hspace{4px}\mathrm{I} $ $ \mathrm{and} \hspace{4px} \mathrm{Group} \hspace{4px}\mathrm{II} $
-
প্রাপ্ত পদার্থে চৌম্বকত্ব পরীক্ষা করুন। একটি চুম্বক পদার্থের কাছে আনুন এবং পদার্থটি চুম্বকের দিকে আকৃষ্ট হয় কিনা তা পরীক্ষা করুন। দলগুলির দ্বারা প্রাপ্ত পদার্থের গঠন এবং রঙের তুলনা করুন।
-
প্রাপ্ত পদার্থের এক অংশে কার্বন ডাইসালফাইড যোগ করুন। ভালো করে নাড়ুন এবং পরিস্রুত করুন।
-
প্রাপ্ত পদার্থের অন্য অংশে লঘু সালফিউরিক অ্যাসিড বা লঘু হাইড্রোক্লোরিক অ্যাসিড যোগ করুন। (দ্রষ্টব্য: এই ক্রিয়াকলাপের জন্য শিক্ষকের তত্ত্বাবধান প্রয়োজন)।
-
উভয় মৌল (লোহা এবং গন্ধক) আলাদাভাবে নিয়ে উপরের সমস্ত ধাপ সম্পাদন করুন।
এখন উত্তর দিন
- দুটি দল দ্বারা প্রাপ্ত পদার্থ কি একই রকম দেখাচ্ছিল?
- কোন দলটি চৌম্বকীয় ধর্ম বিশিষ্ট পদার্থ পেয়েছে?
- আমরা কি প্রাপ্ত পদার্থের উপাদানগুলিকে আলাদা করতে পারি?
- লঘু সালফিউরিক অ্যাসিড বা লঘু হাইড্রোক্লোরিক অ্যাসিড যোগ করলে, উভয় দলই কি একটি গ্যাস পেয়েছে? উভয় ক্ষেত্রেই গ্যাসের গন্ধ কি একই ছিল নাকি ভিন্ন?
দল I দ্বারা প্রাপ্ত গ্যাসটি হল হাইড্রোজেন, এটি বর্ণহীন, গন্ধহীন এবং দাহ্য- শ্রেণীকক্ষে হাইড্রোজেনের জন্য দহন পরীক্ষা করার পরামর্শ দেওয়া হয় না। দল II দ্বারা প্রাপ্ত গ্যাসটি হল হাইড্রোজেন সালফাইড। এটি পচা ডিমের গন্ধযুক্ত একটি বর্ণহীন গ্যাস।
আপনি অবশ্যই লক্ষ্য করেছেন যে উভয় দল দ্বারা প্রাপ্ত উৎপাদগুলি বিভিন্ন ধর্ম দেখায়, যদিও প্রারম্ভিক উপাদানগুলি একই ছিল। দল I একটি ভৌত পরিবর্তন জড়িত ক্রিয়াকলাপটি সম্পাদন করেছে যেখানে দল II-এর ক্ষেত্রে, একটি রাসায়নিক পরিবর্তন (একটি রাসায়নিক বিক্রিয়া) ঘটেছে।
- দল I দ্বারা প্রাপ্ত পদার্থটি হল দুটি পদার্থের মিশ্রণ। প্রদত্ত পদার্থগুলি হল মৌল-লোহা এবং গন্ধক।
- মিশ্রণের ধর্মগুলি এর উপাদানগুলির মতোই।
সারণী ২.২: মিশ্রণ এবং যৌগ
| মিশ্রণ | যৌগ |
|---|---|
| ১. মৌল বা যৌগগুলি কেবল মিশ্রণ গঠনের জন্য একসাথে মেশে এবং কোন নতুন যৌগ গঠিত হয় না। | ১. মৌলগুলি নতুন যৌগ গঠনের জন্য বিক্রিয়া করে। |
| ২. একটি মিশ্রণের গঠন পরিবর্তনশীল। | ২. প্রতিটি নতুন পদার্থের গঠন সর্বদা নির্দিষ্ট। |
| ৩. একটি মিশ্রণ উপাদান পদার্থগুলির ধর্ম দেখায়। | ৩. নতুন পদার্থের সম্পূর্ণ ভিন্ন ধর্ম রয়েছে। |
| ৪. উপাদানগুলিকে ভৌত পদ্ধতি দ্বারা মোটামুটি সহজেই আলাদা করা যেতে পারে। | ৪. উপাদানগুলিকে শুধুমাত্র রাসায়নিক বা তড়িৎ রাসায়নিক বিক্রিয়া দ্বারা আলাদা করা যেতে পারে। |
- দল II দ্বারা প্রাপ্ত পদার্থটি হল একটি যৌগ।
- দুটি মৌলকে প্রবলভাবে গরম করলে আমরা একটি যৌগ পাই, যার ধর্ম মিলিত মৌলগুলির তুলনায় সম্পূর্ণ ভিন্ন।
- একটি যৌগের গঠন সর্বত্র একই। আমরা আরও লক্ষ্য করতে পারি যে যৌগের গঠন এবং রঙ সর্বত্র একই। সুতরাং, আমরা নিম্নলিখিত গ্রাফিকাল সংগঠকে বস্তুর ভৌত ও রাসায়নিক প্রকৃতি সংক্ষিপ্ত করতে পারি:
আপনি যা শিখলেন
- একটি মিশ্রণে একাধিক পদার্থ (মৌল এবং/অথবা যৌগ) যেকোনো অনুপাতে মিশ্রিত থাকে।
- উপযুক্ত পৃথকীকরণ কৌশল ব্যবহার করে মিশ্রণগুলিকে বিশুদ্ধ পদার্থে আলাদা করা যেতে পারে।
- একটি দ্রবণ হল দুই বা ততোধিক পদার্থের একটি সমজাতীয় মিশ্রণ। একটি দ্রবণের প্রধান উপাদানকে বলা হয় দ্রাবক, এবং গৌণ উপাদানকে বলা হয় দ্রব।
- একটি দ্রবণের ঘনত্ব হল প্রতি একক আয়তন বা প্রতি একক ভর দ্রবণে উপস্থিত দ্রবের পরিমাণ।
- যে পদার্থগুলি একটি দ্রাবকে অদ্রবণীয় এবং যার কণাগুলি খালি চোখে দৃশ্যমান, সেগুলি একটি নিলম্বন গঠন করে। একটি নিলম্বন হল একটি বিষমজাতীয় মিশ্রণ।
- কোলয়েডগুলি হল বিষমজাতীয় মিশ্রণ যাতে কণার আকার এত ছোট যে খালি চোখে দেখা যায় না, কিন্তু আলো বিচ্ছুরিত করার জন্য যথেষ্ট বড়। কোলয়েডগুলি শিল্প এবং দৈনন্দিন জীবনে উপযোগী। কণাগুলিকে বলা হয় বিক্ষিপ্ত পর্যায় এবং যে মাধ্যমটিতে সেগুলি বিতরণ করা হয় তাকে বলা হয় বিসরণ মাধ্যম।
- বিশুদ্ধ পদার্থগুলি মৌল বা যৌগ হতে পারে। একটি মৌল হল বস্তুর একটি রূপ যা রাসায়নিক বিক্রিয়া দ্বারা সরল পদার্থে ভাঙা যায় না। একটি যৌগ হল দুই বা ততোধিক বিভিন্ন ধরনের মৌল দ্বারা গঠিত একটি পদার্থ, একটি নির্দিষ্ট অনুপাতে রাসায়নিকভাবে মিলিত।
- একটি যৌগের ধর্ম তার উপাদান মৌলগুলি থেকে আলাদা, যেখানে একটি মিশ্রণ দেখায়
দলগত ক্রিয়াকলাপ

একটি মাটির কলস (মটকা), কিছু নুড়ি এবং বালি নিন। একটি ছোট আকারের পরিস্রাবণ উদ্ভিদ ডিজাইন করুন যা আপনি ঘোলা জল পর











