आपल्या सभोवतालचे पदार्थ शुद्ध आहेत का?
आपण बाजारातून विकत घेतलेले दूध, तूप, लोणी, मीठ, मसाले, खनिज पाणी किंवा रस हे शुद्ध आहेत की नाही हे आपण कसे ठरवू?

आकृती 2.1: काही खाद्यपदार्थ
या खाद्यपदार्थांच्या पॅकवर ‘शुद्ध’ हा शब्द तुम्ही कधी पाहिला आहे का? एका सामान्य व्यक्तीसाठी शुद्ध म्हणजे मिश्रण नसलेले. परंतु, एका शास्त्रज्ञासाठी हे सर्व पदार्थ प्रत्यक्षात विविध पदार्थांचे मिश्रण आहेत आणि म्हणूनच ते शुद्ध नाहीत. उदाहरणार्थ, दूध हे प्रत्यक्षात पाणी, चरबी, प्रथिने इत्यादींचे मिश्रण आहे. जेव्हा एक शास्त्रज्ञ म्हणतो की काहीतरी शुद्ध आहे, तेव्हा त्याचा अर्थ असा होतो की त्या पदार्थाचे सर्व घटक कण रासायनिक स्वरूपात समान आहेत. एका शुद्ध पदार्थामध्ये एकाच प्रकारचे कण असतात. दुसऱ्या शब्दांत, पदार्थ हा पदार्थाचा एक शुद्ध एकल स्वरूप आहे.
आपण आजूबाजूला पाहतो तेव्हा, आपल्या सभोवतालचा बहुतांश पदार्थ दोन किंवा अधिक शुद्ध घटकांचे मिश्रण म्हणून अस्तित्वात आहे, उदाहरणार्थ, समुद्राचे पाणी, खनिजे, माती इत्यादी सर्व मिश्रणे आहेत.
2.1 मिश्रण म्हणजे काय?
मिश्रण हे एकापेक्षा जास्त प्रकारच्या शुद्ध पदार्थापासून बनलेले असतात. आपल्याला माहित आहे की विरघळलेले सोडियम क्लोराईड पाण्यापासून बाष्पीभवनाच्या भौतिक प्रक्रियेद्वारे वेगळे केले जाऊ शकते. तथापि, सोडियम क्लोराईड स्वतः एक शुद्ध पदार्थ आहे आणि त्याला त्याच्या रासायनिक घटकांमध्ये भौतिक प्रक्रियेद्वारे वेगळे केले जाऊ शकत नाही. त्याचप्रमाणे, साखर हा एक असा पदार्थ आहे ज्यामध्ये फक्त एक प्रकारचा शुद्ध पदार्थ असतो आणि त्याची रचना संपूर्णपणे सारखीच असते.
सॉफ्ट ड्रिंक आणि माती हे एकल शुद्ध पदार्थ नाहीत. शुद्ध पदार्थाचा स्रोत काहीही असो, त्याचे वैशिष्ट्यपूर्ण गुणधर्म नेहमीच तेच असतील.
म्हणून, आपण असे म्हणू शकतो की एका मिश्रणामध्ये एकापेक्षा जास्त शुद्ध पदार्थ असतात.
2.1.1 मिश्रणांचे प्रकार
मिश्रण तयार करणाऱ्या घटकांच्या स्वरूपावर अवलंबून, आपल्याकडे विविध प्रकारची मिश्रणे असू शकतात.
कृती 2.1
चला वर्गाला A, $B, C$ आणि $D$ अशा गटांमध्ये विभागूया.
-
गट A मध्ये $50 mL$ पाणी असलेला बीकर आणि कॉपर सल्फेट पावडरचा एक स्पॅटुला भरून घ्या. गट B मध्ये $50 mL$ पाणी आणि बीकरमध्ये कॉपर सल्फेट पावडरचे दोन स्पॅटुला भरून घ्या.
-
गट C आणि D वेगवेगळ्या प्रमाणात कॉपर सल्फेट आणि पोटॅशियम परमॅंगनेट किंवा सामान्य मीठ (सोडियम क्लोराईड) घेऊन दिलेले घटक मिसळून मिश्रण तयार करू शकतात. रंग आणि पोत यातील एकसमानतेवर निरीक्षणे नोंदवा.
-
गट A आणि B ला असे मिश्रण मिळाले आहे ज्याची रचना संपूर्णपणे एकसमान आहे. अशा मिश्रणांना एकसंध मिश्रणे किंवा द्रावणे म्हणतात. अशा मिश्रणांची काही इतर उदाहरणे आहेत: (i) पाण्यात विरघळलेले मीठ आणि (ii) पाण्यात विरघळलेली साखर. दोन्ही गटांनी मिळवलेल्या कॉपर सल्फेट द्रावणाच्या रंगाची तुलना करा. दोन्ही गटांना कॉपर सल्फेट द्रावण मिळाले असले तरी द्रावणांच्या रंगाची तीव्रता वेगळी आहे. हे दर्शवते की एकसंध मिश्रणाची रचना बदलू शकते.
-
गट C आणि D ला अशी मिश्रणे मिळाली आहेत, ज्यामध्ये भौतिकदृष्ट्या वेगळे भाग असतात आणि त्यांची रचना एकसमान नसते. अशा मिश्रणांना विषमांगी मिश्रणे म्हणतात. सोडियम क्लोराईड आणि लोखंडी भुकटी, मीठ आणि गंधक आणि तेल आणि पाणी यांची मिश्रणे ही विषमांगी मिश्रणांची उदाहरणे आहेत.
कृती 2.2
-
चला पुन्हा वर्गाला चार गटांमध्ये विभागूया - A, B, C आणि D.
-
प्रत्येक गटाला खालील नमुने वितरित करा:
-
गट A ला कॉपर सल्फेटची काही क्रिस्टले.
-
गट B ला कॉपर सल्फेटचा एक स्पॅटुला भरून.
-
गट $C$ ला खडू पावडर किंवा गहू पीठ.
-
गट D ला दुधाचे किंवा शाईचे काही थेंब.
-
-
प्रत्येक गटाने दिलेला नमुना पाण्यात टाकावा आणि काचेच्या काठीने योग्य रीतीने ढवळावे. मिश्रणातील कण दृश्यमान आहेत का?
-
मिश्रण असलेल्या बीकरमधून टॉर्चचा प्रकाशकिरण पाठवा आणि समोरून निरीक्षण करा. प्रकाशकिरणाचा मार्ग दृश्यमान होता का?
-
मिश्रणे काही मिनिटे (आणि दरम्यान गाळणी उपकरण तयार करा) स्थिर ठेवा. मिश्रण स्थिर आहे की काही वेळानंतर कण तळाशी बसू लागतात का?
-
मिश्रण गाळून काढा. गाळणी कागदावर काही अवशेष आहे का?
-
निकालांची चर्चा करा आणि मत तयार करा.
गट $A$ आणि $B$ ला द्रावण मिळाले आहे.
गट $C$ ला निलंबन मिळाले आहे.
गट D ला कोलॉइडल द्रावण मिळाले आहे.
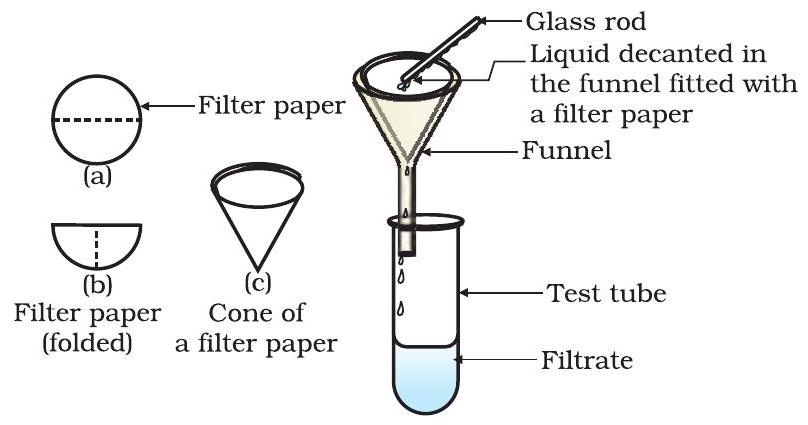
आकृती 2.2: गाळणी
आता, आपण पुढील विभागांमध्ये द्रावणे, निलंबने आणि कोलॉइडल द्रावणे याबद्दल शिकू.
2.2 द्रावण म्हणजे काय?
द्रावण हे दोन किंवा अधिक पदार्थांचे एकसंध मिश्रण असते. तुमच्या दैनंदिन जीवनात तुम्हाला विविध प्रकारची द्रावणे येतात. लिंबू पाणी, सोडा वॉटर इत्यादी सर्व द्रावणांची उदाहरणे आहेत. सहसा आपण द्रावणाचा विचार द्रव म्हणून करतो ज्यामध्ये एक घन, द्रव किंगवा वायू विरघळलेला असतो. परंतु, आपल्याकडे घन द्रावणे (मिश्रधातू) आणि वायू द्रावणे (हवा) देखील असू शकतात. द्रावणामध्ये कण स्तरावर एकसंधता असते. उदाहरणार्थ, लिंबू पाण्याची चव संपूर्णपणे सारखीच असते. हे दर्शवते की साखर किंवा मीठ यांचे कण द्रावणात समान रीतीने वितरित केले जातात.
मिश्रधातू: मिश्रधातू हे दोन किंवा अधिक धातू किंवा धातू आणि अधातू यांचे मिश्रण असतात आणि त्यांना भौतिक पद्धतींद्वारे त्यांच्या घटकांमध्ये वेगळे केले जाऊ शकत नाही. परंतु तरीही, मिश्रधातू हे मिश्रण मानले जाते कारण ते त्याच्या घटकांचे गुणधर्म दर्शवते आणि त्याची रचना बदलू शकते. उदाहरणार्थ, पितळ हे अंदाजे $30 %$ झिंक आणि $70 %$ कॉपरचे मिश्रण आहे.
द्रावणामध्ये द्रावक आणि द्राव्य हे त्याचे घटक असतात. द्रावणाचा जो घटक दुसरा घटक त्यात विरघळवतो (सहसा मोठ्या प्रमाणात असलेला घटक) त्याला द्रावक म्हणतात. द्रावणाचा जो घटक द्रावकात विरघळलेला असतो (सहसा कमी प्रमाणात असतो) त्याला द्राव्य म्हणतात.
उदाहरणे:
(i) पाण्यात साखरेचे द्रावण हे द्रवातील घन द्रावण आहे. या द्रावणात, साखर हे द्राव्य आहे आणि पाणी हे द्रावक आहे.
(ii) अल्कोहोलमध्ये आयोडीनचे द्रावण, ज्याला ‘टिंक्चर ऑफ आयोडीन’ म्हणून ओळखले जाते, त्यात आयोडीन (घन) द्राव्य म्हणून आणि अल्कोहोल (द्रव) द्रावक म्हणून असते.
(iii) सोडा वॉटर सारखे एरिएटेड पेये ही द्रवातील वायू द्रावणे आहेत. यामध्ये कार्बन डायऑक्साइड (वायू) द्राव्य म्हणून आणि पाणी (द्रव) द्रावक म्हणून असते.
(iv) हवा हे वायूमध्ये वायूचे मिश्रण आहे. हवा ही अनेक वायूंची एकसंध मिश्रण आहे. त्याचे दोन मुख्य घटक आहेत: ऑक्सिजन $(21 %)$ आणि नायट्रोजन (78%). इतर वायू अत्यंत कमी प्रमाणात असतात.
द्रावणाचे गुणधर्म
-
द्रावण हे एकसंध मिश्रण असते.
-
द्रावणाचे कण $1 nm(10^{-9}.$ मीटर $)$ व्यासापेक्षा लहान असतात. म्हणून, ते उघड्या डोळ्यांनी दिसत नाहीत.
-
अत्यंत लहान कण आकारामुळे, ते द्रावणातून जाणारा प्रकाशकिरण विखुरत नाहीत. म्हणून, द्रावणात प्रकाशाचा मार्ग दृश्यमान होत नाही.
-
द्राव्य कण गाळणी प्रक्रियेद्वारे मिश्रणापासून वेगळे केले जाऊ शकत नाहीत. द्राव्य कण स्थिर ठेवले तरी तळाशी बसत नाहीत, म्हणजेच द्रावण स्थिर असते.
2.2.1 द्रावणाची संहती
कृती 2.2 मध्ये, आपण पाहिले की गट A आणि B ला द्रावणांचे वेगवेगळे छटा मिळाल्या. म्हणून, आपण समजतो की द्रावणात द्राव्य आणि द्रावक यांचे सापेक्ष प्रमाण बदलू शकते. द्रावणात असलेल्या द्राव्याच्या प्रमाणावर अवलंबून, त्याला विरल, संहत किंवा संतृप्त द्रावण म्हणता येते. विरल आणि संहत ही तुलनात्मक संज्ञा आहेत. कृती 2.2 मध्ये, गट A ने मिळवलेले द्रावण हे गट B ने मिळवलेल्या द्रावणाच्या तुलनेत विरल आहे.
कृती 2.3
-
दोन वेगवेगळ्या बीकरमध्ये प्रत्येकी अंदाजे $50 mL$ पाणी घ्या.
-
एका बीकरमध्ये मीठ आणि दुसऱ्या बीकरमध्ये साखर किंवा बेरियम क्लोराईड सतत ढवळत असताना घाला. जेव्हा आणखी द्राव्य विरघळू शकत नाही, तेव्हा बीकरमधील मिश्रण गरम करून तापमान सुमारे $5^{\circ} C$ ने वाढवा.
-
पुन्हा द्राव्य घालणे सुरू करा.
दिलेल्या तापमानात पाण्यात विरघळू शकणारे मीठ आणि साखर किंवा बेरियम क्लोराईडचे प्रमाण सारखेच आहे का?
कोणत्याही विशिष्ट तापमानात, ज्या द्रावणाने जितके द्राव्य विरघळवण्याची क्षमता आहे तितके द्राव्य विरघळलेले असते, त्या द्रावणाला संतृप्त द्रावण म्हणतात. दुसऱ्या शब्दांत, जेव्हा दिलेल्या तापमानात द्रावणात आणखी द्राव्य विरघळवता येत नाही, तेव्हा त्याला संतृप्त द्रावण म्हणतात. या तापमानात संतृप्त द्रावणात असलेल्या द्राव्याच्या प्रमाणाला त्याची विद्राव्यता म्हणतात.
जर द्रावणात असलेले द्राव्याचे प्रमाण संतृप्तता पातळीपेक्षा कमी असेल, तर त्याला असंतृप्त द्रावण म्हणतात.
जर तुम्ही एका विशिष्ट तापमानात संतृप्त द्रावण घेतले आणि ते हळूहळू थंड केले तर काय होईल?
वरील कृतीवरून आपण असा निष्कर्ष काढू शकतो की दिलेल्या द्रावकातील वेगवेगळ्या पदार्थांची समान तापमानात वेगवेगळी विद्राव्यता असते.
द्रावणाची संहती म्हणजे दिलेल्या द्रावणात (वस्तुमान किंवा आकारमान) असलेले द्राव्याचे प्रमाण (वस्तुमान किंवा आकारमान) होय.
द्रावणाची संहती व्यक्त करण्याचे विविध मार्ग आहेत, परंतु येथे आपण फक्त तीन पद्धती शिकू.
(i) द्रावणाची वस्तुमानानुसार वस्तुमान टक्केवारी
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) द्रावणाची आकारमानानुसार वस्तुमान टक्केवारी
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) द्रावणाची आकारमानानुसार आकारमान टक्केवारी
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
उदाहरण 2.1 एका द्रावणात $40 g$ पाण्यात $320 g$ सामान्य मीठ आहे. द्रावणाची वस्तुमानानुसार वस्तुमान टक्केवारीच्या दृष्टीने संहती काढा.
उकल:
द्राव्याचे वस्तुमान (मीठ) $\quad=40 g$
द्रावकाचे वस्तुमान (पाणी) $=320 g$
आपल्याला माहित आहे,
द्रावणाचे वस्तुमान $=$ द्राव्याचे वस्तुमान + द्रावकाचे वस्तुमान
$$=40 g+320 g$$
$$=360 g$$
द्रावणाची वस्तुमान टक्केवारी
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
2.2.2 निलंबन म्हणजे काय?
कृती 2.2 विषमांगी प्रणाली, जसे की कृती 2.2 मध्ये गट $C$ ने मिळवलेले, ज्यामध्ये घन पदार्थ द्रवात विखुरलेले असतात, त्यांना निलंबन म्हणतात. निलंबन हे एक विषमांगी मिश्रण असते ज्यामध्ये द्राव्य कण विरघळत नाहीत परंतु माध्यमाच्या संपूर्ण आकारमानात तरंगत राहतात. निलंबनाचे कण उघड्या डोळ्यांनी दिसू शकतात.
निलंबनाचे गुणधर्म
-
निलंबन हे विषमांगी मिश्रण असते.
-
निलंबनाचे कण उघड्या डोळ्यांनी पाहता येतात.
-
निलंबनाचे कण त्यातून जाणारा प्रकाशकिरण विखुरतात आणि त्याचा मार्ग दृश्यमान करतात.
-
निलंबन स्थिर ठेवले तर द्राव्य कण तळाशी बसतात, म्हणजेच निलंबन अस्थिर असते. त्यांना गाळणी प्रक्रियेद्वारे मिश्रणापासून वेगळे केले जाऊ शकते. जेव्हा कण तळाशी बसतात, तेव्हा निलंबन मोडते आणि ते यापुढे प्रकाश विखुरत नाही.
2.2.3 कोलॉइडल द्रावण म्हणजे काय?
कृती 2.2 कृती 2.2 मध्ये गट D ने मिळवलेल्या मिश्रणाला कोलॉइड किंवा कोलॉइडल द्रावण म्हणतात. कोलॉइडचे कण द्रावणात एकसमानपणे पसरलेले असतात. निलंबनाच्या तुलनेत कणांचा आकार तुलनेने लहान असल्यामुळे, मिश्रण एकसंध दिसते. परंतु प्रत्यक्षात, कोलॉइडल द्रावण हे एक विषमांगी मिश्रण असते, उदाहरणार्थ, दूध.
कोलॉइडल कणांचा आकार लहान असल्यामुळे, आपण त्यांना उघड्या डोळ्यांनी पाहू शकत नाही. परंतु, हे कण कृती 2.2 मध्ये पाहिल्याप्रमाणे सहजपणे दृश्यमान प्रकाशकिरण विखुरू शकतात. प्रकाशकिरणाच्या या विखुरण्याला टिंडल प्रभाव म्हणतात, हा प्रभाव शोधणाऱ्या शास्त्रज्ञाच्या नावावरून.
जेव्हा एक बारीक प्रकाशकिरण एका छोट्या छिद्रातून खोलीत प्रवेश करतो तेव्हा देखील टिंडल प्रभाव पाहिला जाऊ शकतो. हे हवेतील धूळ आणि धुराच्या कणांद्वारे प्रकाशाच्या विखुरण्यामुळे होते.
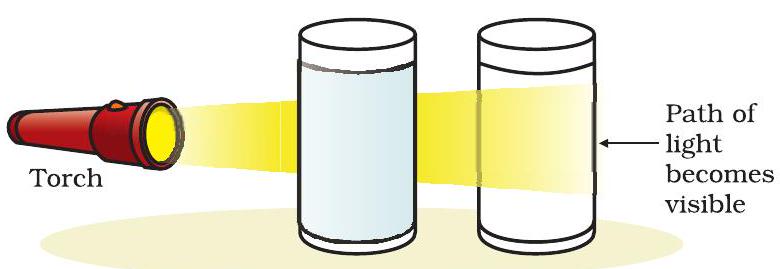
आकृती 2.3: (a) कॉपर सल्फेटचे द्रावण टिंडल प्रभाव दर्शवत नाही, (b) पाणी आणि दुधाचे मिश्रण टिंडल प्रभाव दर्शवते.
जेव्हा सूर्यप्रकाश दाट जंगलाच्या छतरीतून जातो तेव्हा टिंडल प्रभाव पाहिला जाऊ शकतो. जंगलात, धुक्यामध्ये पाण्याचे सूक्ष्म थेंब असतात, जे हवेत विखुरलेल्या कोलॉइडचे कण म्हणून काम करतात.

आकृती 2.4: टिंडल प्रभाव
कोलॉइडचे गुणधर्म
-
कोलॉइड हे विषमांगी मिश्रण असते.
-
कोलॉइडच्या कणांचा आकार उघड्या डोळ्यांनी वैयक्तिकरित्या पाहण्यासाठी खूपच लहान असतो.
-
कोलॉइडचे कण त्यातून जाणारा प्रकाशकिरण विखुरण्यासाठी आणि त्याचा मार्ग दृश्यमान करण्यासाठी पुरेसे मोठे असतात.
-
ते स्थिर ठेवले तरी तळाशी बसत नाहीत, म्हणजेच कोलॉइड अगदी स्थिर असते.
-
त्यांना गाळणी प्रक्रियेद्वारे मिश्रणापासून वेगळे केले जाऊ शकत नाही. परंतु, कोलॉइडल कण वेगळे करण्यासाठी अपकेंद्रण (कृती 2.5 करा) या विशेष पृथक्करण तंत्राचा वापर केला जाऊ शकतो.
कोलॉइडल द्रावणाचे घटक म्हणजे विखुरलेला प्रावस्था आणि विखुरणारे माध्यम. कोलॉइडमधील द्राव्यासारखा घटक किंवा विखुरलेले कण हे विखुरलेला प्रावस्था बनवतात आणि ज्या माध्यमात विखुरलेला प्रावस्था तरंगत असतो त्याला विखुरणारे माध्यम म्हणतात. कोलॉइड्सचे वर्गीकरण विखुरणारे माध्यम आणि विखुरलेला प्रावस्था यांच्या अवस्थेवर (घन, द्रव किंवा वायू) केले जाते. काही सामान्य उदाहरणे तक्ता 2.1 मध्ये दिली आहेत. या तक्त्यावरून तुम्ही पाहू शकता की ते दैनंदिन जीवनात अगदी सामान्य आहेत.
तक्ता 2.1: कोलॉइड्सची सामान्य उदाहरणे
| विखुरलेला प्रावस्था | विखुरणारे माध्यम | प्रकार | उदाहरण |
|---|---|---|---|
| द्रव | वायू | एरोसोल | धुके, ढग, हलका धुका |
| घन | वायू | एरोसोल | धूर, वाहनाचा निकास |
| वायू | द्रव | फेस | शेव्हिंग क्रीम |
| द्रव | द्रव | पायस | दूध, चेहऱ्याची क्रीम |
| घन | द्रव | सोल | मिल्क ऑफ मॅग्नेशिया, चिखल |
| वायू | घन | फोम | फोम, रबर, स्पंज, प्युमिस |
| द्रव | घन | जेल | जेली, चीज, लोणी |
| घन | घन | घन सोल | रंगीत रत्न, दुधाळ काच |
2.3 भौतिक आणि रासायनिक बदल
मागील प्रकरणात, आपण पदार्थाचे काही भौतिक गुणधर्म शिकलो. रंग, कठीणपणा, कडकपणा, प्रवाहिता, घनता, द्रवणांक, उत्कलनांक इत्यादी गुणधर्म जे निरीक्षण करता येतात आणि निर्दिष्ट करता येतात ते भौतिक गुणधर्म आहेत.
अवस्थांचे परस्पर रूपांतर हा एक भौतिक बदल आहे कारण हे बदल रचनेत बदल न करता आणि पदार्थाच्या रासायनिक स्वरूपात बदल न करता घडतात. बर्फ, पाणी आणि पाण्याची वाफ हे सर्व वेगवेगळे दिसतात आणि वेगवेगळे भौतिक गुणधर्म दर्शवत असले तरी, ते रासायनिकदृष्ट्या सारखेच आहेत.
पाणी आणि शेणाचे तेल दोन्ही द्रव आहेत परंतु त्यांची रासायनिक वैशिष्ट्ये वेगवेगळी आहेत. ते वास आणि ज्वलनशीलतेमध्ये भिन्न आहेत. आपल्याला माहित आहे की तेल हवेमध्ये जळते तर पाणी आग विझवते. तेलाचा हा रासायनिक गुणधर्म त्याला पाण्यापेक्षा वेगळा करतो. ज्वलन हा एक रासायनिक बदल आहे. या प्रक्रियेदरम्यान एक पदार्थ दुसऱ्याशी अभिक्रिया करून रासायनिक रचनेत बदल घडवून आणतो. रासायनिक बदलामुळे पदार्थाचे रासायनिक गुणधर्म बदलतात आणि आपल्याला नवीन पदार्थ मिळतात. रासायनिक बदलाला रासायनिक अभिक्रिया असेही म्हणतात.
मेणबत्ती जळत असताना, भौतिक आणि रासायनिक दोन्ही बदल घडतात. तुम्ही यातील फरक करू शकता का?
2.4 शुद्ध पदार्थांचे प्रकार काय आहेत?
त्यांच्या रासायनिक रचनेच्या आधारे, पदार्थांचे वर्गीकरण एकतर मूलद्रव्य किंवा संयुगे असे केले जाऊ शकते.
2.4.1 मूलद्रव्ये
रॉबर्ट बॉयल हे 1661 मध्ये मूलद्रव्य हा शब्द वापरणारे पहिले शास्त्रज्ञ होते. अँटोनी लॉरेंट लाव्हॉइझियर (1743-94), एक फ्रेंच रसायनशास्त्रज्ञ, हे मूलद्रव्याची प्रायोगिकदृष्ट्या उपयुक्त व्याख्या स्थापित करणारे पहिले होते. त्यांनी मूलद्रव्याची व्याख्या पदार्थाचा एक मूलभूत स्वरूप म्हणून केली ज्याला रासायनिक अभिक्रियांद्वारे सोप्या पदार्थांमध्ये मोडता येत नाही.
मूलद्रव्ये सामान्यतः धातू, अधातू आणि धातुसदृश यांमध्ये विभागली जाऊ शकतात.
धातू सहसा खालीलपैकी काही किंवा सर्व गुणधर्म दर्शवतात:
-
त्यांच्यात चमक (झळाळी) असते.
-
त्यांचा रूपेरी-राखाडी किंवा सोनेरी-पिवळा रंग असतो.
-
ते उष्णता आणि विद्युत वाहक असतात.
-
ते तन्य (तारांमध्ये ओढल्या जाऊ शकतात) असतात.
-
ते तार्पण्यक्षम (पातळ पत्र्यांमध्ये हातोड्याने











