क्या हमारे आस-पास के पदार्थ शुद्ध हैं?
हम कैसे निर्णय लेते हैं कि हम बाजार से खरीदा हुआ दूध, घी, मक्खन, नमक, मसाले, खनिज जल या जूस शुद्ध हैं या नहीं?

चित्र 2.1: कुछ उपभोक्ता वस्तुएँ
क्या आपने कभी इन उपभोक्ता वस्तुओं के पैक पर ‘शुद्ध’ शब्द लिखा देखा है? एक आम व्यक्ति के लिए शुद्ध का अर्थ है मिलावट रहित। लेकिन, एक वैज्ञानिक के लिए ये सभी चीजें वास्तव में विभिन्न पदार्थों के मिश्रण हैं और इसलिए शुद्ध नहीं हैं। उदाहरण के लिए, दूध वास्तव में पानी, वसा, प्रोटीन आदि का मिश्रण है। जब एक वैज्ञानिक कहता है कि कोई चीज शुद्ध है, तो इसका मतलब है कि उस पदार्थ के सभी घटक कण अपने रासायनिक स्वभाव में समान हैं। एक शुद्ध पदार्थ एक ही प्रकार के कणों से मिलकर बना होता है। दूसरे शब्दों में, एक पदार्थ पदार्थ का शुद्ध एकल रूप है।
जैसे ही हम चारों ओर देखते हैं, हम देख सकते हैं कि हमारे आस-पास का अधिकांश पदार्थ दो या दो से अधिक शुद्ध घटकों के मिश्रण के रूप में विद्यमान है, उदाहरण के लिए, समुद्री जल, खनिज, मिट्टी, आदि सभी मिश्रण हैं।
2.1 मिश्रण क्या है?
मिश्रण पदार्थ के एक से अधिक प्रकार के शुद्ध रूपों से मिलकर बनते हैं। हम जानते हैं कि घुला हुआ सोडियम क्लोराइड वाष्पन की भौतिक प्रक्रिया द्वारा पानी से अलग किया जा सकता है। हालाँकि, सोडियम क्लोराइड स्वयं एक शुद्ध पदार्थ है और इसे अपने रासायनिक घटकों में भौतिक प्रक्रिया द्वारा अलग नहीं किया जा सकता है। इसी प्रकार, चीनी एक ऐसा पदार्थ है जिसमें केवल एक प्रकार का शुद्ध पदार्थ होता है और इसकी संरचना पूरे में एक समान होती है।
शीतल पेय और मिट्टी एकल शुद्ध पदार्थ नहीं हैं। एक शुद्ध पदार्थ का स्रोत चाहे कुछ भी हो, उसमें हमेशा समान अभिलक्षणिक गुण होंगे।
इसलिए, हम कह सकते हैं कि एक मिश्रण में एक से अधिक शुद्ध पदार्थ होते हैं।
2.1.1 मिश्रण के प्रकार
एक मिश्रण बनाने वाले घटकों की प्रकृति के आधार पर, हमारे पास विभिन्न प्रकार के मिश्रण हो सकते हैं।
क्रियाकलाप 2.1
आइए हम कक्षा को समूह A, $B, C$ और $D$ में विभाजित करें।
-
समूह A एक बीकर लेता है जिसमें $50 mL$ पानी है और एक स्पैचुला भर कॉपर सल्फेट पाउडर। समूह B एक बीकर में $50 mL$ पानी और दो स्पैचुला भर कॉपर सल्फेट पाउडर लेता है।
-
समूह C और D कॉपर सल्फेट और पोटेशियम परमैंगनेट या साधारण नमक (सोडियम क्लोराइड) की अलग-अलग मात्रा ले सकते हैं और दिए गए घटकों को मिलाकर एक मिश्रण बना सकते हैं। रंग और बनावट में एकरूपता पर प्रेक्षणों की रिपोर्ट करें।
-
समूह A और B ने एक मिश्रण प्राप्त किया है जिसकी संरचना पूरे में एक समान है। ऐसे मिश्रणों को समांगी मिश्रण या विलयन कहा जाता है। ऐसे मिश्रणों के कुछ अन्य उदाहरण हैं: (i) पानी में घुला हुआ नमक और (ii) पानी में घुली हुई चीनी। दोनों समूहों के विलयनों के रंग की तुलना करें। हालाँकि दोनों समूहों ने कॉपर सल्फेट विलयन प्राप्त किया है लेकिन विलयनों के रंग की तीव्रता अलग-अलग है। यह दर्शाता है कि एक समांगी मिश्रण की संरचना परिवर्तनशील हो सकती है।
-
समूह C और D ने ऐसे मिश्रण प्राप्त किए हैं, जिनमें भौतिक रूप से भिन्न भाग होते हैं और जिनकी संरचना असमान होती है। ऐसे मिश्रणों को विषमांगी मिश्रण कहा जाता है। सोडियम क्लोराइड और लोहे की छीलन, नमक और सल्फर, तथा तेल और पानी के मिश्रण विषमांगी मिश्रणों के उदाहरण हैं।
क्रियाकलाप 2.2
-
आइए हम फिर से कक्षा को चार समूहों- A, B, C और D में विभाजित करें।
-
प्रत्येक समूह को निम्नलिखित नमूने वितरित करें:
-
समूह A को कॉपर सल्फेट के कुछ क्रिस्टल।
-
समूह B को एक स्पैचुला भर कॉपर सल्फेट।
-
चाक पाउडर या गेहूं का आटा समूह $C$ को।
-
समूह D को दूध या स्याही की कुछ बूँदें।
-
-
प्रत्येक समूह को दिए गए नमूने को पानी में मिलाना चाहिए और काँच की छड़ का उपयोग करके ठीक से हिलाना चाहिए। क्या मिश्रण में कण दिखाई दे रहे हैं?
-
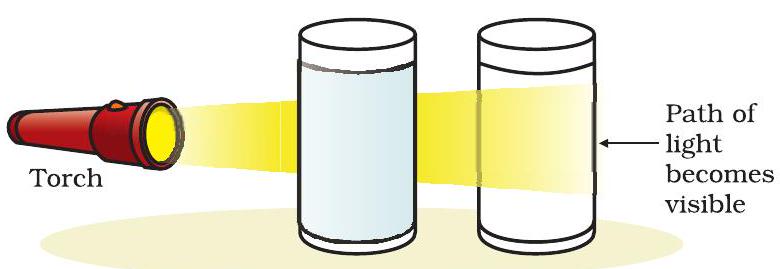
टॉर्च से प्रकाश की एक किरण को मिश्रण वाले बीकर से गुजारें और सामने से देखें। क्या प्रकाश किरण का मार्ग दिखाई दिया?
-
मिश्रणों को कुछ मिनटों के लिए अबाधित छोड़ दें (और इस बीच निस्यंदन उपकरण स्थापित करें)। क्या मिश्रण स्थिर है या कुछ समय बाद कण नीचे बैठने लगते हैं?
-
मिश्रण को निस्यंदित करें। क्या निस्यंदन कागज पर कोई अवशेष है?
-
परिणामों पर चर्चा करें और एक राय बनाएं।
समूह $A$ और $B$ ने एक विलयन प्राप्त किया है।
समूह $C$ ने एक निलंबन प्राप्त किया है।
समूह D ने एक कोलॉइडी विलयन प्राप्त किया है।
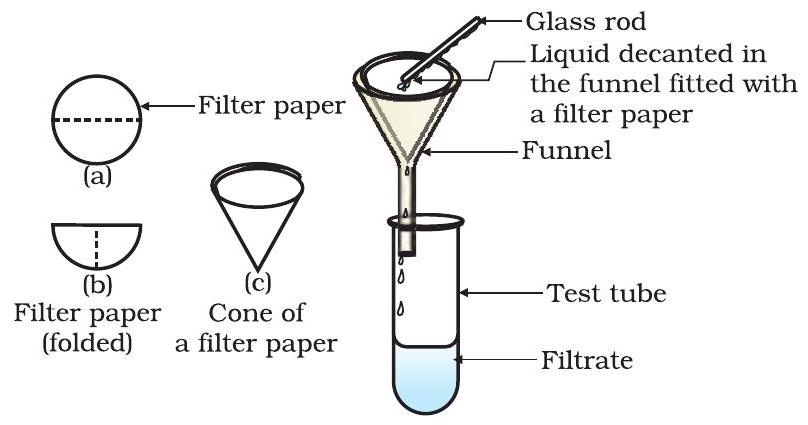
चित्र 2.2: निस्यंदन
अब, हम निम्नलिखित अनुभागों में विलयन, निलंबन और कोलॉइडी विलयन के बारे में सीखेंगे।
2.2 विलयन क्या है?
एक विलयन दो या दो से अधिक पदार्थों का एक समांगी मिश्रण है। आप अपने दैनिक जीवन में विभिन्न प्रकार के विलयनों के संपर्क में आते हैं। नींबू पानी, सोडा वाटर, आदि सभी विलयनों के उदाहरण हैं। आमतौर पर हम एक विलयन को एक तरल के रूप में सोचते हैं जिसमें एक ठोस, तरल या गैस घुली हुई होती है। लेकिन, हमारे पास ठोस विलयन (मिश्रधातु) और गैसीय विलयन (वायु) भी हो सकते हैं। एक विलयन में कण स्तर पर समांगिता होती है। उदाहरण के लिए, नींबू पानी का स्वाद पूरे में एक समान होता है। यह दर्शाता है कि चीनी या नमक के कण विलयन में समान रूप से वितरित हैं।
मिश्रधातु: मिश्रधातु दो या दो से अधिक धातुओं या एक धातु और एक अधातु के मिश्रण होते हैं और इन्हें भौतिक विधियों द्वारा उनके घटकों में अलग नहीं किया जा सकता है। लेकिन फिर भी, एक मिश्रधातु को मिश्रण माना जाता है क्योंकि यह अपने घटकों के गुण दर्शाता है और इसकी संरचना परिवर्तनशील हो सकती है। उदाहरण के लिए, पीतल लगभग $30 %$ जिंक और $70 %$ तांबे का मिश्रण है।
एक विलयन में एक विलायक और एक विलेय इसके घटक के रूप में होते हैं। विलयन का वह घटक जो दूसरे घटक को उसमें घोलता है (आमतौर पर अधिक मात्रा में उपस्थित घटक) विलायक कहलाता है। विलयन का वह घटक जो विलायक में घुला होता है (आमतौर पर कम मात्रा में उपस्थित) विलेय कहलाता है।
उदाहरण:
(i) पानी में चीनी का विलयन एक ठोस-तरल विलयन है। इस विलयन में, चीनी विलेय है और पानी विलायक है।
(ii) अल्कोहल में आयोडीन का विलयन, जिसे ‘आयोडीन की टिंचर’ के नाम से जाना जाता है, में आयोडीन (ठोस) विलेय है और अल्कोहल (तरल) विलायक है।
(iii) एरेटेड पेय जैसे सोडा वाटर, आदि, गैस-तरल विलयन हैं। इनमें कार्बन डाइऑक्साइड (गैस) विलेय के रूप में और पानी (तरल) विलायक के रूप में होता है।
(iv) वायु गैस-गैस मिश्रण है। वायु कई गैसों का एक समांगी मिश्रण है। इसके दो मुख्य घटक हैं: ऑक्सीजन $(21 %)$ और नाइट्रोजन (78%)। अन्य गैसें बहुत कम मात्रा में उपस्थित हैं।
एक विलयन के गुण
-
एक विलयन एक समांगी मिश्रण है।
-
एक विलयन के कणों का व्यास $1 nm(10^{-9}.$ मीटर $)$ से छोटा होता है। इसलिए, उन्हें नग्न आंखों से नहीं देखा जा सकता है।
-
बहुत छोटे कण आकार के कारण, वे विलयन से गुजरने वाली प्रकाश किरण को प्रकीर्णित नहीं करते हैं। इसलिए, एक विलयन में प्रकाश का मार्ग दिखाई नहीं देता है।
-
विलेय कणों को निस्यंदन की प्रक्रिया द्वारा मिश्रण से अलग नहीं किया जा सकता है। विलेय कण अबाधित छोड़ देने पर नीचे नहीं बैठते हैं, अर्थात, एक विलयन स्थिर होता है।
2.2.1 एक विलयन की सांद्रता
क्रियाकलाप 2.2 में, हमने देखा कि समूह A और B ने विलयनों के विभिन्न रंग प्राप्त किए। तो, हम समझते हैं कि एक विलयन में विलेय और विलायक का सापेक्ष अनुपात बदला जा सकता है। एक विलयन में उपस्थित विलेय की मात्रा के आधार पर, इसे तनु, सांद्र या संतृप्त विलयन कहा जा सकता है। तनु और सांद्र तुलनात्मक शब्द हैं। क्रियाकलाप 2.2 में, समूह A द्वारा प्राप्त विलयन, समूह B द्वारा प्राप्त विलयन की तुलना में तनु है।
क्रियाकलाप 2.3
-
दो अलग-अलग बीकरों में प्रत्येक में लगभग $50 mL$ पानी लें।
-
एक बीकर में नमक और दूसरे बीकर में चीनी या बेरियम क्लोराइड लगातार हिलाते हुए मिलाएं। जब कोई और विलेय न घुले, तो बीकर की सामग्री को लगभग $5^{\circ} C$ तापमान बढ़ाने के लिए गर्म करें।
-
फिर से विलेय मिलाना शुरू करें।
क्या दिए गए तापमान पर पानी में घुलने वाले नमक और चीनी या बेरियम क्लोराइड की मात्रा समान है?
किसी विशेष तापमान पर, एक विलयन जिसने उतना ही विलेय घोला है जितना वह घोलने में सक्षम है, संतृप्त विलयन कहलाता है। दूसरे शब्दों में, जब किसी दिए गए तापमान पर एक विलयन में कोई और विलेय नहीं घोला जा सकता है, तो उसे संतृप्त विलयन कहा जाता है। इस तापमान पर संतृप्त विलयन में उपस्थित विलेय की मात्रा को इसकी विलेयता कहते हैं।
यदि किसी विलयन में निहित विलेय की मात्रा संतृप्ति स्तर से कम है, तो इसे असंतृप्त विलयन कहा जाता है।
यदि आप एक निश्चित तापमान पर एक संतृप्त विलयन लेते हैं और इसे धीरे-धीरे ठंडा करते हैं तो क्या होगा?
हम उपरोक्त क्रियाकलाप से यह अनुमान लगा सकते हैं कि एक दिए गए विलायक में विभिन्न पदार्थों की समान तापमान पर विलेयता अलग-अलग होती है।
एक विलयन की सांद्रता, दी गई मात्रा (द्रव्यमान या आयतन) विलयन में उपस्थित विलेय की मात्रा (द्रव्यमान या आयतन) है।
एक विलयन की सांद्रता व्यक्त करने के विभिन्न तरीके हैं, लेकिन यहाँ हम केवल तीन विधियाँ सीखेंगे।
(i) एक विलयन का द्रव्यमान प्रतिशत द्रव्यमान द्वारा
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) एक विलयन का द्रव्यमान प्रतिशत आयतन द्वारा
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) एक विलयन का आयतन प्रतिशत आयतन द्वारा
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
उदाहरण 2.1 एक विलयन में $40 g$ साधारण नमक $320 g$ पानी में है। विलयन की सांद्रता द्रव्यमान प्रतिशत द्रव्यमान द्वारा के रूप में परिकलित कीजिए।
हल:
विलेय (नमक) का द्रव्यमान $\quad=40 g$
विलायक (पानी) का द्रव्यमान $=320 g$
हम जानते हैं,
विलयन का द्रव्यमान $=$ विलेय का द्रव्यमान + विलायक का द्रव्यमान
$$=40 g+320 g$$
$$=360 g$$
विलयन का द्रव्यमान प्रतिशत
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
2.2.2 निलंबन क्या है?
क्रियाकलाप 2.2 असमांगी तंत्र, जैसे कि समूह $C$ द्वारा क्रियाकलाप 2.2 में प्राप्त किए गए, जिनमें ठोस तरल में परिक्षिप्त होते हैं, निलंबन कहलाते हैं। एक निलंबन एक विषमांगी मिश्रण है जिसमें विलेय कण घुलते नहीं हैं बल्कि माध्यम के संपूर्ण आयतन में निलंबित रहते हैं। एक निलंबन के कण नग्न आंखों से दिखाई देते हैं।
एक निलंबन के गुण
-
निलंबन एक विषमांगी मिश्रण है।
-
एक निलंबन के कण नग्न आंखों से देखे जा सकते हैं।
-
एक निलंबन के कण उससे गुजरने वाली प्रकाश किरण को प्रकीर्णित करते हैं और उसके मार्ग को दृश्यमान बनाते हैं।
-
जब एक निलंबन को अबाधित छोड़ दिया जाता है तो विलेय कण नीचे बैठ जाते हैं, अर्थात, एक निलंबन अस्थिर होता है। उन्हें निस्यंदन की प्रक्रिया द्वारा मिश्रण से अलग किया जा सकता है। जब कण नीचे बैठ जाते हैं, तो निलंबन टूट जाता है और यह अब प्रकाश को प्रकीर्णित नहीं करता है।
2.2.3 कोलॉइडी विलयन क्या है?
क्रियाकलाप 2.2 क्रियाकलाप 2.2 में समूह D द्वारा प्राप्त मिश्रण को कोलॉइड या कोलॉइडी विलयन कहा जाता है। एक कोलॉइड के कण विलयन में समान रूप से फैले होते हैं। निलंबन की तुलना में कणों के अपेक्षाकृत छोटे आकार के कारण, मिश्रण समांगी प्रतीत होता है। लेकिन वास्तव में, एक कोलॉइडी विलयन एक विषमांगी मिश्रण होता है, उदाहरण के लिए, दूध।
कोलॉइडी कणों के छोटे आकार के कारण, हम उन्हें नग्न आंखों से नहीं देख सकते हैं। लेकिन, ये कण आसानी से दृश्य प्रकाश की एक किरण को प्रकीर्णित कर सकते हैं जैसा कि क्रियाकलाप 2.2 में देखा गया। प्रकाश की किरण के इस प्रकीर्णन को टिंडल प्रभाव कहा जाता है, जिस वैज्ञानिक ने इस प्रभाव की खोज की उनके नाम पर।
टिंडल प्रभाव तब भी देखा जा सकता है जब प्रकाश की एक पतली किरण एक छोटे से छेद के माध्यम से एक कमरे में प्रवेश करती है। यह हवा में धूल और धुएं के कणों द्वारा प्रकाश के प्रकीर्णन के कारण होता है।
चित्र 2.3: (a) कॉपर सल्फेट का विलयन टिंडल प्रभाव नहीं दर्शाता है, (b) पानी और दूध का मिश्रण टिंडल प्रभाव दर्शाता है।
टिंडल प्रभाव तब देखा जा सकता है जब सूर्य का प्रकाश घने जंगल की छतरी से गुजरता है। जंगल में, कोहरे में पानी की छोटी-छोटी बूंदें होती हैं, जो हवा में परिक्षिप्त कोलॉइड के कणों के रूप में कार्य करती हैं।

चित्र 2.4: टिंडल प्रभाव
एक कोलॉइड के गुण
-
एक कोलॉइड एक विषमांगी मिश्रण है।
-
एक कोलॉइड के कणों का आकार इतना छोटा होता है कि उन्हें नग्न आंखों से अलग-अलग नहीं देखा जा सकता है।
-
कोलॉइड इतने बड़े होते हैं कि उनसे गुजरने वाली प्रकाश किरण को प्रकीर्णित कर सकते हैं और उसके मार्ग को दृश्यमान बना सकते हैं।
-
जब उन्हें अबाधित छोड़ दिया जाता है तो वे नीचे नहीं बैठते हैं, अर्थात, एक कोलॉइड काफी स्थिर होता है।
-
उन्हें निस्यंदन की प्रक्रिया द्वारा मिश्रण से अलग नहीं किया जा सकता है। लेकिन, अपकेंद्रण (क्रियाकलाप 2.5 करें) नामक पृथक्करण की एक विशेष तकनीक का उपयोग कोलॉइडी कणों को अलग करने के लिए किया जा सकता है।
एक कोलॉइडी विलयन के घटक परिक्षिप्त प्रावस्था और परिक्षेपण माध्यम होते हैं। कोलॉइड में विलेय-सदृश घटक या परिक्षिप्त कण परिक्षिप्त प्रावस्था बनाते हैं, और जिस माध्यम में परिक्षिप्त प्रावस्था निलंबित होती है उसे परिक्षेपण माध्यम के रूप में जाना जाता है। कोलॉइड्स को परिक्षेपण माध्यम और परिक्षिप्त प्रावस्था की अवस्था (ठोस, तरल या गैस) के अनुसार वर्गीकृत किया जाता है। कुछ सामान्य उदाहरण तालिका 2.1 में दिए गए हैं। इस तालिका से आप देख सकते हैं कि वे रोजमर्रा की जिंदगी में बहुत आम हैं।
तालिका 2.1: कोलॉइड्स के सामान्य उदाहरण
| परिक्षिप्त प्रावस्था | परिक्षेपण माध्यम | प्रकार | उदाहरण |
|---|---|---|---|
| तरल | गैस | एरोसॉल | कोहरा, बादल, धुंध |
| ठोस | गैस | एरोसॉल | धुआं, ऑटोमोबाइल निकास |
| गैस | तरल | फोम | शेविंग क्रीम |
| तरल | तरल | इमल्शन | दूध, फेस क्रीम |
| ठोस | तरल | सॉल | मैग्नीशिया का दूध, कीचड़ |
| गैस | ठोस | फोम | फोम, रबर, स्पंज, प्यूमिस |
| तरल | ठोस | जेल | जेली, पनीर, मक्खन |
| ठोस | ठोस | ठोस सॉल | रंगीन रत्न, दूधिया कांच |
2.3 भौतिक और रासायनिक परिवर्तन
पिछले अध्याय में, हमने पदार्थ के कुछ भौतिक गुणों के बारे में सीखा है। जिन गुणों को देखा और निर्दिष्ट किया जा सकता है जैसे रंग, कठोरता, दृढ़ता, तरलता, घनत्व, गलनांक, क्वथनांक आदि भौतिक गुण हैं।
अवस्थाओं का परस्पर परिवर्तन एक भौतिक परिवर्तन है क्योंकि ये परिवर्तन संरचना में बिना किसी परिवर्तन के और पदार्थ की रासायनिक प्रकृति में बिना किसी परिवर्तन के होते हैं। हालाँकि बर्फ, पानी और जल वाष्प सभी अलग-अलग दिखते हैं और अलग-अलग भौतिक गुण प्रदर्शित करते हैं, वे रासायनिक रूप से समान हैं।
पानी और खाना पकाने का तेल दोनों तरल हैं लेकिन उनकी रासायनिक विशेषताएँ अलग-अलग हैं। वे गंध और ज्वलनशीलता में भिन्न हैं। हम जानते हैं कि तेल हवा में जलता है जबकि पानी आग बुझाता है। यह तेल का यही रासायनिक गुण है जो इसे पानी से अलग बनाता है। जलना एक रासायनिक परिवर्तन है। इस प्रक्रिया के दौरान एक पदार्थ रासायनिक संरचना में परिवर्तन के लिए दूसरे पदार्थ के साथ अभिक्रिया करता है। रासायनिक परिवर्तन पदार्थ के रासायनिक गुणों में परिवर्तन लाता है और हमें नए पदार्थ प्राप्त होते हैं। एक रासायनिक परिवर्तन को रासायनिक अभिक्रिया भी कहा जाता है।
मोमबत्ती के जलने के दौरान, भौतिक और रासायनिक दोनों परिवर्तन होते हैं। क्या आप इनमें अंतर कर सकते हैं?
2.4 शुद्ध पदार्थों के प्रकार क्या हैं?
उनकी रासायनिक संरचना के आधार पर, पदार्थों को तत्वों या यौगिकों के रूप में वर्गीकृत किया जा सकता है।
2.4.1 तत्व
रॉबर्ट बॉयल 1661 में तत्व शब्द का उपयोग करने वाले पहले वैज्ञानिक थे। एंटोनी लॉरेंट लावॉज़ियर (1743-94), एक फ्रांसीसी रसायनज्ञ, एक तत्व की प्रयोगात्मक रूप से उपयोगी परिभाषा स्थापित करने वाले पहले व्यक्ति थे। उन्होंने एक तत्व को पदार्थ के एक मूल रूप के रूप में परिभाषित किया जिसे रासायनिक अभिक्रियाओं द्वारा सरल पदार्थों में नहीं तोड़ा जा सकता है।
तत्वों को सामान्यतः धातुओं, अधातुओं और उपधातुओं में विभाजित किया जा सकता है।
धातुएं आमतौर पर निम्नलिखित में से कुछ या सभी गुण प्रदर्शित करती हैं:
-
उनमें चमक होती है।
-
उनका रंग चांदी-स्लेटी या सुनहरा-पीला होता है।
-
वे ऊष्मा और विद्युत का चालन करती हैं।
-
वे तन्य होती हैं (तारों में खींची जा सकती हैं)।
-
वे आघातवर्ध्य होती हैं (पतली चादरों में ढाली जा सकती हैं)।
-
वे ध्वनिक होती हैं (टकराने पर घंटी जैसी ध्वनि उत्पन्न करती हैं)।
धातुओं के उदाहरण हैं सोना, चांदी, तांबा, लोहा, सोडियम, पोटेशियम आदि। पारा एकमात्र धातु है जो कमरे के तापमान पर तरल होती है।
अधातुएं आमतौर पर निम्नलिखित में से कुछ या सभी गुण प्रदर्शित करती हैं:
-
वे विभिन्न प्रकार के रंग प्रदर्शित करती हैं।
-
वे ऊष्मा और विद्युत की कुचालक होती हैं।
-
वे चमकदार, ध्वनिक या आघातवर्ध्य नहीं होती हैं।
अधातुओं के उदाहरण हैं हाइड्रोजन, ऑक्सीजन, आयोडीन, कार्बन (कोयला, कोक), ब











