మన చుట్టూ ఉన్న పదార్థం శుద్ధమైనదేనా?
మనం మార్కెట్ నుండి కొనుగోలు చేసే పాలు, నెయ్యి, వెన్న, ఉప్పు, మసాలా దినుసులు, మినరల్ వాటర్ లేదా జ్యూస్ శుద్ధమైనవేనా అని ఎలా నిర్ణయిస్తాము?

Fig. 2.1: కొన్ని ఉపయోగించదగిన వస్తువులు
ఈ ఉపయోగించదగిన వస్తువుల ప్యాకెట్లపై ‘ప్యూర్’ (శుద్ధం) అనే పదాన్ని మీరు ఎప్పుడైనా గమనించారా? ఒక సామాన్య వ్యక్తికి శుద్ధం అంటే కల్తీ లేకపోవడం. కానీ, ఒక శాస్త్రవేత్తకు ఈ వస్తువులన్నీ వాస్తవానికి వివిధ పదార్థాల మిశ్రమాలు మరియు అందువలన శుద్ధమైనవి కావు. ఉదాహరణకు, పాలు వాస్తవానికి నీరు, కొవ్వు, ప్రోటీన్లు మొదలైనవాటి మిశ్రమం. ఒక శాస్త్రవేత్త ఏదైనా శుద్ధమైనది అని చెప్పినప్పుడు, ఆ పదార్థం యొక్క అన్ని భాగ కణాలు వాటి రసాయన స్వభావంలో ఒకేలా ఉంటాయి అని అర్థం. ఒక శుద్ధ పదార్థం ఒకే రకమైన కణాలతో కూడి ఉంటుంది. మరో మాటలో చెప్పాలంటే, ఒక పదార్థం అనేది పదార్థం యొక్క శుద్ధమైన ఏక రూపం.
మనం చుట్టూ చూస్తే, మన చుట్టూ ఉన్న పదార్థంలో ఎక్కువ భాగం రెండు లేదా అంతకంటే ఎక్కువ శుద్ధ భాగాల మిశ్రమంగా ఉందని మనం చూడవచ్చు, ఉదాహరణకు, సముద్రపు నీరు, ఖనిజాలు, నేల మొదలైనవన్నీ మిశ్రమాలు.
2.1 మిశ్రమం అంటే ఏమిటి?
మిశ్రమాలు ఒకటి కంటే ఎక్కువ రకాల శుద్ధ పదార్థ రూపాలతో నిర్మితమవుతాయి. కరిగిన సోడియం క్లోరైడ్ నీటి నుండి బాష్పీభవనం అనే భౌతిక ప్రక్రియ ద్వారా వేరు చేయబడుతుందని మనకు తెలుసు. అయితే, సోడియం క్లోరైడ్ కూడా ఒక శుద్ధ పదార్థం మరియు దాని రసాయన భాగాలుగా భౌతిక ప్రక్రియ ద్వారా వేరు చేయబడదు. అదేవిధంగా, చక్కెర అనేది ఒక రకమైన శుద్ధ పదార్థాన్ని మాత్రమే కలిగి ఉండే పదార్థం మరియు దాని కూర్పు అంతటా ఒకేలా ఉంటుంది.
సాఫ్ట్ డ్రింక్ మరియు నేల ఒకే శుద్ధ పదార్థాలు కావు. ఒక శుద్ధ పదార్థం యొక్క మూలం ఏదైనప్పటికీ, దానికి ఎల్లప్పుడూ ఒకే లక్షణ గుణాలు ఉంటాయి.
కాబట్టి, ఒక మిశ్రమంలో ఒకటి కంటే ఎక్కువ శుద్ధ పదార్థాలు ఉంటాయి అని మనం చెప్పవచ్చు.
2.1.1 మిశ్రమాల రకాలు
మిశ్రమాన్ని ఏర్పరిచే భాగాల స్వభావాన్ని బట్టి, మనకు వివిధ రకాల మిశ్రమాలు ఉంటాయి.
కృత్యం 2.1
తరగతిని A, $B, C$ మరియు $D$ గ్రూపులుగా విభజిద్దాం.
-
గ్రూప్ A $50 mL$ నీటిని కలిగి ఉన్న బీకర్ మరియు ఒక స్పాటులా నిండా కాపర్ సల్ఫేట్ పొడిని తీసుకుంటుంది. గ్రూప్ B బీకర్లో $50 mL$ నీరు మరియు రెండు స్పాటులా నిండా కాపర్ సల్ఫేట్ పొడిని తీసుకుంటుంది.
-
గ్రూపులు C మరియు D వివిధ మొత్తాలలో కాపర్ సల్ఫేట్ మరియు పొటాషియం పెర్మాంగనేట్ లేదా సాధారణ ఉప్పు (సోడియం క్లోరైడ్) తీసుకొని ఇచ్చిన భాగాలను కలిపి మిశ్రమాన్ని ఏర్పరచవచ్చు. రంగు మరియు నిర్మాణంలో ఏకరూపతపై పరిశీలనలను నివేదించండి.
-
గ్రూపులు A మరియు B అంతటా ఏకరూప కూర్పు ఉన్న మిశ్రమాన్ని పొందాయి. అటువంటి మిశ్రమాలను సజాతీయ మిశ్రమాలు లేదా ద్రావణాలు అంటారు. అటువంటి మిశ్రమాలకు ఇతర ఉదాహరణలు: (i) నీటిలో కరిగిన ఉప్పు మరియు (ii) నీటిలో కరిగిన చక్కెర. రెండు గ్రూపుల ద్రావణాల రంగును పోల్చండి. రెండు గ్రూపులూ కాపర్ సల్ఫేట్ ద్రావణాన్ని పొందాయి కానీ ద్రావణాల రంగు తీవ్రత భిన్నంగా ఉంది. ఇది ఒక సజాతీయ మిశ్రమానికి మారుతున్న కూర్పు ఉండవచ్చు అని చూపిస్తుంది.
-
గ్రూపులు C మరియు D మిశ్రమాలను పొందాయి, అవి భౌతికంగా విభిన్న భాగాలను కలిగి ఉంటాయి మరియు ఏకరూపం కాని కూర్పును కలిగి ఉంటాయి. అటువంటి మిశ్రమాలను విజాతీయ మిశ్రమాలు అంటారు. సోడియం క్లోరైడ్ మరియు ఇనుప దుమ్ము, ఉప్పు మరియు గంధకం, మరియు నూనె మరియు నీటి మిశ్రమాలు విజాతీయ మిశ్రమాలకు ఉదాహరణలు.
కృత్యం 2.2
-
మళ్ళీ తరగతిని నాలుగు గ్రూపులుగా- A, B, C మరియు D గా విభజిద్దాం.
-
ప్రతి గ్రూపుకు ఈ క్రింది నమూనాలను పంపిణీ చేయండి:
-
గ్రూప్ A కి కాపర్ సల్ఫేట్ యొక్క కొన్ని స్ఫటికాలు.
-
గ్రూప్ B కి ఒక స్పాటులా నిండా కాపర్ సల్ఫేట్.
-
గ్రూప్ $C$ కి సుద్ద లేదా గోధుమ పిండి.
-
గ్రూప్ D కి పాలు లేదా శాశ్వి యొక్క కొన్ని చుక్కలు.
-
-
ప్రతి గ్రూపు ఇచ్చిన నమూనాను నీటిలో కలిపి గాజు కడ్డీతో సరిగా కలియబెట్టాలి. మిశ్రమంలోని కణాలు కనిపిస్తున్నాయా?
-
టార్చ్ నుండి కాంతి పుంజాన్ని మిశ్రమాన్ని కలిగి ఉన్న బీకర్ గుండా నేరుగా ప్రసారం చేయండి మరియు ముందు నుండి గమనించండి. కాంతి పుంజం యొక్క మార్గం కనిపించిందా?
-
మిశ్రమాలను కొన్ని నిమిషాలు శాంతంగా వదిలివేయండి (మరియు ఈ సమయంలో వడపోత సాధనాన్ని ఏర్పాటు చేయండి). మిశ్రమం స్థిరంగా ఉందా లేదా కొంత సమయం తర్వాత కణాలు స్థిరపడటం ప్రారంభిస్తాయా?
-
మిశ్రమాన్ని వడపోత చేయండి. వడపోత కాగితంపై ఏదైనా అవశేషం ఉందా?
-
ఫలితాలను చర్చించి ఒక అభిప్రాయాన్ని రూపొందించండి.
గ్రూపులు $A$ మరియు $B$ ఒక ద్రావణాన్ని పొందాయి.
గ్రూప్ $C$ ఒక సస్పెన్షన్ ను పొందింది.
గ్రూప్ D ఒక కొలాయిడల్ ద్రావణాన్ని పొందింది.
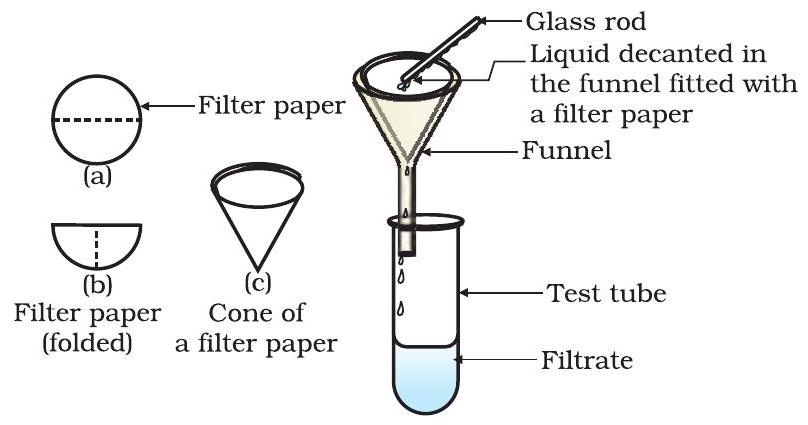
Fig. 2.2: వడపోత
ఇప్పుడు, మనం ద్రావణాలు, సస్పెన్షన్లు మరియు కొలాయిడల్ ద్రావణాల గురించి క్రింది విభాగాలలో తెలుసుకుంటాము.
2.2 ద్రావణం అంటే ఏమిటి?
ద్రావణం అనేది రెండు లేదా అంతకంటే ఎక్కువ పదార్థాల సజాతీయ మిశ్రమం. మీ రోజువారీ జీవితంలో మీరు వివిధ రకాల ద్రావణాలను చూస్తారు. నిమ్మరసం, సోడా వాటర్ మొదలైనవన్నీ ద్రావణాలకు ఉదాహరణలు. సాధారణంగా మనం ద్రావణాన్ని ద్రవంగా భావిస్తాము, దానిలో ఘన, ద్రవ లేదా వాయువు కరిగి ఉంటుంది. కానీ, మనకు ఘన ద్రావణాలు (మిశ్రమ లోహాలు) మరియు వాయు ద్రావణాలు (గాలి) కూడా ఉంటాయి. ఒక ద్రావణంలో కణ స్థాయిలో సజాతీయత ఉంటుంది. ఉదాహరణకు, నిమ్మరసం అంతటా ఒకే రుచి ఉంటుంది. ఇది చక్కెర లేదా ఉప్పు కణాలు ద్రావణంలో సమానంగా పంపిణీ చేయబడతాయని చూపిస్తుంది.
మిశ్రమ లోహాలు: మిశ్రమ లోహాలు రెండు లేదా అంతకంటే ఎక్కువ లోహాలు లేదా ఒక లోహం మరియు అలోహం యొక్క మిశ్రమాలు మరియు వాటి భాగాలుగా భౌతిక పద్ధతుల ద్వారా వేరు చేయబడవు. అయినప్పటికీ, ఒక మిశ్రమ లోహం మిశ్రమంగా పరిగణించబడుతుంది ఎందుకంటే అది దాని భాగాల లక్షణాలను చూపుతుంది మరియు మారుతున్న కూర్పును కలిగి ఉండవచ్చు. ఉదాహరణకు, పిత్తడి అనేది సుమారు $30 %$ జింక్ మరియు $70 %$ రాగి యొక్క మిశ్రమం.
ఒక ద్రావణానికి ద్రావకం మరియు ద్రావితం దాని భాగాలుగా ఉంటాయి. ఇతర భాగాన్ని దానిలో కరిగించే ద్రావణ భాగం (సాధారణంగా ఎక్కువ మొత్తంలో ఉండే భాగం) ద్రావకం అంటారు. ద్రావకంలో కరిగిన ద్రావణ భాగం (సాధారణంగా తక్కువ మొత్తంలో ఉంటుంది) ద్రావితం అంటారు.
ఉదాహరణలు:
(i) నీటిలో చక్కెర ద్రావణం ఘన-ద్రవ ద్రావణం. ఈ ద్రావణంలో, చక్కెర ద్రావితం మరియు నీరు ద్రావకం.
(ii) ఆల్కహాల్లో అయోడిన్ ద్రావణం ‘టింక్చర్ ఆఫ్ అయోడిన్’గా పిలువబడుతుంది, ఇందులో అయోడిన్ (ఘన) ద్రావితంగా మరియు ఆల్కహాల్ (ద్రవ) ద్రావకంగా ఉంటాయి.
(iii) సోడా వాటర్ వంటి ఎరేటెడ్ పానీయాలు వాయు-ద్రవ ద్రావణాలు. ఇవి కార్బన్ డయాక్సైడ్ (వాయువు) ను ద్రావితంగా మరియు నీటిని (ద్రవ) ద్రావకంగా కలిగి ఉంటాయి.
(iv) గాలి వాయు-వాయు మిశ్రమం. గాలి అనేక వాయువుల సజాతీయ మిశ్రమం. దీని రెండు ప్రధాన భాగాలు: ఆక్సిజన్ $(21 %)$ మరియు నత్రజని (78%). ఇతర వాయువులు చాలా తక్కువ మొత్తంలో ఉంటాయి.
ద్రావణం యొక్క లక్షణాలు
-
ద్రావణం ఒక సజాతీయ మిశ్రమం.
-
ద్రావణం యొక్క కణాలు $1 nm(10^{-9}.$ మీటర్ $)$ వ్యాసం కంటే చిన్నవి. కాబట్టి, అవి నగ్న కళ్ళతో చూడబడవు.
-
చాలా చిన్న కణ పరిమాణం కారణంగా, అవి ద్రావణం గుండా వెళ్ళే కాంతి పుంజాన్ని చెదరగొట్టవు. కాబట్టి, ద్రావణంలో కాంతి మార్గం కనిపించదు.
-
ద్రావిత కణాలను వడపోత ప్రక్రియ ద్వారా మిశ్రమం నుండి వేరు చేయలేము. ద్రావిత కణాలు శాంతంగా వదిలివేసినప్పుడు స్థిరపడవు, అంటే, ద్రావణం స్థిరంగా ఉంటుంది.
2.2.1 ద్రావణం యొక్క గాఢత
కృత్యం 2.2 లో, గ్రూపులు A మరియు B వివిధ రంగుల ద్రావణాలను పొందాయని మనం గమనించాము. కాబట్టి, ఒక ద్రావణంలో ద్రావితం మరియు ద్రావకం యొక్క సాపేక్ష నిష్పత్తి మారుతూ ఉంటుందని మనం అర్థం చేసుకుంటాము. ఒక ద్రావణంలో ఉన్న ద్రావితం మొత్తాన్ని బట్టి, దానిని విలీన ద్రావణం, గాఢ ద్రావణం లేదా సంతృప్త ద్రావణం అని పిలవవచ్చు. విలీనం మరియు గాఢం అనేవి సాపేక్ష పదాలు. కృత్యం 2.2 లో, గ్రూప్ A పొందిన ద్రావణం గ్రూప్ B పొందిన ద్రావణంతో పోల్చినప్పుడు విలీనమైనది.
కృత్యం 2.3
-
రెండు వేర్వేరు బీకర్లలో ఒక్కొక్కటి సుమారు $50 mL$ నీటిని తీసుకోండి.
-
ఒక బీకర్లో ఉప్పును మరియు రెండవ బీకర్లో చక్కెర లేదా బేరియం క్లోరైడ్ ను నిరంతరం కలిపేస్తూ కలపండి. ఇంకే ద్రావితం కరగలేనప్పుడు, ఉష్ణోగ్రతను సుమారు $5^{\circ} C$ పెంచడానికి బీకర్ లోని పదార్థాన్ని వేడి చేయండి.
-
మళ్ళీ ద్రావితాన్ని కలపడం ప్రారంభించండి.
ఇచ్చిన ఉష్ణోగ్రత వద్ద నీటిలో కరిగే ఉప్పు మరియు చక్కెర లేదా బేరియం క్లోరైడ్ మొత్తం ఒకేలా ఉంటుందా?
ఏదైనా నిర్దిష్ట ఉష్ణోగ్రత వద్ద, దానిలో కరగగలిగినంత ద్రావితాన్ని కరిగించిన ద్రావణాన్ని సంతృప్త ద్రావణం అంటారు. మరో మాటలో చెప్పాలంటే, ఇచ్చిన ఉష్ణోగ్రత వద్ద ఒక ద్రావణంలో ఇంకే ద్రావితం కరగలేనప్పుడు, దానిని సంతృప్త ద్రావణం అంటారు. ఈ ఉష్ణోగ్రత వద్ద సంతృప్త ద్రావణంలో ఉన్న ద్రావితం మొత్తాన్ని దాని ద్రావణీయత అంటారు.
ఒక ద్రావణంలో ఉన్న ద్రావితం మొత్తం సంతృప్తత స్థాయి కంటే తక్కువగా ఉంటే, దానిని అసంతృప్త ద్రావణం అంటారు.
మీరు ఒక నిర్దిష్ట ఉష్ణోగ్రత వద్ద సంతృప్త ద్రావణాన్ని తీసుకొని నెమ్మదిగా చల్లబరిస్తే ఏమి జరుగుతుంది.
పై కృత్యం నుండి మనం ఇచ్చిన ద్రావకంలోని వివిధ పదార్థాలు ఒకే ఉష్ణోగ్రత వద్ద వివిధ ద్రావణీయతను కలిగి ఉంటాయని నిర్ధారించవచ్చు.
ద్రావణం యొక్క గాఢత అనేది ఇచ్చిన ద్రావణం (ద్రవ్యరాశి లేదా ఘనపరిమాణం) లో ఉన్న ద్రావితం యొక్క మొత్తం (ద్రవ్యరాశి లేదా ఘనపరిమాణం).
ద్రావణం యొక్క గాఢతను వ్యక్తపరిచే వివిధ మార్గాలు ఉన్నాయి, కానీ ఇక్కడ మనం మూడు పద్ధతులను మాత్రమే నేర్చుకుంటాము.
(i) ద్రావణం యొక్క ద్రవ్యరాశి-ద్వారా-ద్రవ్యరాశి శాతం
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) ద్రావణం యొక్క ద్రవ్యరాశి-ద్వారా-ఘనపరిమాణం శాతం
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) ద్రావణం యొక్క ఘనపరిమాణం-ద్వారా-ఘనపరిమాణం శాతం
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
ఉదాహరణ 2.1 ఒక ద్రావణంలో $40 g$ సాధారణ ఉప్పు $320 g$ నీటిలో ఉంది. ద్రవ్యరాశి-ద్వారా-ద్రవ్యరాశి శాతం పరంగా ద్రావణం యొక్క గాఢతను లెక్కించండి.
సాధన:
ద్రావితం యొక్క ద్రవ్యరాశి (ఉప్పు) $\quad=40 g$
ద్రావకం యొక్క ద్రవ్యరాశి (నీరు) $=320 g$
మనకు తెలుసు,
ద్రావణం యొక్క ద్రవ్యరాశి $=$ ద్రావితం యొక్క ద్రవ్యరాశి + ద్రావకం యొక్క ద్రవ్యరాశి
$$=40 g+320 g$$
$$=360 g$$
ద్రావణం యొక్క ద్రవ్యరాశి శాతం
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
2.2.2 సస్పెన్షన్ అంటే ఏమిటి?
కృత్యం 2.2 సజాతీయం కాని వ్యవస్థలు, కృత్యం 2.2 లో గ్రూప్ $C$ పొందిన వాటి వలె, ఇందులో ఘనపదార్థాలు ద్రవాలలో చెదరగొట్టబడతాయి, వాటిని సస్పెన్షన్లు అంటారు. సస్పెన్షన్ అనేది ఒక విజాతీయ మిశ్రమం, ఇందులో ద్రావిత కణాలు కరగవు కానీ మాధ్యమం మొత్తం పరిమాణంలో నిలుపుదలగా ఉంటాయి. సస్పెన్షన్ యొక్క కణాలు నగ్న కళ్ళతో కనిపిస్తాయి.
సస్పెన్షన్ యొక్క లక్షణాలు
-
సస్పెన్షన్ ఒక విజాతీయ మిశ్రమం.
-
సస్పెన్షన్ యొక్క కణాలు నగ్న కళ్ళతో చూడవచ్చు.
-
సస్పెన్షన్ యొక్క కణాలు దాని గుండా వెళ్ళే కాంతి పుంజాన్ని చెదరగొట్టి దాని మార్గాన్ని కనిపించేలా చేస్తాయి.
-
సస్పెన్షన్ శాంతంగా వదిలివేసినప్పుడు ద్రావిత కణాలు స్థిరపడతాయి, అంటే, సస్పెన్షన్ అస్థిరంగా ఉంటుంది. వాటిని వడపోత ప్రక్రియ ద్వారా మిశ్రమం నుండి వేరు చేయవచ్చు. కణాలు స్థిరపడినప్పుడు, సస్పెన్షన్ విడిపోతుంది మరియు అది ఇంకెప్పుడూ కాంతిని చెదరగొట్టదు.
2.2.3 కొలాయిడల్ ద్రావణం అంటే ఏమిటి?
కృత్యం 2.2 కృత్యం 2.2 లో గ్రూప్ D పొందిన మిశ్రమాన్ని కొలాయిడ్ లేదా కొలాయిడల్ ద్రావణం అంటారు. కొలాయిడ్ యొక్క కణాలు ద్రావణం అంతటా ఏకరీతిగా వ్యాపించి ఉంటాయి. సస్పెన్షన్ కంటే చిన్న పరిమాణంలో ఉన్న కణాల కారణంగా, మిశ్రమం సజాతీయంగా కనిపిస్తుంది. కానీ వాస్తవానికి, కొలాయిడల్ ద్రావణం ఒక విజాతీయ మిశ్రమం, ఉదాహరణకు, పాలు.
కొలాయిడల్ కణాలు చిన్న పరిమాణం కారణంగా, మనం వాటిని నగ్న కళ్ళతో చూడలేము. కానీ, ఈ కణాలు కృత్యం 2.2 లో గమనించినట్లుగా దృశ్యమాన కాంతి పుంజాన్ని సులభంగా చెదరగొట్టగలవు. కాంతి పుంజం యొక్క ఈ చెదరగొట్టడాన్ని ఈ ప్రభావాన్ని కనుగొన్న శాస్త్రవేత్త పేరు మీద టిండాల్ ప్రభావం అంటారు.
ఒక సన్నని కాంతి పుంజం ఒక చిన్న రంధ్రం ద్వారా గదిలోకి ప్రవేశించినప్పుడు కూడా టిండాల్ ప్రభావాన్ని గమనించవచ్చు. గాలిలోని దుమ్ము మరియు పొగ కణాల ద్వారా కాంతి చెదరగొట్టబడటం వలన ఇది జరుగుతుంది.
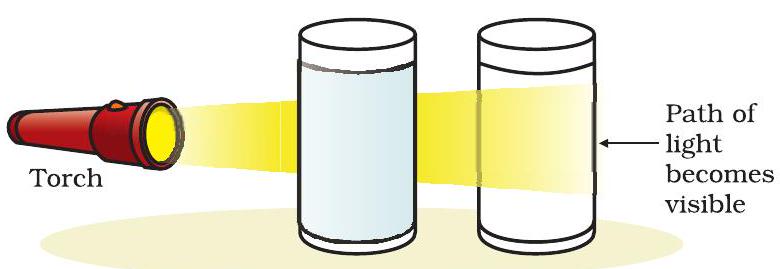
Fig. 2.3: (a) కాపర్ సల్ఫేట్ ద్రావణం టిండాల్ ప్రభావాన్ని చూపించదు, (b) నీరు మరియు పాల మిశ్రమం టిండాల్ ప్రభావాన్ని చూపిస్తుంది.
సూర్యకాంతి దట్టమైన అడవి కానోపీ గుండా వెళ్ళినప్పుడు టిండాల్ ప్రభావాన్ని గమనించవచ్చు. అడవిలో, పొగమంచు నీటి సూక్ష్మ బిందువులను కలిగి ఉంటుంది, అవి గాలిలో చెదరగొట్టబడిన కొలాయిడ్ కణాలుగా పనిచేస్తాయి.

Fig. 2.4: టిండాల్ ప్రభావం
కొలాయిడ్ యొక్క లక్షణాలు
-
కొలాయిడ్ ఒక విజాతీయ మిశ్రమం.
-
కొలాయిడ్ యొక్క కణాల పరిమాణం నగ్న కళ్ళతో వ్యక్తిగతంగా చూడడానికి చాలా చిన్నది.
-
కొలాయిడ్లు దాని గుండా వెళ్ళే కాంతి పుంజాన్ని చెదరగొట్టడానికి మరియ











