நம்மைச் சுற்றியுள்ள பருப்பொருள் தூய்மையானதா?
நாம் சந்தையில் வாங்கும் பால், நெய், வெண்ணெய், உப்பு, மசாலாப் பொருட்கள், கனிம நீர் அல்லது பழச்சாறு ஆகியவை தூய்மையானவையா என்பதை எவ்வாறு முடிவு செய்வது?

படம் 2.1: சில நுகர்வுப் பொருட்கள்
இந்த நுகர்வுப் பொருட்களின் பாக்கெட்டுகளில் ‘தூய்மை’ என்ற வார்த்தை எழுதப்பட்டிருப்பதை நீங்கள் எப்போதாவது கவனித்திருக்கிறீர்களா? ஒரு சாதாரண நபருக்கு தூய்மை என்றால் கலப்படம் இல்லாதது என்று பொருள். ஆனால், ஒரு விஞ்ஞானிக்கு இந்த அனைத்துப் பொருட்களும் உண்மையில் வெவ்வேறு பொருட்களின் கலவைகளாகும், எனவே அவை தூய்மையானவை அல்ல. எடுத்துக்காட்டாக, பால் என்பது உண்மையில் நீர், கொழுப்பு, புரதங்கள் போன்றவற்றின் கலவையாகும். ஒரு விஞ்ஞானி ஏதேனும் ஒன்று தூய்மையானது என்று சொல்லும்போது, அந்தப் பொருளின் அனைத்து கூறு துகள்களும் அவற்றின் வேதியியல் தன்மையில் ஒரே மாதிரியானவை என்பதாகும். ஒரு தூய பொருள் ஒரே வகையான துகள்களைக் கொண்டிருக்கும். வேறுவிதமாகக் கூறினால், ஒரு பொருள் என்பது பருப்பொருளின் தூய ஒற்றை வடிவமாகும்.
நாம் சுற்றிப் பார்க்கும்போது, நம்மைச் சுற்றியுள்ள பெரும்பாலான பருப்பொருட்கள் இரண்டு அல்லது அதற்கு மேற்பட்ட தூய கூறுகளின் கலவையாகவே உள்ளன என்பதைக் காணலாம். எடுத்துக்காட்டாக, கடல் நீர், கனிமங்கள், மண் போன்றவை அனைத்தும் கலவைகளே.
2.1 கலவை என்றால் என்ன?
கலவைகள் ஒன்றுக்கு மேற்பட்ட வகையான தூய பருப்பொருள் வடிவங்களால் உருவாக்கப்படுகின்றன. கரைந்த சோடியம் குளோரைடு நீரிலிருந்து ஆவியாதல் என்ற இயற்பியல் செயல்முறை மூலம் பிரிக்கப்படலாம் என்பது நமக்குத் தெரியும். இருப்பினும், சோடியம் குளோரைடே ஒரு தூய பொருள் மற்றும் அதன் வேதியியல் கூறுகளாக இயற்பியல் செயல்முறை மூலம் பிரிக்க முடியாது. இதேபோல், சர்க்கரை என்பது ஒரே ஒரு வகையான தூய பருப்பொருளை மட்டுமே கொண்ட ஒரு பொருள் மற்றும் அதன் கலவை முழுவதும் ஒரே மாதிரியாக இருக்கும்.
பழச்சாறு மற்றும் மண் ஆகியவை ஒற்றை தூய பொருட்கள் அல்ல. ஒரு தூய பொருளின் மூலம் எதுவாக இருந்தாலும், அது எப்போதும் ஒரே மாதிரியான பண்புகளைக் கொண்டிருக்கும்.
எனவே, ஒரு கலவையானது ஒன்றுக்கு மேற்பட்ட தூய பொருட்களைக் கொண்டிருக்கும் என்று நாம் கூறலாம்.
2.1.1 கலவைகளின் வகைகள்
ஒரு கலவையை உருவாக்கும் கூறுகளின் தன்மையைப் பொறுத்து, நம்மிடம் வெவ்வேறு வகையான கலவைகள் இருக்கலாம்.
செயல்பாடு 2.1
வகுப்பை A, $B, C$ மற்றும் $D$ என்ற குழுக்களாகப் பிரிப்போம்.
-
குழு A, $50 mL$ தண்ணீர் மற்றும் ஒரு ஸ்பேடுலா நிறைய காப்பர் சல்பேட் தூள் கொண்ட ஒரு குடுவையை எடுக்கும். குழு B, $50 mL$ தண்ணீர் மற்றும் இரண்டு ஸ்பேடுலா நிறைய காப்பர் சல்பேட் தூளை ஒரு குடுவையில் எடுக்கும்.
-
குழு C மற்றும் D வெவ்வேறு அளவு காப்பர் சல்பேட் மற்றும் பொட்டாசியம் பெர்மாங்கனேட் அல்லது சாதாரண உப்பு (சோடியம் குளோரைடு) ஆகியவற்றை எடுத்து, கொடுக்கப்பட்ட கூறுகளைக் கலந்து ஒரு கலவையை உருவாக்கலாம். நிறம் மற்றும் அமைப்பில் உள்ள ஒருமைப்பாடு குறித்த கவனிப்புகளைப் பதிவு செய்யவும்.
-
குழு A மற்றும் B முழுவதும் ஒரே மாதிரியான கலவையைக் கொண்ட ஒரு கலவையைப் பெற்றுள்ளன. இத்தகைய கலவைகள் ஒரே மாதிரியான கலவைகள் அல்லது கரைசல்கள் என்று அழைக்கப்படுகின்றன. இத்தகைய கலவைகளின் வேறு சில எடுத்துக்காட்டுகள்: (i) உப்பு நீரில் கரைக்கப்பட்டது மற்றும் (ii) சர்க்கரை நீரில் கரைக்கப்பட்டது. இரண்டு குழுக்களின் கரைசல்களின் நிறத்தை ஒப்பிடுக. இரண்டு குழுக்களும் காப்பர் சல்பேட் கரைசலைப் பெற்றிருந்தாலும், கரைசல்களின் நிறத்தின் செறிவு வித்தியாசமாக உள்ளது. இது ஒரு ஒரே மாதிரியான கலவையானது மாறுபட்ட கலவையைக் கொண்டிருக்கலாம் என்பதைக் காட்டுகிறது.
-
குழு C மற்றும் D கலவைகளைப் பெற்றுள்ளன, அவை இயற்பியல் ரீதியாக வேறுபட்ட பகுதிகளைக் கொண்டிருக்கின்றன மற்றும் ஒரே மாதிரியற்ற கலவையைக் கொண்டிருக்கின்றன. இத்தகைய கலவைகள் ஒரே மாதிரியற்ற கலவைகள் என்று அழைக்கப்படுகின்றன. சோடியம் குளோரைடு மற்றும் இரும்பு தூள், உப்பு மற்றும் கந்தகம், எண்ணெய் மற்றும் நீர் ஆகியவற்றின் கலவைகள் ஒரே மாதிரியற்ற கலவைகளுக்கு எடுத்துக்காட்டுகள்.
செயல்பாடு 2.2
-
வகுப்பை மீண்டும் நான்கு குழுக்களாகப் பிரிப்போம்- A, B, C மற்றும் D.
-
ஒவ்வொரு குழுவிற்கும் பின்வரும் மாதிரிகளை விநியோகிக்கவும்:
-
குழு A க்கு சில காப்பர் சல்பேட் படிகங்கள்.
-
குழு B க்கு ஒரு ஸ்பேடுலா நிறைய காப்பர் சல்பேட்.
-
சுண்ணாம்பு தூள் அல்லது கோதுமை மாவு குழு $C$ க்கு.
-
சில துளி பால் அல்லது மை குழு D க்கு.
-
-
ஒவ்வொரு குழுவும் கொடுக்கப்பட்ட மாதிரியை நீரில் சேர்த்து, கண்ணாடி கோலைப் பயன்படுத்தி சரியாகக் கிளற வேண்டும். கலவையில் உள்ள துகள்கள் தெரிகின்றனவா?
-
ஒரு டார்ச் மூலம் ஒரு ஒளிக்கற்றையை கலவையைக் கொண்ட குடுவை வழியாக நேரடியாகச் செலுத்தி, முன்பக்கத்திலிருந்து கவனிக்கவும். ஒளிக்கற்றையின் பாதை தெரிந்ததா?
-
கலவைகளை சில நிமிடங்கள் அசையாமல் விட்டு விடுங்கள் (இதற்கிடையில் வடிகட்டும் கருவியமைப்பை அமைக்கவும்). கலவை நிலையானதா அல்லது சிறிது நேரம் கழித்து துகள்கள் தங்க ஆரம்பிக்கின்றனவா?
-
கலவையை வடிகட்டவும். வடிகட்டி தாளில் எந்த எச்சமும் உள்ளதா?
-
முடிவுகளைப் பற்றி விவாதித்து, ஒரு கருத்தை உருவாக்குங்கள்.
குழுக்கள் $A$ மற்றும் $B$ ஒரு கரைசலைப் பெற்றுள்ளன.
குழு $C$ ஒரு கலங்கல் கரைசலைப் பெற்றுள்ளது.
குழு D ஒரு கூழ்மக் கரைசலைப் பெற்றுள்ளது.
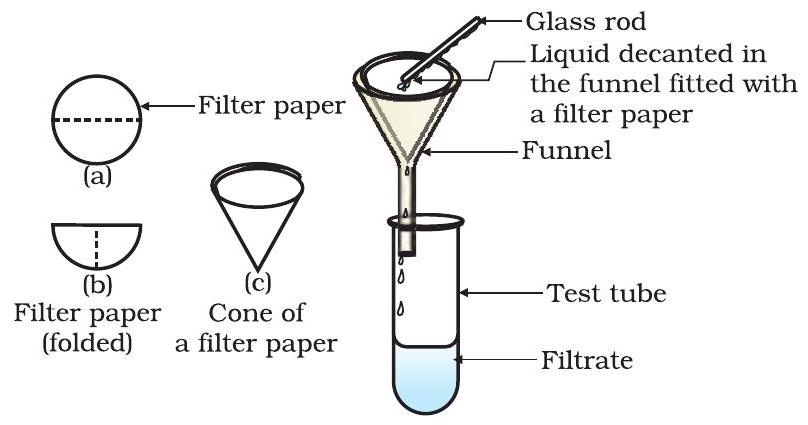
படம் 2.2: வடிகட்டுதல்
இப்போது, பின்வரும் பிரிவுகளில் கரைசல்கள், கலங்கல் கரைசல்கள் மற்றும் கூழ்மக் கரைசல்கள் பற்றி நாம் கற்றுக்கொள்வோம்.
2.2 கரைசல் என்றால் என்ன?
ஒரு கரைசல் என்பது இரண்டு அல்லது அதற்கு மேற்பட்ட பொருட்களின் ஒரே மாதிரியான கலவையாகும். உங்கள் அன்றாட வாழ்க்கையில் பல்வேறு வகையான கரைசல்களை நீங்கள் சந்திக்கிறீர்கள். எலுமிச்சைப் பழச்சாறு, சோடா நீர் போன்றவை அனைத்தும் கரைசல்களின் எடுத்துக்காட்டுகள். பொதுவாக ஒரு கரைசலை ஒரு திரவமாக நாம் கருதுகிறோம், அது ஒரு திடப்பொருள், திரவம் அல்லது வாயுவைக் கொண்டிருக்கும். ஆனால், நம்மிடம் திட கரைசல்களும் (கலப்புலோகங்கள்) மற்றும் வாயு கரைசல்களும் (காற்று) இருக்கலாம். ஒரு கரைசலில் துகள் மட்டத்தில் ஒருமைப்பாடு உள்ளது. எடுத்துக்காட்டாக, எலுமிச்சைப் பழச்சாறு முழுவதும் ஒரே சுவையைக் கொண்டிருக்கும். இது சர்க்கரை அல்லது உப்பின் துகள்கள் கரைசலில் சமமாக பரவியுள்ளன என்பதைக் காட்டுகிறது.
கலப்புலோகங்கள்: கலப்புலோகங்கள் என்பது இரண்டு அல்லது அதற்கு மேற்பட்ட உலோகங்கள் அல்லது ஒரு உலோகம் மற்றும் அலோகம் ஆகியவற்றின் கலவைகள் மற்றும் அவற்றின் கூறுகளாக இயற்பியல் முறைகளால் பிரிக்க முடியாது. ஆனாலும், ஒரு கலப்புலோகம் அதன் கூறுகளின் பண்புகளைக் காட்டுவதாலும், மாறுபட்ட கலவையைக் கொண்டிருக்கலாம் என்பதாலும் ஒரு கலவையாகக் கருதப்படுகிறது. எடுத்துக்காட்டாக, பித்தளை என்பது தோராயமாக $30 %$ துத்தநாகம் மற்றும் $70 %$ செம்பின் கலவையாகும்.
ஒரு கரைசலில் ஒரு கரைப்பான் மற்றும் ஒரு கரைபொருள் ஆகியவை அதன் கூறுகளாக உள்ளன. மற்ற கூறுகளைத் தன்னுள் கரைக்கும் கரைசலின் கூறு (பொதுவாக அதிக அளவில் இருக்கும் கூறு) கரைப்பான் என்று அழைக்கப்படுகிறது. கரைப்பானில் கரைக்கப்படும் கரைசலின் கூறு (பொதுவாக குறைந்த அளவில் இருக்கும்) கரைபொருள் என்று அழைக்கப்படுகிறது.
எடுத்துக்காட்டுகள்:
(i) நீரில் சர்க்கரையின் கரைசல் என்பது ஒரு திடப்பொருள்-திரவ கரைசலாகும். இந்த கரைசலில், சர்க்கரை கரைபொருள் மற்றும் நீர் கரைப்பான் ஆகும்.
(ii) அயோடின் மற்றும் ஆல்கஹாலின் கரைசல் ‘அயோடின் டிங்சர்’ என்று அழைக்கப்படுகிறது, இதில் அயோடின் (திடப்பொருள்) கரைபொருளாகவும், ஆல்கஹால் (திரவம்) கரைப்பானாகவும் உள்ளது.
(iii) சோடா நீர் போன்ற கார்பனேற்றப்பட்ட பானங்கள், வாயு-திரவ கரைசல்களாகும். இவை கார்பன் டை ஆக்சைடு (வாயு) கரைபொருளாகவும், நீர் (திரவம்) கரைப்பானாகவும் கொண்டிருக்கின்றன.
(iv) காற்று என்பது வாயு-வாயு கலவையாகும். காற்று என்பது பல வாயுக்களின் ஒரே மாதிரியான கலவையாகும். அதன் இரண்டு முக்கிய கூறுகள்: ஆக்ஸிஜன் $(21 %)$ மற்றும் நைட்ரஜன் (78%). மற்ற வாயுக்கள் மிகச் சிறிய அளவில் உள்ளன.
ஒரு கரைசலின் பண்புகள்
-
ஒரு கரைசல் என்பது ஒரே மாதிரியான கலவையாகும்.
-
ஒரு கரைசலின் துகள்கள் $1 nm(10^{-9}.$ மீட்டர் $)$ விட்டத்தை விட சிறியவை. எனவே, அவை நaked கண்களால் பார்க்க முடியாது.
-
மிகச் சிறிய துகள் அளவு காரணமாக, அவை கரைசல் வழியாகச் செல்லும் ஒளிக்கற்றையை சிதறடிப்பதில்லை. எனவே, ஒரு கரைசலில் ஒளியின் பாதை தெரியாது.
-
கரைபொருள் துகள்களை வடிகட்டுதல் செயல்முறை மூலம் கலவையிலிருந்து பிரிக்க முடியாது. கரைபொருள் துகள்கள் கலவையை அசையாமல் விட்டுவிட்டால் தங்குவதில்லை, அதாவது ஒரு கரைசல் நிலையானது.
2.2.1 ஒரு கரைசலின் செறிவு
செயல்பாடு 2.2 இல், குழு A மற்றும் B வெவ்வேறு நிற அளவுகளில் கரைசல்களைப் பெற்றதை நாம் கவனித்தோம். எனவே, ஒரு கரைசலில் கரைபொருள் மற்றும் கரைப்பானின் தொடர்புடைய விகிதம் மாறுபடலாம் என்பதை நாம் புரிந்துகொள்கிறோம். ஒரு கரைசலில் இருக்கும் கரைபொருளின் அளவைப் பொறுத்து, அதை நீர்த்த, செறிவூட்டப்பட்ட அல்லது செறிவூட்டப்பட்ட கரைசல் என்று அழைக்கலாம். நீர்த்த மற்றும் செறிவூட்டப்பட்டவை ஒப்பீட்டு சொற்களாகும். செயல்பாடு 2.2 இல், குழு A பெற்ற கரைசல் குழு B பெற்ற கரைசலை விட நீர்த்தமானது.
செயல்பாடு 2.3
-
இரண்டு தனி குடுவைகளில் தோராயமாக $50 mL$ தண்ணீர் எடுத்துக் கொள்ளுங்கள்.
-
ஒரு குடுவையில் உப்பையும், இரண்டாவது குடுவையில் சர்க்கரை அல்லது பேரியம் குளோரைடையும் தொடர்ந்து கிளறியபடி சேர்க்கவும். இனி கரைபொருள் கரையாதபோது, வெப்பநிலையை சுமார் $5^{\circ} C$ உயர்த்த குடுவையின் உள்ளடக்கங்களை சூடாக்கவும்.
-
மீண்டும் கரைபொருளைச் சேர்க்கத் தொடங்குங்கள்.
கொடுக்கப்பட்ட வெப்பநிலையில் நீரில் கரையக்கூடிய உப்பு மற்றும் சர்க்கரை அல்லது பேரியம் குளோரைட்டின் அளவு ஒரே மாதிரியானதா?
எந்தவொரு குறிப்பிட்ட வெப்பநிலையிலும், அது கரைக்கக்கூடிய அளவுக்கு கரைபொருள் கரைக்கப்பட்ட ஒரு கரைசல், செறிவூட்டப்பட்ட கரைசல் என்று கூறப்படுகிறது. வேறுவிதமாகக் கூறினால், கொடுக்கப்பட்ட வெப்பநிலையில் ஒரு கரைசலில் இனி கரைபொருள் கரையாதபோது, அது செறிவூட்டப்பட்ட கரைசல் என்று அழைக்கப்படுகிறது. இந்த வெப்பநிலையில் செறிவூட்டப்பட்ட கரைசலில் இருக்கும் கரைபொருளின் அளவு அதன் கரைதிறன் என்று அழைக்கப்படுகிறது.
ஒரு கரைசலில் உள்ள கரைபொருளின் அளவு செறிவூட்டல் அளவை விடக் குறைவாக இருந்தால், அது செறிவூட்டப்படாத கரைசல் என்று அழைக்கப்படுகிறது.
நீங்கள் ஒரு குறிப்பிட்ட வெப்பநிலையில் ஒரு செறிவூட்டப்பட்ட கரைசலை எடுத்து மெதுவாக குளிர்வித்தால் என்ன நடக்கும்?
மேலே உள்ள செயல்பாட்டிலிருந்து, ஒரே வெப்பநிலையில் ஒரு கரைப்பானில் வெவ்வேறு பொருட்கள் வெவ்வேறு கரைதிறனைக் கொண்டிருக்கின்றன என்பதை நாம் ஊகிக்கலாம்.
ஒரு கரைசலின் செறிவு என்பது கொடுக்கப்பட்ட அளவு (நிறை அல்லது கனஅளவு) கரைசலில் இருக்கும் கரைபொருளின் அளவு (நிறை அல்லது கனஅளவு) ஆகும்.
ஒரு கரைசலின் செறிவை வெளிப்படுத்த பல்வேறு வழிகள் உள்ளன, ஆனால் இங்கு நாம் மூன்று முறைகளை மட்டுமே கற்றுக்கொள்வோம்.
(i) ஒரு கரைசலின் நிறை-நிறை சதவீதம்
$$ =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 $$
(ii) ஒரு கரைசலின் நிறை-கனஅளவு சதவீதம்
$$ =\frac{\text{ Mass of solute }}{\text{ Volume of solution }} \times 100 $$
(iii) ஒரு கரைசலின் கனஅளவு-கனஅளவு சதவீதம்
$$ =\frac{\text{ Volume of solute }}{\text{ Volume of solution }} \times 100 $$
எடுத்துக்காட்டு 2.1 ஒரு கரைசலில் $40 g$ சாதாரண உப்பு $320 g$ நீரில் உள்ளது. நிறை-நிறை சதவீதத்தின் அடிப்படையில் கரைசலின் செறிவைக் கணக்கிடுங்கள்.
தீர்வு:
கரைபொருளின் நிறை (உப்பு) $\quad=40 g$
கரைப்பானின் நிறை (நீர்) $=320 g$
நமக்குத் தெரியும்,
கரைசலின் நிறை $=$ கரைபொருளின் நிறை + கரைப்பானின் நிறை
$$=40 g+320 g$$
$$=360 g$$
கரைசலின் நிறை சதவீதம்
$$ \begin{aligned} & =\frac{\text{ Mass of solute }}{\text{ Mass of solution }} \times 100 \\ & =\frac{40}{360} \times 100=11.1 \% \end{aligned} $$
2.2.2 கலங்கல் கரைசல் என்றால் என்ன?
செயல்பாடு 2.2 ஒரே மாதிரியற்ற அமைப்புகள், செயல்பாடு 2.2 இல் குழு $C$ பெற்றது போன்றவை, இதில் திடப்பொருட்கள் திரவங்களில் சிதறடிக்கப்படுகின்றன, அவை கலங்கல் கரைசல்கள் என்று அழைக்கப்படுகின்றன. ஒரு கலங்கல் கரைசல் என்பது ஒரு ஒரே மாதிரியற்ற கலவையாகும், இதில் கரைபொருள் துகள்கள் கரைவதில்லை, ஆனால் ஊடகம் முழுவதும் தொங்கிக் கொண்டிருக்கும். ஒரு கலங்கல் கரைசலின் துகள்கள் நaked கண்களால் பார்க்க முடியும்.
ஒரு கலங்கல் கரைசலின் பண்புகள்
-
கலங்கல் கரைசல் என்பது ஒரு ஒரே மாதிரியற்ற கலவையாகும்.
-
ஒரு கலங்கல் கரைசலின் துகள்கள் நaked கண்களால் பார்க்க முடியும்.
-
ஒரு கலங்கல் கரைசலின் துகள்கள் அதன் வழியாகச் செல்லும் ஒளிக்கற்றையை சிதறடித்து, அதன் பாதையைத் தெரியச் செய்கின்றன.
-
ஒரு கலங்கல் கரைசலை அசையாமல் விட்டுவிட்டால் கரைபொருள் துகள்கள் தங்குகின்றன, அதாவது ஒரு கலங்கல் கரைசல் நிலையற்றது. அவை வடிகட்டுதல் செயல்முறை மூலம் கலவையிலிருந்து பிரிக்கப்படலாம். துகள்கள் தங்கும்போது, கலங்கல் கரைசல் உடைந்து, அது இனி ஒளியை சிதறடிப்பதில்லை.
2.2.3 கூழ்மக் கரைசல் என்றால் என்ன?
செயல்பாடு 2.2 செயல்பாடு 2.2 இல் குழு D பெற்ற கலவை கூழ்மம் அல்லது கூழ்மக் கரைசல் என்று அழைக்கப்படுகிறது. ஒரு கூழ்மத்தின் துகள்கள் கரைசல் முழுவதும் சமமாக பரவியுள்ளன. ஒரு கலங்கல் கரைசலுடன் ஒப்பிடும்போது, துகள்களின் ஒப்பீட்டளவில் சிறிய அளவு காரணமாக, கலவை ஒரே மாதிரியாகத் தோன்றுகிறது. ஆனால் உண்மையில், ஒரு கூழ்மக் கரைசல் என்பது ஒரு ஒரே மாதிரியற்ற கலவையாகும், எடுத்துக்காட்டாக, பால்.
கூழ்மத் துகள்களின் சிறிய அளவு காரணமாக, நaked கண்களால் அவற்றைப் பார்க்க முடியாது. ஆனால், இந்த துகள்கள் செயல்பாடு 2.2 இல் கவனிக்கப்பட்டது போல் ஒரு புலப்படும் ஒளிக்கற்றையை எளிதாக சிதறடிக்க முடியும். ஒளிக்கற்றையின் இந்த சிதறல் டிண்டால் விளைவு என்று அழைக்கப்படுகிறது, இந்த விளைவைக் கண்டுபிடித்த விஞ்ஞானியின் பெயரால்.
ஒரு சிறிய துளை வழியாக ஒரு அறைக்குள் ஒரு நேரான ஒளிக்கற்றை நுழையும் போதும் டிண்டால் விளைவைக் காணலாம். இது காற்றில் உள்ள தூசி மற்றும் புகைத் துகள்களால் ஒளி சிதறடிப்பதால் நிகழ்கிறது.
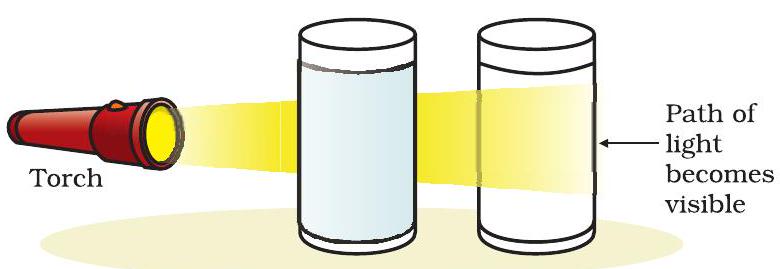
படம் 2.3: (அ) காப்பர் சல்பேட்டின் கரைசல் டிண்டால் விளைவைக் காட்டவில்லை, (ஆ) நீர் மற்றும் பாலின் கலவை டிண்டால் விளைவைக் காட்டுகிறது.
சூரிய ஒளி ஒரு அடர்ந்த காட்டின் விதானம் வழியாகச் செல்லும் போது டிண்டால் விளைவைக் காணலாம். காட்டில், மூடுபனியில் நீரின் நுண்ணிய துளிகள் உள்ளன, அவை காற்றில் சிதறடிக்கப்பட்ட கூழ்மத் துகள்களாக செயல்படுகின்றன.

படம் 2.4: டிண்டால் விளைவு
ஒரு கூழ்மத்தின் பண்புகள்
-
ஒரு கூழ்மம் என்பது ஒரு ஒரே மாதிரியற்ற கலவையாகும்.
-
ஒரு கூழ்மத்தின் துகள்களின் அளவு மிகவும் சிறியதாக இருப்பதால் நaked கண்களால் தனித்தனியாகப் பார்க்க முடியாது.
-
கூழ்மங்கள் அதன் வழியாகச் செல்லும் ஒளிக்கற்றையை சிதறடிக்கவும், அதன் பாதையைத் தெரியச் செய்யவும் போதுமான அளவு பெரியவை.
-
அவை அசையாமல் விடப்பட்டால் தங்குவதில்லை, அதாவது ஒரு கூழ்மம் மிகவும் நிலையானது.
-
அவை வடிகட்டுதல் செயல்முறை மூலம் கலவையிலிருந்து பிரிக்க முடியாது. ஆனால், மையவிலக்கு முறை (செயல்பாடு 2.5 ஐச் செய்யுங்கள்) என்று அழைக்கப்படும் பிரித்தெடுக்கும் ஒரு சிறப்பு நுட்பத்தைக் கூழ்மத் துகள்களைப் பிரிக்கப் பயன்படுத்தலாம்.
ஒரு கூழ்மக் கரைசலின் கூறுகள் சிதறிய கட்டம் மற்றும் சிதறல் ஊடகம் ஆகும். ஒரு கூழ்மத்தில் கரைபொருள் போன்ற கூறு அல்லது சிதறடிக்கப்பட்ட துகள்கள் சிதறிய கட்டத்தை உருவாக்குகின்றன, மேலும் சிதறிய கட்டம் தொங்கவிடப்படும் ஊடகம் சிதறல் ஊடகம் என்று அழைக்கப்படுகிறது. கூழ்மங்கள் சிதறல் ஊடகம் மற்றும் சிதறிய கட்டத்தின் நிலை (திட, திரவ அல்லது வாயு) ஆகியவற்றின் அடிப்படையில் வகைப்படுத்தப்படுகின்றன. சில பொதுவான எடுத்துக்காட்டுகள் அட்டவணை 2.1 இல் கொடுக்கப்பட்டுள்ளன. இந்த அட்டவணையில் இருந்து, அவை அன்றாட வாழ்க்கையில் மிகவும் பொதுவானவை என்பதை நீங்கள் காணலாம்.
அட்டவணை 2.1: கூழ்மங்களின் பொதுவான எடுத்துக்காட்டுகள்
| சிதறிய கட்டம் | சிதறல் ஊடகம் | வகை | எடுத்துக்காட்டு |
|---|---|---|---|
| திரவம் | வாயு | ஏரோசால் | மூடுபனி, மேகங்கள், மூடுபனி |
| திடம் | வாயு | ஏரோசால் | புகை, வாகன வெளியேற்றம் |
| வாயு | திரவம் | நுரை | சவரக் களிம்பு |
| திரவம் | திரவம் | பால்மம் | பால், முகக் களிம்பு |
| திடம் | திரவம் | கூழ் | மக்னீசியா பால், சேறு |
| வாயு | திடம் | நுரை | நுரை, ரப்பர், கடற்பாசி, பியூமைஸ் |
| திரவம் | திடம் | களி | ஜெல்லி, சீஸ், வெண்ணெய் |
| திடம் | திடம் | திட கூழ் | வண்ண ரத்தினக் கல், பால் கண்ணாடி |
2.3 இயற்பியல் மற்றும் வேதியியல் மாற்றங்கள்
முந்தைய அத்தியாயத்தில், பருப்பொருளின் சில இயற்பியல் பண்புகளைப் பற்றி நாம் கற்றுக்கொண்டோம். நிறம், கடினத்தன்மை, விறைப்புத்தன்மை, பாய்மத்தன்மை, அடர்த்தி, உருகுநிலை, கொதிநிலை போன்றவற்றைக் கவனிக்கவும் குறிப்பிடவும் முடியும் என்ற பண்புகள் இயற்பியல் பண்புகளாகும்.
நிலைகளின் பரிமாற்றம் என்பது ஒரு இயற்பியல் மாற்றமாகும், ஏனெனில் இந்த மாற்றங்கள் கலவையில் எந்த மாற்றமும் இல்லாமல் மற்றும் பொருளின் வேதியியல் தன்மையில் எந்த மாற்றமும் இல்லாமல் நிகழ்கின்றன. பனி, நீர் மற்றும் நீராவி ஆகியவை அனைத்தும் வெவ்வேறு விதமாகத் தோன்றினாலும் மற்றும் வெவ்வேறு இயற்பியல் பண்புகளைக் காட்டினாலும், அவை வேதியியல் ரீதியாக ஒரே மாதிரியானவை.
நீர் மற்றும் சமையல் எண்ணெய் இரண்டும் திரவமாக இருந்தாலும் அவற்றின் வேதியியல் பண்புகள் வேறுபட்டவை. அவை மணம் மற்றும் எளிதில் தீப்பற்றும் தன்மையில் வேறுபடுகின்றன. எண்ணெய் காற்றில் எரியும், ஆனால் நீர் தீயை அணைக்கும் என்பது நமக்குத் தெரியும். எண்ணெயை நீரிலிருந்து வேறுபடுத்துவது இந்த வேதியியல் பண்புதான். எரிதல் என்பது ஒரு வேதியியல் மாற்றமாகும். இந்த செயல்பாட்டின் போது ஒரு பொருள் வேறொரு பொருளுடன் வினைபுரிந்து வேதியியல் கலவையில் ம











