باب 04 کاربن اور اس کے مرکبات
گزشتہ باب میں، ہم اپنے لیے اہمیت رکھنے والے بہت سے مرکبات سے واقف ہوئے۔ اس باب میں ہم کچھ اور دلچسپ مرکبات اور ان کے خواص کا مطالعہ کریں گے۔ نیز، ہم کاربن کے بارے میں سیکھیں گے، ایک ایسا عنصر جو اپنی عنصری شکل اور مرکب شکل دونوں میں ہمارے لیے بہت زیادہ اہمیت رکھتا ہے۔
سرگرمی 4.1
- صبح سے اب تک آپ نے جو دس چیزیں استعمال کی ہیں یا جن کا استعمال کیا ہے ان کی فہرست بنائیں۔
- اس فہرست کو اپنے ہم جماعتوں کی بنائی ہوئی فہرستوں کے ساتھ مرتب کریں اور پھر اشیاء کو متصل جدول میں ترتیب دیں۔
- اگر ایسی اشیاء ہیں جو ایک سے زیادہ مواد سے بنی ہیں، تو انہیں جدول کے دونوں متعلقہ کالموں میں رکھیں۔
| دھات سے بنی چیزیں | دھات سے بنی چیزیں | دیگر |
|---|---|---|
اس جدول کے آخری کالم میں آنے والی اشیاء کو دیکھیں جو آپ نے بھری ہیں - آپ کے استاد آپ کو بتا سکیں گے کہ ان میں سے زیادہ تر کاربن کے مرکبات سے بنی ہیں۔ کیا آپ اس کی جانچ کے لیے کوئی طریقہ سوچ سکتے ہیں؟ اگر کاربن پر مشتمل کوئی مرکب جلایا جائے تو کیا مصنوعہ ہوگا؟ کیا آپ اس کی تصدیق کے لیے کوئی ٹیسٹ جانتے ہیں؟
خوراک، کپڑے، ادویات، کتابیں، یا بہت سی چیزیں جو آپ نے فہرست میں شامل کی ہیں وہ سب اس کثیر الاستعمال عنصر کاربن پر مبنی ہیں۔ اس کے علاوہ، تمام جاندار ڈھانچے کاربن پر مبنی ہیں۔ زمین کی پرت اور فضا میں موجود کاربن کی مقدار بہت کم ہے۔ زمین کی پرت میں صرف $0.02 %$ کاربن معدنیات (جیسے کاربونیٹس، ہائیڈروجن کاربونیٹس، کوئلہ اور پٹرولیم) کی شکل میں ہے اور فضا میں کاربن ڈائی آکسائیڈ کی مقدار $0.03 %$ ہے۔ فطرت میں دستیاب کاربن کی اس کم مقدار کے باوجود، کاربن کی اہمیت بہت زیادہ معلوم ہوتی ہے۔ اس باب میں، ہم کاربن کے ان خواص کے بارے میں جانیں گے جو کاربن کو ہمارے لیے اتنا اہم بناتے ہیں۔
4.1 کاربن میں بانڈنگ - کوویلنٹ بانڈ
گزشتہ باب میں، ہم نے آئونک مرکبات کے خواص کا مطالعہ کیا تھا۔ ہم نے دیکھا کہ آئونک مرکبات کے پگھلنے اور ابلنے کے اعلی درجہ حرارت ہوتے ہیں اور محلول یا پگھلی ہوئی حالت میں بجلی کی موصل ہوتے ہیں۔ ہم نے یہ بھی دیکھا کہ آئونک مرکبات میں بانڈنگ کی نوعیت ان خواص کی وضاحت کیسے کرتی ہے۔ آئیے اب کچھ کاربن مرکبات کے خواص کا مطالعہ کریں۔
زیادہ تر کاربن مرکبات بجلی کے کم موصل ہوتے ہیں جیسا کہ ہم نے باب 2 میں دیکھا تھا۔ کاربن مرکبات کے ابلتے اور پگھلتے درجہ حرارت کے بارے میں جدول 4.1 میں دیے گئے اعداد و شمار سے، ہم دیکھتے ہیں کہ ان مرکبات کے پگھلنے اور ابلنے کے درجہ حرارت آئونک مرکبات (باب 3) کے مقابلے میں کم ہوتے ہیں۔ ہم یہ نتیجہ اخذ کر سکتے ہیں کہ ان مالیکیولز کے درمیان کشش کی قوتیں بہت مضبوط نہیں ہیں۔ چونکہ یہ مرکبات بڑی حد تک بجلی کے غیر موصل ہیں، ہم یہ نتیجہ اخذ کر سکتے ہیں کہ ان مرکبات میں بانڈنگ سے کوئی آئن پیدا نہیں ہوتے۔
جدول 4.1 کاربن کے کچھ مرکبات کے پگھلنے اور ابلنے کے درجہ حرارت
| مرکب | پگھلنے کا درجہ حرارت $(\mathbf{K})$ | ابلنے کا درجہ حرارت $(\mathbf{K})$ |
|---|---|---|
| ایسیٹک ایسڈ $(CH_3 COOH)$ | 290 | 391 |
| کلوروفارم $(CHCl_3)$ | 209 | 334 |
| ایتھانول $(CH_3 CH_2 OH)$ | 156 | 351 |
| میتھین $(CH_4)$ | 90 | 111 |
کلاس نہم میں، ہم نے مختلف عناصر کی ملانے کی صلاحیت اور یہ کہ یہ کیسے ظرفی الیکٹرانز کی تعداد پر منحصر ہے، کے بارے میں سیکھا تھا۔ آئیے اب کاربن کی الیکٹرانک ترتیب کو دیکھتے ہیں۔ کاربن کا ایٹمی نمبر 6 ہے۔ کاربن کے مختلف شیلز میں الیکٹرانز کی تقسیم کیا ہوگی؟ کاربن کے کتنے ظرفی الیکٹران ہوں گے؟
ہم جانتے ہیں کہ عناصر کی فعالیت کو ان کی بیرونی شیل کو مکمل طور پر بھرنے، یعنی عالی گیس کی ترتیب حاصل کرنے کی خواہش کے طور پر بیان کیا جاتا ہے۔ آئونک مرکبات بنانے والے عناصر بیرونی شیل سے الیکٹرانز حاصل کرکے یا کھو کر یہ حاصل کرتے ہیں۔ کاربن کے معاملے میں، اس کی بیرونی شیل میں چار الیکٹران ہیں اور اسے عالی گیس کی ترتیب حاصل کرنے کے لیے چار الیکٹران حاصل کرنے یا کھونے کی ضرورت ہے۔ اگر یہ الیکٹران حاصل کرے یا کھوئے -
(i) یہ چار الیکٹران حاصل کرکے $C^{4-}$ اینائن بنا سکتا ہے۔ لیکن چھ پروٹون والے مرکزے کے لیے دس الیکٹرانز، یعنی چار اضافی الیکٹرانز کو تھامنا مشکل ہوگا۔
(ii) یہ چار الیکٹران کھو کر $C^{4+}$ کیٹائن بنا سکتا ہے۔ لیکن چار الیکٹرانز کو ہٹانے کے لیے بڑی مقدار میں توانائی درکار ہوگی جس سے صرف دو الیکٹرانز کو تھامے ہوئے چھ پروٹون والا کاربن کیٹائن پیچھے رہ جائے گا۔
کاربن اس مسئلے پر قابو پاتا ہے اپنے ظرفی الیکٹرانز کو کاربن کے دوسرے ایٹموں یا دیگر عناصر کے ایٹموں کے ساتھ بانٹ کر۔ صرف کاربن ہی نہیں، بلکہ بہت سے دیگر عناصر بھی الیکٹرانز کو اس طرح بانٹ کر مالیکیول بناتے ہیں۔ بانٹے گئے الیکٹران دونوں ایٹموں کی بیرونی ترین شیلوں سے ‘تعلق’ رکھتے ہیں اور دونوں ایٹموں کو عالی گیس کی ترتیب حاصل کرنے کا باعث بنتے ہیں۔ کاربن کے مرکبات پر جانے سے پہلے، آئیے ظرفی الیکٹرانز کے بانٹنے سے بننے والے کچھ سادہ مالیکیولز کو دیکھتے ہیں۔
اس طرح بننے والا سب سے سادہ مالیکیول ہائیڈروجن کا ہے۔ جیسا کہ آپ نے پہلے سیکھا، ہائیڈروجن کا ایٹمی نمبر 1 ہے۔ لہٰذا ہائیڈروجن کے پاس اس کی $K$ شیل میں ایک الیکٹران ہے اور اسے $K$ شیل کو بھرنے کے لیے ایک اور الیکٹران کی ضرورت ہے۔ لہٰذا دو ہائیڈروجن ایٹم اپنے الیکٹرانز بانٹ کر ہائیڈروجن کا مالیکیول، $H_2$ بناتے ہیں۔ یہ ہر ہائیڈروجن ایٹم کو قریبی عالی گیس، ہیلیم، کی الیکٹرانک ترتیب حاصل کرنے دیتا ہے، جس کی K شیل میں دو الیکٹران ہیں۔ ہم اسے ظرفی الیکٹرانز کی نمائندگی کرنے کے لیے نقطوں یا کراسز کا استعمال کرتے ہوئے دکھا سکتے ہیں (شکل 4.1)۔
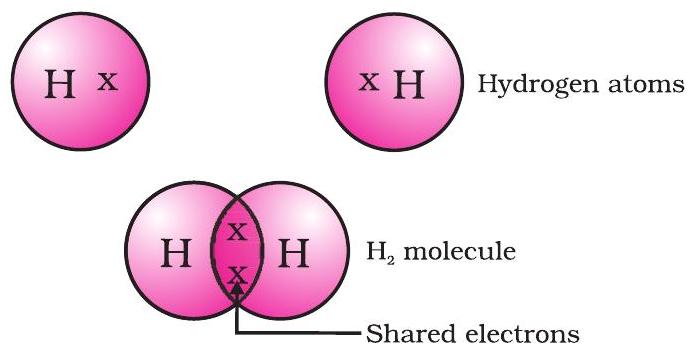
شکل 4.1 ہائیڈروجن کا ایک مالیکیول
الیکٹرانز کے بانٹے گئے جوڑے کو دو ہائیڈروجن ایٹموں کے درمیان ایک سنگل کوویلنٹ بانڈ قائم کرنے والا کہا جاتا ہے۔ ایک سنگل کوویلنٹ بانڈ کو دو ایٹموں کے درمیان ایک لکیر سے بھی ظاہر کیا جاتا ہے، جیسا کہ شکل 4.2 میں دکھایا گیا ہے۔
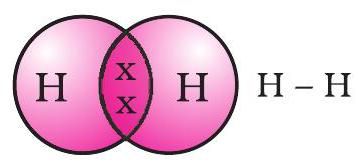
شکل 4.2 دو ہائیڈروجن ایٹموں کے درمیان سنگل بانڈ
کلورین کا ایٹمی نمبر 17 ہے۔ اس کی الیکٹرانک ترتیب اور اس کی ظرفیت کیا ہوگی؟ کلورین ایک دو ایٹمی مالیکیول، $Cl_2$ بناتی ہے۔ کیا آپ اس مالیکیول کے لیے الیکٹران ڈاٹ ڈھانچہ بنا سکتے ہیں؟ نوٹ کریں کہ صرف ظرفی شیل کے الیکٹرانز کو دکھانے کی ضرورت ہے۔
آکسیجن کے معاملے میں، ہم دو آکسیجن ایٹموں کے درمیان ڈبل بانڈ کی تشکیل دیکھتے ہیں۔ یہ اس لیے ہے کہ آکسیجن کے ایک ایٹم کی L شیل میں چھ الیکٹران ہوتے ہیں (آکسیجن کا ایٹمی نمبر آٹھ ہے) اور اسے اپنا آکٹیٹ مکمل کرنے کے لیے دو مزید الیکٹرانز کی ضرورت ہوتی ہے۔ لہٰذا آکسیجن کا ہر ایٹم دو الیکٹران دوسرے آکسیجن ایٹم کے ساتھ بانٹتا ہے تاکہ ہمیں شکل 4.3 میں دکھایا گیا ڈھانچہ ملے۔ ہر آکسیجن ایٹم کے ذریعے دیے گئے دو الیکٹران الیکٹرانز کے دو بانٹے گئے جوڑے پیدا کرتے ہیں۔ کہا جاتا ہے کہ یہ دو ایٹموں کے درمیان ایک ڈبل بانڈ قائم کرتا ہے۔
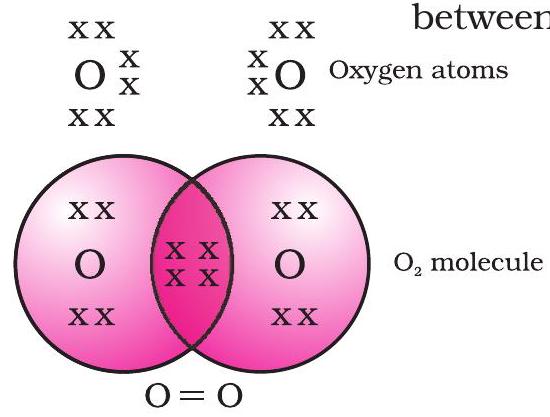
شکل 4.3 دو آکسیجن ایٹموں کے درمیان ڈبل بانڈ
کیا آپ اب پانی کا ایک مالیکیول اس طرح دکھا سکتے ہیں جو ایک آکسیجن ایٹم اور دو ہائیڈروجن ایٹموں کے درمیان بانڈنگ کی نوعیت ظاہر کرے؟ کیا مالیکیول میں سنگل بانڈ ہیں یا ڈبل بانڈ؟
نائٹروجن کے دو ایٹمی مالیکیول کے معاملے میں کیا ہوگا؟ نائٹروجن کا ایٹمی نمبر 7 ہے۔ اس کی الیکٹرانک ترتیب اور اس کی ملانے کی صلاحیت کیا ہوگی؟ آکٹیٹ حاصل کرنے کے لیے، نائٹروجن کے مالیکیول میں ہر نائٹروجن ایٹم تین الیکٹران فراہم کرتا ہے جس سے الیکٹرانز کے تین بانٹے گئے جوڑے بنتے ہیں۔ کہا جاتا ہے کہ یہ دو ایٹموں کے درمیان ایک ٹرپل بانڈ قائم کرتا ہے۔ شکل 4.3 $N_2$ اور دو آکسیجن ایٹموں کے درمیان ڈبل بانڈ کے الیکٹران ڈاٹ ڈھانچے کو شکل 4.4 میں دکھایا گیا ہے۔
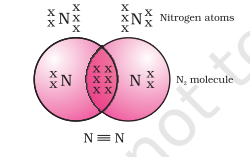
شکل 4.4 دو نائٹروجن ایٹموں کے درمیان ٹرپل بانڈ
ایمونیا کے مالیکیول کا فارمولا $NH_3$ ہے۔ کیا آپ اس مالیکیول کے لیے الیکٹران ڈاٹ ڈھانچہ بنا سکتے ہیں جو دکھائے کہ کیسے تمام چار ایٹم عالی گیس کی ترتیب حاصل کرتے ہیں؟ کیا مالیکیول میں سنگل، ڈبل یا ٹرپل بانڈ ہوں گے؟
آئیے اب میتھین کو دیکھتے ہیں، جو کاربن کا ایک مرکب ہے۔ میتھین بطور ایندھن وسیع پیمانے پر استعمال ہوتی ہے اور بائیو گیس اور کمپریسڈ نیچرل گیس (CNG) کا ایک اہم جزو ہے۔ یہ کاربن کے ذریعے بننے والے سب سے سادہ مرکبات میں سے ایک بھی ہے۔ میتھین کا فارمولا $CH_4$ ہے۔ ہائیڈروجن، جیسا کہ آپ جانتے ہیں، کی ظرفیت 1 ہے۔ کاربن ٹیٹراویلنٹ ہے کیونکہ اس کے چار ظرفی الیکٹران ہیں۔ عالی گیس کی ترتیب حاصل کرنے کے لیے، کاربن ان الیکٹرانز کو ہائیڈروجن کے چار ایٹموں کے ساتھ بانٹتا ہے جیسا کہ شکل 4.5 میں دکھایا گیا ہے۔
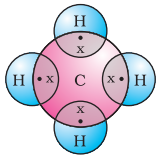
شکل 4.5 میتھین کے لیے الیکٹران ڈاٹ ڈھانچہ
ایسے بانڈ جو دو ایٹموں کے درمیان الیکٹران کے ایک جوڑے کے بانٹنے سے بنتے ہیں، کوویلنٹ بانڈز کہلاتے ہیں۔ کوویلنٹی طور پر بندھے ہوئے مالیکیولز میں مالیکیول کے اندر مضبوط بانڈ دیکھے جاتے ہیں، لیکن انٹرمالیکیولر قوتیں کمزور ہوتی ہیں۔ یہ ان مرکبات کے کم پگھلنے اور ابلنے کے درجہ حرارت کا باعث بنتا ہے۔ چونکہ الیکٹرانز ایٹموں کے درمیان بانٹے جاتے ہیں اور کوئی چارجڈ ذرات نہیں بنتے، اس لیے ایسے کوویلنٹ مرکبات عام طور پر بجلی کے کم موصل ہوتے ہیں۔
مزید جاننے کے لیے!
کاربن کے ایلوٹروپس
عنصر کاربن فطرت میں مختلف شکلوں میں پایا جاتا ہے جن کے طبعی خواص بہت مختلف ہوتے ہیں۔ ہیرا اور گرافائٹ دونوں کاربن ایٹموں سے بنتے ہیں، فرق اس طریقے میں ہے جس میں کاربن کے ایٹم ایک دوسرے سے بندھے ہوتے ہیں۔ ہیرے میں، ہر کاربن ایٹم چار دیگر کاربن ایٹموں سے جڑا ہوتا ہے جس سے ایک سخت تین جہتی ڈھانچہ بنتا ہے۔ گرافائٹ میں، ہر کاربن ایٹم ایک ہی سطح میں تین دیگر کاربن ایٹموں سے جڑا ہوتا ہے جس سے ایک مسدسی ترتیب بنتی ہے۔ ان میں سے ایک بانڈ ڈبل بانڈ ہوتا ہے، اور اس طرح کاربن کی ظرفیت پوری ہو جاتی ہے۔ گرافائٹ کا ڈھانچہ مسدسی ترتیبوں کو ایک دوسرے کے اوپر تہوں میں رکھنے سے بنتا ہے۔
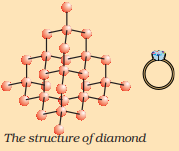
ہیرے کا ڈھانچہ
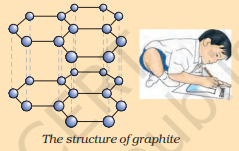
گرافائٹ کا ڈھانچہ
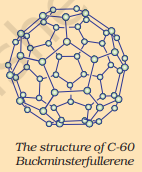
C-60 بکمنسٹرفلرین کا ڈھانچہ
یہ دو مختلف ڈھانچے ہیرے اور گرافائٹ کے بہت مختلف طبعی خواص رکھنے کا باعث بنتے ہیں حالانکہ ان کے کیمیائی خواص ایک جیسے ہیں۔ ہیرا جانا جانے والا سب سے سخت مادہ ہے جبکہ گرافائٹ ہموار اور پھسلن والا ہوتا ہے۔ گرافائٹ بجلی کا بہت اچھا موصل بھی ہے، گزشتہ باب میں آپ نے پڑھے ہوئے دیگر غیر دھاتوں کے برعکس۔
ہیرے خالص کاربن کو بہت زیادہ دباؤ اور درجہ حرارت کے تابع کرکے ترکیب کیے جا سکتے ہیں۔ یہ مصنوعی ہیرے چھوٹے ہوتے ہیں لیکن دوسرے پہلوؤں سے قدرتی ہیروں سے ممتاز نہیں ہوتے۔
فلرینز کاربن کے ایلوٹروپس کی ایک اور قسم بناتے ہیں۔ پہلا شناخت شدہ C-60 تھا جس میں کاربن کے ایٹم فٹ بال کی شکل میں ترتیب پائے ہوتے ہیں۔ چونکہ یہ امریکی معمار بکمنسٹر فلر کے ڈیزائن کردہ جیوڈیسک گنبد جیسا لگتا تھا، اس لیے مالیکیول کا نام فلرین رکھا گیا۔
4.2 کاربن کی کثیر الاستعمال فطرت
ہم نے مختلف عناصر اور مرکبات میں الیکٹرانز کے بانٹنے سے کوویلنٹ بانڈز کی تشکیل دیکھی ہے۔ ہم نے کاربن کے ایک سادہ مرکب، میتھین کا ڈھانچہ بھی دیکھا ہے۔ باب کے آغاز میں، ہم نے دیکھا کہ ہم جو بہت سی چیزیں استعمال کرتے ہیں ان میں کاربن کیسے شامل ہوتا ہے۔ درحقیقت، ہم خود کاربن مرکبات سے بنے ہیں۔ کاربن مرکبات کی تعداد جن کے فارمولے کیمیا دانوں کو معلوم ہیں، حال ہی میں لاکھوں میں تخمینہ لگایا گیا تھا! یہ تمام دیگر عناصر کے مل کر بننے والے مرکبات سے بہت زیادہ تعداد میں ہے۔ یہ خاصیت کاربن میں کیوں دیکھی جاتی ہے اور کسی دوسرے عنصر میں نہیں؟ کوویلنٹ بانڈ کی نوعیت کاربن کو بڑی تعداد میں مرکبات بنانے کے قابل بناتی ہے۔ کاربن کے معاملے میں نوٹ کیے گئے دو عوامل ہیں -
(i) کاربن میں دوسرے کاربن ایٹموں کے ساتھ بانڈ بنانے کی منفرد صلاحیت ہے، جس سے بڑے مالیکیول بنتے ہیں۔ اس خاصیت کو کیٹینیشن کہتے ہیں۔ ان مرکبات میں کاربن کی لمبی زنجیریں، شاخ دار کاربن زنجیریں یا یہاں تک کہ حلقوں میں ترتیب پائے ہوئے کاربن ایٹم ہو سکتے ہیں۔ اس کے علاوہ، کاربن ایٹم سنگل، ڈبل یا ٹرپل بانڈز سے جڑ سکتے ہیں۔ کاربن کے وہ مرکبات، جن میں کاربن ایٹموں کے درمیان صرف سنگل بانڈ ہوتے ہیں، سیچوریٹڈ مرکبات کہلاتے ہیں۔ کاربن کے وہ مرکبات جن میں ان کے کاربن ایٹموں کے درمیان ڈبل یا ٹرپل بانڈ ہوتے ہیں، انسیچوریٹڈ مرکبات کہلاتے ہیں۔
کوئی دوسرا عنصر کاربن مرکبات میں دیکھی جانے والی حد تک کیٹینیشن کی خاصیت نہیں دکھاتا۔ سلیکان ہائیڈروجن کے ساتھ ایسے مرکبات بناتا ہے جن میں سات یا آٹھ ایٹموں تک کی زنجیریں ہوتی ہیں، لیکن یہ مرکبات بہت فعال ہوتے ہیں۔ کاربن-کاربن بانڈ بہت مضبوط اور اس لیے مستحکم ہوتا ہے۔ یہ ہمیں بہت سے کاربن ایٹموں کے ایک دوسرے سے جڑے ہونے والے مرکبات کی بڑی تعداد دیتا ہے۔
(ii) چونکہ کاربن کی ظرفیت چار ہے، یہ کاربن کے چار دیگر ایٹموں یا کسی دوسرے مونوویلنٹ عنصر کے ایٹموں کے ساتھ بانڈ بنانے کے قابل ہے۔ کاربن کے مرکبات آکسیجن، ہائیڈروجن، نائٹروجن، سلفر، کلورین اور بہت سے دیگر عناصر کے ساتھ بنتے ہیں جس سے مخصوص خواص والے مرکبات بنتے ہیں جو مالیکیول میں موجود کاربن کے علاوہ دیگر عناصر پر منحصر ہوتے ہیں۔
ایک بار پھر، کاربن کے زیادہ تر دیگر عناصر کے ساتھ بننے والے بانڈ بہت مضبوط ہوتے ہیں جو ان مرکبات کو غیر معمولی طور پر مستحکم بناتے ہیں۔ کاربن کے ذریعے مضبوط بانڈ بننے کی ایک وجہ اس کا چھوٹا سائز ہے۔ یہ مرکزے کو بانٹے گئے الیکٹرانز کے جوڑوں کو مضبوطی سے تھامنے کے قابل بناتا ہے۔ بڑے ایٹموں والے عناصر کے ذریعے بننے والے بانڈ بہت کمزور ہوتے ہیں۔
کیا آپ جانتے ہیں؟
نامیاتی مرکبات
کاربن میں دیکھی جانے والی دو خصوصیات، یعنی ٹیٹراویلنسی اور کیٹینیشن، مل کر بڑی تعداد میں مرکبات پیدا کرتی ہیں۔ بہت سے میں وہی غیر کاربن ایٹم یا ایٹموں کا گروپ مختلف کاربن زنجیروں سے جڑا ہوتا ہے۔ یہ مرکبات ابتدائی طور پر قدرتی مادوں سے نکالے گئے تھے اور یہ خیال کیا جاتا تھا کہ یہ کاربن مرکبات یا نامیاتی مرکبات صرف کسی جاندار نظام کے اندر ہی بن سکتے ہیں۔ یعنی، یہ مفروضہ قائم کیا گیا تھا کہ ان کی ترکیب کے لیے ایک ‘حیاتیاتی قوت’ ضروری ہے۔ فریڈرک وولر نے 1828 میں ایمونیم سائنیٹ سے یوریا تیار کرکے اسے غلط ثابت کیا۔ لیکن کاربن مرکبات، سوائے کاربائیڈز، کاربن کے آکسائیڈز، کاربونیٹ اور ہائیڈروجن کاربونیٹ نمکیات کے، نامیاتی کیمیا کے تحت مطالعہ کیے جاتے رہتے ہیں۔
4.2.1 سیچوریٹڈ اور انسیچوریٹڈ کاربن مرکبات
ہم پہلے ہی میتھین کا ڈھانچہ دیکھ چکے ہیں۔ کاربن اور ہائیڈروجن کے درمیان بننے والا ایک اور مرکب ایتھین ہے جس کا فارمولا $C_2 H_6$ ہے۔ سادہ کاربن مرکبات کے ڈھانچے تک پہنچنے کے لیے، پہلا قدم کاربن ایٹموں کو ایک سنگل بانڈ کے ساتھ جوڑنا ہے (شکل 4.6a) اور پھر کاربن کی باقی ظرفیتوں کو پورا کرنے کے لیے ہائیڈروجن ایٹموں کا استعمال کرنا ہے (شکل 4.6b)۔ مثال کے طور پر، ایتھین کا ڈھانچہ درج ذیل مراحل سے حاصل ہوتا ہے -
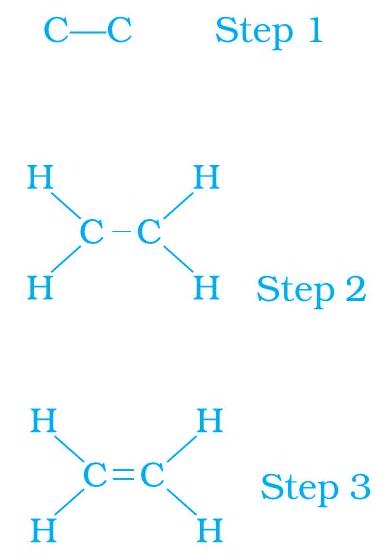
$ C-C \qquad $ مرحلہ 1
شکل 4.6 (a) سنگل بانڈ کے ساتھ جڑے ہوئے کاربن ایٹم
ہر کاربن ایٹم کی تین ظرفیتیں غیر مطمئن رہ جاتی ہیں، لہٰذا ہر ایک تین ہائیڈروجن ایٹموں سے جڑا ہوتا ہے جس سے ملتا ہے:
$H-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}}-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}} - H \qquad $ مرحلہ 2
شکل 4.6 (b) ہر کاربن ایٹم تین ہائیڈروجن ایٹموں سے جڑا ہوا
ایتھین کا الیکٹران ڈاٹ ڈھانچہ شکل 4.6(c) میں دکھایا گیا ہے۔
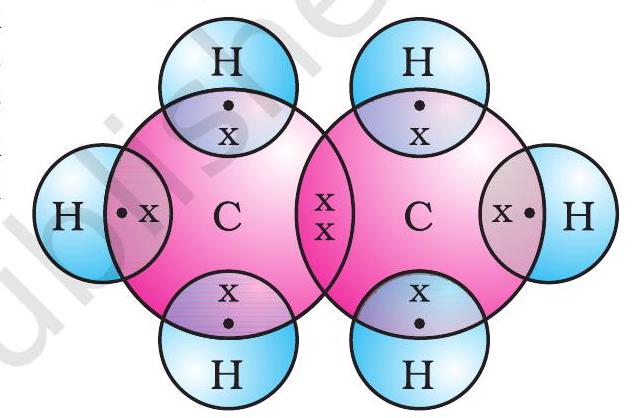
شکل 4.6 (c) ایتھین کا الیکٹران ڈاٹ ڈھانچہ
کیا آپ پروپین کا ڈھانچہ بنا سکتے ہیں، جس کا سالماتی فارمولا $C_3 H_8$ ہے، اسی طرح سے؟ آپ دیکھیں گے کہ تمام ایٹموں کی ظرفیتیں ان کے درمیان سنگل بانڈز سے پوری ہو جاتی ہیں۔ ایسے کاربن مرکبات کو سیچوریٹڈ مرکبات کہتے ہیں۔ یہ مرکبات عام طور پر بہت فعال نہیں ہوتے۔
تاہم، کاربن اور ہائیڈروجن کا ایک اور مرکب فارمولا $C_2 H_4$ رکھتا ہے اور اسے ایتھین کہتے ہیں۔ اس مالیکیول کو کیسے دکھایا جا سکتا ہے؟ ہم اوپر والے جیسے ہی مرحلہ وار نقطہ نظر پر عمل کرتے ہیں۔
کاربن-کاربن ایٹم سنگل بانڈ کے ساتھ جڑے ہوئے (مرحلہ 1)۔
ہم دیکھتے ہیں کہ کاربن ایٹم فی ایٹم ایک ظرفیت غیر مطمئن رہ جاتی ہے (مرحلہ 2)۔ یہ صرف اس صورت میں پوری ہو سکتی ہے اگر دو کاربنوں کے درمیان ڈبل بانڈ ہو (مرحلہ 3)۔
ایتھین کے لیے الیکٹران ڈاٹ ڈھانچہ شکل 4.7 میں دیا گیا ہے۔
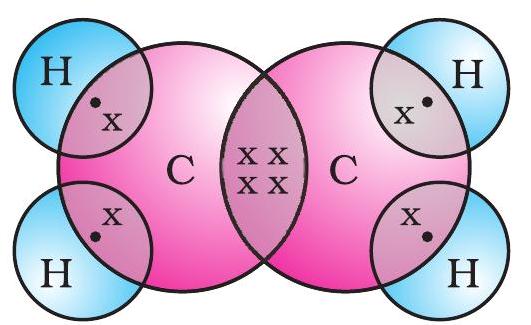
شکل 4.7 ایتھین کا ڈھانچہ
ہائیڈروجن اور کاربن کا ایک اور مرکب فارمولا $C_2 H_2$ رکھتا ہے اور اسے ایتھائن کہتے ہیں۔ کیا آپ ایتھائن کے لیے الیکٹران ڈاٹ ڈھانچہ بنا سکتے ہیں؟ دو کاربن ایٹموں کے درمیان ان کی ظرفیتوں کو پورا کرنے کے لیے کتنے بانڈ ضروری ہیں؟ کاربن کے ایسے مرکبات جن میں کاربن ایٹموں کے درمیان ڈبل یا ٹرپل بانڈ ہوتے ہیں، انسیچوریٹڈ کاربن مرکبات کہلاتے ہیں اور یہ سیچوریٹڈ کاربن مرکبات سے زیادہ فعال ہوتے ہیں۔
4.2.2 زنجیریں، شاخیں اور حلقے
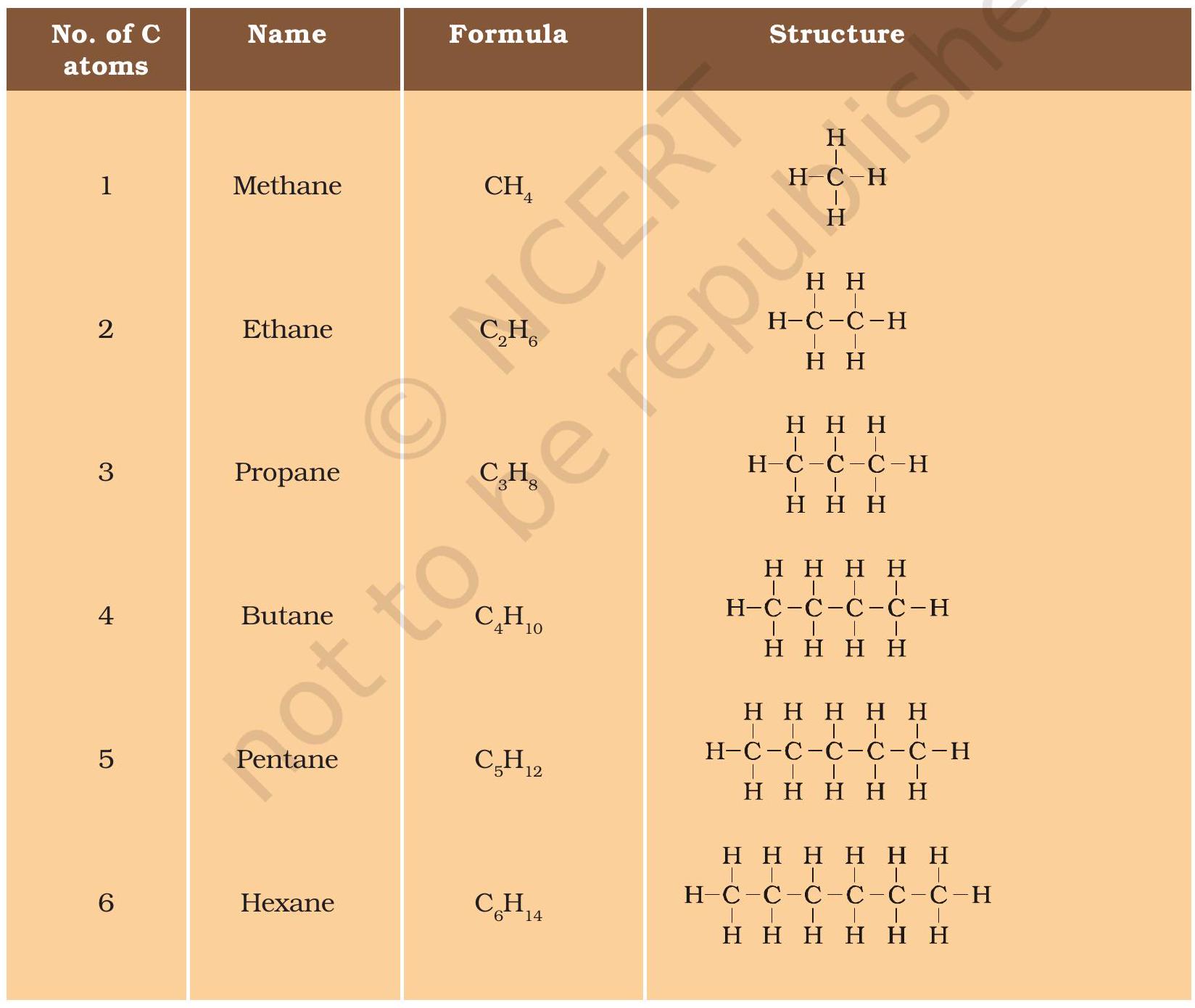
پچھلے حصے میں، ہم نے کاربن مرکبات میتھین، ایتھین اور پروپین کا ذکر کیا تھا، جن میں بالترتیب 1،2 اور 3 کاربن ایٹم ہوتے ہیں۔ کاربن ایٹموں کی ایسی ‘زنجیریں’ بہت سے مزید کاربن ایٹم رکھ سکتی ہیں۔ ان میں سے چھ کے نام اور ڈھانچے جدول 4.2 میں دیے گئے ہیں۔
جدول 4.2 کاربن اور ہائیڈروجن کے سیچوریٹڈ مرکبات کے فارمولے اور ڈھانچے
لیکن، آئیے بیوٹین پر ایک اور نظر ڈالتے ہیں۔ اگر ہم چار کاربن ایٹموں والا کاربن ‘اسکیلیٹن’ بنائیں، تو ہم دیکھتے ہیں کہ دو مختلف ممکنہ ‘اسکیلیٹن’ ہیں -

شکل 4.8 (a) دو ممکنہ کاربن-اسکیلیٹن
باقی ظرفیتوں کو ہائیڈروجن سے بھرنے سے ہمیں ملتا ہے -
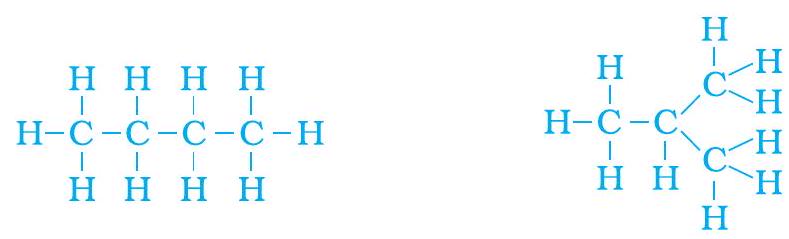
شکل 4.8 (b) فارمولا $C_4 H _{10}$ والے دو ڈھانچوں کے لیے مکمل مالیکیول
ہم دیکھتے ہیں کہ ان دونوں ڈھانچوں کا ایک ہی فارمولا $C_4 H _{10}$ ہے۔ ایک جیسے سالماتی فارمولا لیکن مختلف ڈھانچے رکھنے والے ایسے مرکبات کو ساختی اسومرز کہتے ہیں۔
سیدھی اور شاخ دار کاربن زنجیروں کے علاوہ، کچھ مرکبات میں کاربن ایٹم حلقے کی شکل میں ترتیب پائے ہوتے ہیں۔ مثال کے طور پر، سائیکلوہیکسین کا فارمولا $C_6 H _{12}$ ہے اور درج ذیل ڈھانچہ ہے -
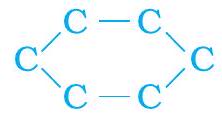
(a)
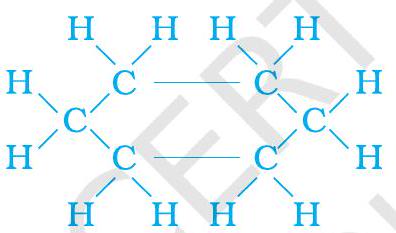
(b)
شکل 4.9 سائیکلوہیکسین کا ڈھانچہ (a) کاربن اسکیلیٹن (b) مکمل مالیکیول
کیا آپ سائیکلوہیکسین کے لیے الیکٹران ڈاٹ ڈھانچہ بنا سکتے ہیں؟ سیدھی زنجیر، شاخ دار زنجیر اور حلقوی کاربن مرکبات، سب سیچوریٹڈ یا انسیچوریٹڈ ہو سکتے ہیں۔ مثال کے طور پر، بینزین، $C_6 H_6$، کا درج ذیل ڈھانچہ ہے-
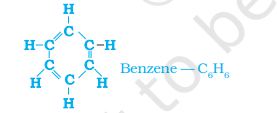
شکل 4.10 بینزین کا ڈھانچہ
یہ تمام کاربن مرکبات جو صرف کاربن اور ہائیڈروجن پر مشتمل ہوتے ہیں، ہائیڈروکاربنز کہلاتے ہیں۔ ان میں، سیچوریٹڈ ہائیڈروکاربنز کو











