प्रकरण ०४ कार्बन आणि त्याची संयुगे
मागील प्रकरणात, आपण आपल्यासाठी महत्त्वाची अनेक संयुगे जाणून घेतली. या प्रकरणात आपण आणखी काही मनोरंजक संयुगे व त्यांचे गुणधर्म यांचा अभ्यास करू. तसेच, आपण कार्बन या मूलद्रव्याबद्दल शिकू, जे मूलद्रव्य स्वरूपात व संयुगीत स्वरूपात दोन्ही प्रकारे आपल्यासाठी अतिशय महत्त्वाचे आहे.
कृती 4.1
- सकाळपासून तुम्ही वापरलेल्या किंवा ग्रहण केलेल्या दहा वस्तूंची यादी करा.
- ही यादी तुमच्या वर्गमित्रांनी बनवलेल्या याद्यांसह संकलित करा आणि नंतर वस्तूंचे समीप असलेल्या सारणीत वर्गीकरण करा.
- जर एकापेक्षा जास्त सामग्रीपासून बनलेल्या वस्तू असतील, तर त्या सारणीतील दोन्ही संबंधित स्तंभात ठेवा.
| धातूपासून बनलेल्या वस्तू | धातूपासून बनलेल्या वस्तू | इतर |
|---|---|---|
वरील सारणीच्या तुम्ही भरलेल्या शेवटच्या स्तंभात येणाऱ्या वस्तूंकडे पहा - तुमचे शिक्षक तुम्हाला सांगू शकतील की त्यापैकी बहुतेक कार्बनच्या संयुगांपासून बनलेल्या आहेत. हे तपासण्याची काही पद्धत तुम्हाला सुचते का? कार्बन असलेले संयुग जळवल्यास काय उत्पादन मिळेल? हे निश्चित करण्यासाठी तुम्हाला काही चाचणी माहिती आहे का?
अन्न, कपडे, औषधे, पुस्तके किंवा तुम्ही यादी केलेल्या अनेक वस्तू या सर्व या बहुमुखी मूलद्रव्य कार्बनवर आधारित आहेत. याव्यतिरिक्त, सर्व सजीव रचना कार्बनाधारित आहेत. पृथ्वीच्या कवचात आणि वातावरणात उपलब्ध कार्बनचे प्रमाण अगदी कमी आहे. पृथ्वीच्या कवचात फक्त $0.02 %$ कार्बन खनिजांच्या रूपात (जसे कार्बोनेट्स, हायड्रोजनकार्बोनेट्स, कोळसा आणि पेट्रोलियम) आहे आणि वातावरणात $0.03 %$ कार्बन डायऑक्साइड आहे. निसर्गात उपलब्ध कार्बनचे हे लहान प्रमाण असूनही, कार्बनचे महत्त्व प्रचंड वाटते. या प्रकरणात, आपण कार्बनचे असे कोणते गुणधर्म आहेत जे कार्बनला आपल्यासाठी इतके महत्त्वाचे बनवतात ते जाणून घेऊ.
4.1 कार्बनमधील बंध - सहसंयुज बंध
मागील प्रकरणात, आपण आयनिक संयुगांचे गुणधर्म अभ्यासले. आपण पाहिले की आयनिक संयुगांमध्ये उच्च द्रवणांक व उत्कलनांक असतात आणि ते द्रावणात किंवा द्रवित अवस्थेत विद्युत वाहक असतात. तसेच आयनिक संयुगांमधील बंधनाचे स्वरूप हे गुणधर्म कसे स्पष्ट करते ते आपण पाहिले. आता आपण काही कार्बन संयुगांचे गुणधर्म अभ्यासू.
बहुतेक कार्बन संयुगे विद्युतचे कमकुवत वाहक असतात, हे आपण प्रकरण 2 मध्ये पाहिले आहे. कार्बन संयुगांचे उत्कलनांक व द्रवणांक यांची माहिती सारणी 4.1 मध्ये दिली आहे, त्यावरून आपल्याला आढळते की या संयुगांचे द्रवणांक व उत्कलनांक आयनिक संयुगांच्या (प्रकरण 3) तुलनेत कमी असतात. आपण असा निष्कर्ष काढू शकतो की रेणूंमधील आकर्षण बल फार प्रबळ नसते. ही संयुगे मोठ्या प्रमाणात विद्युत अपवाहक असल्यामुळे, आपण असा निष्कर्ष काढू शकतो की या संयुगांमधील बंधनामुळे कोणतेही आयन तयार होत नाहीत.
सारणी 4.1 काही कार्बन संयुगांचे द्रवणांक व उत्कलनांक
| संयुग | द्रवणांक $(\mathbf{K})$ | उत्कलनांक $(\mathbf{K})$ |
|---|---|---|
| ऍसिटिक आम्ल $(CH_3 COOH)$ | 290 | 391 |
| क्लोरोफॉर्म $(CHCl_3)$ | 209 | 334 |
| इथेनॉल $(CH_3 CH_2 OH)$ | 156 | 351 |
| मिथेन $(CH_4)$ | 90 | 111 |
इयत्ता नववी मध्ये, आपण विविध मूलद्रव्यांची संयुजन क्षमता व ती संयुजा इलेक्ट्रॉनांच्या संख्येवर कशी अवलंबून असते हे शिकलो. आता कार्बनची इलेक्ट्रॉनी संरूपण पाहू. कार्बनचा अणुक्रमांक 6 आहे. कार्बनच्या विविध कवचांमध्ये इलेक्ट्रॉनचे वितरण कसे असेल? कार्बनला किती संयुजा इलेक्ट्रॉन असतील?
आपल्याला माहित आहे की मूलद्रव्यांची क्रियाशीलता ही त्यांच्या बाह्य कवच पूर्णपणे भरण्याची, म्हणजेच उदात्त वायूंचे संरूपण प्राप्त करण्याची प्रवृत्ती म्हणून स्पष्ट केली जाते. आयनिक संयुगे तयार करणारी मूलद्रव्ये हे सर्वात बाहेरील कवचातून इलेक्ट्रॉन मिळवून किंवा गमावून साध्य करतात. कार्बनच्या बाबतीत, त्याच्या सर्वात बाहेरील कवचात चार इलेक्ट्रॉन आहेत आणि उदात्त वायू संरूपण प्राप्त करण्यासाठी त्याला चार इलेक्ट्रॉन मिळवावे लागतील किंवा गमावावे लागतील. जर त्याने इलेक्ट्रॉन मिळवले किंवा गमावले तर -
(i) तो चार इलेक्ट्रॉन मिळवून $C^{4-}$ ऋण आयन तयार करू शकतो. परंतु सहा प्रोटॉन असलेल्या केंद्रकासाठी दहा इलेक्ट्रॉन, म्हणजेच चार अतिरिक्त इलेक्ट्रॉन धरून ठेवणे कठीण होईल.
(ii) तो चार इलेक्ट्रॉन गमावून $C^{4+}$ धन आयन तयार करू शकतो. परंतु चार इलेक्ट्रॉन काढून टाकण्यासाठी मोठ्या प्रमाणात ऊर्जेची आवश्यकता असेल, त्यामुळे फक्त दोन इलेक्ट्रॉन धरून ठेवणारा कार्बन धन आयन त्याच्या केंद्रकात सहा प्रोटॉनसह राहील.
कार्बन ही समस्या त्याचे संयुजा इलेक्ट्रॉन कार्बनच्या इतर अणूंसोबत किंवा इतर मूलद्रव्यांच्या अणूंसोबत सामायिक करून दूर करतो. फक्त कार्बनच नव्हे तर इतर अनेक मूलद्रव्येही या पद्धतीने इलेक्ट्रॉन सामायिक करून रेणू तयार करतात. सामायिक केलेले इलेक्ट्रॉन दोन्ही अणूंच्या सर्वात बाहेरील कवचांचे ‘मालक’ असतात आणि दोन्ही अणूंना उदात्त वायू संरूपण प्राप्त होण्यास कारणीभूत ठरतात. कार्बनच्या संयुगांकडे जाण्यापूर्वी, संयुजा इलेक्ट्रॉनच्या सामायिकरणाने तयार झालेल्या काही साध्या रेणूंकडे पाहू.
अशा प्रकारे तयार होणारा सर्वात सोपा रेणू म्हणजे हायड्रोजनचा. तुम्ही आधी शिकलात की, हायड्रोजनचा अणुक्रमांक 1 आहे. म्हणून हायड्रोजनच्या $K$ कवचात एक इलेक्ट्रॉन आहे आणि $K$ कवच भरण्यासाठी त्याला आणखी एक इलेक्ट्रॉन आवश्यक आहे. म्हणून दोन हायड्रोजन अणू त्यांचे इलेक्ट्रॉन सामायिक करून हायड्रोजनचा एक रेणू, $H_2$ तयार करतात. यामुळे प्रत्येक हायड्रोजन अणूला जवळच्या उदात्त वायू हेलियमचे इलेक्ट्रॉनी संरूपण प्राप्त होते, ज्याच्या K कवचात दोन इलेक्ट्रॉन असतात. आपण हे संयुजा इलेक्ट्रॉन दर्शवण्यासाठी टिंबे किंवा क्रॉस वापरून दर्शवू शकतो (आकृती 4.1).
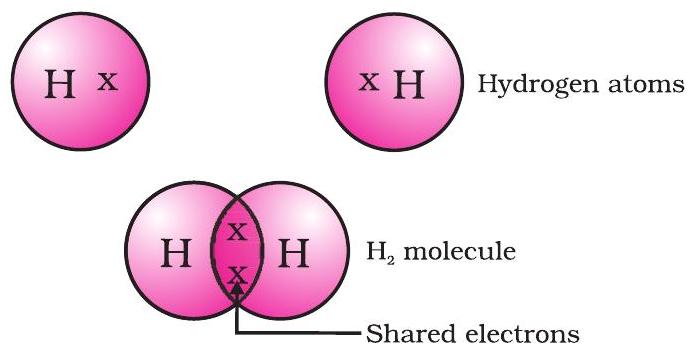
आकृती 4.1 हायड्रोजनचा एक रेणू
सामायिक केलेल्या इलेक्ट्रॉनच्या जोडीमुळे दोन हायड्रोजन अणूंदरम्यान एकल सहसंयुज बंध तयार होतो असे म्हटले जाते. एकल सहसंयुज बंध हा दोन अणूंदरम्यान एक रेषेद्वारे देखील दर्शविला जातो, जसे आकृती 4.2 मध्ये दाखवले आहे.
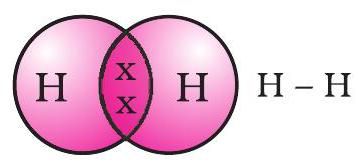
आकृती 4.2 दोन हायड्रोजन अणूंदरम्यान एकल बंध
क्लोरीनचा अणुक्रमांक 17 आहे. त्याचे इलेक्ट्रॉनी संरूपण व संयुजा क्षमता काय असेल? क्लोरीन एक द्विपरमाणुक रेणू $Cl_2$ तयार करते. तुम्ही या रेणूसाठी इलेक्ट्रॉन टिंब संरचना काढू शकता का? लक्षात ठेवा, फक्त संयुजा कवच इलेक्ट्रॉन दर्शविणे आवश्यक आहे.
ऑक्सिजनच्या बाबतीत, आपल्याला दोन ऑक्सिजन अणूंदरम्यान द्विबंध तयार होताना दिसतो. याचे कारण असे की ऑक्सिजनच्या अणूच्या L कवचात सहा इलेक्ट्रॉन असतात (ऑक्सिजनचा अणुक्रमांक आठ आहे) आणि त्याचा अष्टक पूर्ण करण्यासाठी त्याला आणखी दोन इलेक्ट्रॉन आवश्यक असतात. म्हणून प्रत्येक ऑक्सिजन अणू दुसऱ्या ऑक्सिजन अणूसोबत दोन इलेक्ट्रॉन सामायिक करतो आणि आकृती 4.3 मध्ये दाखवलेली संरचना देते. प्रत्येक ऑक्सिजन अणूने दिलेले दोन इलेक्ट्रॉन इलेक्ट्रॉनच्या दोन सामायिक जोड्या तयार करतात. असे म्हटले जाते की यामुळे दोन अणूंदरम्यान द्विबंध तयार होतो.
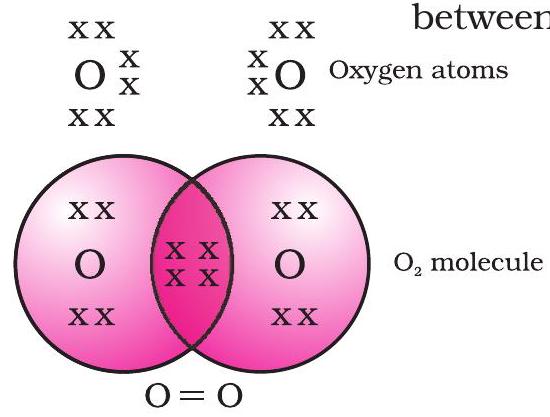
आकृती 4.3 दोन ऑक्सिजन अणूंदरम्यान द्विबंध
आता तुम्ही एका ऑक्सिजन अणू आणि दोन हायड्रोजन अणूंदरम्यान असलेल्या बंधनाचे स्वरूप दर्शवणारा पाण्याचा रेणू काढू शकता का? या रेणूमध्ये एकल बंध आहेत की द्विबंध आहेत?
नायट्रोजनच्या द्विपरमाणुक रेणूच्या बाबतीत काय होईल? नायट्रोजनचा अणुक्रमांक 7 आहे. त्याचे इलेक्ट्रॉनी संरूपण व संयुजन क्षमता काय असेल? अष्टक प्राप्त करण्यासाठी, नायट्रोजनच्या रेणूतील प्रत्येक नायट्रोजन अणू तीन इलेक्ट्रॉन देतो, ज्यामुळे इलेक्ट्रॉनच्या तीन सामायिक जोड्या तयार होतात. असे म्हटले जाते की यामुळे दोन अणूंदरम्यान त्रिबंध तयार होतो आकृती 4.3 दोन ऑक्सिजन अणूंदरम्यान द्विबंध $N_2$ ची इलेक्ट्रॉन टिंब संरचना आणि त्याचा त्रिबंध आकृती 4.4 प्रमाणे दर्शविला जाऊ शकतो.
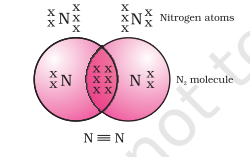
आकृती 4.4 दोन नायट्रोजन अणूंदरम्यान त्रिबंध
अमोनियाच्या रेणूचे सूत्र $NH_3$ आहे. तुम्ही हा रेणू दर्शविणारी इलेक्ट्रॉन टिंब संरचना काढू शकता का, ज्यामध्ये चारही अणूंना उदात्त वायू संरूपण कसे प्राप्त होते ते दाखवले आहे? या रेणूमध्ये एकल, द्विबंध किंवा त्रिबंध असतील का?
आता मिथेनकडे पाहू, जे कार्बनचे एक संयुग आहे. मिथेनचा इंधन म्हणून मोठ्या प्रमाणावर वापर केला जातो आणि ते बायोगॅस आणि कंप्रेस्ड नैसर्गिक वायू (CNG) चा एक प्रमुख घटक आहे. ते कार्बनाद्वारे तयार झालेल्या सर्वात सोप्या संयुगांपैकी एक देखील आहे. मिथेनचे सूत्र $CH_4$ आहे. तुम्हाला माहिती आहे की, हायड्रोजनची संयुजा 1 आहे. कार्बन चतुःसंयुजी आहे कारण त्याला चार संयुजा इलेक्ट्रॉन आहेत. उदात्त वायू संरूपण प्राप्त करण्यासाठी, कार्बन हे इलेक्ट्रॉन हायड्रोजनच्या चार अणूंसोबत सामायिक करतो जसे आकृती 4.5 मध्ये दाखवले आहे.
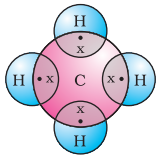
आकृती 4.5 मिथेनसाठी इलेक्ट्रॉन टिंब संरचना
असे बंध जे दोन अणूंदरम्यान इलेक्ट्रॉन जोडीच्या सामायिकरणाने तयार होतात त्यांना सहसंयुज बंध म्हणतात. सहसंयुज बंध असलेले रेणू रेणूमध्ये प्रबळ बंध असलेले दिसतात, परंतु आंतररेण्वीय बल कमकुवत असतात. यामुळे या संयुगांचे द्रवणांक व उत्कलनांक कमी असतात. इलेक्ट्रॉन अणूंदरम्यान सामायिक केले जातात आणि कोणतेही प्रभारित कण तयार होत नसल्यामुळे, अशी सहसंयुज संयुगे सामान्यतः विद्युतचे कमकुवत वाहक असतात.
अधिक जाणून घ्या!
कार्बनचे अपरूप
कार्बन मूलद्रव्य निसर्गात विविध स्वरूपात आढळते ज्यांचे भौतिक गुणधर्म मोठ्या प्रमाणात बदलतात. हिरा आणि ग्रॅफाइट दोन्ही कार्बन अणूंपासून तयार झालेले आहेत, फरक असा आहे की कार्बन अणू एकमेकांशी कशा प्रकारे बद्ध आहेत. हिर्यामध्ये, प्रत्येक कार्बन अणू इतर चार कार्बन अणूंशी बद्ध असतो ज्यामुळे कठोर त्रिमितीय रचना तयार होते. ग्रॅफाइटमध्ये, प्रत्येक कार्बन अणू समान समतलातील इतर तीन कार्बन अणूंशी बद्ध असतो ज्यामुळे षटकोनी रचना मिळते. यापैकी एक बंध द्विबंध असतो, आणि अशा प्रकारे कार्बनची संयुजा पूर्ण होते. ग्रॅफाइटची रचना षटकोनी रचना एकामागून एक स्तरांमध्ये ठेवल्यामुळे तयार होते.
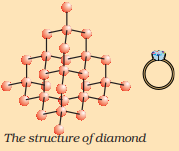
हिर्याची रचना
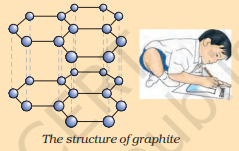
ग्रॅफाइटची रचना
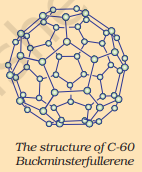
C-60 बकमिन्स्टरफुलरीनची रचना
ह्या दोन भिन्न रचनांमुळे हिरा आणि ग्रॅफाइट यांचे रासायनिक गुणधर्म सारखेच असूनही त्यांचे भौतिक गुणधर्म अगदी वेगळे असतात. हिरा हे ज्ञात सर्वात कठीण पदार्थ आहे तर ग्रॅफाइट गुळगुळीत आणि निसरडे असते. ग्रॅफाइट हा इतर अधातूंपेक्षा देखील विद्युतचा अतिशय चांगला वाहक आहे, जसे तुम्ही मागील प्रकरणात अभ्यासले.
शुद्ध कार्बनवर अतिशय उच्च दाब आणि तापमान लावून हिरे संश्लेषित केले जाऊ शकतात. हे कृत्रिम हिरे लहान असतात परंतु नैसर्गिक हिर्यांपेक्षा वेगळे ओळखता येत नाहीत.
फुलरीन्स कार्बनच्या अपरूपांची दुसरी श्रेणी तयार करतात. प्रथम ओळखले गेलेले C-60 होते ज्यात कार्बन अणू फुटबॉलच्या आकारात मांडलेले आहेत. हे यूएस आर्किटेक्ट बकमिन्स्टर फुलर यांनी डिझाइन केलेल्या जिओडेसिक घुमटासारखे दिसल्यामुळे, रेणूला फुलरीन असे नाव देण्यात आले.
4.2 कार्बनचे बहुमुखी स्वरूप
आपण विविध मूलद्रव्ये आणि संयुगांमध्ये इलेक्ट्रॉन सामायिक करून सहसंयुज बंध तयार होताना पाहिले आहेत. आपण एका साध्या कार्बन संयुग, मिथेनची रचना देखील पाहिली आहे. प्रकरणाच्या सुरुवातीला, आपण पाहिले की आपण वापरत असलेल्या अनेक गोष्टींमध्ये कार्बन असते. खरेतर, आपण स्वतः कार्बन संयुगांपासून बनलेले आहोत. रसायनशास्त्रज्ञांना ज्ञात असलेल्या कार्बन संयुगांची संख्या अलीकडेच दशलक्षांमध्ये असल्याचा अंदाज होता! ही संख्या इतर सर्व मूलद्रव्यांनी मिळून तयार केलेल्या संयुगांपेक्षा मोठ्या प्रमाणात जास्त आहे. हा गुणधर्म फक्त कार्बनमध्येच का आढळतो आणि इतर कोणत्याही मूलद्रव्यात का नाही? सहसंयुज बंधाचे स्वरूप कार्बनला मोठ्या संख्येने संयुगे तयार करण्यास सक्षम करते. कार्बनच्या बाबतीत लक्षात आलेले दोन घटक आहेत -
(i) कार्बनमध्ये इतर कार्बन अणूंसोबत बंध तयार करण्याची अनन्य क्षमता आहे, ज्यामुळे मोठे रेणू तयार होतात. या गुणधर्माला शृंखलन म्हणतात. या संयुगांमध्ये कार्बनच्या लांब शृंखला, कार्बनच्या शाखायुक्त शृंखला किंवा अगदी कार्बन अणूंची रिंगांमध्ये मांडणी असू शकते. याव्यतिरिक्त, कार्बन अणू एकल, द्विबंध किंवा त्रिबंधांनी जोडलेले असू शकतात. कार्बनची अशी संयुगे, ज्यात कार्बन अणूंदरम्यान फक्त एकल बंध असतात त्यांना संतृप्त संयुगे म्हणतात. कार्बनची अशी संयुगे, ज्यात त्यांच्या कार्बन अणूंदरम्यान द्विबंध किंवा त्रिबंध असतात त्यांना असंतृप्त संयुगे म्हणतात.
कार्बन संयुगांमध्ये दिसून येणाऱ्या प्रमाणात शृंखलनाचा गुणधर्म इतर कोणत्याही मूलद्रव्यात आढळत नाही. सिलिकॉन हायड्रोजनसह अशी संयुगे तयार करते ज्यात सात किंवा आठ अणूंपर्यंत शृंखला असतात, परंतु ही संयुगे अतिशय क्रियाशील असतात. कार्बन-कार्बन बंध अतिशय मजबूत आणि म्हणून स्थिर असतो. हे आपल्याला अनेक कार्बन अणू एकमेकांशी जोडलेली मोठ्या संख्येने संयुगे देते.
(ii) कार्बनची संयुजा चार असल्यामुळे, तो इतर चार कार्बन अणू किंवा काही इतर एकसंयुजी मूलद्रव्यांच्या अणूंशी बंध तयार करण्यास सक्षम आहे. कार्बनची संयुगे ऑक्सिजन, हायड्रोजन, नायट्रोजन, सल्फर, क्लोरीन आणि इतर अनेक मूलद्रव्यांसह तयार होतात, ज्यामुळे विशिष्ट गुणधर्म असलेली संयुगे मिळतात जी रेणूमध्ये उपस्थित कार्बन व्यतिरिक्त इतर मूलद्रव्यांवर अवलंबून असतात.
पुन्हा, कार्बन इतर बहुतेक मूलद्रव्यांसह तयार करतो ते बंध अतिशय मजबूत असतात ज्यामुळे ही संयुगे विशेषतः स्थिर होतात. कार्बनाद्वारे मजबूत बंध तयार होण्याचे एक कारण म्हणजे त्याचा लहान आकार. हे केंद्रकाला सामायिक केलेल्या इलेक्ट्रॉन जोड्या मजबूतपणे धरून ठेवण्यास सक्षम करते. मोठे अणू असलेल्या मूलद्रव्यांद्वारे तयार केलेले बंध खूपच कमकुवत असतात.
तुम्हाला माहिती आहे का?
कार्बनी संयुगे
कार्बनमध्ये दिसून येणारी दोन वैशिष्ट्यपूर्ण वैशिष्ट्ये, म्हणजे चतुःसंयुजता आणि शृंखलन, एकत्रितपणे मोठ्या संख्येने संयुगे निर्माण करतात. अनेकांमध्ये समान अकार्बन अणू किंवा अणूंचा समूह वेगवेगळ्या कार्बन शृंखलांशी जोडलेला असतो. ही संयुगे सुरुवातीला नैसर्गिक पदार्थांमधून काढली गेली होती आणि असे मानले जात होते की ही कार्बनसंयुगे किंवा कार्बनी संयुगे फक्त सजीव प्रणालीमध्येच तयार होऊ शकतात. म्हणजेच, त्यांच्या संश्लेषणासाठी ‘जीवनशक्ती’ आवश्यक आहे असे गृहीत धरले होते. फ्रेडरिक वोहलर यांनी 1828 मध्ये अमोनियम सायनेटमधून युरिया तयार करून हे खोटे ठरवले. परंतु कार्बन संयुगे, कार्बाइड्स, कार्बनचे ऑक्साइड, कार्बोनेट आणि हायड्रोजनकार्बोनेट क्षार यांव्यतिरिक्त, कार्बनी रसायनशास्त्र अंतर्गत अभ्यासली जात राहिली आहेत.
4.2.1 संतृप्त व असंतृप्त कार्बन संयुगे
आपण आधीच मिथेनची रचना पाहिली आहे. कार्बन आणि हायड्रोजन दरम्यान तयार होणारे आणखी एक संयुग म्हणजे इथेन ज्याचे सूत्र $C_2 H_6$ आहे. साध्या कार्बन संयुगांच्या रचनेवर पोहोचण्यासाठी, पहिली पायरी म्हणजे कार्बन अणू एकमेकांशी एकल बंधाने जोडणे (आकृती 4.6a) आणि नंतर कार्बनची उर्वरित संयुजा पूर्ण करण्यासाठी हायड्रोजन अणू वापरणे (आकृती 4.6b). उदाहरणार्थ, इथेनची रचना खालील पायऱ्यांनी मिळते -
$ C-C \qquad $ पायरी 1
आकृती 4.6 (a) एकल बंधाने एकत्र जोडलेले कार्बन अणू
प्रत्येक कार्बन अणूच्या तीन संयुजा अपूर्ण राहतात, म्हणून प्रत्येक तीन हायड्रोजन अणूंशी बद्ध होते ज्यामुळे मिळते:
$H-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}}-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}} - H \qquad $ पायरी 2
आकृती 4.6 (b) प्रत्येक कार











