अध्याय 04 कार्बन और उसके यौगिक
पिछले अध्याय में, हम अपने लिए महत्वपूर्ण कई यौगिकों के बारे में जाने। इस अध्याय में हम कुछ और रोचक यौगिकों और उनके गुणों का अध्ययन करेंगे। साथ ही, हम कार्बन के बारे में सीखेंगे, एक ऐसा तत्व जो अपने मौलिक रूप और संयुक्त रूप दोनों में हमारे लिए अत्यधिक महत्व रखता है।
क्रियाकलाप 4.1
- सुबह से आपके द्वारा उपयोग या उपभोग की गई दस वस्तुओं की एक सूची बनाइए।
- इस सूची को अपने सहपाठियों द्वारा बनाई गई सूचियों के साथ संकलित कीजिए और फिर वस्तुओं को सारणी में वर्गीकृत कीजिए।
- यदि कोई वस्तुएँ एक से अधिक पदार्थों से बनी हैं, तो उन्हें सारणी के दोनों संबंधित स्तंभों में रखिए।
| धातु से बनी वस्तुएँ | धातु से बनी वस्तुएँ | अन्य |
|---|---|---|
आपके द्वारा भरी गई उपरोक्त सारणी के अंतिम स्तंभ में आने वाली वस्तुओं को देखिए - आपके शिक्षक आपको बता सकेंगे कि उनमें से अधिकांश कार्बन के यौगिकों से बनी हैं। क्या आप इसकी जाँच करने के लिए कोई विधि सोच सकते हैं? यदि कार्बन युक्त कोई यौगिक जलाया जाए तो उत्पाद क्या होगा? क्या आप इसकी पुष्टि के लिए कोई परीक्षण जानते हैं?
भोजन, वस्त्र, दवाइयाँ, पुस्तकें, या आपके द्वारा सूचीबद्ध कई वस्तुएँ सभी इस बहुमुखी तत्व कार्बन पर आधारित हैं। इसके अतिरिक्त, सभी जीवित संरचनाएँ कार्बन आधारित हैं। पृथ्वी की पर्पटी और वायुमंडल में उपस्थित कार्बन की मात्रा काफी कम है। पृथ्वी की पर्पटी में केवल $0.02 %$ कार्बन खनिजों (जैसे कार्बोनेट, हाइड्रोजनकार्बोनेट, कोयला और पेट्रोलियम) के रूप में है और वायुमंडल में कार्बन डाइऑक्साइड की मात्रा $0.03 %$ है। प्रकृति में उपलब्ध कार्बन की इस छोटी मात्रा के बावजूद, कार्बन का महत्व अत्यधिक प्रतीत होता है। इस अध्याय में, हम कार्बन के उन गुणों के बारे में जानेंगे जो कार्बन को हमारे लिए इतना महत्वपूर्ण बनाते हैं।
4.1 कार्बन में आबंधन - सहसंयोजक आबंध
पिछले अध्याय में, हमने आयनिक यौगिकों के गुणों का अध्ययन किया था। हमने देखा कि आयनिक यौगिकों के गलनांक और क्वथनांक उच्च होते हैं और वे विलयन या गलित अवस्था में विद्युत का चालन करते हैं। हमने यह भी देखा कि आयनिक यौगिकों में आबंधन की प्रकृति इन गुणों की व्याख्या कैसे करती है। आइए अब कुछ कार्बन यौगिकों के गुणों का अध्ययन करें।
अधिकांश कार्बन यौगिक विद्युत के कुचालक होते हैं जैसा कि हमने अध्याय 2 में देखा था। सारणी 4.1 में दिए गए कार्बन यौगिकों के क्वथनांक और गलनांक के आँकड़ों से, हम पाते हैं कि इन यौगिकों के गलनांक और क्वथनांक आयनिक यौगिकों (अध्याय 3) की तुलना में कम होते हैं। हम यह निष्कर्ष निकाल सकते हैं कि अणुओं के बीच आकर्षण बल बहुत प्रबल नहीं होते हैं। चूँकि ये यौगिक विद्युत के अचालक होते हैं, हम यह निष्कर्ष निकाल सकते हैं कि इन यौगिकों में आबंधन से कोई आयन उत्पन्न नहीं होते हैं।
सारणी 4.1 कार्बन के कुछ यौगिकों के गलनांक और क्वथनांक
| यौगिक | गलनांक $(\mathbf{K})$ | क्वथनांक $(\mathbf{K})$ |
|---|---|---|
| एसीटिक अम्ल $(CH_3 COOH)$ | 290 | 391 |
| क्लोरोफॉर्म $(CHCl_3)$ | 209 | 334 |
| एथेनॉल $(CH_3 CH_2 OH)$ | 156 | 351 |
| मीथेन $(CH_4)$ | 90 | 111 |
कक्षा IX में, हमने विभिन्न तत्वों की संयोजन क्षमता और यह कैसे संयोजकता इलेक्ट्रॉनों की संख्या पर निर्भर करती है, के बारे में सीखा था। आइए अब कार्बन के इलेक्ट्रॉनिक विन्यास को देखें। कार्बन की परमाणु संख्या 6 है। कार्बन के विभिन्न कोशों में इलेक्ट्रॉनों का वितरण क्या होगा? कार्बन के कितने संयोजकता इलेक्ट्रॉन होंगे?
हम जानते हैं कि तत्वों की अभिक्रियाशीलता को उनकी बाह्यतम कोश को पूर्णतः भरने, अर्थात् उत्कृष्ट गैस विन्यास प्राप्त करने की प्रवृत्ति के रूप में समझाया जाता है। आयनिक यौगिक बनाने वाले तत्व बाह्यतम कोश से इलेक्ट्रॉनों को प्राप्त करके या खोकर यह प्राप्त करते हैं। कार्बन के मामले में, इसके बाह्यतम कोश में चार इलेक्ट्रॉन हैं और उत्कृष्ट गैस विन्यास प्राप्त करने के लिए इसे चार इलेक्ट्रॉन प्राप्त करने या खोने की आवश्यकता है। यदि यह इलेक्ट्रॉन प्राप्त करे या खोए तो -
(i) यह चार इलेक्ट्रॉन प्राप्त करके $C^{4-}$ ऋणायन बना सकता है। लेकिन छह प्रोटॉन वाले नाभिक के लिए दस इलेक्ट्रॉनों, अर्थात् चार अतिरिक्त इलेक्ट्रॉनों को धारण करना कठिन होगा।
(ii) यह चार इलेक्ट्रॉन खोकर $C^{4+}$ धनायन बना सकता है। लेकिन चार इलेक्ट्रॉनों को हटाने के लिए बड़ी मात्रा में ऊर्जा की आवश्यकता होगी, जिससे केवल दो इलेक्ट्रॉनों को धारण करने वाले नाभिक में छह प्रोटॉनों के साथ एक कार्बन धनायन शेष रह जाएगा।
कार्बन इस समस्या को अपने संयोजकता इलेक्ट्रॉनों को कार्बन के अन्य परमाणुओं या अन्य तत्वों के परमाणुओं के साथ साझा करके दूर करता है। केवल कार्बन ही नहीं, बल्कि कई अन्य तत्व भी इस प्रकार इलेक्ट्रॉनों को साझा करके अणु बनाते हैं। साझा किए गए इलेक्ट्रॉन दोनों परमाणुओं के बाह्यतम कोशों के ‘अंतर्गत’ आते हैं और दोनों परमाणुओं को उत्कृष्ट गैस विन्यास प्राप्त करने की ओर ले जाते हैं। कार्बन के यौगिकों पर जाने से पहले, आइए संयोजकता इलेक्ट्रॉनों के साझा होने से बने कुछ सरल अणुओं को देखें।
इस प्रकार बना सबसे सरल अणु हाइड्रोजन का है। जैसा कि आपने पहले सीखा है, हाइड्रोजन की परमाणु संख्या 1 है। अतः हाइड्रोजन के $K$ कोश में एक इलेक्ट्रॉन है और $K$ कोश को भरने के लिए इसे एक और इलेक्ट्रॉन की आवश्यकता है। इसलिए दो हाइड्रोजन परमाणु अपने इलेक्ट्रॉनों को साझा करके हाइड्रोजन का एक अणु, $H_2$ बनाते हैं। यह प्रत्येक हाइड्रोजन परमाणु को निकटतम उत्कृष्ट गैस, हीलियम, का इलेक्ट्रॉनिक विन्यास प्राप्त करने की अनुमति देता है, जिसके K कोश में दो इलेक्ट्रॉन हैं। हम इसे संयोजकता इलेक्ट्रॉनों को निरूपित करने के लिए बिंदुओं या क्रॉस का उपयोग करके दर्शा सकते हैं (चित्र 4.1)।
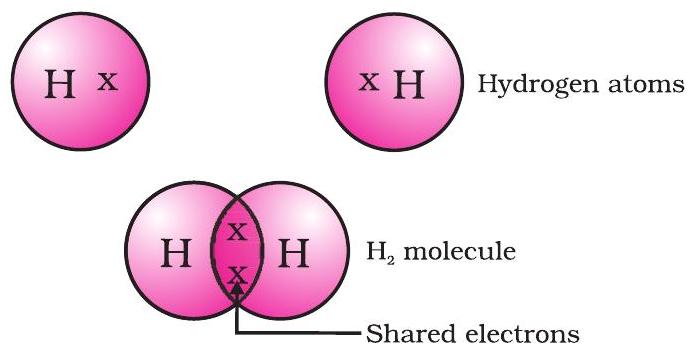
चित्र 4.1 हाइड्रोजन का एक अणु
साझा किए गए इलेक्ट्रॉनों के युग्म को दो हाइड्रोजन परमाणुओं के बीच एक एकल सहसंयोजक आबंध बनाने वाला कहा जाता है। एक एकल सहसंयोजक आबंध को दो परमाणुओं के बीच एक रेखा द्वारा भी निरूपित किया जाता है, जैसा कि चित्र 4.2 में दिखाया गया है।
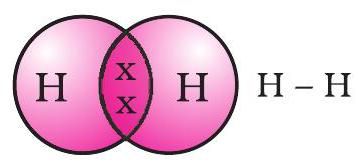
चित्र 4.2 दो हाइड्रोजन परमाणुओं के बीच एकल आबंध
क्लोरीन की परमाणु संख्या 17 है। इसका इलेक्ट्रॉनिक विन्यास और इसकी संयोजकता क्या होगी? क्लोरीन एक द्विपरमाणुक अणु, $Cl_2$ बनाती है। क्या आप इस अणु के लिए इलेक्ट्रॉन बिंदु संरचना बना सकते हैं? ध्यान दें कि केवल संयोजकता कोश के इलेक्ट्रॉनों को दर्शाने की आवश्यकता है।
ऑक्सीजन के मामले में, हम दो ऑक्सीजन परमाणुओं के बीच एक द्वि-आबंध के निर्माण को देखते हैं। ऐसा इसलिए है क्योंकि ऑक्सीजन के एक परमाणु के L कोश (ऑक्सीजन की परमाणु संख्या आठ है) में छह इलेक्ट्रॉन होते हैं और इसके अष्टक को पूरा करने के लिए इसे दो और इलेक्ट्रॉनों की आवश्यकता होती है। इसलिए ऑक्सीजन का प्रत्येक परमाणु दो इलेक्ट्रॉनों को ऑक्सीजन के दूसरे परमाणु के साथ साझा करता है, जिससे हमें चित्र 4.3 में दिखाई गई संरचना प्राप्त होती है। प्रत्येक ऑक्सीजन परमाणु द्वारा दिए गए दो इलेक्ट्रॉन दो साझा इलेक्ट्रॉन युग्म उत्पन्न करते हैं। इसे दो परमाणुओं के बीच एक द्वि-आबंध बनाने वाला कहा जाता है।
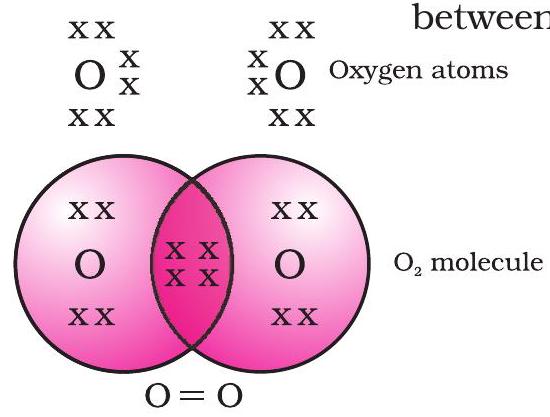
चित्र 4.3 दो ऑक्सीजन परमाणुओं के बीच द्वि-आबंध
क्या आप अब पानी के एक अणु को एक ऑक्सीजन परमाणु और दो हाइड्रोजन परमाणुओं के बीच आबंधन की प्रकृति दिखाते हुए चित्रित कर सकते हैं? क्या अणु में एकल आबंध हैं या द्वि-आबंध?
नाइट्रोजन के द्विपरमाणुक अणु के मामले में क्या होगा? नाइट्रोजन की परमाणु संख्या 7 है। इसका इलेक्ट्रॉनिक विन्यास और इसकी संयोजन क्षमता क्या होगी? एक अष्टक प्राप्त करने के लिए, नाइट्रोजन के अणु में नाइट्रोजन का प्रत्येक परमाणु तीन इलेक्ट्रॉन देता है, जिससे तीन साझा इलेक्ट्रॉन युग्म बनते हैं। इसे दो परमाणुओं के बीच एक त्रि-आबंध बनाने वाला कहा जाता है चित्र 4.3 दो ऑक्सीजन परमाणुओं के बीच द्वि-आबंध और $N_2$ की इलेक्ट्रॉन बिंदु संरचना और इसके त्रि-आबंध को चित्र 4.4 के अनुसार दर्शाया जा सकता है।
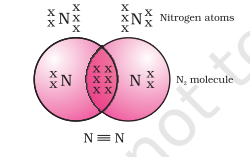
चित्र 4.4 दो नाइट्रोजन परमाणुओं के बीच त्रि-आबंध
अमोनिया के अणु का सूत्र $NH_3$ है। क्या आप इस अणु के लिए इलेक्ट्रॉन बिंदु संरचना बना सकते हैं जो दर्शाती है कि कैसे सभी चार परमाणु उत्कृष्ट गैस विन्यास प्राप्त करते हैं? क्या अणु में एकल, द्वि या त्रि आबंध होंगे?
आइए अब मीथेन पर एक नज़र डालें, जो कार्बन का एक यौगिक है। मीथेन का व्यापक रूप से ईंधन के रूप में उपयोग किया जाता है और यह बायोगैस और संपीडित प्राकृतिक गैस (CNG) का एक प्रमुख घटक है। यह कार्बन द्वारा बने सबसे सरल यौगिकों में से एक भी है। मीथेन का सूत्र $CH_4$ है। हाइड्रोजन की संयोजकता, जैसा कि आप जानते हैं, 1 है। कार्बन चतुःसंयोजक है क्योंकि इसके चार संयोजकता इलेक्ट्रॉन हैं। उत्कृष्ट गैस विन्यास प्राप्त करने के लिए, कार्बन इन इलेक्ट्रॉनों को हाइड्रोजन के चार परमाणुओं के साथ साझा करता है जैसा कि चित्र 4.5 में दिखाया गया है।
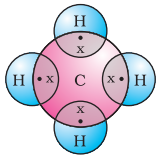
चित्र 4.5 मीथेन के लिए इलेक्ट्रॉन बिंदु संरचना
ऐसे आबंध जो दो परमाणुओं के बीच एक इलेक्ट्रॉन युग्म के साझा होने से बनते हैं, सहसंयोजक आबंध के रूप में जाने जाते हैं। देखा गया है कि सहसंयोजक आबंधित अणुओं में अणु के भीतर प्रबल आबंध होते हैं, लेकिन अंतराअणुक बल दुर्बल होते हैं। इससे इन यौगिकों के निम्न गलनांक और क्वथनांक उत्पन्न होते हैं। चूँकि इलेक्ट्रॉन परमाणुओं के बीच साझा किए जाते हैं और कोई आवेशित कण नहीं बनते हैं, इसलिए ऐसे सहसंयोजक यौगिक आम तौर पर विद्युत के कुचालक होते हैं।
और जानिए!
कार्बन के अपररूप
तत्व कार्बन प्रकृति में भिन्न-भिन्न भौतिक गुणों वाले विभिन्न रूपों में पाया जाता है। हीरा और ग्रेफाइट दोनों कार्बन परमाणुओं द्वारा बने होते हैं, अंतर कार्बन परमाणुओं के एक-दूसरे से आबंधित होने के तरीके में निहित है। हीरे में, प्रत्येक कार्बन परमाणु चार अन्य कार्बन परमाणुओं से आबंधित होकर एक दृढ़ त्रि-विमीय संरचना बनाता है। ग्रेफाइट में, प्रत्येक कार्बन परमाणु तीन अन्य कार्बन परमाणुओं से समान तल में आबंधित होकर एक षट्कोणीय व्यूह बनाता है। इनमें से एक आबंध द्वि-आबंध होता है, और इस प्रकार कार्बन की संयोजकता संतुष्ट हो जाती है। ग्रेफाइट संरचना षट्कोणीय व्यूहों को एक-दूसरे के ऊपर परतों में व्यवस्थित करने से बनती है।
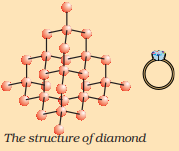
हीरे की संरचना
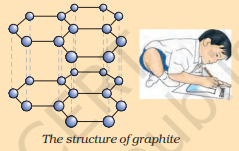
ग्रेफाइट की संरचना
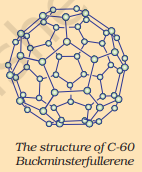
C-60 बकमिंस्टरफुलेरीन की संरचना
इन दो भिन्न संरचनाओं के परिणामस्वरूप हीरे और ग्रेफाइट के भौतिक गुण बहुत भिन्न होते हैं, भले ही उनके रासायनिक गुण समान हों। हीरा ज्ञात सबसे कठोर पदार्थ है जबकि ग्रेफाइट चिकना और फिसलन भरा होता है। ग्रेफाइट विद्युत का एक बहुत अच्छा चालक भी है, जो पिछले अध्याय में आपके द्वारा पढ़े गए अन्य अधातुओं के विपरीत है।
शुद्ध कार्बन को अत्यधिक उच्च दाब और ताप के अधीन करके हीरे का संश्लेषण किया जा सकता है। ये संश्लेषित हीरे छोटे होते हैं लेकिन अन्यथा प्राकृतिक हीरों से अभिन्न होते हैं।
फुलेरीन कार्बन के अपररूपों का एक अन्य वर्ग बनाते हैं। पहला पहचाना गया C-60 था जिसमें कार्बन परमाणु एक फुटबॉल के आकार में व्यवस्थित होते हैं। चूँकि यह अमेरिकी वास्तुकार बकमिंस्टर फुलर द्वारा डिजाइन किए गए जियोडेसिक गुंबद जैसा दिखता था, इसलिए अणु का नाम फुलेरीन रखा गया।
4.2 कार्बन की बहुमुखी प्रकृति
हमने विभिन्न तत्वों और यौगिकों में इलेक्ट्रॉनों के साझा होने से सहसंयोजक आबंधों के निर्माण को देखा है। हमने एक सरल कार्बन यौगिक, मीथेन की संरचना भी देखी है। अध्याय की शुरुआत में, हमने देखा कि हम जिन कई चीजों का उपयोग करते हैं उनमें कार्बन होता है। वास्तव में, हम स्वयं कार्बन यौगिकों से बने हैं। कार्बन यौगिकों की संख्या जिनके सूत्र रसायनज्ञों को ज्ञात हैं, हाल ही में लाखों में अनुमानित की गई थी! यह संख्या अन्य सभी तत्वों द्वारा मिलकर बने यौगिकों की संख्या से बहुत अधिक है। ऐसा क्यों है कि यह गुण केवल कार्बन में देखा जाता है और किसी अन्य तत्व में नहीं? सहसंयोजक आबंध की प्रकृति कार्बन को बड़ी संख्या में यौगिक बनाने में सक्षम बनाती है। कार्बन के मामले में देखे गए दो कारक हैं -
(i) कार्बन में अन्य कार्बन परमाणुओं के साथ आबंध बनाने की अद्वितीय क्षमता होती है, जिससे बड़े अणु बनते हैं। इस गुण को श्रृंखलन कहा जाता है। इन यौगिकों में कार्बन की लंबी श्रृंखलाएँ, कार्बन की शाखित श्रृंखलाएँ या यहाँ तक कि वलयों में व्यवस्थित कार्बन परमाणु हो सकते हैं। इसके अतिरिक्त, कार्बन परमाणु एकल, द्वि या त्रि आबंधों द्वारा जुड़े हो सकते हैं। कार्बन के वे यौगिक, जिनमें कार्बन परमाणुओं के बीच केवल एकल आबंध होते हैं, संतृप्त यौगिक कहलाते हैं। कार्बन के वे यौगिक जिनमें उनके कार्बन परमाणुओं के बीच द्वि या त्रि आबंध होते हैं, असंतृप्त यौगिक कहलाते हैं।
कार्बन यौगिकों में देखे गए सीमा तक श्रृंखलन का गुण कोई अन्य तत्व प्रदर्शित नहीं करता है। सिलिकॉन हाइड्रोजन के साथ ऐसे यौगिक बनाता है जिनमें सात या आठ परमाणुओं तक की श्रृंखलाएँ होती हैं, लेकिन ये यौगिक बहुत अभिक्रियाशील होते हैं। कार्बन-कार्बन आबंध बहुत प्रबल और इसलिए स्थायी होता है। यह हमें बड़ी संख्या में यौगिक देता है जिनमें कई कार्बन परमाणु एक-दूसरे से जुड़े होते हैं।
(ii) चूँकि कार्बन की संयोजकता चार है, यह कार्बन के चार अन्य परमाणुओं या किसी अन्य एक-संयोजक तत्व के परमाणुओं के साथ आबंध बनाने में सक्षम है। कार्बन के यौगिक ऑक्सीजन, हाइड्रोजन, नाइट्रोजन, सल्फर, क्लोरीन और कई अन्य तत्वों के साथ बनते हैं, जिससे विशिष्ट गुणों वाले यौगिक बनते हैं जो अणु में उपस्थित कार्बन के अलावा अन्य तत्वों पर निर्भर करते हैं।
पुनः, कार्बन द्वारा अधिकांश अन्य तत्वों के साथ बने आबंध बहुत प्रबल होते हैं जो इन यौगिकों को असाधारण रूप से स्थायी बनाते हैं। कार्बन द्वारा प्रबल आबंध बनने का एक कारण इसका छोटा आकार है। यह नाभिक को साझा किए गए इलेक्ट्रॉन युग्मों को दृढ़ता से धारण करने में सक्षम बनाता है। बड़े परमाणुओं वाले तत्वों द्वारा बने आबंध बहुत दुर्बल होते हैं।
क्या आप जानते हैं?
कार्बनिक यौगिक
कार्बन में देखे गए दो विशिष्ट लक्षण, अर्थात् चतुःसंयोजकता और श्रृंखलन, मिलकर बड़ी संख्या में यौगिक उत्पन्न करते हैं। कई में समान अ-कार्बन परमाणु या परमाणुओं का समूह विभिन्न कार्बन श्रृंखलाओं से जुड़ा होता है। इन यौगिकों को प्रारंभ में प्राकृतिक पदार्थों से निष्कर्षित किया गया था और यह सोचा गया था कि ये कार्बन यौगिक या कार्बनिक यौगिक केवल एक जीवित प्रणाली के भीतर ही बन सकते हैं। अर्थात्, यह परिकल्पना की गई थी कि उनके संश्लेषण के लिए एक ‘जीवन शक्ति’ आवश्यक थी। फ्रेडरिक वोहलर ने 1828 में अमोनियम सायनेट से यूरिया तैयार करके इसे गलत साबित किया। लेकिन कार्बन यौगिकों, कार्बाइड, कार्बन के ऑक्साइड, कार्बोनेट और हाइड्रोजनकार्बोनेट लवणों को छोड़कर, कार्बनिक रसायन के अंतर्गत अध्ययन किए जाते रहते हैं।
4.2.1 संतृप्त और असंतृप्त कार्बन यौगिक
हमने पहले ही मीथेन की संरचना देखी है। कार्बन और हाइड्रोजन के बीच बना एक अन्य यौगिक एथेन है जिसका सूत्र $C_2 H_6$ है। सरल कार्बन यौगिकों की संरचना पर पहुँचने के लिए, पहला चरण कार्बन परमाणुओं को एक एकल आबंध (चित्र 4.6a) के साथ जोड़ना है और फिर कार्बन की शेष संयोजकताओं को संतुष्ट करने के लिए हाइड्रोजन परमाणुओं का उपयोग करना है (चित्र 4.6b)। उदाहरण के लिए, एथेन की संरचना निम्नलिखित चरणों में प्राप्त की जाती है -
$ C-C \qquad $ चरण 1
चित्र 4.6 (a) एकल आबंध से जुड़े कार्बन परमाणु
प्रत्येक कार्बन परमाणु की तीन संयोजकताएँ असंतुष्ट रहती हैं, इसलिए प्रत्येक तीन हाइड्रोजन परमाणुओं से आबंधित होता है, जिससे प्राप्त होता है:
$H-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}}-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}} - H \qquad $ चरण 2
चित्र 4.6 (b) प्रत्येक कार्बन परमाणु तीन हाइड्रोजन परमाणुओं से आबंधित
एथेन की इलेक्ट्रॉन बिंदु संरचना चित्र 4.6(c) में दिखाई गई है।
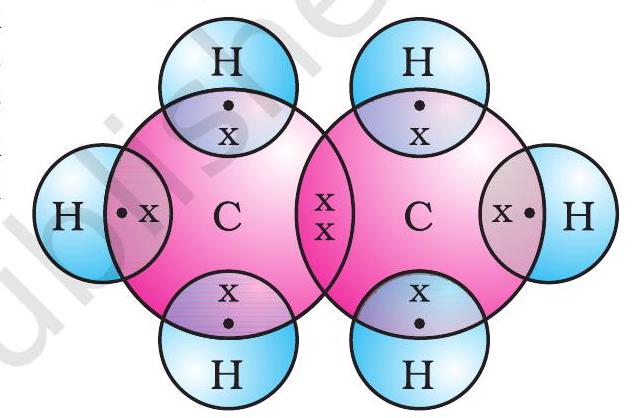
चित्र 4.6 (c) एथेन की इलेक्ट्रॉन बिंदु संरचना
क्या आप प्रोपेन की संरचना, जिसका आणविक सूत्र $C_3 H_8$ है, इसी प्रकार बना सकते हैं? आप देखेंगे कि सभी परमाणुओं की संयोजकताएँ उनके बीच एकल आबंधों द्वारा संतुष्ट हो जाती हैं। ऐसे कार्बन यौगिकों को संतृप्त यौगिक कहा जाता है। ये यौगिक आम तौर पर बहुत अभिक्रियाशील नहीं होते हैं।
हालाँकि, कार्बन और हाइड्रोजन के एक अन्य यौगिक का सूत्र $C_2 H_4$ है और इसे एथीन कहा जाता है। इस अणु को कैसे चित्रित किया जा सकता है? हम ऊपर के समान चरणबद्ध दृष्टिकोण का पालन करते हैं।
कार्बन-कार्बन परमाणु एकल आबंध (चरण 1) से जुड़े











