ਅਧਿਆਇ 04 ਕਾਰਬਨ ਅਤੇ ਇਸਦੇ ਯੋਗਿਕ
ਪਿਛਲੇ ਅਧਿਆਇ ਵਿੱਚ, ਅਸੀਂ ਆਪਣੇ ਲਈ ਮਹੱਤਵਪੂਰਨ ਬਹੁਤ ਸਾਰੇ ਯੋਗਿਕਾਂ ਬਾਰੇ ਜਾਣਿਆ। ਇਸ ਅਧਿਆਇ ਵਿੱਚ ਅਸੀਂ ਕੁਝ ਹੋਰ ਦਿਲਚਸਪ ਯੋਗਿਕਾਂ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਗੁਣਾਂ ਬਾਰੇ ਅਧਿਐਨ ਕਰਾਂਗੇ। ਇਸ ਤੋਂ ਇਲਾਵਾ, ਅਸੀਂ ਕਾਰਬਨ ਬਾਰੇ ਸਿੱਖਾਂਗੇ, ਇੱਕ ਅਜਿਹਾ ਤੱਤ ਜੋ ਆਪਣੇ ਤੱਤ ਰੂਪ ਅਤੇ ਸੰਯੁਕਤ ਰੂਪ ਦੋਨਾਂ ਵਿੱਚ ਸਾਡੇ ਲਈ ਬਹੁਤ ਮਹੱਤਵਪੂਰਨ ਹੈ।
ਕਿਰਿਆ 4.1
- ਸਵੇਰ ਤੋਂ ਹੁਣ ਤੱਕ ਤੁਸੀਂ ਜੋ ਦਸ ਚੀਜ਼ਾਂ ਵਰਤੀਆਂ ਜਾਂ ਖਾਧੀਆਂ ਹਨ, ਉਨ੍ਹਾਂ ਦੀ ਇੱਕ ਸੂਚੀ ਬਣਾਓ।
- ਇਸ ਸੂਚੀ ਨੂੰ ਆਪਣੇ ਸਹਿਪਾਠੀਆਂ ਦੁਆਰਾ ਬਣਾਈਆਂ ਗਈਆਂ ਸੂਚੀਆਂ ਨਾਲ ਮਿਲਾਓ ਅਤੇ ਫਿਰ ਆਈਟਮਾਂ ਨੂੰ ਨਾਲ ਦੀ ਟੇਬਲ ਵਿੱਚ ਵਰਗੀਕ੍ਰਿਤ ਕਰੋ।
- ਜੇਕਰ ਕੋਈ ਆਈਟਮ ਇੱਕ ਤੋਂ ਵੱਧ ਸਮੱਗਰੀ ਤੋਂ ਬਣੀ ਹੋਵੇ, ਤਾਂ ਉਨ੍ਹਾਂ ਨੂੰ ਟੇਬਲ ਦੇ ਦੋਨਾਂ ਸੰਬੰਧਿਤ ਕਾਲਮਾਂ ਵਿੱਚ ਰੱਖੋ।
| ਧਾਤੂ ਤੋਂ ਬਣੀਆਂ ਚੀਜ਼ਾਂ | ਧਾਤੂ ਤੋਂ ਬਣੀਆਂ ਚੀਜ਼ਾਂ | ਹੋਰ |
|---|---|---|
ਉਪਰੋਕਤ ਟੇਬਲ ਦੇ ਆਖਰੀ ਕਾਲਮ ਵਿੱਚ ਆਉਣ ਵਾਲੀਆਂ ਆਈਟਮਾਂ ਨੂੰ ਵੇਖੋ ਜੋ ਤੁਹਾਡੇ ਦੁਆਰਾ ਭਰੀਆਂ ਗਈਆਂ ਹਨ - ਤੁਹਾਡੇ ਅਧਿਆਪਕ ਤੁਹਾਨੂੰ ਦੱਸ ਸਕਣਗੇ ਕਿ ਉਨ੍ਹਾਂ ਵਿੱਚੋਂ ਜ਼ਿਆਦਾਤਰ ਕਾਰਬਨ ਦੇ ਯੋਗਿਕਾਂ ਤੋਂ ਬਣੀਆਂ ਹਨ। ਕੀ ਤੁਸੀਂ ਇਸ ਦੀ ਜਾਂਚ ਕਰਨ ਲਈ ਕੋਈ ਵਿਧੀ ਬਾਰੇ ਸੋਚ ਸਕਦੇ ਹੋ? ਜੇਕਰ ਕਾਰਬਨ ਵਾਲਾ ਕੋਈ ਯੋਗਿਕ ਸਾੜਿਆ ਜਾਵੇ ਤਾਂ ਉਤਪਾਦ ਕੀ ਹੋਵੇਗਾ? ਕੀ ਤੁਸੀਂ ਇਸ ਦੀ ਪੁਸ਼ਟੀ ਕਰਨ ਲਈ ਕੋਈ ਟੈਸਟ ਜਾਣਦੇ ਹੋ?
ਭੋਜਨ, ਕੱਪੜੇ, ਦਵਾਈਆਂ, ਕਿਤਾਬਾਂ, ਜਾਂ ਤੁਹਾਡੇ ਦੁਆਰਾ ਸੂਚੀਬੱਧ ਬਹੁਤ ਸਾਰੀਆਂ ਚੀਜ਼ਾਂ ਇਸ ਬਹੁਪੱਖੀ ਤੱਤ ਕਾਰਬਨ ‘ਤੇ ਅਧਾਰਿਤ ਹਨ। ਇਸ ਤੋਂ ਇਲਾਵਾ, ਸਾਰੀਆਂ ਜੀਵਤ ਬਣਤਰਾਂ ਕਾਰਬਨ-ਅਧਾਰਿਤ ਹਨ। ਧਰਤੀ ਦੀ ਪਰਤ ਅਤੇ ਵਾਯੂਮੰਡਲ ਵਿੱਚ ਮੌਜੂਦ ਕਾਰਬਨ ਦੀ ਮਾਤਰਾ ਕਾਫ਼ੀ ਘੱਟ ਹੈ। ਧਰਤੀ ਦੀ ਪਰਤ ਵਿੱਚ ਸਿਰਫ਼ $0.02 %$ ਕਾਰਬਨ ਖਣਿਜਾਂ (ਜਿਵੇਂ ਕਾਰਬੋਨੇਟ, ਹਾਈਡ੍ਰੋਜਨਕਾਰਬੋਨੇਟ, ਕੋਲਾ ਅਤੇ ਪੈਟ੍ਰੋਲੀਅਮ) ਦੇ ਰੂਪ ਵਿੱਚ ਹੈ ਅਤੇ ਵਾਯੂਮੰਡਲ ਵਿੱਚ $0.03 %$ ਕਾਰਬਨ ਡਾਈਆਕਸਾਈਡ ਹੈ। ਕੁਦਰਤ ਵਿੱਚ ਉਪਲਬਧ ਕਾਰਬਨ ਦੀ ਇਸ ਘੱਟ ਮਾਤਰਾ ਦੇ ਬਾਵਜੂਦ, ਕਾਰਬਨ ਦਾ ਮਹੱਤਵ ਬਹੁਤ ਜ਼ਿਆਦਾ ਲੱਗਦਾ ਹੈ। ਇਸ ਅਧਿਆਇ ਵਿੱਚ, ਅਸੀਂ ਕਾਰਬਨ ਦੇ ਉਹ ਗੁਣਾਂ ਬਾਰੇ ਜਾਣਾਂਗੇ ਜੋ ਕਾਰਬਨ ਨੂੰ ਸਾਡੇ ਲਈ ਇੰਨਾ ਮਹੱਤਵਪੂਰਨ ਬਣਾਉਂਦੇ ਹਨ।
4.1 ਕਾਰਬਨ ਵਿੱਚ ਬੰਧਨ - ਸਹਿਸੰਯੋਜਕ ਬੰਧ
ਪਿਛਲੇ ਅਧਿਆਇ ਵਿੱਚ, ਅਸੀਂ ਆਇਨਿਕ ਯੋਗਿਕਾਂ ਦੇ ਗੁਣਾਂ ਦਾ ਅਧਿਐਨ ਕੀਤਾ ਸੀ। ਅਸੀਂ ਵੇਖਿਆ ਕਿ ਆਇਨਿਕ ਯੋਗਿਕਾਂ ਦੇ ਪਿਘਲਣ ਅਤੇ ਉਬਾਲ ਦੇ ਬਿੰਦੂ ਉੱਚੇ ਹੁੰਦੇ ਹਨ ਅਤੇ ਘੋਲ ਜਾਂ ਪਿਘਲੀ ਹਾਲਤ ਵਿੱਚ ਬਿਜਲੀ ਦਾ ਸੰਚਾਲਨ ਕਰਦੇ ਹਨ। ਅਸੀਂ ਇਹ ਵੀ ਵੇਖਿਆ ਕਿ ਆਇਨਿਕ ਯੋਗਿਕਾਂ ਵਿੱਚ ਬੰਧਨ ਦੀ ਪ੍ਰਕਿਰਤੀ ਇਨ੍ਹਾਂ ਗੁਣਾਂ ਦੀ ਵਿਆਖਿਆ ਕਿਵੇਂ ਕਰਦੀ ਹੈ। ਆਓ ਹੁਣ ਕੁਝ ਕਾਰਬਨ ਯੋਗਿਕਾਂ ਦੇ ਗੁਣਾਂ ਦਾ ਅਧਿਐਨ ਕਰੀਏ।
ਜਿਵੇਂ ਕਿ ਅਸੀਂ ਅਧਿਆਇ 2 ਵਿੱਚ ਵੇਖਿਆ ਹੈ, ਜ਼ਿਆਦਾਤਰ ਕਾਰਬਨ ਯੋਗਿਕ ਬਿਜਲੀ ਦੇ ਮਾੜੇ ਸੰਚਾਲਕ ਹੁੰਦੇ ਹਨ। ਕਾਰਬਨ ਯੋਗਿਕਾਂ ਦੇ ਉਬਾਲ ਅਤੇ ਪਿਘਲਣ ਦੇ ਬਿੰਦੂਆਂ ਬਾਰੇ ਟੇਬਲ 4.1 ਵਿੱਚ ਦਿੱਤੇ ਡੇਟਾ ਤੋਂ, ਅਸੀਂ ਪਾਉਂਦੇ ਹਾਂ ਕਿ ਇਨ੍ਹਾਂ ਯੋਗਿਕਾਂ ਦੇ ਪਿਘਲਣ ਅਤੇ ਉਬਾਲ ਦੇ ਬਿੰਦੂ ਆਇਨਿਕ ਯੋਗਿਕਾਂ (ਅਧਿਆਇ 3) ਦੇ ਮੁਕਾਬਲੇ ਘੱਟ ਹੁੰਦੇ ਹਨ। ਅਸੀਂ ਇਹ ਨਿਸ਼ਕਰਸ਼ ਕੱਢ ਸਕਦੇ ਹਾਂ ਕਿ ਅਣੂਆਂ ਵਿਚਕਾਰ ਆਕਰਸ਼ਣ ਦੀਆਂ ਸ਼ਕਤੀਆਂ ਬਹੁਤ ਮਜ਼ਬੂਤ ਨਹੀਂ ਹਨ। ਕਿਉਂਕਿ ਇਹ ਯੋਗਿਕ ਬਹੁਤ ਹੱਦ ਤੱਕ ਬਿਜਲੀ ਦੇ ਗੈਰ-ਸੰਚਾਲਕ ਹਨ, ਅਸੀਂ ਇਹ ਨਿਸ਼ਕਰਸ਼ ਕੱਢ ਸਕਦੇ ਹਾਂ ਕਿ ਇਨ੍ਹਾਂ ਯੋਗਿਕਾਂ ਵਿੱਚ ਬੰਧਨ ਕਿਸੇ ਵੀ ਆਇਨ ਦਾ ਨਿਰਮਾਣ ਨਹੀਂ ਕਰਦਾ।
ਟੇਬਲ 4.1 ਕਾਰਬਨ ਦੇ ਕੁਝ ਯੋਗਿਕਾਂ ਦੇ ਪਿਘਲਣ ਅਤੇ ਉਬਾਲ ਦੇ ਬਿੰਦੂ
| ਯੋਗਿਕ | ਪਿਘਲਣ ਬਿੰਦੂ $(\mathbf{K})$ | ਉਬਾਲ ਬਿੰਦੂ $(\mathbf{K})$ |
|---|---|---|
| ਐਸੀਟਿਕ ਐਸਿਡ $(CH_3 COOH)$ | 290 | 391 |
| ਕਲੋਰੋਫਾਰਮ $(CHCl_3)$ | 209 | 334 |
| ਈਥਾਨੋਲ $(CH_3 CH_2 OH)$ | 156 | 351 |
| ਮੀਥੇਨ $(CH_4)$ | 90 | 111 |
ਕਲਾਸ IX ਵਿੱਚ, ਅਸੀਂ ਵੱਖ-ਵੱਖ ਤੱਤਾਂ ਦੀ ਸੰਯੋਜਨ ਸਮਰੱਥਾ ਅਤੇ ਇਹ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਗਿਣਤੀ ‘ਤੇ ਕਿਵੇਂ ਨਿਰਭਰ ਕਰਦੀ ਹੈ, ਇਸ ਬਾਰੇ ਸਿੱਖਿਆ। ਆਓ ਹੁਣ ਕਾਰਬਨ ਦੀ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਉਂਤ ਨੂੰ ਵੇਖੀਏ। ਕਾਰਬਨ ਦਾ ਪਰਮਾਣੂ ਨੰਬਰ 6 ਹੈ। ਕਾਰਬਨ ਦੇ ਵੱਖ-ਵੱਖ ਖੋਲਾਂ ਵਿੱਚ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਵੰਡ ਕੀ ਹੋਵੇਗੀ? ਕਾਰਬਨ ਦੇ ਕਿੰਨੇ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੋਨ ਹੋਣਗੇ?
ਅਸੀਂ ਜਾਣਦੇ ਹਾਂ ਕਿ ਤੱਤਾਂ ਦੀ ਪ੍ਰਤੀਕ੍ਰਿਆਸ਼ੀਲਤਾ ਨੂੰ ਉਨ੍ਹਾਂ ਦੀ ਪੂਰੀ ਤਰ੍ਹਾਂ ਭਰੀ ਹੋਈ ਬਾਹਰੀ ਖੋਲ ਪ੍ਰਾਪਤ ਕਰਨ ਦੀ ਪ੍ਰਵਿਰਤੀ ਦੇ ਰੂਪ ਵਿੱਚ ਸਮਝਾਇਆ ਜਾਂਦਾ ਹੈ, ਯਾਨੀ ਕਿ ਨੋਬਲ ਗੈਸ ਵਿਉਂਤ ਪ੍ਰਾਪਤ ਕਰਨਾ। ਆਇਨਿਕ ਯੋਗਿਕ ਬਣਾਉਣ ਵਾਲੇ ਤੱਤ ਬਾਹਰੀ ਖੋਲ ਤੋਂ ਇਲੈਕਟ੍ਰੌਨ ਪ੍ਰਾਪਤ ਕਰਕੇ ਜਾਂ ਗੁਆ ਕੇ ਇਹ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ। ਕਾਰਬਨ ਦੇ ਮਾਮਲੇ ਵਿੱਚ, ਇਸਦੀ ਬਾਹਰੀ ਖੋਲ ਵਿੱਚ ਚਾਰ ਇਲੈਕਟ੍ਰੌਨ ਹਨ ਅਤੇ ਨੋਬਲ ਗੈਸ ਵਿਉਂਤ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਚਾਰ ਇਲੈਕਟ੍ਰੌਨ ਪ੍ਰਾਪਤ ਕਰਨ ਜਾਂ ਗੁਆਉਣ ਦੀ ਲੋੜ ਹੈ। ਜੇਕਰ ਇਹ ਇਲੈਕਟ੍ਰੌਨ ਪ੍ਰਾਪਤ ਕਰੇ ਜਾਂ ਗੁਆਏ -
(i) ਇਹ ਚਾਰ ਇਲੈਕਟ੍ਰੌਨ ਪ੍ਰਾਪਤ ਕਰਕੇ $C^{4-}$ ਐਨਾਇਨ ਬਣਾ ਸਕਦਾ ਹੈ। ਪਰ ਛੇ ਪ੍ਰੋਟੋਨ ਵਾਲੇ ਨਾਭਿਕ ਲਈ ਦਸ ਇਲੈਕਟ੍ਰੌਨਾਂ, ਯਾਨੀ ਕਿ ਚਾਰ ਵਾਧੂ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਫੜ ਕੇ ਰੱਖਣਾ ਮੁਸ਼ਕਲ ਹੋਵੇਗਾ।
(ii) ਇਹ ਚਾਰ ਇਲੈਕਟ੍ਰੌਨ ਗੁਆ ਕੇ $C^{4+}$ ਕੈਟਾਇਨ ਬਣਾ ਸਕਦਾ ਹੈ। ਪਰ ਚਾਰ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਹਟਾਉਣ ਲਈ ਵੱਡੀ ਮਾਤਰਾ ਵਿੱਚ ਊਰਜਾ ਦੀ ਲੋੜ ਹੋਵੇਗੀ, ਜਿਸ ਨਾਲ ਕਾਰਬਨ ਕੈਟਾਇਨ ਰਹਿ ਜਾਵੇਗਾ ਜਿਸਦੇ ਨਾਭਿਕ ਵਿੱਚ ਛੇ ਪ੍ਰੋਟੋਨ ਸਿਰਫ਼ ਦੋ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਫੜ ਕੇ ਰੱਖਦੇ ਹਨ।
ਕਾਰਬਨ ਇਸ ਸਮੱਸਿਆ ਨੂੰ ਆਪਣੇ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਕਾਰਬਨ ਦੇ ਹੋਰ ਪਰਮਾਣੂਆਂ ਜਾਂ ਹੋਰ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਨਾਲ ਸਾਂਝਾ ਕਰਕੇ ਦੂਰ ਕਰਦਾ ਹੈ। ਸਿਰਫ਼ ਕਾਰਬਨ ਹੀ ਨਹੀਂ, ਬਲਕਿ ਬਹੁਤ ਸਾਰੇ ਹੋਰ ਤੱਤ ਵੀ ਇਸ ਤਰੀਕੇ ਨਾਲ ਇਲੈਕਟ੍ਰੌਨ ਸਾਂਝੇ ਕਰਕੇ ਅਣੂ ਬਣਾਉਂਦੇ ਹਨ। ਸਾਂਝੇ ਕੀਤੇ ਗਏ ਇਲੈਕਟ੍ਰੌਨ ਦੋਨਾਂ ਪਰਮਾਣੂਆਂ ਦੀਆਂ ਬਾਹਰੀ ਖੋਲਾਂ ਦੇ ‘ਮਾਲਕ’ ਹੁੰਦੇ ਹਨ ਅਤੇ ਦੋਨਾਂ ਪਰਮਾਣੂਆਂ ਨੂੰ ਨੋਬਲ ਗੈਸ ਵਿਉਂਤ ਪ੍ਰਾਪਤ ਕਰਨ ਵੱਲ ਲੈ ਜਾਂਦੇ ਹਨ। ਕਾਰਬਨ ਦੇ ਯੋਗਿਕਾਂ ਵੱਲ ਜਾਣ ਤੋਂ ਪਹਿਲਾਂ, ਆਓ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੇ ਸਾਂਝੇ ਕਰਨ ਨਾਲ ਬਣੇ ਕੁਝ ਸਧਾਰਨ ਅਣੂਆਂ ਨੂੰ ਵੇਖੀਏ।
ਇਸ ਤਰੀਕੇ ਨਾਲ ਬਣਿਆ ਸਭ ਤੋਂ ਸਧਾਰਨ ਅਣੂ ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਹੈ। ਜਿਵੇਂ ਕਿ ਤੁਸੀਂ ਪਹਿਲਾਂ ਸਿੱਖਿਆ ਹੈ, ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਪਰਮਾਣੂ ਨੰਬਰ 1 ਹੈ। ਇਸ ਲਈ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਇਸਦੀ $K$ ਖੋਲ ਵਿੱਚ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਹੈ ਅਤੇ $K$ ਖੋਲ ਨੂੰ ਭਰਨ ਲਈ ਇਸਨੂੰ ਇੱਕ ਹੋਰ ਇਲੈਕਟ੍ਰੌਨ ਦੀ ਲੋੜ ਹੈ। ਇਸ ਲਈ ਦੋ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂ ਆਪਣੇ ਇਲੈਕਟ੍ਰੌਨ ਸਾਂਝੇ ਕਰਕੇ ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਇੱਕ ਅਣੂ, $H_2$ ਬਣਾਉਂਦੇ ਹਨ। ਇਹ ਹਰੇਕ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂ ਨੂੰ ਨਜ਼ਦੀਕੀ ਨੋਬਲ ਗੈਸ, ਹੀਲੀਅਮ ਦੀ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਉਂਤ ਪ੍ਰਾਪਤ ਕਰਨ ਦਿੰਦਾ ਹੈ, ਜਿਸਦੀ K ਖੋਲ ਵਿੱਚ ਦੋ ਇਲੈਕਟ੍ਰੌਨ ਹਨ। ਅਸੀਂ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਦਰਸਾਉਣ ਲਈ ਬਿੰਦੀਆਂ ਜਾਂ ਕਰਾਸਾਂ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਇਸਨੂੰ ਦਰਸਾ ਸਕਦੇ ਹਾਂ (ਚਿੱਤਰ 4.1)।
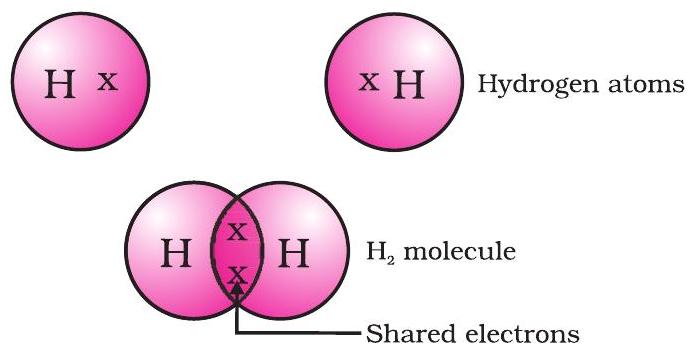
ਚਿੱਤਰ 4.1 ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਇੱਕ ਅਣੂ
ਸਾਂਝੇ ਕੀਤੇ ਗਏ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੇ ਜੋੜੇ ਨੂੰ ਦੋ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਸਿੰਗਲ ਸਹਿਸੰਯੋਜਕ ਬੰਧ ਬਣਾਉਣ ਵਾਲਾ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਇੱਕ ਸਿੰਗਲ ਸਹਿਸੰਯੋਜਕ ਬੰਧ ਨੂੰ ਦੋ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਲਾਈਨ ਦੁਆਰਾ ਵੀ ਦਰਸਾਇਆ ਜਾਂਦਾ ਹੈ, ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 4.2 ਵਿੱਚ ਦਿਖਾਇਆ ਗਿਆ ਹੈ।
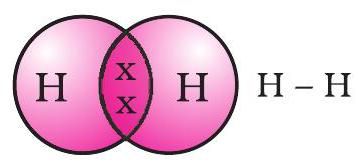
ਚਿੱਤਰ 4.2 ਦੋ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਸਿੰਗਲ ਬੰਧ
ਕਲੋਰੀਨ ਦਾ ਪਰਮਾਣੂ ਨੰਬਰ 17 ਹੈ। ਇਸਦੀ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਉਂਤ ਅਤੇ ਇਸਦੀ ਵੈਲੈਂਸੀ ਕੀ ਹੋਵੇਗੀ? ਕਲੋਰੀਨ ਇੱਕ ਦੋ-ਪਰਮਾਣੂਕ ਅਣੂ, $Cl_2$ ਬਣਾਉਂਦੀ ਹੈ। ਕੀ ਤੁਸੀਂ ਇਸ ਅਣੂ ਲਈ ਇਲੈਕਟ੍ਰੌਨ ਡੌਟ ਬਣਤਰ ਬਣਾ ਸਕਦੇ ਹੋ? ਧਿਆਨ ਦਿਓ ਕਿ ਸਿਰਫ਼ ਵੈਲੈਂਸ ਖੋਲ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਦਰਸਾਉਣ ਦੀ ਲੋੜ ਹੈ।
ਆਕਸੀਜਨ ਦੇ ਮਾਮਲੇ ਵਿੱਚ, ਅਸੀਂ ਦੋ ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਡਬਲ ਬੰਧ ਦਾ ਨਿਰਮਾਣ ਵੇਖਦੇ ਹਾਂ। ਇਹ ਇਸ ਲਈ ਹੈ ਕਿਉਂਕਿ ਆਕਸੀਜਨ ਦੇ ਇੱਕ ਪਰਮਾਣੂ ਦੀ L ਖੋਲ ਵਿੱਚ ਛੇ ਇਲੈਕਟ੍ਰੌਨ ਹਨ (ਆਕਸੀਜਨ ਦਾ ਪਰਮਾਣੂ ਨੰਬਰ ਅੱਠ ਹੈ) ਅਤੇ ਇਸਦੇ ਅੱਠਕ ਪੂਰਾ ਕਰਨ ਲਈ ਇਸਨੂੰ ਦੋ ਹੋਰ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਲੋੜ ਹੈ। ਇਸ ਲਈ ਆਕਸੀਜਨ ਦਾ ਹਰੇਕ ਪਰਮਾਣੂ ਆਕਸੀਜਨ ਦੇ ਇੱਕ ਹੋਰ ਪਰਮਾਣੂ ਨਾਲ ਦੋ ਇਲੈਕਟ੍ਰੌਨ ਸਾਂਝੇ ਕਰਦਾ ਹੈ ਤਾਂ ਕਿ ਸਾਨੂੰ ਚਿੱਤਰ 4.3 ਵਿੱਚ ਦਿਖਾਈ ਗਈ ਬਣਤਰ ਮਿਲ ਸਕੇ। ਹਰੇਕ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਦੁਆਰਾ ਦਿੱਤੇ ਗਏ ਦੋ ਇਲੈਕਟ੍ਰੌਨ ਦੋ ਸਾਂਝੇ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੇ ਬਣਾਉਂਦੇ ਹਨ। ਇਹ ਦੋ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਡਬਲ ਬੰਧ ਬਣਾਉਂਦਾ ਹੈ।
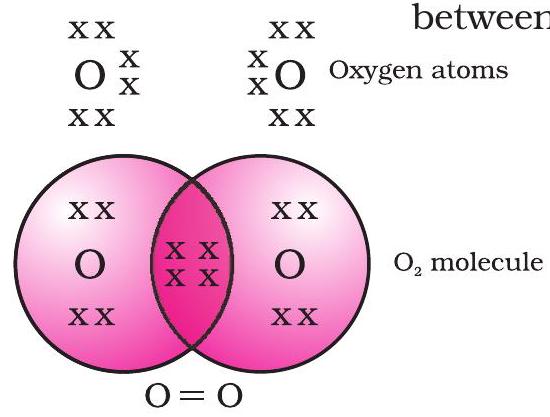
ਚਿੱਤਰ 4.3 ਦੋ ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਡਬਲ ਬੰਧ
ਕੀ ਤੁਸੀਂ ਹੁਣ ਪਾਣੀ ਦਾ ਇੱਕ ਅਣੂ ਦਰਸਾ ਸਕਦੇ ਹੋ ਜੋ ਇੱਕ ਆਕਸੀਜਨ ਪਰਮਾਣੂ ਅਤੇ ਦੋ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਬੰਧਨ ਦੀ ਪ੍ਰਕਿਰਤੀ ਦਿਖਾਉਂਦਾ ਹੈ? ਕੀ ਅਣੂ ਵਿੱਚ ਸਿੰਗਲ ਬੰਧ ਹਨ ਜਾਂ ਡਬਲ ਬੰਧ?
ਨਾਈਟ੍ਰੋਜਨ ਦੇ ਦੋ-ਪਰਮਾਣੂਕ ਅਣੂ ਦੇ ਮਾਮਲੇ ਵਿੱਚ ਕੀ ਹੋਵੇਗਾ? ਨਾਈਟ੍ਰੋਜਨ ਦਾ ਪਰਮਾਣੂ ਨੰਬਰ 7 ਹੈ। ਇਸਦੀ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਉਂਤ ਅਤੇ ਇਸਦੀ ਸੰਯੋਜਨ ਸਮਰੱਥਾ ਕੀ ਹੋਵੇਗੀ? ਇੱਕ ਅੱਠਕ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ, ਨਾਈਟ੍ਰੋਜਨ ਦੇ ਅਣੂ ਵਿੱਚ ਹਰੇਕ ਨਾਈਟ੍ਰੋਜਨ ਪਰਮਾਣੂ ਤਿੰਨ ਇਲੈਕਟ੍ਰੌਨ ਦਿੰਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਤਿੰਨ ਸਾਂਝੇ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੇ ਬਣਦੇ ਹਨ। ਇਹ ਦੋ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਟ੍ਰਿਪਲ ਬੰਧ ਬਣਾਉਂਦਾ ਹੈ। $N_2$ ਦੀ ਇਲੈਕਟ੍ਰੌਨ ਡੌਟ ਬਣਤਰ ਅਤੇ ਦੋ ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਡਬਲ ਬੰਧ ਨੂੰ ਚਿੱਤਰ 4.4 ਵਿੱਚ ਦਰਸਾਏ ਅਨੁਸਾਰ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ।
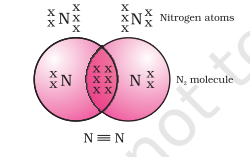
ਚਿੱਤਰ 4.4 ਦੋ ਨਾਈਟ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਟ੍ਰਿਪਲ ਬੰਧ
ਅਮੋਨੀਆ ਦੇ ਇੱਕ ਅਣੂ ਦਾ ਫਾਰਮੂਲਾ $NH_3$ ਹੈ। ਕੀ ਤੁਸੀਂ ਇਸ ਅਣੂ ਲਈ ਇਲੈਕਟ੍ਰੌਨ ਡੌਟ ਬਣਤਰ ਬਣਾ ਸਕਦੇ ਹੋ ਜੋ ਦਿਖਾਉਂਦਾ ਹੈ ਕਿ ਸਾਰੇ ਚਾਰ ਪਰਮਾਣੂ ਨੋਬਲ ਗੈਸ ਵਿਉਂਤ ਕਿਵੇਂ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ? ਕੀ ਅਣੂ ਵਿੱਚ ਸਿੰਗਲ, ਡਬਲ ਜਾਂ ਟ੍ਰਿਪਲ ਬੰਧ ਹੋਣਗੇ?
ਆਓ ਹੁਣ ਮੀਥੇਨ ਨੂੰ ਵੇਖੀਏ, ਜੋ ਕਿ ਕਾਰਬਨ ਦਾ ਇੱਕ ਯੋਗਿਕ ਹੈ। ਮੀਥੇਨ ਨੂੰ ਵਿਆਪਕ ਤੌਰ ‘ਤੇ ਇੱਕ ਬਾਲਣ ਦੇ ਰੂਪ ਵਿੱਚ ਵਰਤਿਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਇਹ ਬਾਇਓ-ਗੈਸ ਅਤੇ ਕੰਪ੍ਰੈੱਸਡ ਨੈਚੁਰਲ ਗੈਸ (CNG) ਦਾ ਇੱਕ ਪ੍ਰਮੁੱਖ ਘਟਕ ਹੈ। ਇਹ ਕਾਰਬਨ ਦੁਆਰਾ ਬਣਾਏ ਗਏ ਸਭ ਤੋਂ ਸਧਾਰਨ ਯੋਗਿਕਾਂ ਵਿੱਚੋਂ ਇੱਕ ਵੀ ਹੈ। ਮੀਥੇਨ ਦਾ ਫਾਰਮੂਲਾ $CH_4$ ਹੈ। ਹਾਈਡ੍ਰੋਜਨ, ਜਿਵੇਂ ਕਿ ਤੁਸੀਂ ਜਾਣਦੇ ਹੋ, ਦੀ ਵੈਲੈਂਸੀ 1 ਹੈ। ਕਾਰਬਨ ਟੈਟ੍ਰਾਵੇਲੈਂਟ ਹੈ ਕਿਉਂਕਿ ਇਸਦੇ ਚਾਰ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨ ਹਨ। ਨੋਬਲ ਗੈਸ ਵਿਉਂਤ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ, ਕਾਰਬਨ ਇਨ੍ਹਾਂ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਚਾਰ ਪਰਮਾਣੂਆਂ ਨਾਲ ਸਾਂਝਾ ਕਰਦਾ ਹੈ ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 4.5 ਵਿੱਚ ਦਿਖਾਇਆ ਗਿਆ ਹੈ।
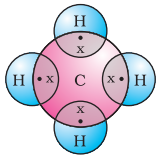
ਚਿੱਤਰ 4.5 ਮੀਥੇਨ ਲਈ ਇਲੈਕਟ੍ਰੌਨ ਡੌਟ ਬਣਤਰ
ਅਜਿਹੇ ਬੰਧ ਜੋ ਦੋ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੇ ਨੂੰ ਸਾਂਝਾ ਕਰਕੇ ਬਣਾਏ ਜਾਂਦੇ ਹਨ, ਉਨ੍ਹਾਂ ਨੂੰ ਸਹਿਸੰਯੋਜਕ ਬੰਧ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਸਹਿਸੰਯੋਜਕ ਬੰਧਿਤ ਅਣੂਆਂ ਵਿੱਚ ਅਣੂ ਦੇ ਅੰਦਰ ਮਜ਼ਬੂਤ ਬੰਧ ਦੇਖੇ ਜਾਂਦੇ ਹਨ, ਪਰ ਅੰਤਰ-ਅਣੂ ਸ਼ਕਤੀਆਂ ਕਮਜ਼ੋਰ ਹੁੰਦੀਆਂ ਹਨ। ਇਹ ਇਨ੍ਹਾਂ ਯੋਗਿਕਾਂ ਦੇ ਘੱਟ ਪਿਘਲਣ ਅਤੇ ਉਬਾਲ ਦੇ ਬਿੰਦੂਆਂ ਨੂੰ ਜਨਮ ਦਿੰਦਾ ਹੈ। ਕਿਉਂਕਿ ਇਲੈਕਟ੍ਰੌਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਸਾਂਝੇ ਕੀਤੇ ਜਾਂਦੇ ਹਨ ਅਤੇ ਕੋਈ ਚਾਰਜਿਤ ਕਣ ਨਹੀਂ ਬਣਦੇ, ਇਸ ਲਈ ਅਜਿਹੇ ਸਹਿਸੰਯੋਜਕ ਯੋਗਿਕ ਆਮ ਤੌਰ ‘ਤੇ ਬਿਜਲੀ ਦੇ ਮਾੜੇ ਸੰਚਾਲਕ ਹੁੰਦੇ ਹਨ।
ਹੋਰ ਜਾਣਨ ਲਈ!
ਕਾਰਬਨ ਦੇ ਅਲੋਟ੍ਰੋਪ
ਤੱਤ ਕਾਰਬਨ ਕੁਦਰਤ ਵਿੱਚ ਵੱਖ-ਵੱਖ ਰੂਪਾਂ ਵਿੱਚ ਮਿਲਦਾ ਹੈ ਜਿਨ੍ਹਾਂ ਦੇ ਭੌਤਿਕ ਗੁਣ ਬਹੁਤ ਵੱਖਰੇ ਹੁੰਦੇ ਹਨ। ਹੀਰਾ ਅਤੇ ਗ੍ਰੈਫਾਈਟ ਦੋਨਾਂ ਦਾ ਨਿਰਮਾਣ ਕਾਰਬਨ ਪਰਮਾਣੂਆਂ ਦੁਆਰਾ ਹੁੰਦਾ ਹੈ, ਫਰਕ ਇਸ ਤਰੀਕੇ ਵਿੱਚ ਹੈ ਜਿਸ ਵਿੱਚ ਕਾਰਬਨ ਪਰਮਾਣੂ ਇੱਕ-ਦੂਜੇ ਨਾਲ ਬੰਧਿਤ ਹੁੰਦੇ ਹਨ। ਹੀਰੇ ਵਿੱਚ, ਹਰੇਕ ਕਾਰਬਨ ਪਰਮਾਣੂ ਚਾਰ ਹੋਰ ਕਾਰਬਨ ਪਰਮਾਣੂਆਂ ਨਾਲ ਬੰਧਿਤ ਹੋ ਕੇ ਇੱਕ ਕਠੋਰ ਤਿੰਨ-ਆਯਾਮੀ ਬਣਤਰ ਬਣਾਉਂਦਾ ਹੈ। ਗ੍ਰੈਫਾਈਟ ਵਿੱਚ, ਹਰੇਕ ਕਾਰਬਨ ਪਰਮਾਣੂ ਇੱਕ ਹੀ ਸਮਤਲ ਵਿੱਚ ਤਿੰਨ ਹੋਰ ਕਾਰਬਨ ਪਰਮਾਣੂਆਂ ਨਾਲ ਬੰਧਿਤ ਹੁੰਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਇੱਕ ਛੇ-ਭੁਜੀ ਸਾਰਣੀ ਬਣਦੀ ਹੈ। ਇਨ੍ਹਾਂ ਬੰਧਾਂ ਵਿੱਚੋਂ ਇੱਕ ਡਬਲ-ਬੰਧ ਹੈ, ਅਤੇ ਇਸ ਤਰ੍ਹਾਂ ਕਾਰਬਨ ਦੀ ਵੈਲੈਂਸੀ ਸੰਤੁਸ਼ਟ ਹੋ ਜਾਂਦੀ ਹੈ। ਗ੍ਰੈਫਾਈਟ ਦੀ ਬਣਤਰ ਛੇ-ਭੁਜੀ ਸਾਰਣੀਆਂ ਨੂੰ ਇੱਕ ਦੇ ਉੱਪਰ ਇੱਕ ਪਰਤਾਂ ਵਿੱਚ ਰੱਖ ਕੇ ਬਣਦੀ ਹੈ।
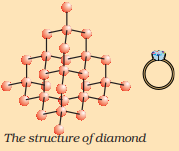
ਹੀਰੇ ਦੀ ਬਣਤਰ
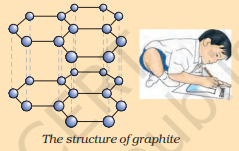
ਗ੍ਰੈਫਾਈਟ ਦੀ ਬਣਤਰ
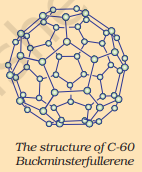
C-60 ਬਕਮਿੰਸਟਰਫੁੱਲੇਰੀਨ ਦੀ ਬਣਤਰ
ਇਹ ਦੋ ਵੱਖਰੀਆਂ ਬਣਤਰਾਂ ਦੇ ਨਤੀਜੇ ਵਜੋਂ ਹੀਰਾ ਅਤੇ ਗ੍ਰੈਫਾਈਟ ਦੇ ਭੌਤਿਕ ਗੁਣ ਬਹੁਤ ਵੱਖਰੇ ਹੋ ਜਾਂਦੇ ਹਨ ਭਾਵੇਂ ਉਨ੍ਹਾਂ ਦੇ ਰਸਾਇਣਕ ਗੁਣ ਇੱਕੋ ਜਿਹੇ ਹਨ। ਹੀਰਾ ਸਭ ਤੋਂ ਸਖ਼ਤ ਪਦ











