ಅಧ್ಯಾಯ 04 ಇಂಗಾಲ ಮತ್ತು ಅದರ ಸಂಯುಕ್ತಗಳು
ಕಳೆದ ಅಧ್ಯಾಯದಲ್ಲಿ, ನಮಗೆ ಮಹತ್ವದ ಅನೇಕ ಸಂಯುಕ್ತಗಳ ಬಗ್ಗೆ ತಿಳಿಯಲು ಸಾಧ್ಯವಾಯಿತು. ಈ ಅಧ್ಯಾಯದಲ್ಲಿ ನಾವು ಇನ್ನೂ ಕೆಲವು ಆಸಕ್ತಿದಾಯಕ ಸಂಯುಕ್ತಗಳು ಮತ್ತು ಅವುಗಳ ಗುಣಲಕ್ಷಣಗಳ ಬಗ್ಗೆ ಅಧ್ಯಯನ ಮಾಡುತ್ತೇವೆ. ಹಾಗೆಯೇ, ಇಂಗಾಲ ಎಂಬ ಮೂಲಧಾತುವಿನ ಬಗ್ಗೆ ಕಲಿಯಲಿದ್ದೇವೆ, ಇದು ಅದರ ಮೂಲಧಾತು ರೂಪದಲ್ಲೂ ಮತ್ತು ಸಂಯುಕ್ತ ರೂಪದಲ್ಲೂ ನಮಗೆ ಅಪಾರ ಮಹತ್ವದ್ದಾಗಿದೆ.
ಕ್ರಿಯಾಶೀಲತೆ 4.1
- ನೀವು ಬೆಳಗಿನಿಂದ ಬಳಸಿದ ಅಥವಾ ಸೇವಿಸಿದ ಹತ್ತು ವಸ್ತುಗಳ ಪಟ್ಟಿಯನ್ನು ಮಾಡಿ.
- ನಿಮ್ಮ ಸಹಪಾಠಿಗಳು ಮಾಡಿದ ಪಟ್ಟಿಗಳೊಂದಿಗೆ ಈ ಪಟ್ಟಿಯನ್ನು ಸಂಕಲಿಸಿ ಮತ್ತು ನಂತರ ವಸ್ತುಗಳನ್ನು ಪಕ್ಕದ ಕೋಷ್ಟಕದಲ್ಲಿ ವಿಂಗಡಿಸಿ.
- ಒಂದಕ್ಕಿಂತ ಹೆಚ್ಚು ವಸ್ತುಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟ ವಸ್ತುಗಳಿದ್ದರೆ, ಅವುಗಳನ್ನು ಕೋಷ್ಟಕದ ಎರಡೂ ಸಂಬಂಧಿತ ಕಾಲಮ್ಗಳಲ್ಲಿ ಇರಿಸಿ.
| ಲೋಹದಿಂದ ಮಾಡಿದ ವಸ್ತುಗಳು | ಲೋಹದಿಂದ ಮಾಡಿದ ವಸ್ತುಗಳು | ಇತರೆ |
|---|---|---|
ನೀವು ತುಂಬಿದ ಮೇಲಿನ ಕೋಷ್ಟಕದ ಕೊನೆಯ ಕಾಲಮ್ನಲ್ಲಿ ಬರುವ ವಸ್ತುಗಳನ್ನು ನೋಡಿ - ಅವುಗಳಲ್ಲಿ ಹೆಚ್ಚಿನವು ಇಂಗಾಲದ ಸಂಯುಕ್ತಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿವೆ ಎಂದು ನಿಮ್ಮ ಶಿಕ್ಷಕರು ನಿಮಗೆ ತಿಳಿಸಲು ಸಾಧ್ಯವಾಗುತ್ತದೆ. ಇದನ್ನು ಪರೀಕ್ಷಿಸಲು ಒಂದು ವಿಧಾನದ ಬಗ್ಗೆ ನೀವು ಯೋಚಿಸಬಹುದೇ? ಇಂಗಾಲವನ್ನು ಹೊಂದಿರುವ ಸಂಯುಕ್ತವನ್ನು ಸುಡುವುದಾದರೆ ಉತ್ಪನ್ನ ಏನಾಗುತ್ತದೆ? ಇದನ್ನು ದೃಢೀಕರಿಸಲು ಯಾವುದೇ ಪರೀಕ್ಷೆಯ ಬಗ್ಗೆ ನಿಮಗೆ ತಿಳಿದಿದೆಯೇ?
ಆಹಾರ, ಬಟ್ಟೆ, ಔಷಧಿಗಳು, ಪುಸ್ತಕಗಳು, ಅಥವಾ ನೀವು ಪಟ್ಟಿ ಮಾಡಿದ ಅನೇಕ ವಸ್ತುಗಳು ಎಲ್ಲವೂ ಈ ಬಹುಮುಖಿ ಮೂಲಧಾತು ಇಂಗಾಲವನ್ನು ಆಧರಿಸಿವೆ. ಇದರ ಜೊತೆಗೆ, ಎಲ್ಲಾ ಜೀವಂತ ರಚನೆಗಳು ಇಂಗಾಲ ಆಧಾರಿತವಾಗಿವೆ. ಭೂಮಿಯ ಕವಚ ಮತ್ತು ವಾತಾವರಣದಲ್ಲಿ ಇರುವ ಇಂಗಾಲದ ಪ್ರಮಾಣ ಸಾಕಷ್ಟು ಕಡಿಮೆಯಾಗಿದೆ. ಭೂಮಿಯ ಕವಚದಲ್ಲಿ ಖನಿಜಗಳ ರೂಪದಲ್ಲಿ (ಕಾರ್ಬೊನೇಟ್ಗಳು, ಹೈಡ್ರೋಜನ್ ಕಾರ್ಬೊನೇಟ್ಗಳು, ಕಲ್ಲಿದ್ದಲು ಮತ್ತು ಪೆಟ್ರೋಲಿಯಂ) ಕೇವಲ $0.02 %$ ಇಂಗಾಲವಿದೆ ಮತ್ತು ವಾತಾವರಣದಲ್ಲಿ $0.03 %$ ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ ಇದೆ. ಪ್ರಕೃತಿಯಲ್ಲಿ ಲಭ್ಯವಿರುವ ಈ ಸಣ್ಣ ಪ್ರಮಾಣದ ಇಂಗಾಲದ ಹೊರತಾಗಿಯೂ, ಇಂಗಾಲದ ಮಹತ್ವ ಅಪಾರವಾಗಿದೆ ಎಂದು ತೋರುತ್ತದೆ. ಈ ಅಧ್ಯಾಯದಲ್ಲಿ, ಇಂಗಾಲವು ನಮಗೆ ಅಷ್ಟು ಮಹತ್ವದ್ದಾಗಿರಲು ಕಾರಣವಾದ ಇಂಗಾಲದ ಗುಣಲಕ್ಷಣಗಳ ಬಗ್ಗೆ ತಿಳಿಯುತ್ತೇವೆ.
4.1 ಇಂಗಾಲದಲ್ಲಿ ಬಂಧನ - ಸಹಸಂಯೋಜಕ ಬಂಧ
ಹಿಂದಿನ ಅಧ್ಯಾಯದಲ್ಲಿ, ನಾವು ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡಿದ್ದೇವೆ. ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳು ಹೆಚ್ಚು ಕರಗುವ ಮತ್ತು ಕುದಿಯುವ ಬಿಂದುಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ ಮತ್ತು ದ್ರಾವಣದಲ್ಲಿ ಅಥವಾ ಕರಗಿದ ಸ್ಥಿತಿಯಲ್ಲಿ ವಿದ್ಯುತ್ ವಾಹಕತೆಯನ್ನು ಹೊಂದಿರುತ್ತವೆ ಎಂದು ನಾವು ನೋಡಿದ್ದೇವೆ. ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಬಂಧನದ ಸ್ವರೂಪವು ಈ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೇಗೆ ವಿವರಿಸುತ್ತದೆ ಎಂಬುದನ್ನು ಸಹ ನಾವು ನೋಡಿದ್ದೇವೆ. ಈಗ ಕೆಲವು ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡೋಣ.
ಹೆಚ್ಚಿನ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳು ವಿದ್ಯುತ್ನ ಕಳಪೆ ವಾಹಕಗಳಾಗಿವೆ, ಇದನ್ನು ನಾವು ಅಧ್ಯಾಯ 2 ರಲ್ಲಿ ನೋಡಿದ್ದೇವೆ. ಕೋಷ್ಟಕ 4.1 ರಲ್ಲಿ ನೀಡಲಾದ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಕುದಿಯುವ ಮತ್ತು ಕರಗುವ ಬಿಂದುಗಳ ದತ್ತಾಂಶದಿಂದ, ಈ ಸಂಯುಕ್ತಗಳು ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳಿಗೆ ಹೋಲಿಸಿದರೆ (ಅಧ್ಯಾಯ 3) ಕಡಿಮೆ ಕರಗುವ ಮತ್ತು ಕುದಿಯುವ ಬಿಂದುಗಳನ್ನು ಹೊಂದಿವೆ ಎಂದು ನಾವು ಕಂಡುಕೊಳ್ಳುತ್ತೇವೆ. ಅಣುಗಳ ನಡುವಿನ ಆಕರ್ಷಣೆಯ ಬಲಗಳು ಬಹಳ ಬಲವಾಗಿರುವುದಿಲ್ಲ ಎಂದು ನಾವು ತೀರ್ಮಾನಿಸಬಹುದು. ಈ ಸಂಯುಕ್ತಗಳು ಹೆಚ್ಚಾಗಿ ವಿದ್ಯುತ್ ಅವಾಹಕಗಳಾಗಿರುವುದರಿಂದ, ಈ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ಬಂಧನವು ಯಾವುದೇ ಅಯಾನುಗಳನ್ನು ಉಂಟುಮಾಡುವುದಿಲ್ಲ ಎಂದು ನಾವು ತೀರ್ಮಾನಿಸಬಹುದು.
ಕೋಷ್ಟಕ 4.1 ಕೆಲವು ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಕರಗುವ ಬಿಂದುಗಳು ಮತ್ತು ಕುದಿಯುವ ಬಿಂದುಗಳು
| ಸಂಯುಕ್ತ | ಕರಗುವ ಬಿಂದು $(\mathbf{K})$ | ಕುದಿಯುವ ಬಿಂದು $(\mathbf{K})$ |
|---|---|---|
| ಅಸಿಟಿಕ್ ಆಮ್ಲ $(CH_3 COOH)$ | 290 | 391 |
| ಕ್ಲೋರೋಫಾರ್ಮ್ $(CHCl_3)$ | 209 | 334 |
| ಈಥನಾಲ್ $(CH_3 CH_2 OH)$ | 156 | 351 |
| ಮೀಥೇನ್ $(CH_4)$ | 90 | 111 |
ಒಂಬತ್ತನೇ ತರಗತಿಯಲ್ಲಿ, ನಾವು ವಿವಿಧ ಮೂಲಧಾತುಗಳ ಸಂಯೋಜನಾ ಸಾಮರ್ಥ್ಯ ಮತ್ತು ಅದು ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯ ಮೇಲೆ ಹೇಗೆ ಅವಲಂಬಿತವಾಗಿದೆ ಎಂಬುದನ್ನು ಕಲಿತಿದ್ದೇವೆ. ಈಗ ಇಂಗಾಲದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸವನ್ನು ನೋಡೋಣ. ಇಂಗಾಲದ ಪರಮಾಣು ಸಂಖ್ಯೆ 6. ಇಂಗಾಲದ ವಿವಿಧ ಕಕ್ಷೆಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿತರಣೆ ಏನಾಗಿರುತ್ತದೆ? ಇಂಗಾಲಕ್ಕೆ ಎಷ್ಟು ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಇರುತ್ತವೆ?
ಮೂಲಧಾತುಗಳ ಕ್ರಿಯಾಶೀಲತೆಯು ಸಂಪೂರ್ಣವಾಗಿ ತುಂಬಿದ ಹೊರಗಿನ ಕಕ್ಷೆಯನ್ನು ಪಡೆಯುವ ಪ್ರವೃತ್ತಿಯಾಗಿ ವಿವರಿಸಲ್ಪಡುತ್ತದೆ ಎಂದು ನಮಗೆ ತಿಳಿದಿದೆ, ಅಂದರೆ, ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸವನ್ನು ಪಡೆಯುವುದು. ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳನ್ನು ರೂಪಿಸುವ ಮೂಲಧಾತುಗಳು ಹೊರಗಿನ ಕಕ್ಷೆಯಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಗಳಿಸುವುದರಿಂದ ಅಥವಾ ಕಳೆದುಕೊಳ್ಳುವುದರಿಂದ ಇದನ್ನು ಸಾಧಿಸುತ್ತವೆ. ಇಂಗಾಲದ ಸಂದರ್ಭದಲ್ಲಿ, ಅದರ ಹೊರಗಿನ ಕಕ್ಷೆಯಲ್ಲಿ ನಾಲ್ಕು ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿವೆ ಮತ್ತು ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸವನ್ನು ಪಡೆಯಲು ನಾಲ್ಕು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಗಳಿಸಬೇಕು ಅಥವಾ ಕಳೆದುಕೊಳ್ಳಬೇಕು. ಅದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಗಳಿಸಿದರೆ ಅಥವಾ ಕಳೆದುಕೊಂಡರೆ -
(i) ಅದು ನಾಲ್ಕು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಗಳಿಸಿ $C^{4-}$ ಆನಯನವನ್ನು ರೂಪಿಸಬಹುದು. ಆದರೆ ಆರು ಪ್ರೋಟಾನ್ಗಳಿರುವ ನ್ಯೂಕ್ಲಿಯಸ್ಗೆ ಹತ್ತು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು, ಅಂದರೆ, ನಾಲ್ಕು ಹೆಚ್ಚುವರಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಿಡಿದಿಟ್ಟುಕೊಳ್ಳುವುದು ಕಷ್ಟಕರವಾಗಿರುತ್ತದೆ.
(ii) ಅದು ನಾಲ್ಕು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಕಳೆದುಕೊಂಡು $C^{4+}$ ಕ್ಯಾಟಯನ್ ಅನ್ನು ರೂಪಿಸಬಹುದು. ಆದರೆ ನಾಲ್ಕು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ತೆಗೆದುಹಾಕಲು ದೊಡ್ಡ ಪ್ರಮಾಣದ ಶಕ್ತಿ ಅಗತ್ಯವಿರುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಇಂಗಾಲ ಕ್ಯಾಟಯನ್ ಅದರ ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿ ಆರು ಪ್ರೋಟಾನ್ಗಳೊಂದಿಗೆ ಕೇವಲ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಿಡಿದಿಟ್ಟುಕೊಳ್ಳುತ್ತದೆ.
ಇಂಗಾಲವು ತನ್ನ ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಇಂಗಾಲದ ಇತರ ಪರಮಾಣುಗಳೊಂದಿಗೆ ಅಥವಾ ಇತರ ಮೂಲಧಾತುಗಳ ಪರಮಾಣುಗಳೊಂದಿಗೆ ಹಂಚಿಕೊಳ್ಳುವ ಮೂಲಕ ಈ ಸಮಸ್ಯೆಯನ್ನು ನಿವಾರಿಸುತ್ತದೆ. ಕೇವಲ ಇಂಗಾಲವಲ್ಲ, ಆದರೆ ಅನೇಕ ಇತರ ಮೂಲಧಾತುಗಳು ಈ ರೀತಿಯಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಂಚಿಕೊಳ್ಳುವ ಮೂಲಕ ಅಣುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ. ಹಂಚಿಕೊಂಡ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಎರಡೂ ಪರಮಾಣುಗಳ ಹೊರಗಿನ ಕಕ್ಷೆಗಳಿಗೆ ‘ಸೇರಿದವು’ ಮತ್ತು ಎರಡೂ ಪರಮಾಣುಗಳು ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸವನ್ನು ಪಡೆಯಲು ಕಾರಣವಾಗುತ್ತವೆ. ಇಂಗಾಲದ ಸಂಯುಕ್ತಗಳ ಬಗ್ಗೆ ಹೋಗುವ ಮೊದಲು, ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯಿಂದ ರೂಪುಗೊಂಡ ಕೆಲವು ಸರಳ ಅಣುಗಳನ್ನು ನೋಡೋಣ.
ಈ ರೀತಿಯಲ್ಲಿ ರೂಪುಗೊಂಡ ಸರಳ ಅಣುವು ಹೈಡ್ರೋಜನ್ನದಾಗಿದೆ. ನೀವು ಈಗಾಗಲೇ ಕಲಿತಂತೆ, ಹೈಡ್ರೋಜನ್ನ ಪರಮಾಣು ಸಂಖ್ಯೆ 1. ಆದ್ದರಿಂದ ಹೈಡ್ರೋಜನ್ನಲ್ಲಿ ಅದರ $K$ ಕಕ್ಷೆಯಲ್ಲಿ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಇರುತ್ತದೆ ಮತ್ತು $K$ ಕಕ್ಷೆಯನ್ನು ತುಂಬಲು ಇನ್ನೂ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಅಗತ್ಯವಿರುತ್ತದೆ. ಆದ್ದರಿಂದ ಎರಡು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳು ತಮ್ಮ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಂಚಿಕೊಂಡು ಹೈಡ್ರೋಜನ್ ಅಣುವನ್ನು ರೂಪಿಸುತ್ತವೆ, $H_2$. ಇದು ಪ್ರತಿ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುವಿಗೆ ಹೆಲಿಯಂ ಎಂಬ ಹತ್ತಿರದ ಉದಾತ್ತ ಅನಿಲದ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸವನ್ನು ಪಡೆಯಲು ಅನುಮತಿಸುತ್ತದೆ, ಇದರ K ಕಕ್ಷೆಯಲ್ಲಿ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿವೆ. ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪ್ರತಿನಿಧಿಸಲು ಚುಕ್ಕೆಗಳು ಅಥವಾ ಶಿಲುಬೆಗಳನ್ನು ಬಳಸಿಕೊಂಡು ಇದನ್ನು ನಾವು ಚಿತ್ರಿಸಬಹುದು (ಚಿತ್ರ 4.1).
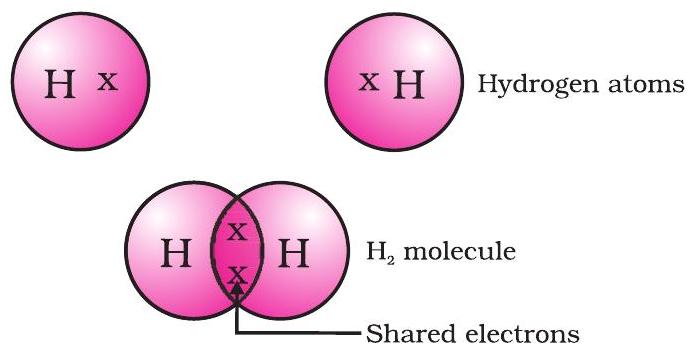
ಚಿತ್ರ 4.1 ಹೈಡ್ರೋಜನ್ನ ಅಣು
ಹಂಚಿಕೊಂಡ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯು ಎರಡು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಏಕ ಸಹಸಂಯೋಜಕ ಬಂಧವನ್ನು ರೂಪಿಸುತ್ತದೆ ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ. ಒಂದು ಏಕ ಸಹಸಂಯೋಜಕ ಬಂಧವನ್ನು ಎರಡು ಪರಮಾಣುಗಳ ನಡುವಿನ ರೇಖೆಯಿಂದಲೂ ಸಹ ಪ್ರತಿನಿಧಿಸಲಾಗುತ್ತದೆ, ಇದನ್ನು ಚಿತ್ರ 4.2 ರಲ್ಲಿ ತೋರಿಸಲಾಗಿದೆ.
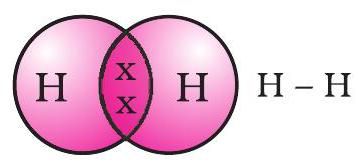
ಚಿತ್ರ 4.2 ಎರಡು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳ ನಡುವಿನ ಏಕ ಬಂಧ
ಕ್ಲೋರಿನ್ನ ಪರಮಾಣು ಸಂಖ್ಯೆ 17. ಅದರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸ ಮತ್ತು ಅದರ ಸಂಯೋಜಕತೆ ಏನಾಗಿರುತ್ತದೆ? ಕ್ಲೋರಿನ್ ಒಂದು ದ್ವಿಪರಮಾಣುಕ ಅಣುವನ್ನು ರೂಪಿಸುತ್ತದೆ, $Cl_2$. ಈ ಅಣುವಿಗೆ ನೀವು ಎಲೆಕ್ಟ್ರಾನ್ ಚುಕ್ಕೆ ರಚನೆಯನ್ನು ಬರೆಯಬಹುದೇ? ಸಂಯೋಜಕತಾ ಕಕ್ಷೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಮಾತ್ರ ಚಿತ್ರಿಸಬೇಕು ಎಂಬುದನ್ನು ಗಮನಿಸಿ.
ಆಕ್ಸಿಜನ್ನ ಸಂದರ್ಭದಲ್ಲಿ, ನಾವು ಎರಡು ಆಕ್ಸಿಜನ್ ಪರಮಾಣುಗಳ ನಡುವೆ ದ್ವಿ ಬಂಧದ ರಚನೆಯನ್ನು ನೋಡುತ್ತೇವೆ. ಇದಕ್ಕೆ ಕಾರಣ, ಆಕ್ಸಿಜನ್ ಪರಮಾಣುವಿನ L ಕಕ್ಷೆಯಲ್ಲಿ ಆರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿವೆ (ಆಕ್ಸಿಜನ್ನ ಪರಮಾಣು ಸಂಖ್ಯೆ ಎಂಟು) ಮತ್ತು ಅದರ ಅಷ್ಟಕವನ್ನು ಪೂರ್ಣಗೊಳಿಸಲು ಇನ್ನೂ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಅಗತ್ಯವಿರುತ್ತದೆ. ಆದ್ದರಿಂದ ಪ್ರತಿ ಆಕ್ಸಿಜನ್ ಪರಮಾಣುವು ಇನ್ನೊಂದು ಆಕ್ಸಿಜನ್ ಪರಮಾಣುವಿನೊಂದಿಗೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಂಚಿಕೊಳ್ಳುತ್ತದೆ, ಇದು ನಮಗೆ ಚಿತ್ರ 4.3 ರಲ್ಲಿ ತೋರಿಸಿರುವ ರಚನೆಯನ್ನು ನೀಡುತ್ತದೆ. ಪ್ರತಿ ಆಕ್ಸಿಜನ್ ಪರಮಾಣುವಿನಿಂದ ಕೊಡುಗೆಯಾಗುವ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಎರಡು ಹಂಚಿಕೊಂಡ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ. ಇದು ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ದ್ವಿ ಬಂಧವನ್ನು ರೂಪಿಸುತ್ತದೆ ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ.
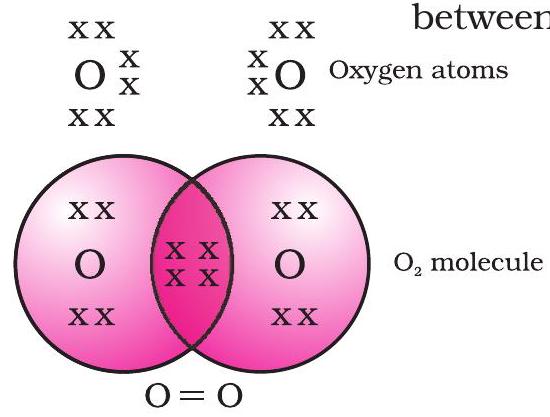
ಚಿತ್ರ 4.3 ಎರಡು ಆಕ್ಸಿಜನ್ ಪರಮಾಣುಗಳ ನಡುವಿನ ದ್ವಿ ಬಂಧ
ಈಗ ನೀವು ಒಂದು ಆಕ್ಸಿಜನ್ ಪರಮಾಣು ಮತ್ತು ಎರಡು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳ ನಡುವಿನ ಬಂಧನದ ಸ್ವರೂಪವನ್ನು ತೋರಿಸುವ ನೀರಿನ ಅಣುವನ್ನು ಚಿತ್ರಿಸಬಹುದೇ? ಅಣುವು ಏಕ ಬಂಧಗಳನ್ನು ಅಥವಾ ದ್ವಿ ಬಂಧಗಳನ್ನು ಹೊಂದಿದೆಯೇ?
ನೈಟ್ರೋಜನ್ನ ದ್ವಿಪರಮಾಣುಕ ಅಣುವಿನ ಸಂದರ್ಭದಲ್ಲಿ ಏನಾಗುತ್ತದೆ? ನೈಟ್ರೋಜನ್ನ ಪರಮಾಣು ಸಂಖ್ಯೆ 7. ಅದರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸ ಮತ್ತು ಅದರ ಸಂಯೋಜನಾ ಸಾಮರ್ಥ್ಯ ಏನಾಗಿರುತ್ತದೆ? ಅಷ್ಟಕವನ್ನು ಪಡೆಯಲು, ನೈಟ್ರೋಜನ್ ಅಣುವಿನಲ್ಲಿನ ಪ್ರತಿ ನೈಟ್ರೋಜನ್ ಪರಮಾಣುವು ಮೂರು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಕೊಡುಗೆಯಾಗಿ ನೀಡುತ್ತದೆ, ಇದು ಮೂರು ಹಂಚಿಕೊಂಡ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. ಇದು ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ತ್ರಿ ಬಂಧವನ್ನು ರೂಪಿಸುತ್ತದೆ ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ ಚಿತ್ರ 4.3 ಎರಡು ಆಕ್ಸಿಜನ್ ಪರಮಾಣುಗಳ ನಡುವಿನ ದ್ವಿ ಬಂಧ $N_2$ ನ ಎಲೆಕ್ಟ್ರಾನ್ ಚುಕ್ಕೆ ರಚನೆ ಮತ್ತು ಅದರ ತ್ರಿ ಬಂಧವನ್ನು ಚಿತ್ರ 4.4 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ಚಿತ್ರಿಸಬಹುದು.
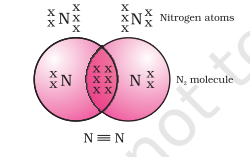
ಚಿತ್ರ 4.4 ಎರಡು ನೈಟ್ರೋಜನ್ ಪರಮಾಣುಗಳ ನಡುವಿನ ತ್ರಿ ಬಂಧ
ಅಮೋನಿಯಾ ಅಣುವಿನ ಸೂತ್ರ $NH_3$. ಎಲ್ಲಾ ನಾಲ್ಕು ಪರಮಾಣುಗಳು ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸವನ್ನು ಹೇಗೆ ಸಾಧಿಸುತ್ತವೆ ಎಂಬುದನ್ನು ತೋರಿಸುವ ಈ ಅಣುವಿಗೆ ನೀವು ಎಲೆಕ್ಟ್ರಾನ್ ಚುಕ್ಕೆ ರಚನೆಯನ್ನು ಬರೆಯಬಹುದೇ? ಅಣುವು ಏಕ, ದ್ವಿ ಅಥವಾ ತ್ರಿ ಬಂಧಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆಯೇ?
ಈಗ ನಾವು ಮೀಥೇನ್ ಅನ್ನು ನೋಡೋಣ, ಇದು ಇಂಗಾಲದ ಸಂಯುಕ್ತವಾಗಿದೆ. ಮೀಥೇನ್ ಅನ್ನು ವ್ಯಾಪಕವಾಗಿ ಇಂಧನವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ ಮತ್ತು ಇದು ಬಯೋ-ಗ್ಯಾಸ್ ಮತ್ತು ಸಂಕುಚಿತ ನೈಸರ್ಗಿಕ ಅನಿಲದ (ಸಿಎನ್ಜಿ) ಒಂದು ಪ್ರಮುಖ ಘಟಕವಾಗಿದೆ. ಇದು ಇಂಗಾಲದಿಂದ ರೂಪುಗೊಂಡ ಸರಳ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ. ಮೀಥೇನ್ ಸೂತ್ರ $CH_4$ ಅನ್ನು ಹೊಂದಿದೆ. ನಿಮಗೆ ತಿಳಿದಿರುವಂತೆ, ಹೈಡ್ರೋಜನ್ನ ಸಂಯೋಜಕತೆ 1. ಇಂಗಾಲವು ಚತುಃಸಂಯೋಜಕವಾಗಿದೆ ಏಕೆಂದರೆ ಅದು ನಾಲ್ಕು ಸಂಯೋಜಕತಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿದೆ. ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸವನ್ನು ಸಾಧಿಸಲು, ಇಂಗಾಲವು ಈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಚಿತ್ರ 4.5 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ನಾಲ್ಕು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳೊಂದಿಗೆ ಹಂಚಿಕೊಳ್ಳುತ್ತದೆ.
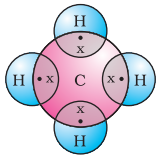
ಚಿತ್ರ 4.5 ಮೀಥೇನ್ಗಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ ಚುಕ್ಕೆ ರಚನೆ
ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯ ಹಂಚಿಕೆಯಿಂದ ರೂಪುಗೊಂಡ ಇಂತಹ ಬಂಧಗಳನ್ನು ಸಹಸಂಯೋಜಕ ಬಂಧಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸಹಸಂಯೋಜಕವಾಗಿ ಬಂಧಿತ ಅಣುಗಳು ಅಣುವಿನೊಳಗೆ ಬಲವಾದ ಬಂಧಗಳನ್ನು ಹೊಂದಿರುವುದು ಕಂಡುಬರುತ್ತದೆ, ಆದರೆ ಅಂತರ-ಅಣು ಬಲಗಳು ದುರ್ಬಲವಾಗಿರುತ್ತವೆ. ಇದು ಈ ಸಂಯುಕ್ತಗಳ ಕಡಿಮೆ ಕರಗುವ ಮತ್ತು ಕುದಿಯುವ ಬಿಂದುಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪರಮಾಣುಗಳ ನಡುವೆ ಹಂಚಿಕೊಳ್ಳಲಾಗುತ್ತದೆ ಮತ್ತು ಯಾವುದೇ ಆವೇಶಿತ ಕಣಗಳು ರೂಪುಗೊಳ್ಳುವುದಿಲ್ಲವಾದ್ದರಿಂದ, ಅಂತಹ ಸಹಸಂಯೋಜಕ ಸಂಯುಕ್ತಗಳು ಸಾಮಾನ್ಯವಾಗಿ ವಿದ್ಯುತ್ನ ಕಳಪೆ ವಾಹಕಗಳಾಗಿರುತ್ತವೆ.
ಇನ್ನಷ್ಟು ತಿಳಿಯಿರಿ!
ಇಂಗಾಲದ ಅಪರೂಪ ರೂಪಗಳು
ಮೂಲಧಾತು ಇಂಗಾಲವು ವ್ಯಾಪಕವಾಗಿ ಬದಲಾಗುವ ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳೊಂದಿಗೆ ಪ್ರಕೃತಿಯಲ್ಲಿ ವಿವಿಧ ರೂಪಗಳಲ್ಲಿ ಕಂಡುಬರುತ್ತದೆ. ವಜ್ರ ಮತ್ತು ಗ್ರಾಫೈಟ್ ಎರಡೂ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಂದ ರೂಪುಗೊಂಡಿವೆ, ಇಂಗಾಲದ ಪರಮಾಣುಗಳು ಪರಸ್ಪರ ಹೇಗೆ ಬಂಧಿತವಾಗಿವೆ ಎಂಬುದರಲ್ಲಿ ವ್ಯತ್ಯಾಸವಿದೆ. ವಜ್ರದಲ್ಲಿ, ಪ್ರತಿ ಇಂಗಾಲದ ಪರಮಾಣುವು ನಾಲ್ಕು ಇತರ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಗೆ ಬಂಧಿತವಾಗಿರುತ್ತದೆ, ಇದು ಕಟ್ಟುನಿಟ್ಟಾದ ತ್ರಿಮಾಪಕ ರಚನೆಯನ್ನು ರೂಪಿಸುತ್ತದೆ. ಗ್ರಾಫೈಟ್ನಲ್ಲಿ, ಪ್ರತಿ ಇಂಗಾಲದ ಪರಮಾಣುವು ಅದೇ ಸಮತಲದಲ್ಲಿ ಮೂರು ಇತರ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಗೆ ಬಂಧಿತವಾಗಿರುತ್ತದೆ, ಇದು ಷಡ್ಭುಜಾಕೃತಿಯ ಜೋಡಣೆಯನ್ನು ನೀಡುತ್ತದೆ. ಈ ಬಂಧಗಳಲ್ಲಿ ಒಂದು ದ್ವಿ-ಬಂಧವಾಗಿದೆ, ಮತ್ತು ಆದ್ದರಿಂದ ಇಂಗಾಲದ ಸಂಯೋಜಕತೆ ತೃಪ್ತಿಗೊಳ್ಳುತ್ತದೆ. ಗ್ರಾಫೈಟ್ ರಚನೆಯು ಷಡ್ಭುಜಾಕೃತಿಯ ಜೋಡಣೆಗಳನ್ನು ಪದರಗಳಲ್ಲಿ ಒಂದರ ಮೇಲೊಂದರಂತೆ ಇರಿಸುವ ಮೂಲಕ ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
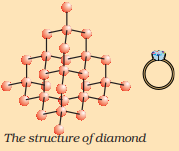
ವಜ್ರದ ರಚನೆ
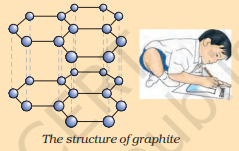
ಗ್ರಾಫೈಟ್ನ ರಚನೆ
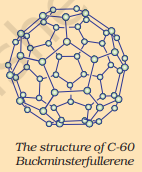
ಸಿ-60 ಬಕ್ಮಿನ್ಸ್ಟರ್ಫುಲ್ಲರೀನ್ನ ರಚನೆ
ಈ ಎರಡು ವಿಭಿನ್ನ ರಚನೆಗಳು ವಜ್ರ ಮತ್ತು ಗ್ರಾಫೈಟ್ ಅವುಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು ಒಂದೇ ಆಗಿದ್ದರೂ ಸಹ ಬಹಳ ವಿಭಿನ್ನ ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೊಂದಲು ಕಾರಣವಾಗುತ್ತವೆ. ವಜ್ರವು ತಿಳಿದಿರುವ ಅತ್ಯಂತ ಗಟ್ಟಿಯಾದ ವಸ್ತುವಾಗಿದೆ ಆದರೆ ಗ್ರಾಫೈಟ್ ನುಣುಪಾಗಿ ಮತ್ತು ಜಾರುವಂತಿರುತ್ತದೆ. ಗ್ರಾಫೈಟ್ ಸಹ ನೀವು ಹಿಂದಿನ ಅಧ್ಯಾಯದಲ್ಲಿ ಅಧ್ಯಯನ ಮಾಡಿದ ಇತರ ಅಲೋಹಗಳಿಗಿಂತ ಭಿನ್ನವಾಗಿ ವಿದ್ಯುತ್ನ ಅತ್ಯುತ್ತಮ ವಾಹಕವಾಗಿದೆ.
ಶುದ್ಧ ಇಂಗಾಲವನ್ನು ಅತ್ಯಂತ ಹೆಚ್ಚಿನ ಒತ್ತಡ ಮತ್ತು ತಾಪಮಾನಕ್ಕೆ ಒಳಪಡಿಸುವ ಮೂಲಕ ವಜ್ರಗಳನ್ನು ಸಂಶ್ಲೇಷಿಸಬಹುದು. ಈ ಸಂಶ್ಲೇಷಿತ ವಜ್ರಗಳು ಸಣ್ಣವಾಗಿರುತ್ತವೆ ಆದರೆ ಇವು ನೈಸರ್ಗಿಕ ವಜ್ರಗಳಿಂದ ಪ್ರತ್ಯೇಕಿಸಲಾಗುವುದಿಲ್ಲ.
ಫುಲ್ಲರೀನ್ಗಳು ಇಂಗಾಲದ ಅಪರೂಪ ರೂಪಗಳ ಇನ್ನೊಂದು ವರ್ಗವನ್ನು ರೂಪಿಸುತ್ತವೆ. ಗುರುತಿಸಲಾದ ಮೊದಲನೆಯದು ಸಿ-60 ಆಗಿತ್ತು, ಇದು ಫುಟ್ಬಾಲ್ನ ಆಕಾರದಲ್ಲಿ ಇಂಗಾಲದ ಪರಮಾಣುಗಳನ್ನು ಜೋಡಿಸಲಾಗಿದೆ. ಇದು ಯುಎಸ್ ವಾಸ್ತುಶಿಲ್ಪಿ ಬಕ್ಮಿನ್ಸ್ಟರ್ ಫುಲ್ಲರ್ ವಿನ್ಯಾಸಗೊಳಿಸಿದ ಜಿಯೋಡೆಸಿಕ್ ಗುಮ್ಮಟದಂತೆ ಕಾಣುತ್ತದೆ, ಆದ್ದರಿಂದ ಅಣುವನ್ನು ಫುಲ್ಲರೀನ್ ಎಂದು ಹೆಸರಿಸಲಾಯಿತು.
4.2 ಇಂಗಾಲದ ಬಹುಮುಖಿ ಸ್ವರೂಪ
ವಿವಿಧ ಮೂಲಧಾತುಗಳು ಮತ್ತು ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯಿಂದ ಸಹಸಂಯೋಜಕ ಬಂಧಗಳ ರಚನೆಯನ್ನು ನಾವು ನೋಡಿದ್ದೇವೆ. ನಾವು ಸರಳ ಇಂಗಾಲ ಸಂಯುಕ್ತವಾದ ಮೀಥೇನ್ನ ರಚನೆಯನ್ನು ಸಹ ನೋಡಿದ್ದೇವೆ. ಅಧ್ಯಾಯದ ಆರಂಭದಲ್ಲಿ, ನಾವು ಬಳಸುವ ಎಷ್ಟು ವಸ್ತುಗಳು ಇಂಗಾಲವನ್ನು ಹೊಂದಿವೆ ಎಂಬುದನ್ನು ನಾವು ನೋಡಿದ್ದೇವೆ. ವಾಸ್ತವವಾಗಿ, ನಾವೇ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದ್ದೇವೆ. ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರಿಗೆ ತಿಳಿದಿರುವ ಸೂತ್ರಗಳನ್ನು ಹೊಂದಿರುವ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಸಂಖ್ಯೆಯನ್ನು ಇತ್ತೀಚೆಗೆ ಮಿಲಿಯನ್ಗಳಲ್ಲಿ ಅಂದಾಜಿಸಲಾಗಿದೆ! ಇದು ಎಲ್ಲಾ ಇತರ ಮೂಲಧಾತುಗಳು ಒಟ್ಟಿಗೆ ರೂಪಿಸಿದ ಸಂಯುಕ್ತಗಳನ್ನು ದೊಡ್ಡ ಅಂತರದಿಂದ ಮೀರುತ್ತದೆ. ಈ ಗುಣಲಕ್ಷಣವು ಇಂಗಾಲದಲ್ಲಿ ಮಾತ್ರ ಮತ್ತು ಯಾವುದೇ ಇತರ ಮೂಲಧಾತುವಿನಲ್ಲಿ ಕಂಡುಬರುವುದು ಏಕೆ? ಸಹಸಂಯೋಜಕ ಬಂಧದ ಸ್ವರೂಪವು ಇಂಗಾಲವು ಬಹಳಷ್ಟು ಸಂಯುಕ್ತಗಳನ್ನು ರೂಪಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ. ಇಂಗಾಲದ ಸಂದರ್ಭದಲ್ಲಿ ಗಮನಿಸಿದ ಎರಡು ಅಂಶಗಳು -
(i) ಇಂಗಾಲವು ಇತರ ಇಂಗಾಲದ ಪರಮಾಣುಗಳೊಂದಿಗೆ ಬಂಧಗಳನ್ನು ರೂಪಿಸುವ ಅನನ್ಯ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿದೆ, ಇದು ದೊಡ್ಡ ಅಣುಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಈ ಗುಣವನ್ನು ಸರಣೀಕರಣ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಈ ಸಂಯುಕ್ತಗಳು ಇಂಗಾಲದ ದೀರ್ಘ ಸರಪಳಿಗಳು, ಇಂಗಾಲದ ಕವಲೊಡೆದ ಸರಪಳಿಗಳು ಅಥವಾ ಉಂಗುರಗಳಲ್ಲಿ ಜೋಡಿಸಲಾದ ಇಂಗಾಲದ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರಬಹುದು. ಇದರ ಜೊತೆಗೆ











