அத்தியாயம் 04 கார்பன் மற்றும் அதன் சேர்மங்கள்
=== முன்னுரை புலங்கள் === தலைப்பு: அத்தியாயம் 04 கார்பன் மற்றும் அதன் சேர்மங்கள்
=== உடல் ===
கடந்த அத்தியாயத்தில், நமக்கு முக்கியமான பல சேர்மங்களைப் பற்றி அறிந்தோம். இந்த அத்தியாயத்தில் இன்னும் சில சுவாரஸ்யமான சேர்மங்கள் மற்றும் அவற்றின் பண்புகளைப் பற்றி படிப்போம். மேலும், கார்பன் என்ற தனிமத்தைப் பற்றியும் கற்றுக்கொள்வோம், இது அதன் தனிம வடிவிலும் சேர்ம வடிவிலும் நமக்கு மிகுந்த முக்கியத்துவம் வாய்ந்த ஒரு தனிமமாகும்.
செயல்பாடு 4.1
- காலையிலிருந்து நீங்கள் பயன்படுத்திய அல்லது உட்கொண்ட பத்து பொருட்களின் பட்டியலை உருவாக்கவும்.
- உங்கள் வகுப்புத் தோழர்கள் உருவாக்கிய பட்டியல்களுடன் இந்த பட்டியலை இணைத்து, பின்னர் பொருட்களை அடுத்துள்ள அட்டவணையில் வரிசைப்படுத்தவும்.
- ஒன்றுக்கு மேற்பட்ட பொருட்களால் ஆன பொருட்கள் இருந்தால், அவற்றை அட்டவணையின் தொடர்புடைய இரு நெடுவரிசைகளிலும் வைக்கவும்.
| உலோகத்தால் ஆன பொருட்கள் | உலோகத்தால் ஆன பொருட்கள் | மற்றவை |
|---|---|---|
நீங்கள் நிரப்பிய மேலே உள்ள அட்டவணையின் கடைசி நெடுவரிசையில் வரும் பொருட்களைப் பாருங்கள் - அவற்றில் பெரும்பாலானவை கார்பன் சேர்மங்களால் ஆனவை என்பதை உங்கள் ஆசிரியர் உங்களுக்குச் சொல்ல முடியும். இதைச் சோதிக்க ஒரு முறையைப் பற்றி நீங்கள் யோசிக்க முடியுமா? கார்பன் கொண்ட ஒரு சேர்மம் எரிக்கப்பட்டால் என்ன விளைபொருள் கிடைக்கும்? இதை உறுதிப்படுத்த எந்த சோதனை உங்களுக்குத் தெரியுமா?
உணவு, உடைகள், மருந்துகள், புத்தகங்கள் அல்லது நீங்கள் பட்டியலிட்ட பல பொருட்கள் அனைத்தும் இந்த பல்துறை தனிமமான கார்பனை அடிப்படையாகக் கொண்டவை. கூடுதலாக, அனைத்து உயிரின அமைப்புகளும் கார்பன் அடிப்படையிலானவை. பூமியின் மேலோட்டிலும் வளிமண்டலத்திலும் உள்ள கார்பனின் அளவு மிகவும் குறைவு. பூமியின் மேலோட்டில் $0.02 %$ கார்பன் மட்டுமே கனிமங்களின் வடிவில் (கார்பனேட்டுகள், ஹைட்ரஜன் கார்பனேட்டுகள், நிலக்கரி மற்றும் பெட்ரோலியம் போன்றவை) உள்ளது மற்றும் வளிமண்டலத்தில் $0.03 %$ கார்பன் டை ஆக்சைடு உள்ளது. இயற்கையில் கிடைக்கும் இந்த சிறிய அளவு கார்பன் இருந்தபோதிலும், கார்பனின் முக்கியத்துவம் மிகப்பெரியதாகத் தெரிகிறது. இந்த அத்தியாயத்தில், கார்பன் நமக்கு மிகவும் முக்கியமானதாக இருக்கும் கார்பனின் பண்புகளைப் பற்றி அறிந்து கொள்வோம்.
4.1 கார்பனில் பிணைப்பு - சக பிணைப்பு
முந்தைய அத்தியாயத்தில், அயனி சேர்மங்களின் பண்புகளைப் படித்தோம். அயனி சேர்மங்கள் உயர்ந்த உருகு மற்றும் கொதிநிலைகளைக் கொண்டுள்ளன மற்றும் கரைசலில் அல்லது உருகிய நிலையில் மின்சாரத்தைக் கடத்துகின்றன என்பதைக் கண்டோம். மேலும் அயனி சேர்மங்களில் உள்ள பிணைப்பின் தன்மை இந்த பண்புகளை எவ்வாறு விளக்குகிறது என்பதையும் கண்டோம். இப்போது சில கார்பன் சேர்மங்களின் பண்புகளைப் படிப்போம்.
அத்தியாயம் 2 இல் பார்த்தது போல, பெரும்பாலான கார்பன் சேர்மங்கள் மின்சாரத்தின் மோசமான கடத்திகளாகும். கார்பன் சேர்மங்களின் கொதிநிலை மற்றும் உருகு நிலைகள் குறித்த அட்டவணை 4.1 இல் கொடுக்கப்பட்ட தரவுகளிலிருந்து, இந்த சேர்மங்கள் அயனி சேர்மங்களுடன் (அத்தியாயம் 3) ஒப்பிடும்போது குறைந்த உருகு மற்றும் கொதிநிலைகளைக் கொண்டுள்ளன என்பதைக் காண்கிறோம். மூலக்கூறுகளுக்கிடையேயான ஈர்ப்பு விசைகள் மிகவும் வலுவாக இல்லை என்று நாம் முடிவு செய்யலாம். இந்த சேர்மங்கள் பெரும்பாலும் மின்சாரத்தைக் கடத்தாததால், இந்த சேர்மங்களில் உள்ள பிணைப்பு எந்த அயனிகளையும் உருவாக்காது என்று நாம் முடிவு செய்யலாம்.
அட்டவணை 4.1 சில கார்பன் சேர்மங்களின் உருகு நிலைகள் மற்றும் கொதிநிலைகள்
| சேர்மம் | உருகு நிலை $(\mathbf{K})$ | கொதிநிலை $(\mathbf{K})$ |
|---|---|---|
| அசிட்டிக் அமிலம் $(CH_3 COOH)$ | 290 | 391 |
| குளோரோஃபார்ம் $(CHCl_3)$ | 209 | 334 |
| எத்தனால் $(CH_3 CH_2 OH)$ | 156 | 351 |
| மீத்தேன் $(CH_4)$ | 90 | 111 |
தரம் IX இல், பல்வேறு தனிமங்களின் இணைதிறன் மற்றும் அது இணைதிறன் எலக்ட்ரான்களின் எண்ணிக்கையை எவ்வாறு சார்ந்துள்ளது என்பதைப் பற்றி கற்றோம். இப்போது கார்பனின் மின்னணு அமைப்பைப் பார்ப்போம். கார்பனின் அணு எண் 6. கார்பனின் பல்வேறு கூடுகளில் எலக்ட்ரான்களின் பரவல் என்னவாக இருக்கும்? கார்பனுக்கு எத்தனை இணைதிறன் எலக்ட்ரான்கள் இருக்கும்?
தனிமங்களின் வினைத்திறன் என்பது அவை முற்றிலும் நிரம்பிய வெளிக்கூட்டை அடையும் போக்கால் விளக்கப்படுகிறது, அதாவது, உன்னத வாயு அமைப்பை அடைதல். அயனி சேர்மங்களை உருவாக்கும் தனிமங்கள் வெளிப்புற கூட்டிலிருந்து எலக்ட்ரான்களைப் பெறுவதன் மூலமோ அல்லது இழப்பதன் மூலமோ இதை அடைகின்றன. கார்பனின் விஷயத்தில், அதன் வெளிப்புற கூட்டில் நான்கு எலக்ட்ரான்கள் உள்ளன மற்றும் உன்னத வாயு அமைப்பை அடைய நான்கு எலக்ட்ரான்களைப் பெறவோ அல்லது இழக்கவோ வேண்டும். அது எலக்ட்ரான்களைப் பெற்றால் அல்லது இழந்தால் -
(i) அது நான்கு எலக்ட்ரான்களைப் பெற்று $C^{4-}$ அயனியை உருவாக்கும். ஆனால் ஆறு புரோட்டான்களைக் கொண்ட கருவுக்கு பத்து எலக்ட்ரான்களை வைத்திருக்க கடினமாக இருக்கும், அதாவது, நான்கு கூடுதல் எலக்ட்ரான்கள்.
(ii) அது நான்கு எலக்ட்ரான்களை இழந்து $C^{4+}$ நேரயனியை உருவாக்கும். ஆனால் நான்கு எலக்ட்ரான்களை அகற்றுவதற்கு அதிக ஆற்றல் தேவைப்படும், இதனால் கார்பன் நேரயனி அதன் கருவில் ஆறு புரோட்டான்களைக் கொண்டு இரண்டு எலக்ட்ரான்களை மட்டுமே வைத்திருக்கும்.
கார்பன் இந்த சிக்கலை தனது இணைதிறன் எலக்ட்ரான்களை கார்பனின் பிற அணுக்களுடன் அல்லது பிற தனிமங்களின் அணுக்களுடன் பகிர்வதன் மூலம் தீர்க்கிறது. கார்பன் மட்டுமல்ல, பல பிற தனிமங்களும் இந்த முறையில் எலக்ட்ரான்களைப் பகிர்வதன் மூலம் மூலக்கூறுகளை உருவாக்குகின்றன. பகிரப்பட்ட எலக்ட்ரான்கள் இரு அணுக்களின் வெளிப்புற கூடுகளுக்கும் ‘சொந்தமானவை’ மற்றும் இரு அணுக்களும் உன்னத வாயு அமைப்பை அடைய வழிவகுக்கும். கார்பன் சேர்மங்களைப் பற்றிச் செல்வதற்கு முன், இணைதிறன் எலக்ட்ரான்களைப் பகிர்வதன் மூலம் உருவாக்கப்படும் சில எளிய மூலக்கூறுகளைப் பார்ப்போம்.
இந்த முறையில் உருவாக்கப்பட்ட எளிய மூலக்கூறு ஹைட்ரஜனின் மூலக்கூறு ஆகும். நீங்கள் முன்பு கற்றது போல், ஹைட்ரஜனின் அணு எண் 1. எனவே ஹைட்ரஜனுக்கு அதன் $K$ கூட்டில் ஒரு எலக்ட்ரான் உள்ளது மற்றும் $K$ கூட்டை நிரப்ப இன்னும் ஒரு எலக்ட்ரான் தேவை. எனவே இரண்டு ஹைட்ரஜன் அணுக்கள் அவற்றின் எலக்ட்ரான்களைப் பகிர்ந்து கொண்டு ஹைட்ரஜன் மூலக்கூறை உருவாக்குகின்றன, $H_2$. இது ஒவ்வொரு ஹைட்ரஜன் அணுவும் அருகிலுள்ள உன்னத வாயுவான ஹீலியத்தின் மின்னணு அமைப்பை அடைய அனுமதிக்கிறது, இதன் K கூட்டில் இரண்டு எலக்ட்ரான்கள் உள்ளன. இணைதிறன் எலக்ட்ரான்களைக் குறிக்க புள்ளிகள் அல்லது குறுக்குகளைப் பயன்படுத்தி இதை சித்தரிக்கலாம் (படம் 4.1).
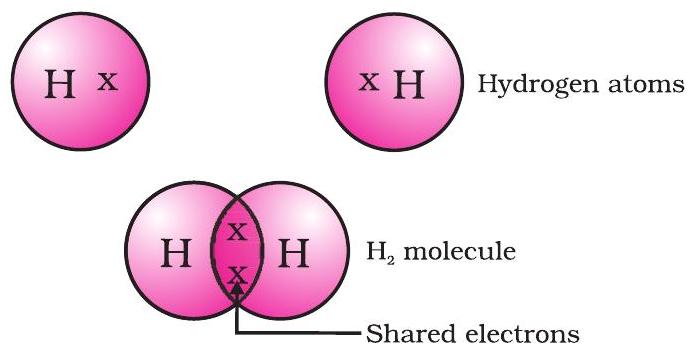
படம் 4.1 ஹைட்ரஜனின் மூலக்கூறு
பகிரப்பட்ட எலக்ட்ரான் இணை இரண்டு ஹைட்ரஜன் அணுக்களுக்கு இடையே ஒரு ஒற்றை சக பிணைப்பை உருவாக்குகிறது என்று கூறப்படுகிறது. ஒற்றை சக பிணைப்பு இரண்டு அணுக்களுக்கு இடையே ஒரு கோடு மூலமாகவும் குறிப்பிடப்படுகிறது, படம் 4.2 இல் காட்டப்பட்டுள்ளது.
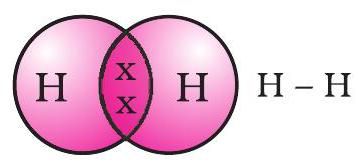
படம் 4.2 இரண்டு ஹைட்ரஜன் அணுக்களுக்கு இடையேயான ஒற்றை பிணைப்பு
குளோரினின் அணு எண் 17. அதன் மின்னணு அமைப்பு மற்றும் அதன் இணைதிறன் என்னவாக இருக்கும்? குளோரின் ஒரு இரு அணு மூலக்கூறை உருவாக்குகிறது, $Cl_2$. இந்த மூலக்கூறுக்கான எலக்ட்ரான் புள்ளி அமைப்பை நீங்கள் வரைய முடியுமா? இணைதிறன் கூட்டு எலக்ட்ரான்கள் மட்டுமே சித்தரிக்கப்பட வேண்டும் என்பதை கவனிக்கவும்.
ஆக்ஸிஜனின் விஷயத்தில், இரண்டு ஆக்ஸிஜன் அணுக்களுக்கு இடையே இரட்டை பிணைப்பு உருவாகிறதைக் காண்கிறோம். ஏனெனில் ஆக்ஸிஜன் அணுவின் L கூட்டில் ஆறு எலக்ட்ரான்கள் உள்ளன (ஆக்ஸிஜனின் அணு எண் எட்டு) மற்றும் அதன் எண்மத்தை நிறைவு செய்ய இன்னும் இரண்டு எலக்ட்ரான்கள் தேவை. எனவே ஒவ்வொரு ஆக்ஸிஜன் அணுவும் மற்றொரு ஆக்ஸிஜன் அணுவுடன் இரண்டு எலக்ட்ரான்களைப் பகிர்ந்து கொள்கிறது, இது படம் 4.3 இல் காட்டப்பட்டுள்ள அமைப்பைத் தருகிறது. ஒவ்வொரு ஆக்ஸிஜன் அணுவும் வழங்கும் இரண்டு எலக்ட்ரான்கள் இரண்டு பகிரப்பட்ட எலக்ட்ரான் இணைகளை உருவாக்குகின்றன. இது இரண்டு அணுக்களுக்கு இடையே ஒரு இரட்டை பிணைப்பை உருவாக்குகிறது என்று கூறப்படுகிறது.
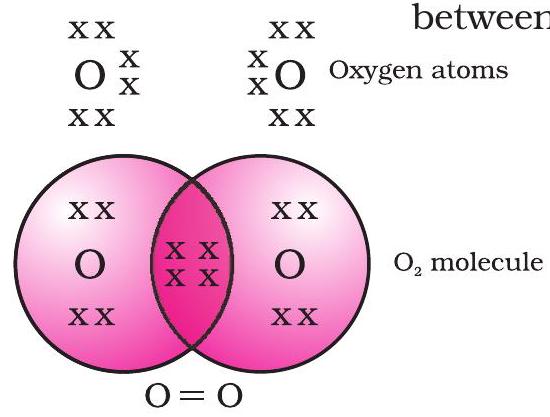
படம் 4.3 இரண்டு ஆக்ஸிஜன் அணுக்களுக்கு இடையேயான இரட்டை பிணைப்பு
இப்போது நீங்கள் ஒரு ஆக்ஸிஜன் அணுவுக்கும் இரண்டு ஹைட்ரஜன் அணுக்களுக்கும் இடையே உள்ள பிணைப்பின் தன்மையைக் காட்டும் நீரின் மூலக்கூறை சித்தரிக்க முடியுமா? மூலக்கூறுக்கு ஒற்றை பிணைப்புகள் உள்ளதா அல்லது இரட்டை பிணைப்புகள் உள்ளதா?
நைட்ரஜனின் இரு அணு மூலக்கூறின் விஷயத்தில் என்ன நடக்கும்? நைட்ரஜனின் அணு எண் 7. அதன் மின்னணு அமைப்பு மற்றும் அதன் இணைதிறன் என்னவாக இருக்கும்? ஒரு எண்மத்தை அடைய, நைட்ரஜன் மூலக்கூறில் உள்ள ஒவ்வொரு நைட்ரஜன் அணுவும் மூன்று எலக்ட்ரான்களை வழங்குகிறது, இது மூன்று பகிரப்பட்ட எலக்ட்ரான் இணைகளை உருவாக்குகிறது. இது இரண்டு அணுக்களுக்கு இடையே ஒரு முப்பிணைப்பை உருவாக்குகிறது என்று கூறப்படுகிறது படம் 4.3 $N_2$ மற்றும் இரண்டு ஆக்ஸிஜன் அணுக்களுக்கு இடையேயான இரட்டை பிணைப்பு அதன் முப்பிணைப்பு படம் 4.4 இல் சித்தரிக்கப்பட்டுள்ளது.
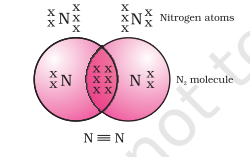
படம் 4.4 இரண்டு நைட்ரஜன் அணுக்களுக்கு இடையேயான முப்பிணைப்பு
அம்மோனியாவின் மூலக்கூறுக்கு $NH_3$ என்ற வாய்ப்பாடு உள்ளது. நான்கு அணுக்களும் உன்னத வாயு அமைப்பை எவ்வாறு அடைகின்றன என்பதைக் காட்டும் இந்த மூலக்கூறுக்கான எலக்ட்ரான் புள்ளி அமைப்பை நீங்கள் வரைய முடியுமா? மூலக்கூறுக்கு ஒற்றை, இரட்டை அல்லது முப்பிணைப்புகள் இருக்குமா?
இப்போது மீத்தேனைப் பார்ப்போம், இது கார்பனின் ஒரு சேர்மமாகும். மீத்தேன் ஒரு எரிபொருளாக பரவலாகப் பயன்படுத்தப்படுகிறது மற்றும் உயிரிவாயு மற்றும் சுருக்கப்பட்ட இயற்கை எரிவாயு (CNG) இன் முக்கிய கூறு ஆகும். இது கார்பனால் உருவாக்கப்பட்ட எளிய சேர்மங்களில் ஒன்றாகும். மீத்தேனுக்கு $CH_4$ என்ற வாய்ப்பாடு உள்ளது. உங்களுக்குத் தெரிந்தபடி, ஹைட்ரஜனின் இணைதிறன் 1 ஆகும். கார்பன் நான்கு இணைதிறன் எலக்ட்ரான்களைக் கொண்டிருப்பதால் நான்கிணைதிறன் கொண்டது. உன்னத வாயு அமைப்பை அடைய, கார்பன் இந்த எலக்ட்ரான்களை நான்கு ஹைட்ரஜன் அணுக்களுடன் பகிர்ந்து கொள்கிறது, படம் 4.5 இல் காட்டப்பட்டுள்ளது.
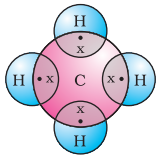
படம் 4.5 மீத்தேனுக்கான எலக்ட்ரான் புள்ளி அமைப்பு
இரண்டு அணுக்களுக்கு இடையே ஒரு எலக்ட்ரான் இணையைப் பகிர்வதன் மூலம் உருவாகும் இத்தகைய பிணைப்புகள் சக பிணைப்புகள் என்று அழைக்கப்படுகின்றன. சக பிணைப்பு கொண்ட மூலக்கூறுகள் மூலக்கூறுக்குள் வலுவான பிணைப்புகளைக் கொண்டிருப்பதாகக் காணப்படுகின்றன, ஆனால் மூலக்கூறுகளுக்கிடையேயான விசைகள் பலவீனமாக இருக்கும். இது இந்த சேர்மங்களின் குறைந்த உருகு மற்றும் கொதிநிலைகளை உருவாக்குகிறது. எலக்ட்ரான்கள் அணுக்களுக்கு இடையே பகிரப்படுவதால் மற்றும் மின்னூட்டம் கொண்ட துகள்கள் உருவாகாததால், இத்தகைய சக சேர்மங்கள் பொதுவாக மின்சாரத்தின் மோசமான கடத்திகளாக இருக்கும்.
மேலும் தெரிந்து கொள்ள!
கார்பனின் அலோட்ரோப்புகள்
கார்பன் தனிமம் இயற்கையில் மிகவும் மாறுபட்ட இயற்பியல் பண்புகளுடன் பல்வேறு வடிவங்களில் காணப்படுகிறது. வைரம் மற்றும் கிராஃபைட் இரண்டும் கார்பன் அணுக்களால் உருவாக்கப்படுகின்றன, கார்பன் அணுக்கள் ஒன்றுக்கொன்று பிணைக்கப்படும் முறையில் வேறுபாடு உள்ளது. வைரத்தில், ஒவ்வொரு கார்பன் அணுவும் நான்கு பிற கார்பன் அணுக்களுடன் பிணைக்கப்பட்டு ஒரு கடினமான முப்பரிமாண அமைப்பை உருவாக்குகிறது. கிராஃபைட்டில், ஒவ்வொரு கார்பன் அணுவும் ஒரே தளத்தில் மூன்று பிற கார்பன் அணுக்களுடன் பிணைக்கப்பட்டு ஒரு அறுகோண வரிசையைக் கொடுக்கிறது. இந்த பிணைப்புகளில் ஒன்று இரட்டை பிணைப்பு, இதனால் கார்பனின் இணைதிறன் திருப்தி அடைகிறது. கிராஃபைட் அமைப்பு அறுகோண வரிசைகள் ஒன்றன் மேல் ஒன்றாக அடுக்கப்பட்டு உருவாகிறது.
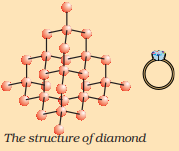
வைரத்தின் அமைப்பு
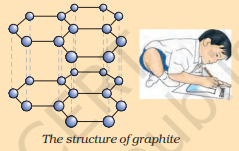
கிராஃபைட்டின் அமைப்பு
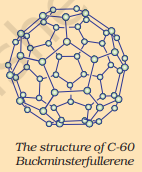
C-60 பக்மின்ஸ்டர்ஃபுலரீனின் அமைப்பு
இந்த இரண்டு வெவ்வேறு அமைப்புகள் வைரம் மற்றும் கிராஃபைட் மிகவும் வெவ்வேறு இயற்பியல் பண்புகளைக் கொண்டிருக்க வழிவகுக்கிறது, அவற்றின் வேதியியல் பண்புகள் ஒரே மாதிரியாக இருந்தாலும் கூட. வைரம் அறியப்பட்ட மிகவும் கடினமான பொருளாகும், அதே நேரத்தில் கிராஃபைட் மென்மையானது மற்றும் வழுக்கும். முந்தைய அத்தியாயத்தில் நீங்கள் படித்த பிற உலோகமல்லாதவற்றைப் போலல்லாமல், கிராஃபைட் மின்சாரத்தின் மிகச் சிறந்த கடத்தியாகும்.
தூய கார்பனை மிக அதிக அழுத்தம் மற்றும் வெப்பநிலைக்கு உட்படுத்துவதன் மூலம் வைரங்களை தொகுக்க முடியும். இந்த செயற்கை வைரங்கள் சிறியவை, ஆனால் இயற்கை வைரங்களிலிருந்து வேறுபடுத்த முடியாதவை.
ஃபுலரீன்கள் கார்பன் அலோட்ரோப்புகளின் மற்றொரு வகுப்பை உருவாக்குகின்றன. முதலில் அடையாளம் காணப்பட்டது C-60 ஆகும், இது கால்பந்து வடிவில் கார்பன் அணுக்களைக் கொண்டுள்ளது. இது அமெரிக்க கட்டிடக் கலைஞர் பக்மின்ஸ்டர் ஃபுல்லர் வடிவமைத்த புவியியல் குவிமாடத்தைப் போல இருந்ததால், இந்த மூலக்கூறுக்கு ஃபுலரீன் என்று பெயரிடப்பட்டது.
4.2 கார்பனின் பல்துறை தன்மை
பல்வேறு தனிமங்கள் மற்றும் சேர்மங்களில் எலக்ட்ரான்களைப் பகிர்வதன் மூலம் சக பிணைப்புகள் உருவாகுவதை நாங்கள் பார்த்துள்ளோம். ஒரு எளிய கார்பன் சேர்மமான மீத்தேனின் அமைப்பையும் பார்த்துள்ளோம். அத்தியாயத்தின் தொடக்கத்தில், நாம் பயன்படுத்தும் பல பொருட்கள் கார்பனைக் கொண்டிருக்கின்றன என்பதைக் கண்டோம். உண்மையில், நாமே கார்பன் சேர்மங்களால் ஆனவர்கள். வேதியியலாளர்களுக்குத் தெரிந்த வாய்ப்பாடுகளைக் கொண்ட கார்பன் சேர்மங்களின் எண்ணிக்கை சமீபத்தில் மில்லியன் கணக்கில் மதிப்பிடப்பட்டது! மற்ற அனைத்து தனிமங்களாலும் உருவாக்கப்பட்ட சேர்மங்களை விட இது பெரிய அளவில் அதிகமாகும். இந்த பண்பு கார்பனில் மட்டும் ஏன் காணப்படுகிறது, வேறு எந்த தனிமத்திலும் இல்லை? சக பிணைப்பின் தன்மை கார்பனைப் பெருமளவிலான சேர்மங்களை உருவாக்க அனுமதிக்கிறது. கார்பனின் விஷயத்தில் கவனிக்கப்பட்ட இரண்டு காரணிகள் -
(i) கார்பனுக்கு பிற கார்பன் அணுக்களுடன் பிணைப்புகளை உருவாக்கும் தனித்துவமான திறன் உள்ளது, இது பெரிய மூலக்கூறுகளை உருவாக்குகிறது. இந்த பண்பு சங்கிலியாக்கம் என்று அழைக்கப்படுகிறது. இந்த சேர்மங்கள் நீண்ட கார்பன் சங்கிலிகளைக் கொண்டிருக்கலாம், கிளைத்த கார்பன் சங்கிலிகளைக் கொண்டிருக்கலாம் அல்லது கார்பன் அணுக்கள் வளையங்களில் அமைக்கப்பட்டிருக்கலாம். கூடுதலாக, கார்பன் அணுக்கள் ஒற்றை, இரட்டை அல்லது முப்பிணைப்புகளால் இணைக்கப்படலாம். கார்பன் அணுக்களுக்கு இடையே ஒற்றை பிணைப்புகளால் மட்டுமே இணைக்கப்பட்ட கார்பனின் சேர்மங்கள் நிறைவுற்ற சேர்மங்கள் என்று அழைக்கப்படுகின்றன. அவற்றின் கார்பன் அணுக்களுக்கு இடையே இரட்டை அல்லது முப்பிணைப்புகளைக் கொண்ட கார்பன் சேர்மங்கள் நிறைவுறா சேர்மங்கள் என்று அழைக்கப்படுகின்றன.
கார்பன் சேர்மங்களில் காணப்படும் அளவிற்கு சங்கிலியாக்கம் பண்பை வேறு எந்த தனிமமும் வெளிப்படுத்துவதில்லை. சிலிக்கான் ஹைட்ரஜனுடன் சேர்மங்களை உருவாக்குகிறது, இவை ஏழு அல்லது எட்டு அணுக்கள் வரை சங்கிலிகளைக் கொண்டுள்ளன, ஆனால் இந்த சேர்மங்கள் மிகவும் வினைத்திறன் கொண்டவை. கார்பன்-கார்பன் பிணைப்பு மிகவும் வலுவானது மற்றும் எனவே நிலையானது. இது பல கார்பன் அணுக்கள் ஒன்றோடொன்று இணைக்கப்பட்ட பல சேர்மங்களை நமக்குத் தருகிறது.
(ii) கார்பனுக்கு நான்கு இணைதிறன் இருப்பதால், அது நான்கு பிற கார்பன் அணுக்களுடன் அல்லது வேறு சில ஒற்றை இணைதிறன் கொண்ட தனிமங்களின் அணுக்களுடன் பிணைக்கும் திறன் கொண்டது. கார்பனின் சேர்மங்கள் ஆக்ஸிஜன், ஹைட்ரஜன், நைட்ரஜன், கந்தகம், குளோரின் மற்றும் பல தனிமங்களுடன் உருவாகின்றன, இது கார்பன் தவிர மூலக்கூறில் உள்ள தனிமங்களைப் பொறுத்து குறிப்பிட்ட பண்புகளைக் கொண்ட சேர்மங்களை உருவாக்குகிறது.
மீண்டும், கார்பன் பெரும்பாலான பிற தனிமங்களுடன் உருவாக்கும் பிணைப்புகள் மிகவும் வலுவானவை, இந்த சேர்மங்களை விதிவிலக்காக நிலையானதாக ஆக்குகின்றன. கார்பன் வலுவான பிணைப்புகளை உருவாக்குவதற்கான ஒரு காரணம் அதன் சிறிய அளவு. இது பகிரப்பட்ட எலக்ட்ரான் இணைகளை கருவால் வலுவாகப் பிடித்துக் கொள்ள அனுமதிக்கிறது. பெரிய அணுக்களைக் கொண்ட தனிமங்களால் உருவாக்கப்பட்ட பிணைப்புகள் மிகவும் பலவீனமானவை.
உங்களுக்குத் தெரியுமா?
கரிம சேர்மங்கள்
கார்பனில் காணப்படும் இரண்டு சிறப்பியல்பு அம்சங்கள், அதாவது, நான்கிணைதிறன் மற்றும் சங்கிலியாக்கம், ஒன்றாக இணைந்து பெருமளவிலான சேர்மங்களை உருவாக்குகின்றன. பலவற்றில் ஒரே உலோகமல்லாத அணு அல்லது அணுக்களின் குழு வெவ்வேறு கார்பன் சங்கிலிகளுடன் இணைக்கப்பட்டுள்ளது. இந்த சேர்மங்கள் ஆரம்பத்தில் இயற்கைப் பொருட்களிலிருந்து பிரித்தெடுக்கப்பட்டன, மேலும் இந்த கார்பன் சேர்மங்கள் அல்லது கரிம சேர்மங்கள் ஒரு உயிரின அமைப்புக்குள் மட்டுமே உருவாக்கப்பட முடியும் என்று நினைக்கப்பட்டது. அதாவது, அவற்றின் தொகுப்பிற்கு ஒரு ‘முக்கிய விசை’ தேவை என்று கருதப்பட்டது. 1828 இல் அம்மோனியம் சயனேட்டிலிருந்து யூரியாவைத் தயாரிப்பதன் மூலம் ஃப்ரீட்ரிக் வோலர் இதை மறுத்தார். ஆனால் கார்பைடுகள், கார்பனின் ஆக்சைடுகள், கார்பனேட் மற்றும் ஹைட்ரஜன் கார்பனேட்டு உப்புகள் தவிர, கார்பன் சேர்மங்கள் கரிம வேதியியலின் கீழ் தொடர்ந்து படிக்கப்படுகின்றன.
4.2.1 நிறைவுற்ற மற்றும் நிறைவுறா கார்பன் சேர்மங்கள்
மீத்தேனின் அமைப்பை நாம் ஏற்கனவே பார்த்துள்ளோம். கார்பன் மற்றும் ஹைட்ரஜனுக்கு இடையே உருவாகும் மற்றொரு சேர்மம் $C_2 H_6$ என்ற வாய்ப்பாட்டுடன் கூடிய எத்தேன் ஆகும். எளிய கார்பன் சேர்மங்களின் அமைப்பை அடைய, முதல் படி கார்பன் அணுக்களை ஒரு ஒற்றை பிணைப்புடன் இணைப்பதாகும் (படம் 4.6a) பின்னர் கார்பனின் மீதமுள்ள இணைதிறன்களை திருப்திப்படுத்த ஹைட்ரஜன் அணுக்களைப் பயன்படுத்தவும் (படம் 4.6b). எடுத்துக்காட்டாக, எத்தேனின்











