অধ্যায় ০৪ কার্বন ও এর যৌগ
গত অধ্যায়ে, আমরা আমাদের জন্য গুরুত্বপূর্ণ অনেক যৌগ সম্পর্কে জানতে পেরেছিলাম। এই অধ্যায়ে আমরা আরও কিছু আকর্ষণীয় যৌগ এবং তাদের ধর্ম নিয়ে অধ্যয়ন করব। এছাড়াও, আমরা কার্বন সম্পর্কে শিখব, একটি মৌল যা তার মৌলিক রূপে এবং যৌগিক রূপে উভয়ই আমাদের জন্য অপরিসীম গুরুত্ব বহন করে।
কার্যকলাপ 4.1
- সকাল থেকে আপনি যে দশটি জিনিস ব্যবহার করেছেন বা গ্রহণ করেছেন তার একটি তালিকা তৈরি করুন।
- আপনার সহপাঠীদের তৈরি তালিকার সাথে এই তালিকাটি সংকলন করুন এবং তারপর আইটেমগুলিকে সংলগ্ন সারণিতে বিন্যস্ত করুন।
- যদি এমন আইটেম থাকে যা একাধিক উপাদান দিয়ে তৈরি, তবে সেগুলিকে সারণির উভয় প্রাসঙ্গিক কলামে রাখুন।
| ধাতু দিয়ে তৈরি জিনিস | ধাতু দিয়ে তৈরি জিনিস | অন্যান্য |
|---|---|---|
আপনার দ্বারা পূরণ করা উপরের সারণির শেষ কলামে আসা আইটেমগুলি দেখুন - আপনার শিক্ষক আপনাকে বলতে সক্ষম হবেন যে তাদের বেশিরভাগই কার্বন যৌগ দিয়ে তৈরি। এটি পরীক্ষা করার একটি পদ্ধতি আপনি ভাবতে পারেন? কার্বনযুক্ত একটি যৌগ পোড়ালে কী উৎপাদ হবে? এটি নিশ্চিত করার জন্য আপনার কি কোনো পরীক্ষা জানা আছে?
খাদ্য, বস্ত্র, ওষুধ, বই, বা আপনি যে অনেক জিনিস তালিকাভুক্ত করেছেন তা সবই এই বহুমুখী মৌল কার্বনের উপর ভিত্তি করে। তদুপরি, সমস্ত জীবন্ত কাঠামো কার্বন-ভিত্তিক। ভূত্বক এবং বায়ুমণ্ডলে উপস্থিত কার্বনের পরিমাণ বেশ অল্প। ভূত্বকের মাত্র $0.02 %$ কার্বন খনিজ (যেমন কার্বনেট, হাইড্রোজেনকার্বনেট, কয়লা এবং পেট্রোলিয়াম) আকারে রয়েছে এবং বায়ুমণ্ডলে রয়েছে $0.03 %$ কার্বন ডাই অক্সাইড। প্রকৃতিতে কার্বনের এই অল্প পরিমাণ উপলব্ধ থাকা সত্ত্বেও, কার্বনের গুরুত্ব অপরিসীম বলে মনে হয়। এই অধ্যায়ে, আমরা কার্বনের সেইসব ধর্ম সম্পর্কে জানব যা কার্বনকে আমাদের জন্য এত গুরুত্বপূর্ণ করে তোলে।
4.1 কার্বনে বন্ধন - সমযোজী বন্ধন
পূর্ববর্তী অধ্যায়ে, আমরা আয়নিক যৌগের ধর্ম অধ্যয়ন করেছি। আমরা দেখেছি যে আয়নিক যৌগগুলির গলনাঙ্ক ও স্ফুটনাঙ্ক উচ্চ এবং দ্রবণ বা গলিত অবস্থায় তারা বিদ্যুৎ পরিবহন করে। আমরা আরও দেখেছি কিভাবে আয়নিক যৌগে বন্ধনের প্রকৃতি এই ধর্মগুলির ব্যাখ্যা দেয়। আসুন এখন কিছু কার্বন যৌগের ধর্ম অধ্যয়ন করি।
বেশিরভাগ কার্বন যৌগ বিদ্যুতের কুপরিবাহী, যেমনটি আমরা অধ্যায় 2 এ দেখেছি। কার্বন যৌগগুলির স্ফুটনাঙ্ক ও গলনাঙ্ক সম্পর্কে সারণী 4.1-এ প্রদত্ত তথ্য থেকে, আমরা দেখতে পাই যে আয়নিক যৌগের (অধ্যায় 3) তুলনায় এই যৌগগুলির গলনাঙ্ক ও স্ফুটনাঙ্ক কম। আমরা সিদ্ধান্তে আসতে পারি যে অণুগুলির মধ্যে আকর্ষণ বল খুব শক্তিশালী নয়। যেহেতু এই যৌগগুলি মূলত বিদ্যুতের অপরিবাহী, আমরা সিদ্ধান্তে আসতে পারি যে এই যৌগগুলিতে বন্ধন কোনো আয়নের সৃষ্টি করে না।
সারণী 4.1 কিছু কার্বন যৌগের গলনাঙ্ক ও স্ফুটনাঙ্ক
| যৌগ | গলনাঙ্ক $(\mathbf{K})$ | স্ফুটনাঙ্ক $(\mathbf{K})$ |
|---|---|---|
| অ্যাসিটিক অ্যাসিড $(CH_3 COOH)$ | 290 | 391 |
| ক্লোরোফর্ম $(CHCl_3)$ | 209 | 334 |
| ইথানল $(CH_3 CH_2 OH)$ | 156 | 351 |
| মিথেন $(CH_4)$ | 90 | 111 |
নবম শ্রেণীতে, আমরা বিভিন্ন মৌলের যোজনী ক্ষমতা এবং এটি যোজ্যতা ইলেকট্রনের সংখ্যার উপর কীভাবে নির্ভর করে তা শিখেছি। আসুন এখন কার্বনের ইলেকট্রন বিন্যাস দেখি। কার্বনের পারমাণবিক সংখ্যা 6। কার্বনের বিভিন্ন কক্ষে ইলেকট্রনের বণ্টন কেমন হবে? কার্বনের কতগুলি যোজ্যতা ইলেকট্রন থাকবে?
আমরা জানি যে মৌলগুলির বিক্রিয়াশীলতা তাদের সম্পূর্ণরূপে পূর্ণ বহিঃস্থ কক্ষ অর্জনের প্রবণতা হিসাবে ব্যাখ্যা করা হয়, অর্থাৎ, নিষ্ক্রিয় গ্যাসের বিন্যাস অর্জন। আয়নিক যৌগ গঠনকারী মৌলগুলি বহিঃস্থ কক্ষ থেকে ইলেকট্রন লাভ বা হারিয়ে এটি অর্জন করে। কার্বনের ক্ষেত্রে, এর বহিঃস্থ কক্ষে চারটি ইলেকট্রন রয়েছে এবং নিষ্ক্রিয় গ্যাস বিন্যাস অর্জনের জন্য চারটি ইলেকট্রন লাভ বা হারাতে হয়। যদি এটি ইলেকট্রন লাভ বা হারায় -
(i) এটি চারটি ইলেকট্রন লাভ করে $C^{4-}$ অ্যানায়ন গঠন করতে পারে। কিন্তু ছয়টি প্রোটন বিশিষ্ট নিউক্লিয়াসের জন্য দশটি ইলেকট্রন ধরে রাখা কঠিন হবে, অর্থাৎ, চারটি অতিরিক্ত ইলেকট্রন।
(ii) এটি চারটি ইলেকট্রন হারিয়ে $C^{4+}$ ক্যাটায়ন গঠন করতে পারে। কিন্তু চারটি ইলেকট্রন অপসারণ করতে প্রচুর শক্তির প্রয়োজন হবে, যার ফলে কার্বন ক্যাটায়ন পিছনে থেকে যায় যার নিউক্লিয়াসে ছয়টি প্রোটন মাত্র দুটি ইলেকট্রন ধরে রাখে।
কার্বন অন্যান্য কার্বন পরমাণু বা অন্যান্য মৌলের পরমাণুর সাথে তার যোজ্যতা ইলেকট্রন ভাগ করে এই সমস্যা কাটিয়ে ওঠে। শুধু কার্বন নয়, আরও অনেক মৌল এইভাবে ইলেকট্রন ভাগ করে অণু গঠন করে। ভাগ করা ইলেকট্রনগুলি উভয় পরমাণুর বহিঃস্থ কক্ষের ‘অন্তর্গত’ এবং উভয় পরমাণুকে নিষ্ক্রিয় গ্যাস বিন্যাস অর্জনে নেতৃত্ব দেয়। কার্বনের যৌগে যাওয়ার আগে, আসুন যোজ্যতা ইলেকট্রন ভাগ করে গঠিত কিছু সরল অণু দেখি।
এইভাবে গঠিত সবচেয়ে সরল অণুটি হল হাইড্রোজেনের। আপনি আগে শিখেছেন, হাইড্রোজেনের পারমাণবিক সংখ্যা 1। তাই হাইড্রোজেনের $K$ কক্ষে একটি ইলেকট্রন রয়েছে এবং $K$ কক্ষ পূরণ করতে এর আরও একটি ইলেকট্রনের প্রয়োজন। তাই দুটি হাইড্রোজেন পরমাণু তাদের ইলেকট্রন ভাগ করে হাইড্রোজেনের একটি অণু, $H_2$ গঠন করে। এটি প্রতিটি হাইড্রোজেন পরমাণুকে নিকটতম নিষ্ক্রিয় গ্যাস হিলিয়ামের ইলেকট্রন বিন্যাস অর্জন করতে দেয়, যার K কক্ষে দুটি ইলেকট্রন রয়েছে। আমরা যোজ্যতা ইলেকট্রন উপস্থাপনের জন্য বিন্দু বা ক্রস ব্যবহার করে এটি চিত্রিত করতে পারি (চিত্র 4.1)।
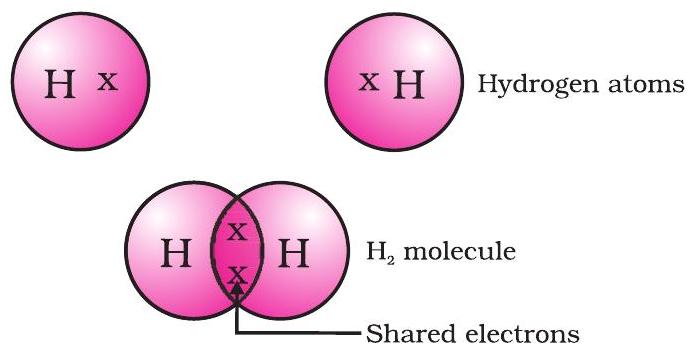
চিত্র 4.1 একটি হাইড্রোজেন অণু
ভাগ করা ইলেকট্রন জোড়াটিকে দুটি হাইড্রোজেন পরমাণুর মধ্যে একটি একক সমযোজী বন্ধন গঠন করেছে বলা হয়। একটি একক সমযোজী বন্ধনকেও দুটি পরমাণুর মধ্যে একটি রেখা দ্বারা উপস্থাপন করা হয়, যেমন চিত্র 4.2-এ দেখানো হয়েছে।
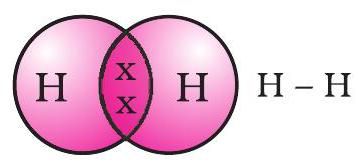
চিত্র 4.2 দুটি হাইড্রোজেন পরমাণুর মধ্যে একক বন্ধন
ক্লোরিনের পারমাণবিক সংখ্যা 17। এর ইলেকট্রন বিন্যাস এবং যোজনী কী হবে? ক্লোরিন একটি দ্বিপরমাণুক অণু গঠন করে, $Cl_2$। আপনি কি এই অণুর জন্য ইলেকট্রন বিন্দু গঠন আঁকতে পারেন? মনে রাখবেন যে শুধুমাত্র যোজ্যতা কক্ষের ইলেকট্রনগুলিকে চিত্রিত করতে হবে।
অক্সিজেনের ক্ষেত্রে, আমরা দুটি অক্সিজেন পরমাণুর মধ্যে একটি দ্বি-বন্ধন গঠন দেখি। এর কারণ হল অক্সিজেনের একটি পরমাণুর L কক্ষে ছয়টি ইলেকট্রন রয়েছে (অক্সিজেনের পারমাণবিক সংখ্যা আট) এবং এর অষ্টক পূর্ণ করতে আরও দুটি ইলেকট্রনের প্রয়োজন। তাই অক্সিজেনের প্রতিটি পরমাণু অন্য একটি অক্সিজেন পরমাণুর সাথে দুটি ইলেকট্রন ভাগ করে আমাদের চিত্র 4.3-এ দেখানো গঠন দেয়। প্রতিটি অক্সিজেন পরমাণু দ্বারা অবদান রাখা দুটি ইলেকট্রন ভাগ করা ইলেকট্রনের দুটি জোড়ার সৃষ্টি করে। এটি দুটি পরমাণুর মধ্যে একটি দ্বি-বন্ধন গঠন করেছে বলা হয়।
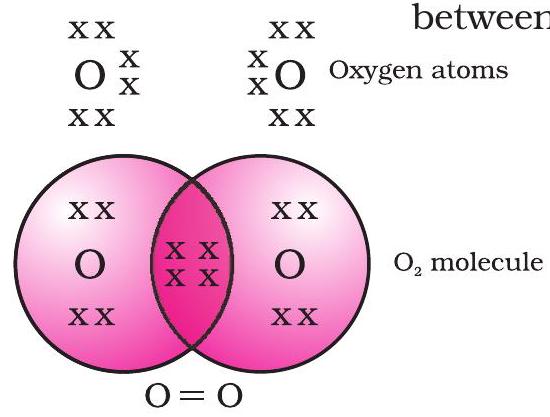
চিত্র 4.3 দুটি অক্সিজেন পরমাণুর মধ্যে দ্বি-বন্ধন
আপনি কি এখন একটি জলের অণু চিত্রিত করতে পারেন একটি অক্সিজেন পরমাণু এবং দুটি হাইড্রোজেন পরমাণুর মধ্যে বন্ধনের প্রকৃতি দেখিয়ে? অণুটিতে কি একক বন্ধন নাকি দ্বি-বন্ধন রয়েছে?
নাইট্রোজেনের একটি দ্বিপরমাণুক অণুর ক্ষেত্রে কী হবে? নাইট্রোজেনের পারমাণবিক সংখ্যা 7। এর ইলেকট্রন বিন্যাস এবং যোজনী ক্ষমতা কী হবে? একটি অষ্টক অর্জনের জন্য, নাইট্রোজেন অণুর প্রতিটি নাইট্রোজেন পরমাণু তিনটি ইলেকট্রন অবদান রাখে যার ফলে ভাগ করা ইলেকট্রনের তিনটি জোড়ার সৃষ্টি হয়। এটি দুটি পরমাণুর মধ্যে একটি ত্রি-বন্ধন গঠন করেছে বলা হয় চিত্র 4.3 দুটি অক্সিজেন পরমাণুর মধ্যে দ্বি-বন্ধন। $N_2$ এবং এর ত্রি-বন্ধনের ইলেকট্রন বিন্দু গঠন চিত্র 4.4-এর মতো চিত্রিত করা যেতে পারে।
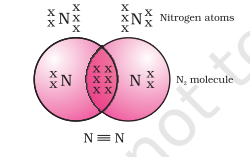
চিত্র 4.4 দুটি নাইট্রোজেন পরমাণুর মধ্যে ত্রি-বন্ধন
অ্যামোনিয়ার একটি অণুর সূত্র $NH_3$। আপনি কি এই অণুর জন্য ইলেকট্রন বিন্দু গঠন আঁকতে পারেন দেখিয়ে যে কীভাবে চারটি পরমাণুই নিষ্ক্রিয় গ্যাস বিন্যাস অর্জন করে? অণুটিতে কি একক, দ্বি- নাকি ত্রি-বন্ধন থাকবে?
আসুন এখন মিথেন দেখি, যা কার্বনের একটি যৌগ। মিথেন ব্যাপকভাবে জ্বালানি হিসাবে ব্যবহৃত হয় এবং এটি বায়োগ্যাস ও সংকুচিত প্রাকৃতিক গ্যাসের (CNG) একটি প্রধান উপাদান। এটি কার্বন দ্বারা গঠিত সরলতম যৌগগুলির মধ্যে একটি। মিথেনের সূত্র $CH_4$। হাইড্রোজেনের, আপনি জানেন, যোজনী 1। কার্বন চতুঃযোজী কারণ এর চারটি যোজ্যতা ইলেকট্রন রয়েছে। নিষ্ক্রিয় গ্যাস বিন্যাস অর্জনের জন্য, কার্বন চিত্র 4.5-এ দেখানো হিসাবে হাইড্রোজেনের চারটি পরমাণুর সাথে এই ইলেকট্রনগুলি ভাগ করে।
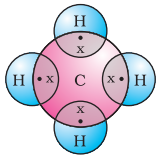
চিত্র 4.5 মিথেনের জন্য ইলেকট্রন বিন্দু গঠন
এই ধরনের বন্ধন যা দুটি পরমাণুর মধ্যে একটি ইলেকট্রন জোড়া ভাগ করে গঠিত হয় তাদের সমযোজী বন্ধন বলে জানা যায়। সমযোজী বন্ধনে আবদ্ধ অণুগুলির মধ্যে অণুর ভিতরে শক্তিশালী বন্ধন দেখা যায়, কিন্তু আন্তঃআণবিক বল দুর্বল। এটি এই যৌগগুলির নিম্ন গলনাঙ্ক ও স্ফুটনাঙ্কের সৃষ্টি করে। যেহেতু ইলেকট্রনগুলি পরমাণুর মধ্যে ভাগ করা হয় এবং কোনো আহিত কণা গঠিত হয় না, তাই এই ধরনের সমযোজী যৌগগুলি সাধারণত বিদ্যুতের কুপরিবাহী।
আরও জানুন!
কার্বনের সম allotrope রূপ
মৌল কার্বন প্রকৃতিতে বিভিন্ন রূপে ঘটে যার ভৌত ধর্ম ব্যাপকভাবে পরিবর্তিত হয়। হীরা এবং গ্রাফাইট উভয়ই কার্বন পরমাণু দ্বারা গঠিত, পার্থক্যটি lies কার্বন পরমাণুগুলি একে অপরের সাথে কীভাবে আবদ্ধ থাকে তার মধ্যে। হীরাতে, প্রতিটি কার্বন পরমাণু চারটি অন্যান্য কার্বন পরমাণুর সাথে আবদ্ধ হয়ে একটি অনমনীয় ত্রিমাত্রিক কাঠামো গঠন করে। গ্রাফাইটে, প্রতিটি কার্বন পরমাণু একই সমতলে তিনটি অন্যান্য কার্বন পরমাণুর সাথে আবদ্ধ হয়ে একটি ষড়ভুজ অ্যারে দেয়। এই বন্ধনগুলির মধ্যে একটি হল দ্বি-বন্ধন, এবং এইভাবে কার্বনের যোজনী সন্তুষ্ট হয়। গ্রাফাইট কাঠামো গঠিত হয় ষড়ভুজ অ্যারেগুলিকে একের পর এক স্তরে স্থাপন করে।
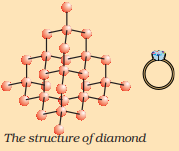
হীরার কাঠামো
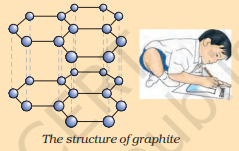
গ্রাফাইটের কাঠামো
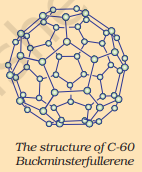
C-60 বাকমিনস্টারফুলারিনের কাঠামো
এই দুটি ভিন্ন কাঠামোর ফলে হীরা এবং গ্রাফাইটের রাসায়নিক ধর্ম একই হওয়া সত্ত্বেও তাদের ভৌত ধর্ম খুব ভিন্ন হয়। হীরা হল পরিচিত hardest পদার্থ যেখানে গ্রাফাইট মসৃণ এবং পিচ্ছিল। গ্রাফাইটও বিদ্যুতের একটি খুব ভাল পরিবাহী, পূর্ববর্তী অধ্যায়ে আপনি যে অন্যান্য অধাতুগুলি অধ্যয়ন করেছেন তার বিপরীতে।
খাঁটি কার্বনকে খুব উচ্চ চাপ ও তাপমাত্রার subject করে হীরা সংশ্লেষিত করা যেতে পারে। এই সংশ্লেষিত হীরাগুলি ছোট কিন্তু অন্যথায় প্রাকৃতিক হীরা থেকে আলাদা করা যায় না।
ফুলারিন কার্বনের সম allotrope রূপের আরেকটি শ্রেণি গঠন করে। প্রথমটি যা চিহ্নিত করা হয়েছিল তা হল C-60 যার কার্বন পরমাণুগুলি একটি ফুটবলের আকৃতিতে সজ্জিত। যেহেতু এটি মার্কিন স্থপতি বাকমিনস্টার ফুলার দ্বারা নকশা করা জিওডেসিক গম্বুজের মতো দেখাচ্ছিল, তাই অণুটির নামকরণ করা হয়েছিল ফুলারিন।
4.2 কার্বনের বহুমুখী প্রকৃতি
আমরা বিভিন্ন মৌল ও যৌগে ইলেকট্রন ভাগ করে সমযোজী বন্ধনের গঠন দেখেছি। আমরা একটি সরল কার্বন যৌগ, মিথেনের কাঠামোও দেখেছি। অধ্যায়ের শুরুতে, আমরা দেখেছি যে আমরা যে অনেক জিনিস ব্যবহার করি তাতে কার্বন রয়েছে। আসলে, আমরা নিজেরাই কার্বন যৌগ দিয়ে তৈরি। কার্বন যৌগের সংখ্যা যাদের সূত্র রসায়নবিদদের জানা তা সম্প্রতি লক্ষাধিক বলে অনুমান করা হয়েছিল! এটি অন্যান্য সমস্ত মৌল দ্বারা গঠিত যৌগের চেয়ে অনেক বেশি সংখ্যায়। কেন এই ধর্মটি কার্বনে এবং অন্য কোনো মৌলে দেখা যায়? সমযোজী বন্ধনের প্রকৃতি কার্বনকে বিপুল সংখ্যক যৌগ গঠন করতে সক্ষম করে। কার্বনের ক্ষেত্রে লক্ষ্য করা দুটি কারণ হল -
(i) কার্বনের অন্যান্য কার্বন পরমাণুর সাথে বন্ধন গঠনের অনন্য ক্ষমতা রয়েছে, যার ফলে বৃহৎ অণুর সৃষ্টি হয়। এই ধর্মটিকে শৃঙ্খলন বলে। এই যৌগগুলিতে দীর্ঘ শৃঙ্খলযুক্ত কার্বন, শাখাযুক্ত শৃঙ্খলযুক্ত কার্বন বা এমনকি বলয়াকারে সজ্জিত কার্বন পরমাণু থাকতে পারে। তদুপরি, কার্বন পরমাণুগুলি একক, দ্বি- বা ত্রি-বন্ধন দ্বারা যুক্ত হতে পারে। কার্বনের যৌগ, যেগুলি শুধুমাত্র কার্বন পরমাণুগুলির মধ্যে একক বন্ধন দ্বারা যুক্ত, তাদের সম্পৃক্ত যৌগ বলে। কার্বনের যৌগ যাদের কার্বন পরমাণুগুলির মধ্যে দ্বি- বা ত্রি-বন্ধন রয়েছে, তাদের অসম্পৃক্ত যৌগ বলে।
কার্বন যৌগে দেখা মাত্রায় শৃঙ্খলনের ধর্ম অন্য কোনো মৌল প্রদর্শন করে না। সিলিকন হাইড্রোজেনের সাথে যৌগ গঠন করে যেগুলিতে সাত বা আটটি পরমাণু পর্যন্ত শৃঙ্খল রয়েছে, কিন্তু এই যৌগগুলি খুব বিক্রিয়াশীল। কার্বন-কার্বন বন্ধন খুব শক্তিশালী এবং তাই স্থিতিশীল। এটি আমাদের অনেক কার্বন পরমাণু একে অপরের সাথে যুক্ত করে বিপুল সংখ্যক যৌগ দেয়।
(ii) যেহেতু কার্বনের যোজনী চার, এটি চারটি অন্যান্য কার্বন পরমাণু বা কিছু অন্যান্য এক-যোজী মৌলের পরমাণুর সাথে বন্ধন গঠনে সক্ষম। কার্বনের যৌগ অক্সিজেন, হাইড্রোজেন, নাইট্রোজেন, সালফার, ক্লোরিন এবং আরও অনেক মৌলের সাথে গঠিত হয়, যার ফলে নির্দিষ্ট ধর্মযুক্ত যৌগের সৃষ্টি হয় যা অণুতে উপস্থিত কার্বন ব্যতীত অন্যান্য মৌলের উপর নির্ভর করে।
আবার কার্বন বেশিরভাগ অন্যান্য মৌলের সাথে যে বন্ধন গঠন করে তা খুব শক্তিশালী, এই যৌগগুলিকে অসাধারণভাবে স্থিতিশীল করে তোলে। কার্বন দ্বারা শক্তিশালী বন্ধন গঠনের একটি কারণ হল এর ছোট আকার। এটি নিউক্লিয়াসকে ভাগ করা ইলেকট্রন জোড়াগুলিকে দৃঢ়ভাবে ধরে রাখতে সক্ষম করে। বড় পরমাণু বিশিষ্ট মৌল দ্বারা গঠিত বন্ধনগুলি অনেক দুর্বল।
আপনি কি জানেন?
জৈব যৌগ
কার্বনে দেখা দুটি বৈশিষ্ট্যগত দিক, অর্থাৎ, চতুঃযোজনী এবং শৃঙ্খলন, একত্রিত হয়ে বিপুল সংখ্যক যৌগের সৃষ্টি করে। অনেকের একই অ-কার্বন পরমাণু বা পরমাণুসমষ্টি বিভিন্ন কার্বন শৃঙ্খলের সাথে যুক্ত থাকে। এই যৌগগুলি প্রাথমিকভাবে প্রাকৃতিক পদার্থ থেকে নিষ্কাশিত হয়েছিল এবং মনে করা হত যে এই কার্বন যৌগ বা জৈব যৌগগুলি শুধুমাত্র একটি জীবন্ত ব্যবস্থার ভিতরেই গঠিত হতে পারে। অর্থাৎ, এটি অনুমান করা হয়েছিল যে তাদের সংশ্লেষণের জন্য একটি ‘প্রাণশক্তি’ প্রয়োজন ছিল। ফ্রিডরিখ ভোলার 1828 সালে অ্যামোনিয়াম সায়ানেট থেকে ইউরিয়া প্রস্তুত করে এটি খণ্ডন করেছিলেন। কিন্তু কার্বন যৌগ, কার্বাইড, কার্বনের অক্সাইড, কার্বনেট এবং হাইড্রোজেনকার্বনেট লবণ ব্যতীত, জৈব রসায়নের অধীনে অধ্যয়ন করা চলতে থাকে।
4.2.1 সম্পৃক্ত ও অসম্পৃক্ত কার্বন যৌগ
আমরা ইতিমধ্যে মিথেনের কাঠামো দেখেছি। কার্বন ও হাইড্রোজেনের মধ্যে গঠিত আরেকটি যৌগ হল ইথেন যার সূত্র $C_2 H_6$। সরল কার্বন যৌগের কাঠামোতে পৌঁছানোর জন্য, প্রথম ধাপ হল কার্বন পরমাণুগুলিকে একটি একক বন্ধন (চিত্র 4.6a) দিয়ে একসাথে যুক্ত করা এবং তারপর হাইড্রোজেন পরমাণু ব্যবহার করে কার্বনের অবশিষ্ট যোজনী সন্তুষ্ট করা (চিত্র 4.6b)। উদাহরণস্বরূপ, ইথেনের কাঠামো নিম্নলিখিত ধাপে পৌঁছেছে -
$ C-C \qquad $ ধাপ 1
চিত্র 4.6 (a) একটি একক বন্ধন দ্বারা যুক্ত কার্বন পরমাণু
প্রতিটি কার্বন পরমাণুর তিনটি যোজনী অসন্তুষ্ট থাকে, তাই প্রতিটি তিনটি হাইড্রোজেন পরমাণুর সাথে আবদ্ধ হয়:
$H-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}}-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}} - H \qquad $ ধাপ 2
চিত্র 4.6 (b) প্রতিটি কার্বন পরমাণু তিনটি হাইড্রোজেন পরমাণুর সাথে আবদ্ধ
ইথেনের ইলেকট্রন বিন্দু গঠন চিত্র 4.6(c)-এ দেখানো হয়েছে।
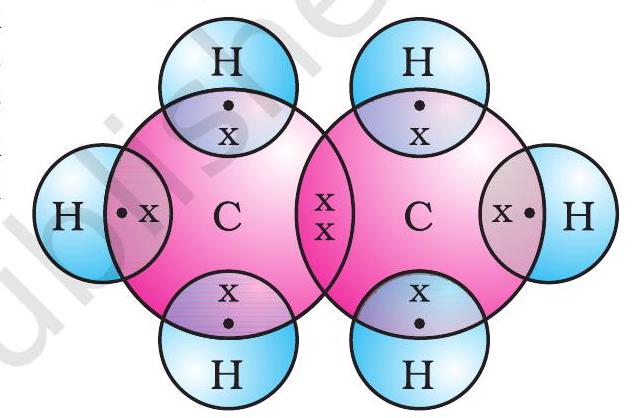
চিত্র 4.6 (c) ইথেনের ইলেকট্রন বিন্দু গঠন
আপনি কি প্রোপেনের কাঠামো আঁকতে পারেন, যার আণবিক সূত্র $C_3 H_8$ একইভাবে? আপনি দেখবেন যে সমস্ত পরমাণুর যোজনী তাদের মধ্যে একক বন্ধন দ্বারা সন্তুষ্ট হয়। এই ধরনের কার্বন যৌগগুলিকে সম্পৃক্ত যৌগ বলে। এই যৌগগুলি সাধারণত খুব বিক্রিয়াশীল নয়।
যাইহোক, কার্বন ও হাইড্রোজেনের আরেকটি যৌগের সূত্র $C_2 H_4$ এবং একে ইথিন বলে। এই অণুটিকে কীভাবে চিত্রিত করা যেতে পারে? আমরা উপরের মতো একই ধাপ অনুসরণ করি।
একটি একক বন্ধন দ্বারা যুক্ত কার্বন-কার্বন পরমাণু (ধাপ 1)।
আমরা দেখি যে কার্বন পরমাণু প্রতি একটি যোজনী অসন্তুষ্ট থাকে (ধাপ 2)। এটি শুধুমাত্র তখনই সন্তুষ্ট হতে পারে যদি দুটি কার্বনের মধ্যে একটি দ্বি-বন্ধন থাকে (ধাপ 3)।
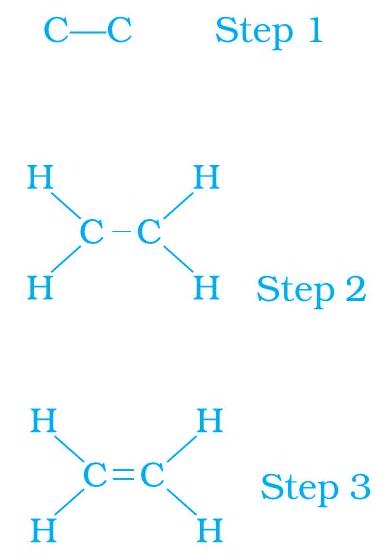
ইথিনের জন্য ইলেকট্রন বিন্দু গঠন চিত্র 4.7-এ দেওয়া হয়েছে।
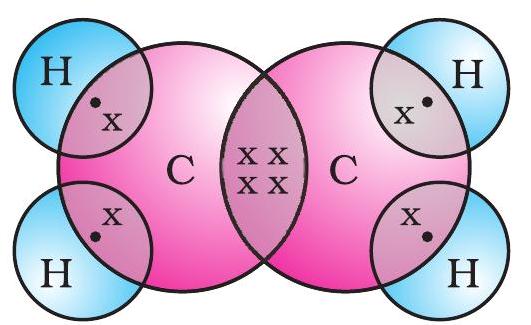
চিত্র 4.7 ইথিনের কাঠামো
হাইড্রোজেন ও কার্বনের আরেকটি যৌগের সূত্র $C_2 H_2$ এবং একে ইথাইন বলে। আপনি কি ইথাইনের জন্য ইলেকট্রন বিন্দু গঠন আঁকতে পারেন? তাদের যোজনী সন্তুষ্ট করার জন্য দুটি কার্বন পরমাণুর মধ্যে কতগুলি বন্ধন প্রয়োজন? কার্বনের এই ধরনের যৌগ যাদের কার্বন পরমাণুগুলির মধ্যে দ্বি- বা ত্রি-বন্ধন রয়েছে তাদের অসম্পৃক্ত কার্বন যৌগ বলে জানা যায় এবং তারা সম্পৃক্ত কার্বন যৌগের চেয়ে বেশি বিক্রিয়াশীল।
4.2.2 শৃঙ্খল, শাখা ও বলয়
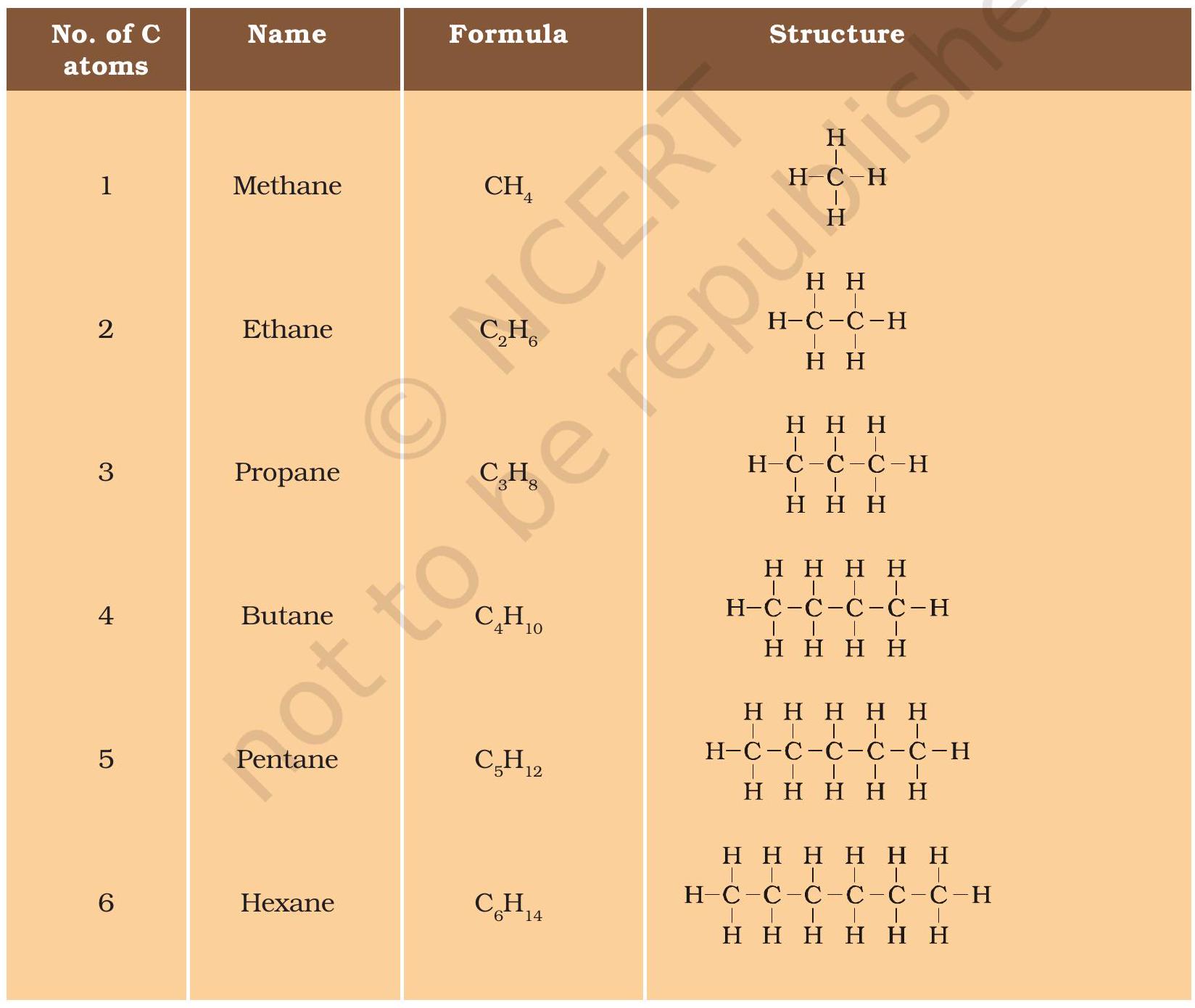
পূর্ববর্তী বিভাগে, আমরা কার্বন যৌগ মিথেন, ইথেন এবং প্রোপেনের কথা উল্লেখ করেছি, যাতে যথাক্রমে 1,2 এবং 3টি কার্বন পরমাণু রয়েছে। কার্বন পরমাণুর এই ধরনের ‘শৃঙ্খল’ অনেক বেশি কার্বন পরমাণু ধারণ করতে পারে। এগুলির মধ্যে ছয়টির নাম ও গঠন সারণী 4.2-এ দেওয়া হয়েছে।
সারণী 4.2 কার্বন ও হাইড্রোজেনের সম্পৃক্ত যৌগের সূত্র ও গঠন
কিন্তু, আসুন বুটেনের আরেকটি দিকে নজর দিই। যদি আমরা চারটি কার্বন পরমাণু দিয়ে কার্বন ‘কঙ্কাল’ তৈরি করি, আমরা দেখি যে দুটি ভিন্ন সম্ভাব্য ‘কঙ্কাল’ হল -

চিত্র 4.8 (a) দুটি সম্ভাব্য কার্বন-কঙ্কাল
অবশিষ্ট যোজনী হাইড্রোজেন দিয়ে পূরণ করলে আমরা পাই -
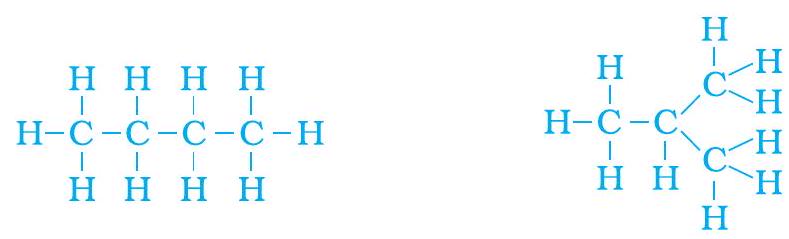
চিত্র 4.8 (b) সূত্র $C_4 H _{10}$ বিশিষ্ট দুটি গঠনের জন্য সম্পূর্ণ অণু
আমরা দেখি যে এই দুটি গঠনেরই একই সূত্র $C_4 H _{10}$ রয়েছে। এই ধরনের যৌগ যাদের আণবিক সূত্র অভিন্ন কিন্তু গঠন ভিন্ন, তাদের গঠনগত সমাবয়বী বলে।
সরল ও শাখাযুক্ত কার্বন শৃঙ্খল ছাড়াও, কিছু যৌগের কার্বন পরমাণু একটি বলয়ের আকারে সজ্জিত থাকে। উদাহরণস্বরূপ, সাইক্লোহেক্সেনের সূত্র $C_6 H _{12}$ এবং নিম্নলিখিত গঠন রয়েছে -
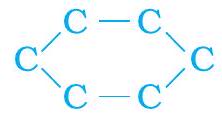
(a)
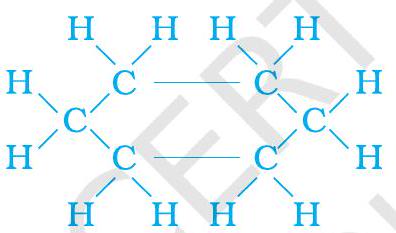
(b)
চিত্র 4.9 সাইক্লোহেক্সেনের কাঠামো (a) কার্বন কঙ্কাল (b) সম্পূর্ণ অণু
আপনি কি সাইক্লোহেক্সেনের জন্য ইলেকট্রন বিন্দু গঠন আঁকতে পারেন? সরল শৃঙ্খল, শাখাযুক্ত শৃঙ্খল এবং চক্রাকার কার্বন যৌগ, সবই সম্পৃক্ত বা অসম্পৃক্ত হতে পারে। উদাহরণস্বরূপ, বেনজিন, $C_6 H_6$, এর নিম্নলিখিত গঠন রয়েছে-
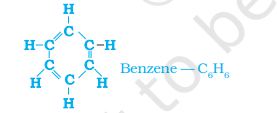
চিত্র 4.10 বেনজিনের কাঠামো
এই সমস্ত কার্বন যৌগ যা শুধুমাত্র কার্বন ও হাইড্রোজেন ধারণ করে তাদের হাইড্রোকার্বন বলে। এর মধ্যে, সম্পৃক্ত হাইড্রোকার্বনগুলিকে অ্যালকেন বলে। অসম্পৃক্ত হাইড্রোকার্বন যেগুলি একটি বা একাধিক দ্বি-বন্ধন ধারণ করে তাদের অ্যালকিন বলে। যেগুলি একটি বা একাধিক ত্রি-বন্ধন ধারণ করে তাদের অ্যালকাইন বলে।
4.2.3 তুমি কি আমার বন্ধু হবে?
কার্বন একটি খুব বন্ধুত্বপূর্ণ মৌল বলে মনে হয়। এখন পর্যন্ত আমরা শুধুমাত্র কার্বন ও হাইড্রোজেন ধারণকারী যৌগ দেখছি। কিন্তু কার্বন হ্যালোজেন, অক্সিজেন, নাইট্রোজেন এবং সালফারের মতো অন্যান্য মৌলের সাথেও বন্ধন গঠন করে। একটি হাইড্রোকার্বন শৃঙ্খলে, একটি বা একাধিক হাইড্রোজেন এই মৌলগুলি দ্বারা প্রতিস্থাপিত হতে পারে, যেমন যে কার্বনের যোজনী সন্তুষ্ট থাকে। এই ধরনের যৌগে, হাইড্রোজেন প্রতিস্থাপনকারী মৌলটিকে একটি বিষম পরমাণু হিসাবে উল্লেখ করা হয়। এই বিষম পরমাণুগুলি সারণী 4.3-এ প্রদত্ত কিছু মূলক হিসাবেও উপস্থিত থাকে।
সারণী 4.3 কার্বন যৌগে কিছু কার্যকরী মূলক
| বিষম পরমাণু | যৌগের শ্রেণি | কার্যকরী মূলকের সূত্র |
|---|---|---|
| $Cl / Br$ | হ্যালো- (ক্লোরো/ব্রোমো) অ্যালকেন | $\quad-Cl,-Br$ (হাইড্রোজেন পরমাণুর জন্য প্রতিস্থাপন করে) |
| অক্সিজেন | 1. অ্যালকোহল | $-OH$ |
| 2. অ্যালডিহাইড | ||
| 3. কিটোন | $\stackrel{\|}{O}$ | |
| 4. কার্বক্সিলিক অ্যাসিড |
এই বিষম পরমাণুগুলি এবং এগুলি ধারণকারী মূলকটি যৌগটিকে নির্দিষ্ট ধর্ম প্রদান করে, কার্বন শৃঙ্খলের দৈর্ঘ্য ও প্রকৃতি নির্বিশেষে এবং তাই এগুলিকে কার্যকরী মূলক বলে। কিছু গুরুত্বপূর্ণ কার্যকরী মূলক সারণী 4.3-এ দেওয়া হয়েছে। মূলকের মুক্ত যোজনী বা যোজনীগুলি একক রেখা দ্বারা দেখানো হয়েছে। কার্যকরী মূলকটি এই যোজনীর মাধ্যমে একটি হাইড্রোজেন পরমাণু বা পরমাণু প্রতিস্থাপন করে কার্বন শৃঙ্খলের সাথে যুক্ত থাকে।
4.2.4 সমধর্মী শ্রেণি
আপনি দেখেছেন যে কার্বন পরমাণুগুলি বিভিন্ন দৈর্ঘ্যের শৃঙ্খল গঠনের জন্য একসাথে যুক্ত হতে পারে। এই শৃঙ্খলগুলি শাখাযুক্তও হতে পারে। তদুপরি, এই কার্বন শৃঙ্খলের হাইড্রোজেন পরমাণু বা অন্যান্য পরমাণু উপরে আমরা দেখেছি এমন যেকোনো কার্যকরী মূলক দ্বারা প্রতিস্থাপিত হতে পারে। অ্যালকোহলের মতো একটি কার্যকরী মূলকের উপস্থিতি কার্বন শৃঙ্খলের দৈর্ঘ্য নির্বিশেষে কার্বন যৌগের ধর্ম নির্ধারণ করে। উদাহরণস্বরূপ, $CH_3 OH, C_2 H_5 OH, C_3 H_7 OH$ এবং $C_4 H_9 OH$ এর রাসায়নিক ধর্ম সবই খুব অনুরূপ। তাই, এই ধরনের একটি যৌগের শ্রেণি যেখানে একই কার্যকরী মূলক একটি কার্বন শৃঙ্খলে হাইড্রোজেনের জন্য প্রতিস্থাপন করে তাকে সমধর্মী শ্রেণি বলে।
আসুন আমরা সারণী 4.2-এ আগে দেখা সমধর্মী শ্রেণিটি দেখি। যদি আমরা পরপর যৌগগুলির সূত্র দেখি, বলুন -
$\mathrm{CH}_4$ এবং $\mathrm{C}_2 \mathrm{H}_6 \quad-$ এগুলি একটি $-\mathrm{CH}_2$ - একক দ্বারা পৃথক
$\mathrm{C}_2 \mathrm{H}_6$ এবং $\mathrm{C}_3 \mathrm{H}_8 \quad-$ এগুলি একটি $-\mathrm{CH}_2^2$ - একক দ্বারা পৃথক
পরবর্তী জোড়ার মধ্যে পার্থক্য কী - প্রোপেন এবং বুটেন $(C_4 H_{10})$ ?
আপনি কি এই জোড়াগুলির মধ্যে আণবিক ভরের পার্থক্য খুঁজে পেতে পারেন (কার্বনের পারমাণবিক ভর $12 u$ এবং হাইড্রোজেনের পারমাণবিক ভর $1 u$) ?
একইভাবে, অ্যালকিনের জন্য সমধর্মী শ্রেণি নিন। শ্রেণিটির প্রথম সদস্য হল ইথিন যা আমরা ইতিমধ্যেই বিভাগ 4.2.1-এ দেখেছি। ইথিনের সূত্র কী? পরবর্তী সদস্যদের সূত্র $C_3 H_6, C_4 H_8$ এবং $C_5 H _{10}$। এগুলিও কি একটি $-CH_2-$ একক দ্বারা পৃথক? আপনি কি এই যৌগগুলিতে কার্বন ও হাইড্রোজেন পরমাণুর সংখ্যার মধ্যে কোনো সম্পর্ক দেখ











