అధ్యాయం 04 కార్బన్ మరియు దాని సమ్మేళనాలు
గత అధ్యాయంలో, మనకు ముఖ్యమైన అనేక సమ్మేళనాలను తెలుసుకున్నాము. ఈ అధ్యాయంలో మనం మరికొన్ని ఆసక్తికరమైన సమ్మేళనాలు మరియు వాటి లక్షణాలను అధ్యయనం చేస్తాము. అలాగే, మనం కార్బన్ గురించి నేర్చుకుంటాము, ఇది మూలక రూపంలో మరియు సంయోగ రూపంలో రెండింటిలోనూ మనకు చాలా ప్రాముఖ్యత కలిగిన మూలకం.
కృత్యం 4.1
- ఉదయం నుండి మీరు ఉపయోగించిన లేదా వినియోగించిన పది వస్తువుల జాబితాను తయారు చేయండి.
- ఈ జాబితాను మీ సహాధ్యాయులు తయారు చేసిన జాబితాలతో కలిపి, ఆపై వస్తువులను ప్రక్కనే ఉన్న పట్టికలో క్రమబద్ధీకరించండి.
- ఒకటి కంటే ఎక్కువ పదార్థాలతో తయారు చేయబడిన వస్తువులు ఉంటే, వాటిని పట్టికలోని రెండు సంబంధిత నిలువు వరుసలలో ఉంచండి.
| లోహంతో తయారైన వస్తువులు | లోహంతో తయారైన వస్తువులు | ఇతరాలు |
|---|---|---|
మీరు పూరించిన పై పట్టికలోని చివరి నిలువు వరుసలో వచ్చే వస్తువులను చూడండి - వాటిలో చాలా వరకు కార్బన్ సమ్మేళనాలతో తయారు చేయబడినవి అని మీ ఉపాధ్యాయుడు మీకు చెప్పగలరు. దీన్ని పరీక్షించడానికి మీరు ఒక పద్ధతి ఆలోచించగలరా? కార్బన్ ఉన్న సమ్మేళనాన్ని మండించినట్లయితే ఉత్పత్తి ఏమిటి? దీన్ని నిర్ధారించడానికి మీకు ఏదైనా పరీక్ష తెలుసా?
ఆహారం, బట్టలు, మందులు, పుస్తకాలు లేదా మీరు జాబితా చేసిన అనేక వస్తువులు ఈ బహుముఖ మూలకమైన కార్బన్ ఆధారంగా ఉంటాయి. అదనంగా, అన్ని జీవ నిర్మాణాలు కార్బన్ ఆధారితమైనవి. భూపటలంలో మరియు వాతావరణంలో ఉన్న కార్బన్ పరిమాణం చాలా తక్కువ. భూపటలంలో ఖనిజాల రూపంలో (కార్బొనేట్లు, హైడ్రోజన్ కార్బొనేట్లు, బొగ్గు మరియు పెట్రోలియం వంటివి) $0.02 %$ కార్బన్ మాత్రమే ఉంటుంది మరియు వాతావరణంలో కార్బన్ డయాక్సైడ్ యొక్క $0.03 %$ ఉంటుంది. ప్రకృతిలో లభించే ఈ చిన్న మొత్తంలో కార్బన్ ఉన్నప్పటికీ, కార్బన్ యొక్క ప్రాముఖ్యత చాలా ఎక్కువగా ఉన్నట్లు కనిపిస్తుంది. ఈ అధ్యాయంలో, కార్బన్ మనకు ఎందుకు ఇంత ముఖ్యమైనదో చేసే కార్బన్ లక్షణాలను తెలుసుకుంటాము.
4.1 కార్బన్లో బంధనం - సహసంయోజక బంధం
మునుపటి అధ్యాయంలో, మనం అయానిక సమ్మేళనాల లక్షణాలను అధ్యయనం చేసాము. అయానిక సమ్మేళనాలు అధిక ద్రవీభవన మరియు బాష్పీభవన స్థానాలను కలిగి ఉంటాయని మరియు ద్రావణంలో లేదా ద్రవీకృత స్థితిలో విద్యుత్ ను ప్రవహింపజేస్తాయని మనం చూశాము. అయానిక సమ్మేళనాలలో బంధన స్వభావం ఈ లక్షణాలను ఎలా వివరిస్తుందో కూడా మనం చూశాము. ఇప్పుడు కొన్ని కార్బన్ సమ్మేళనాల లక్షణాలను అధ్యయనం చేద్దాం.
మనం అధ్యాయం 2లో చూసినట్లుగా, చాలా కార్బన్ సమ్మేళనాలు విద్యుత్ యొక్క పేలవమైన వాహకాలు. కార్బన్ సమ్మేళనాల బాష్పీభవన మరియు ద్రవీభవన స్థానాలపై టేబుల్ 4.1లో ఇచ్చిన డేటా నుండి, ఈ సమ్మేళనాలు అయానిక సమ్మేళనాలతో పోల్చినప్పుడు (అధ్యాయం 3) తక్కువ ద్రవీభవన మరియు బాష్పీభవన స్థానాలను కలిగి ఉన్నాయని మనం కనుగొంటాము. అణువుల మధ్య ఆకర్షణ బలాలు చాలా బలంగా లేవని మనం నిర్ధారించవచ్చు. ఈ సమ్మేళనాలు ఎక్కువగా విద్యుత్ ని ప్రవహింపజేయవు కాబట్టి, ఈ సమ్మేళనాలలోని బంధనం ఏ అయాన్లను ఏర్పరచదని మనం నిర్ధారించవచ్చు.
టేబుల్ 4.1 కొన్ని కార్బన్ సమ్మేళనాల ద్రవీభవన మరియు బాష్పీభవన స్థానాలు
| సమ్మేళనం | ద్రవీభవన స్థానం $(\mathbf{K})$ | బాష్పీభవన స్థానం $(\mathbf{K})$ |
|---|---|---|
| ఎసిటిక్ ఆమ్లం $(CH_3 COOH)$ | 290 | 391 |
| క్లోరోఫారం $(CHCl_3)$ | 209 | 334 |
| ఇథనాల్ $(CH_3 CH_2 OH)$ | 156 | 351 |
| మీథేన్ $(CH_4)$ | 90 | 111 |
తరగతి IXలో, మనం వివిధ మూలకాల సంయోజన సామర్థ్యం మరియు అది వేలెన్స్ ఎలక్ట్రాన్ల సంఖ్యపై ఎలా ఆధారపడి ఉంటుందో నేర్చుకున్నాము. ఇప్పుడు కార్బన్ యొక్క ఎలక్ట్రాన్ విన్యాసాన్ని చూద్దాం. కార్బన్ యొక్క పరమాణు సంఖ్య 6. కార్బన్ యొక్క వివిధ షెల్లలో ఎలక్ట్రాన్ల పంపిణీ ఎలా ఉంటుంది? కార్బన్కు ఎన్ని వేలెన్స్ ఎలక్ట్రాన్లు ఉంటాయి?
మూలకాల చర్యాశీలత వాటి బాహ్య కర్పరాన్ని పూర్తిగా నింపుకోవడానికి ఉన్న ధోరణిగా వివరించబడుతుందని మనకు తెలుసు, అంటే, నోబుల్ వాయువు విన్యాసాన్ని పొందడం. అయానిక సమ్మేళనాలను ఏర్పరిచే మూలకాలు బాహ్య కర్పరం నుండి ఎలక్ట్రాన్లను గెలుచుకోవడం లేదా కోల్పోవడం ద్వారా దీన్ని సాధిస్తాయి. కార్బన్ విషయంలో, దాని బాహ్య కర్పరంలో నాలుగు ఎలక్ట్రాన్లు ఉంటాయి మరియు నోబుల్ వాయువు విన్యాసాన్ని పొందడానికి నాలుగు ఎలక్ట్రాన్లను గెలుచుకోవాలి లేదా కోల్పోవాలి. అది ఎలక్ట్రాన్లను గెలుచుకున్నట్లయితే లేదా కోల్పోయినట్లయితే -
(i) ఇది $C^{4-}$ యానయాన్ని ఏర్పరుస్తూ నాలుగు ఎలక్ట్రాన్లను గెలుచుకోగలదు. కానీ ఆరు ప్రోటాన్లతో కూడిన కేంద్రకం పది ఎలక్ట్రాన్లను, అంటే, నాలుగు అదనపు ఎలక్ట్రాన్లను పట్టుకోవడం కష్టంగా ఉంటుంది.
(ii) ఇది $C^{4+}$ కాటయాన్ని ఏర్పరుస్తూ నాలుగు ఎలక్ట్రాన్లను కోల్పోగలదు. కానీ కేంద్రకంలో ఆరు ప్రోటాన్లతో కూడిన కార్బన్ కాటయాన్ను వదిలిపెట్టి కేవలం రెండు ఎలక్ట్రాన్లను మాత్రమే పట్టుకోవడానికి నాలుగు ఎలక్ట్రాన్లను తొలగించడానికి ఎక్కువ మొత్తంలో శక్తి అవసరం అవుతుంది.
కార్బన్ తన వేలెన్స్ ఎలక్ట్రాన్లను కార్బన్ యొక్క ఇతర పరమాణువులతో లేదా ఇతర మూలకాల పరమాణువులతో పంచుకోవడం ద్వారా ఈ సమస్యను అధిగమిస్తుంది. కేవలం కార్బన్ మాత్రమే కాదు, అనేక ఇతర మూలకాలు కూడా ఈ విధంగా ఎలక్ట్రాన్లను పంచుకోవడం ద్వారా అణువులను ఏర్పరుస్తాయి. పంచుకున్న ఎలక్ట్రాన్లు రెండు పరమాణువుల బాహ్య కర్పరాలకు ‘చెందినవి’ మరియు రెండు పరమాణువులు నోబుల్ వాయువు విన్యాసాన్ని పొందడానికి దారి తీస్తాయి. కార్బన్ సమ్మేళనాలకు వెళ్లే ముందు, వేలెన్స్ ఎలక్ట్రాన్ల పంపిణీ ద్వారా ఏర్పడిన కొన్ని సరళ అణువులను చూద్దాం.
ఈ విధంగా ఏర్పడిన సరళమైన అణువు హైడ్రోజన్ యొక్కది. మీరు ఇంతకు ముందు నేర్చుకున్నట్లుగా, హైడ్రోజన్ యొక్క పరమాణు సంఖ్య 1. అందువల్ల హైడ్రోజన్ దాని $K$ షెల్లో ఒక ఎలక్ట్రాన్ని కలిగి ఉంటుంది మరియు $K$ షెల్ను నింపడానికి ఇంకో ఎలక్ట్రాన్ అవసరం. కాబట్టి రెండు హైడ్రోజన్ పరమాణువులు హైడ్రోజన్ అణువు, $H_2$ ను ఏర్పరచడానికి వాటి ఎలక్ట్రాన్లను పంచుకుంటాయి. ఇది ప్రతి హైడ్రోజన్ పరమాణువు దాని K షెల్లో రెండు ఎలక్ట్రాన్లను కలిగి ఉన్న సమీప నోబుల్ వాయువు, హీలియం యొక్క ఎలక్ట్రాన్ విన్యాసాన్ని పొందడానికి అనుమతిస్తుంది. వేలెన్స్ ఎలక్ట్రాన్లను సూచించడానికి చుక్కలు లేదా క్రాస్లను ఉపయోగించి దీన్ని మనం వర్ణించవచ్చు (Fig. 4.1).
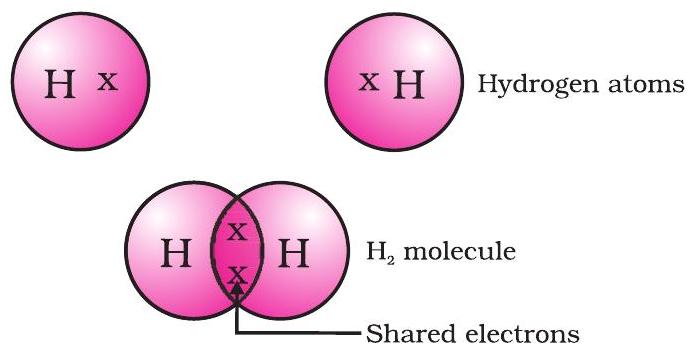
Figure 4.1 హైడ్రోజన్ యొక్క ఒక అణువు
పంచుకున్న ఎలక్ట్రాన్ జత రెండు హైడ్రోజన్ పరమాణువుల మధ్య ఒక సింగిల్ సహసంయోజక బంధాన్ని ఏర్పరుస్తుంది. ఒక సింగిల్ సహసంయోజక బంధం కూడా రెండు పరమాణువుల మధ్య ఒక రేఖ ద్వారా సూచించబడుతుంది, Fig. 4.2లో చూపినట్లుగా.
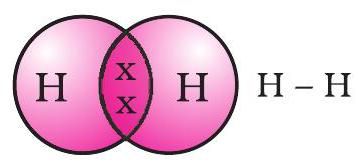
Figure 4.2 రెండు హైడ్రోజన్ పరమాణువుల మధ్య సింగిల్ బంధం
క్లోరిన్ యొక్క పరమాణు సంఖ్య 17. దాని ఎలక్ట్రాన్ విన్యాసం మరియు దాని సంయోజకత ఏమిటి? క్లోరిన్ ఒక డయాటోమిక్ అణువును ఏర్పరుస్తుంది, $Cl_2$. మీరు ఈ అణువు కోసం ఎలక్ట్రాన్ డాట్ నిర్మాణాన్ని గీయగలరా? వేలెన్స్ షెల్ ఎలక్ట్రాన్లను మాత్రమే వర్ణించాల్సిన అవసరం ఉందని గమనించండి.
ఆక్సిజన్ విషయంలో, మనం రెండు ఆక్సిజన్ పరమాణువుల మధ్య డబుల్ బంధం ఏర్పడటాన్ని చూస్తాము. ఎందుకంటే ఆక్సిజన్ పరమాణువు దాని L షెల్లో ఆరు ఎలక్ట్రాన్లను కలిగి ఉంటుంది (ఆక్సిజన్ పరమాణు సంఖ్య ఎనిమిది) మరియు దాని ఆక్టెట్ను పూర్తి చేయడానికి ఇంకో రెండు ఎలక్ట్రాన్లు అవసరం. కాబట్టి ప్రతి ఆక్సిజన్ పరమాణువు మరొక ఆక్సిజన్ పరమాణువుతో రెండు ఎలక్ట్రాన్లను పంచుకుంటుంది, Fig. 4.3లో చూపిన నిర్మాణాన్ని ఇస్తుంది. ప్రతి ఆక్సిజన్ పరమాణువు ద్వారా సహకరించబడిన రెండు ఎలక్ట్రాన్లు రెండు పంచుకున్న ఎలక్ట్రాన్ జతలను ఏర్పరుస్తాయి. ఇది రెండు పరమాణువుల మధ్య డబుల్ బంధాన్ని ఏర్పరుస్తుంది అని చెప్పబడుతుంది.
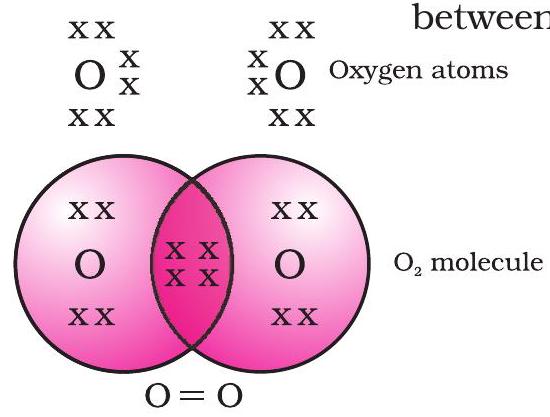
Figure 4.3 రెండు ఆక్సిజన్ పరమాణువుల మధ్య డబుల్ బంధం
మీరు ఇప్పుడు ఒక ఆక్సిజన్ పరమాణువు మరియు రెండు హైడ్రోజన్ పరమాణువుల మధ్య బంధన స్వభావాన్ని చూపించే నీటి అణువును వర్ణించగలరా? అణువు సింగిల్ బంధాలను కలిగి ఉందా లేదా డబుల్ బంధాలను కలిగి ఉందా?
నత్రజని యొక్క డయాటోమిక్ అణువు విషయంలో ఏమి జరుగుతుంది? నత్రజని పరమాణు సంఖ్య 7. దాని ఎలక్ట్రాన్ విన్యాసం మరియు దాని సంయోజన సామర్థ్యం ఏమిటి? ఆక్టెట్ను పొందడానికి, నత్రజని అణువులోని ప్రతి నత్రజని పరమాణువు మూడు ఎలక్ట్రాన్లను సహకరిస్తుంది, మూడు పంచుకున్న ఎలక్ట్రాన్ జతలను ఏర్పరుస్తుంది. ఇది రెండు పరమాణువుల మధ్య ట్రిపుల్ బంధాన్ని ఏర్పరుస్తుంది అని చెప్పబడుతుంది Figure 4.3. $N_2$ యొక్క ఎలక్ట్రాన్ డాట్ నిర్మాణం మరియు రెండు ఆక్సిజన్ పరమాణువుల మధ్య డబుల్ బంధం Fig. 4.4లో చూపినట్లుగా వర్ణించబడుతుంది.
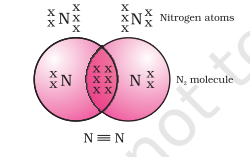
Figure 4.4 రెండు నత్రజని పరమాణువుల మధ్య ట్రిపుల్ బంధం
అమ్మోనియా అణువు సూత్రం $NH_3$ కలిగి ఉంటుంది. నాలుగు పరమాణువులూ నోబుల్ వాయువు విన్యాసాన్ని ఎలా సాధిస్తాయో చూపించే ఈ అణువు కోసం మీరు ఎలక్ట్రాన్ డాట్ నిర్మాణాన్ని గీయగలరా? అణువు సింగిల్, డబుల్ లేదా ట్రిపుల్ బంధాలను కలిగి ఉంటుందా?
ఇప్పుడు మీథేన్ను పరిశీలిద్దాం, ఇది కార్బన్ యొక్క సమ్మేళనం. మీథేన్ ఇంధనంగా విస్తృతంగా ఉపయోగించబడుతుంది మరియు బయో-గ్యాస్ మరియు కంప్రెస్డ్ నేచురల్ గ్యాస్ (CNG) యొక్క ప్రధాన భాగం. ఇది కార్బన్ ద్వారా ఏర్పడిన సరళమైన సమ్మేళనాలలో ఒకటి. మీథేన్ సూత్రం $CH_4$ కలిగి ఉంటుంది. మీకు తెలిసినట్లుగా, హైడ్రోజన్ సంయోజకత 1. కార్బన్ టెట్రావేలెంట్ ఎందుకంటే దానికి నాలుగు వేలెన్స్ ఎలక్ట్రాన్లు ఉన్నాయి. నోబుల్ వాయువు విన్యాసాన్ని సాధించడానికి, కార్బన్ ఈ ఎలక్ట్రాన్లను Fig. 4.5లో చూపినట్లుగా నాలుగు హైడ్రోజన్ పరమాణువులతో పంచుకుంటుంది.
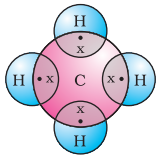
Figure 4.5 మీథేన్ కోసం ఎలక్ట్రాన్ డాట్ నిర్మాణం
రెండు పరమాణువుల మధ్య ఎలక్ట్రాన్ జతను పంచుకోవడం ద్వారా ఏర్పడే ఇటువంటి బంధాలు సహసంయోజక బంధాలు అని పిలువబడతాయి. సహసంయోజకంగా బంధితమైన అణువులు అణువు లోపల బలమైన బంధాలను కలిగి ఉన్నట్లు కనిపిస్తాయి, కానీ అంతర అణు బలాలు బలహీనంగా ఉంటాయి. ఇది ఈ సమ్మేళనాల తక్కువ ద్రవీభవన మరియు బాష్పీభవన స్థానాలకు దారి తీస్తుంది. ఎలక్ట్రాన్లు పరమాణువుల మధ్య పంచుకోబడినందున మరియు ఏ ఆవేశిత కణాలు ఏర్పడవు కాబట్టి, అటువంటి సహసంయోజక సమ్మేళనాలు సాధారణంగా విద్యుత్ యొక్క పేలవమైన వాహకాలు.
మరింత తెలుసుకోవడానికి!
కార్బన్ యొక్క అలోట్రోప్లు
మూలకం కార్బన్ ప్రకృతిలో వివిధ రూపాలలో వ్యాపక భౌతిక లక్షణాలతో సంభవిస్తుంది. డైమండ్ మరియు గ్రాఫైట్ రెండూ కార్బన్ పరమాణువుల ద్వారా ఏర్పడతాయి, వ్యత్యాసం కార్బన్ పరమాణువులు ఒకదానితో ఒకటి బంధించబడిన పద్ధతిలో ఉంటుంది. డైమండ్లో, ప్రతి కార్బన్ పరమాణువు మరో నాలుగు కార్బన్ పరమాణువులతో బంధించబడి దృఢమైన త్రిమితీయ నిర్మాణాన్ని ఏర్పరుస్తుంది. గ్రాఫైట్లో, ప్రతి కార్బన్ పరమాణువు అదే తలంలో ఉన్న మరో మూడు కార్బన్ పరమాణువులతో బంధించబడి షడ్భుజి శ్రేణిని ఇస్తుంది. ఈ బంధాలలో ఒకటి డబుల్-బంధం, మరియు అందువలన కార్బన్ యొక్క సంయోజకత సంతృప్తి చెందుతుంది. గ్రాఫైట్ నిర్మాణం షడ్భుజి శ్రేణులు ఒకదాని పైన ఒకటి పొరలుగా ఉంచడం ద్వారా ఏర్పడుతుంది.
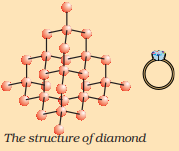
డైమండ్ యొక్క నిర్మాణం
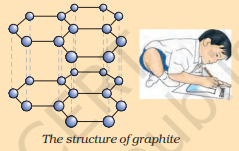
గ్రాఫైట్ యొక్క నిర్మాణం
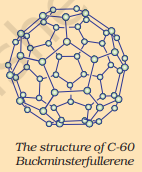
C-60 బక్మిన్స్టర్ఫుల్లరీన్ యొక్క నిర్మాణం
ఈ రెండు వేర్వేరు నిర్మాణాలు డైమండ్ మరియు గ్రాఫైట్ వాటి రసాయన లక్షణాలు ఒకేలా ఉన్నప్పటికీ చాలా వేర్వేరు భౌతిక లక్షణాలను కలిగి ఉండటానికి దారి తీస్తాయి. డైమండ్ తెలిసిన కఠినమైన పదార్థం అయితే గ్రాఫైట్ మృదువుగా మరియు జారుడుగా ఉంటుంది. గ్రాఫైట్ కూడా మీరు మునుపటి అధ్యాయంలో అధ్యయనం చేసిన ఇతర అలోహాలకు భిన్నంగా విద్యుత్ యొక్క చాలా మంచి వాహకం.
స్వచ్ఛమైన కార్బన్ను చాలా అధిక పీడనం మరియు ఉష్ణోగ్రతకు గురిచేయడం ద్వారా డైమండ్లను సంశ్లేషణ చేయవచ్చు. ఈ సింథటిక్ డైమండ్లు చిన్నవి కానీ సహజ డైమండ్ల నుండి వేరుగా గుర్తించలేనివి.
ఫుల్లరీన్లు కార్బన్ అలోట్రోప్ల యొక్క మరొక తరగతిని ఏర్పరుస్తాయి. గుర్తించబడిన మొదటిది C-60, ఇది ఫుట్బాల్ ఆకారంలో అమర్చబడిన కార్బన్ పరమాణువులను కలిగి ఉంటుంది. ఇది US ఆర్కిటెక్ట్ బక్మిన్స్టర్ ఫుల్లర్ రూపకల్పన చేసిన జియోడెసిక్ గుమ్మటం లాగా కనిపించినందున, అణువుకు ఫుల్లరీన్ అని పేరు పెట్టారు.
4.2 కార్బన్ యొక్క బహుముఖ స్వభావం
వివిధ మూలకాలు మరియు సమ్మేళనాలలో ఎలక్ట్రాన్లను పంచుకోవడం ద్వారా సహసంయోజక బంధాల ఏర్పాటును మనం చూశాము. మనం సరళ కార్బన్ సమ్మేళనం, మీథేన్ యొక్క నిర్మాణాన్ని కూడా చూశాము. అధ్యాయం ప్రారంభంలో, మనం ఉపయోగించే ఎన్ని వస్తువులు కార్బన్ను కలిగి ఉన్నాయో చూశాము. వాస్తవానికి, మనమే కార్బన్ సమ్మేళనాలతో తయారు చేయబడ్డాము. రసాయన శాస్త్రవేత్తలకు తెలిసిన సూత్రాలు కలిగిన కార్బన్ సమ్మేళనాల సంఖ్య ఇటీవల మిలియన్లలో ఉంటుందని అంచనా వేయబడింది! ఇది మిగిలిన అన్ని మూలకాలు కలిపి ఏర్పరిచిన సమ్మేళనాల కంటే చాలా ఎక్కువ. ఈ లక్షణం కార్బన్లో మాత్రమే ఎందుకు కనిపిస్తుంది మరియు ఏ ఇతర మూలకంలో కనిపించదు? సహసంయోజక బంధం యొక్క స్వభావం కార్బన్ చాలా సంఖ్యలో సమ్మేళనాలను ఏర్పరచ











