অধ্যায় ০৪ কাৰ্বন আৰু ইয়াৰ যৌগ
আগৰ অধ্যায়ত আমি আমাৰ বাবে গুৰুত্বপূৰ্ণ বহুতো যৌগৰ বিষয়ে জানিব পাৰিছিলো। এই অধ্যায়ত আমি আৰু কেইবাটাও আকৰ্ষণীয় যৌগ আৰু সিহঁতৰ ধৰ্মৰ বিষয়ে অধ্যয়ন কৰিম। লগতে আমি কাৰ্বনৰ বিষয়েও শিকিম, যি এটা মৌল ইয়াৰ মৌলিক ৰূপ আৰু সংযুক্ত ৰূপ দুয়োটাতে আমাৰ বাবে অতি গুৰুত্বপূৰ্ণ।
কাৰ্যকলাপ 4.1
- ৰাতিপুৱাৰে পৰা তুমি ব্যৱহাৰ কৰা বা গ্ৰহণ কৰা দহটা বস্তুৰ তালিকা এখন বনোৱা।
- এই তালিকাখন তোমাৰ সহপাঠীসকলে বনোৱা তালিকাসমূহৰ সৈতে সংকলন কৰা আৰু তাৰ পিছত বস্তুবোৰ তলৰ তালিকাখনত ভাগ কৰা।
- যদি এনে বস্তু থাকে যিবোৰ একাধিক সামগ্ৰীৰে গঠিত, তেন্তে সেইবোৰ তালিকাৰ দুয়োটা প্ৰাসংগিক স্তম্ভত ৰাখিবা।
| ধাতুৰে তৈয়াৰী বস্তু | ধাতুৰে তৈয়াৰী বস্তু | অন্যান্য |
|---|---|---|
তোমাৰ দ্বাৰা পূৰ্ণ কৰা ওপৰৰ তালিকাৰ শেষ স্তম্ভত থকা বস্তুবোৰলৈ চোৱা – তোমাৰ শিক্ষকজনে তোমাক ক’ব পাৰিব যে সেইবোৰৰ বেছিভাগেই কাৰ্বনৰ যৌগৰে গঠিত। এইটো পৰীক্ষা কৰিবলৈ এটা পদ্ধতিৰ কথা ভাবিব পাৰানে? কাৰ্বন থকা যৌগ এটা পোৰিলে কি উৎপন্ন হ’ব? এইটো নিশ্চিত কৰিবলৈ তোমাৰ কোনোবা পৰীক্ষাৰ কথা জনা আছে নেকি?
খাদ্য, কাপোৰ, ঔষধ, কিতাপ, বা তুমি তালিকাভুক্ত কৰা বহুতো বস্তু এই বহুমুখী মৌল কাৰ্বনৰ ওপৰত ভিত্তি কৰি গঢ় লৈছে। ইয়াৰ উপৰি, সকলো জীৱৰ গঠন কাৰ্বন-ভিত্তিক। পৃথিৱীৰ ভূ-ত্বক আৰু বায়ুমণ্ডলত থকা কাৰ্বনৰ পৰিমাণ অতি কম। ভূ-ত্বকত কেৱল $0.02 %$ কাৰ্বন খনিজ পদাৰ্থ (যেনে কাৰ্বনেট, হাইড্ৰজেনকাৰ্বনেট, কয়লা আৰু পেট্ৰ’লিয়াম) ৰ ৰূপত আছে আৰু বায়ুমণ্ডলত $0.03 %$ কাৰ্বন-ডাই-অক্সাইড আছে। প্ৰকৃতিত উপলব্ধ কাৰ্বনৰ এই সীমিত পৰিমাণৰ সত্ত্বেও, কাৰ্বনৰ গুৰুত্ব অতি বেছি যেন লাগে। এই অধ্যায়ত, আমি কাৰ্বনৰ সেই ধৰ্মসমূহৰ বিষয়ে জানিম যিয়ে কাৰ্বনক আমাৰ বাবে ইমান গুৰুত্বপূৰ্ণ কৰি তুলিছে।
4.1 কাৰ্বনত বন্ধন গঠন – সমযোজী বন্ধন
আগৰ অধ্যায়ত, আমি আয়নীয় যৌগৰ ধৰ্মসমূহ অধ্যয়ন কৰিছিলো। আমি দেখিছিলো যে আয়নীয় যৌগৰ উচ্চ গলনাংক আৰু উতলাংক থাকে আৰু দ্ৰৱ বা গলিত অৱস্থাত বিদ্যুৎ পৰিবহণ কৰে। আমি আয়নীয় যৌগত বন্ধনৰ প্ৰকৃতিয়ে কেনেকৈ এই ধৰ্মবোৰ ব্যাখ্যা কৰে তাকো দেখিছিলো। এতিয়া আমি কাৰ্বনৰ কিছুমান যৌগৰ ধৰ্ম অধ্যয়ন কৰো।
বেছিভাগ কাৰ্বন যৌগই বিদ্যুৎৰ কুপৰিবাহী, যিটো আমি অধ্যায় ২ত দেখিছো। কাৰ্বন যৌগৰ উতলাংক আৰু গলনাংকৰ বিষয়ে তালিকা ৪.১ত দিয়া তথ্যৰ পৰা আমি দেখো যে এই যৌগবোৰৰ গলনাংক আৰু উতলাংক আয়নীয় যৌগ (অধ্যায় ৩)ৰ তুলনাত কম। আমি এই সিদ্ধান্তত উপনীত হ’ব পাৰো যে অণুবোৰৰ মাজৰ আকৰ্ষণ বলবোৰ অতি শক্তিশালী নহয়। যিহেতু এই যৌগবোৰ বহুলাংশত বিদ্যুৎৰ অপৰিবাহী, আমি এই সিদ্ধান্তত উপনীত হ’ব পাৰো যে এই যৌগবোৰত বন্ধন গঠনে কোনো আয়নৰ সৃষ্টি নকৰে।
তালিকা 4.1 কিছুমান কাৰ্বন যৌগৰ গলনাংক আৰু উতলাংক
| যৌগ | গলনাংক $(\mathbf{K})$ | উতলাংক $(\mathbf{K})$ |
|---|---|---|
| এছিটিক এছিড $(CH_3 COOH)$ | 290 | 391 |
| ক্ল’ৰ’ফৰ্ম $(CHCl_3)$ | 209 | 334 |
| ইথান’ল $(CH_3 CH_2 OH)$ | 156 | 351 |
| মিথেন $(CH_4)$ | 90 | 111 |
নৱম শ্ৰেণীত, আমি বিভিন্ন মৌলৰ সংযোজন ক্ষমতা আৰু ই কেনেকৈ যোজ্যতা ইলেকট্ৰনৰ সংখ্যাৰ ওপৰত নিৰ্ভৰ কৰে সেই বিষয়ে শিকিছিলো। এতিয়া আমি কাৰ্বনৰ ইলেকট্ৰনীয় বিন্যাসলৈ চাওঁ। কাৰ্বনৰ পাৰমাণৱিক সংখ্যা ৬। কাৰ্বনৰ বিভিন্ন কক্ষত ইলেকট্ৰনৰ বিতৰণ কেনেকুৱা হ’ব? কাৰ্বনৰ কিমানটা যোজ্যতা ইলেকট্ৰন থাকিব?
আমি জানো যে মৌলবোৰৰ সক্ৰিয়তা ইহঁতৰ সম্পূৰ্ণৰূপে পূৰ্ণ বহিঃকক্ষ লাভ কৰাৰ প্ৰৱণতা হিচাপে ব্যাখ্যা কৰা হয়, অৰ্থাৎ, নিষ্ক্ৰিয় গেছৰ বিন্যাস লাভ কৰা। আয়নীয় যৌগ গঠন কৰা মৌলবোৰে বহিঃতম কক্ষৰ পৰা ইলেকট্ৰন লাভ বা হেৰুৱাই এইটো সাধন কৰে। কাৰ্বনৰ ক্ষেত্ৰত, ইয়াৰ বহিঃতম কক্ষত চাৰিটা ইলেকট্ৰন আছে আৰু নিষ্ক্ৰিয় গেছৰ বিন্যাস লাভ কৰিবলৈ চাৰিটা ইলেকট্ৰন লাভ বা হেৰুৱাব লাগিব। যদি ই ইলেকট্ৰন লাভ বা হেৰুৱায় -
(i) ই চাৰিটা ইলেকট্ৰন লাভ কৰি $C^{4-}$ ঋণাত্মক আয়ন গঠন কৰিব পাৰে। কিন্তু ছয়টা প্ৰটন থকা নিউক্লিয়াছে দহটা ইলেকট্ৰন ধৰি ৰাখাটো কঠিন হ’ব, অৰ্থাৎ, চাৰিটা অতিৰিক্ত ইলেকট্ৰন।
(ii) ই চাৰিটা ইলেকট্ৰন হেৰুৱাই $C^{4+}$ ধনাত্মক আয়ন গঠন কৰিব পাৰে। কিন্তু চাৰিটা ইলেকট্ৰন আঁতৰোৱাটোত বেছি শক্তিৰ প্ৰয়োজন হ’ব, যাৰ ফলত কাৰ্বনৰ ধনাত্মক আয়নটোৰ নিউক্লিয়াছত ছয়টা প্ৰটন থাকিব আৰু মাত্ৰ দুটা ইলেকট্ৰন ধৰি ৰাখিব।
কাৰ্বনে ইয়াৰ যোজ্যতা ইলেকট্ৰনবোৰ কাৰ্বনৰ অন্যান্য পৰমাণু বা অন্যান্য মৌলৰ পৰমাণুৰ সৈতে ভাগ বতৰা কৰি এই সমস্যাৰ সমাধান কৰে। কেৱল কাৰ্বনেই নহয়, বহুতো অন্য মৌলেও এই ধৰণে ইলেকট্ৰন ভাগ বতৰা কৰি অণু গঠন কৰে। ভাগ বতৰা কৰা ইলেকট্ৰনবোৰ দুয়োটা পৰমাণুৰ বহিঃতম কক্ষৰ ‘মালিকানা’ হয় আৰু দুয়োটা পৰমাণুৱে নিষ্ক্ৰিয় গেছৰ বিন্যাস লাভ কৰাত সহায় কৰে। কাৰ্বনৰ যৌগলৈ যোৱাৰ আগতে, আমি যোজ্যতা ইলেকট্ৰনৰ ভাগ বতৰাৰ দ্বাৰা গঠিত কিছুমান সৰল অণুলৈ চাওঁ।
এই ধৰণে গঠিত আটাইতকৈ সৰল অণুটো হৈছে হাইড্ৰজেনৰ। তুমি আগতে শিকিছা, হাইড্ৰজেনৰ পাৰমাণৱিক সংখ্যা ১। গতিকে হাইড্ৰজেনৰ $K$ কক্ষত এটা ইলেকট্ৰন আছে আৰু $K$ কক্ষ পূৰণ কৰিবলৈ ইয়াৰ আৰু এটা ইলেকট্ৰনৰ প্ৰয়োজন। গতিকে দুটা হাইড্ৰজেন পৰমাণুৱে ইহঁতৰ ইলেকট্ৰন ভাগ বতৰা কৰি হাইড্ৰজেনৰ এটা অণু, $H_2$ গঠন কৰে। এইটোৱে প্ৰতিটো হাইড্ৰজেন পৰমাণুক ওচৰৰ নিষ্ক্ৰিয় গেছ হিলিয়ামৰ ইলেকট্ৰনীয় বিন্যাস লাভ কৰাত সহায় কৰে, যাৰ K কক্ষত দুটা ইলেকট্ৰন থাকে। আমি যোজ্যতা ইলেকট্ৰনক প্ৰতিনিধিত্ব কৰিবলৈ বিন্দু বা ক্ৰছ ব্যৱহাৰ কৰি এইটো চিত্ৰিত কৰিব পাৰো (চিত্ৰ 4.1)।
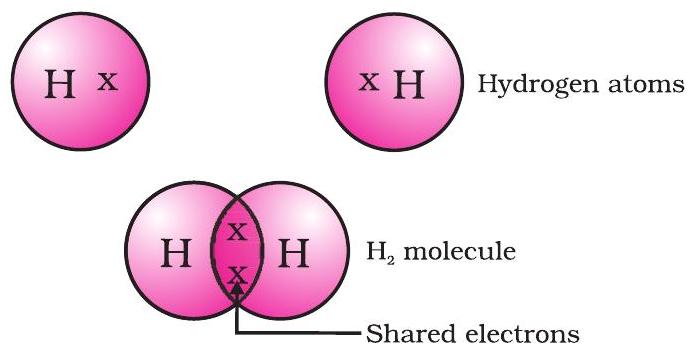
চিত্ৰ 4.1 হাইড্ৰজেনৰ এটা অণু
ভাগ বতৰা কৰা ইলেকট্ৰনৰ যোৰটোক দুটা হাইড্ৰজেন পৰমাণুৰ মাজত এটা একক সমযোজী বন্ধন গঠন কৰা বুলি কোৱা হয়। এটা একক সমযোজী বন্ধনক দুটা পৰমাণুৰ মাজত এডাল ৰেখাৰে চিত্ৰিত কৰা হয়, যেনে চিত্ৰ 4.2ত দেখুওৱা হৈছে।
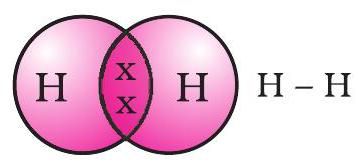
চিত্ৰ 4.2 দুটা হাইড্ৰজেন পৰমাণুৰ মাজৰ একক বন্ধন
ক্ল’ৰিনৰ পাৰমাণৱিক সংখ্যা ১৭। ইয়াৰ ইলেকট্ৰনীয় বিন্যাস আৰু যোজ্যতা কি হ’ব? ক্ল’ৰিনে এটা দ্বি-পাৰমাণৱিক অণু, $Cl_2$ গঠন কৰে। তুমি এই অণুটোৰ বাবে ইলেকট্ৰন বিন্দু গঠন আঁকিব পাৰিবানে? মনত ৰাখিবা যে কেৱল যোজ্যতা কক্ষৰ ইলেকট্ৰনবোৰ চিত্ৰিত কৰাৰ প্ৰয়োজন।
অক্সিজেনৰ ক্ষেত্ৰত, আমি দুটা অক্সিজেন পৰমাণুৰ মাজত এটা দ্বি-বন্ধন গঠন দেখো। এইটো কাৰণ হৈছে যে অক্সিজেনৰ এটা পৰমাণুৰ L কক্ষত ছয়টা ইলেকট্ৰন থাকে (অক্সিজেনৰ পাৰমাণৱিক সংখ্যা আঠ) আৰু ইয়াৰ অষ্টক পূৰ্ণ কৰিবলৈ আৰু দুটা ইলেকট্ৰনৰ প্ৰয়োজন। গতিকে প্ৰতিটো অক্সিজেন পৰমাণুৱে আন এটা অক্সিজেন পৰমাণুৰ সৈতে দুটা ইলেকট্ৰন ভাগ বতৰা কৰি আমাক চিত্ৰ 4.3ত দেখুওৱা গঠনটো দিয়ে। প্ৰতিটো অক্সিজেন পৰমাণুৱে আগবঢ়োৱা দুটা ইলেকট্ৰনে দুটা ভাগ বতৰা কৰা ইলেকট্ৰনৰ যোৰৰ সৃষ্টি কৰে। এইটোক দুটা পৰমাণুৰ মাজত এটা দ্বি-বন্ধন গঠন কৰা বুলি কোৱা হয়।
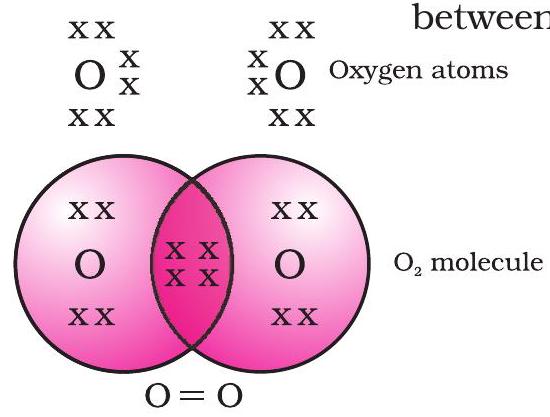
চিত্ৰ 4.3 দুটা অক্সিজেন পৰমাণুৰ মাজৰ দ্বি-বন্ধন
তুমি এতিয়া এটা পানীৰ অণু চিত্ৰিত কৰিব পাৰিবানে য’ত এটা অক্সিজেন পৰমাণু আৰু দুটা হাইড্ৰজেন পৰমাণুৰ মাজৰ বন্ধনৰ প্ৰকৃতি দেখুওৱা হৈছে? অণুটোত একক বন্ধন নে দ্বি-বন্ধন আছে?
নাইট্ৰজেনৰ দ্বি-পাৰমাণৱিক অণুৰ ক্ষেত্ৰত কি হ’ব? নাইট্ৰজেনৰ পাৰমাণৱিক সংখ্যা ৭। ইয়াৰ ইলেকট্ৰনীয় বিন্যাস আৰু সংযোজন ক্ষমতা কি হ’ব? এটা অষ্টক লাভ কৰিবলৈ, নাইট্ৰজেনৰ এটা অণুৰ প্ৰতিটো নাইট্ৰজেন পৰমাণুৱে তিনিটা ইলেকট্ৰন আগবঢ়ায়, যাৰ ফলত তিনিটা ভাগ বতৰা কৰা ইলেকট্ৰনৰ যোৰৰ সৃষ্টি হয়। এইটোক দুটা পৰমাণুৰ মাজত এটা ত্ৰি-বন্ধন চিত্ৰ 4.3 গঠন কৰা বুলি কোৱা হয়। $N_2$ আৰু দুটা অক্সিজেন পৰমাণুৰ মাজৰ দ্বি-বন্ধনৰ ইলেকট্ৰন বিন্দু গঠন চিত্ৰ 4.4ত দেখুওৱাৰ দৰে চিত্ৰিত কৰিব পাৰি।
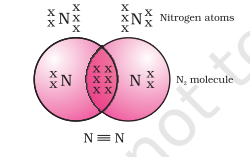
চিত্ৰ 4.4 দুটা নাইট্ৰজেন পৰমাণুৰ মাজৰ ত্ৰি-বন্ধন
এম’নিয়াৰ এটা অণুৰ সূত্ৰ $NH_3$। তুমি এই অণুটোৰ বাবে ইলেকট্ৰন বিন্দু গঠন আঁকিব পাৰিবানে য’ত দেখুওৱা হৈছে যে চাৰিওটা পৰমাণুৱে নিষ্ক্ৰিয় গেছৰ বিন্যাস লাভ কৰিছে? অণুটোত একক, দ্বি-বন্ধন নে ত্ৰি-বন্ধন থাকিব?
এতিয়া আমি মিথেনলৈ চাওঁ, যিটো কাৰ্বনৰ এটা যৌগ। মিথেন ব্যাপকভাৱে ইন্ধন হিচাপে ব্যৱহাৰ কৰা হয় আৰু ই জৈৱ-গেছ আৰু সংকোচিত প্ৰাকৃতিক গেছ (CNG)ৰ এটা প্ৰধান উপাদান। ই কাৰ্বনৰ দ্বাৰা গঠিত আটাইতকৈ সৰল যৌগসমূহৰ ভিতৰত এটাও। মিথেনৰ সূত্ৰ $CH_4$। তুমি জানা, হাইড্ৰজেনৰ যোজ্যতা ১। কাৰ্বন চতুৰ্যোজী কাৰণ ইয়াৰ চাৰিটা যোজ্যতা ইলেকট্ৰন আছে। নিষ্ক্ৰিয় গেছৰ বিন্যাস লাভ কৰিবলৈ, কাৰ্বনে চিত্ৰ 4.5ত দেখুওৱাৰ দৰে হাইড্ৰজেনৰ চাৰিটা পৰমাণুৰ সৈতে এই ইলেকট্ৰনবোৰ ভাগ বতৰা কৰে।
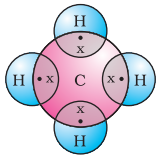
চিত্ৰ 4.5 মিথেনৰ বাবে ইলেকট্ৰন বিন্দু গঠন
এই ধৰণৰ বন্ধনবোৰ, যিবোৰ দুটা পৰমাণুৰ মাজত এটা ইলেকট্ৰন যোৰ ভাগ বতৰা কৰি গঠন কৰা হয়, তাক সমযোজী বন্ধন বুলি জনা যায়। সমযোজীভাৱে বন্ধন গঠন কৰা অণুবোৰৰ ভিতৰত শক্তিশালী বন্ধন থাকে, কিন্তু আন্তঃ-অণু বলবোৰ দুৰ্বল। এইটোৱে এই যৌগবোৰৰ নিম্ন গলনাংক আৰু উতলাংকৰ সৃষ্টি কৰে। যিহেতু ইলেকট্ৰনবোৰ পৰমাণুবোৰৰ মাজত ভাগ বতৰা কৰা হয় আৰু কোনো আহিত কণিকা গঠন নহয়, সেয়েহে এই ধৰণৰ সমযোজী যৌগবোৰ সাধাৰণতে বিদ্যুৎৰ কুপৰিবাহী।
অধিক জানিবলৈ!
কাৰ্বনৰ সমৰূপতা
মৌল কাৰ্বন প্ৰকৃতিত বিভিন্ন ৰূপত ব্যাপকভাৱে ভিন্ন ভৌতিক ধৰ্মৰ সৈতে উপস্থিত হয়। হীৰা আৰু গ্ৰেফাইট দুয়োটাই কাৰ্বন পৰমাণুৰ দ্বাৰা গঠিত, পাৰ্থক্যটো হৈছে যে কাৰ্বন পৰমাণুবোৰ কেনেকৈ ইটোৱে সিটোৰ সৈতে বন্ধন গঠন কৰে। হীৰাত, প্ৰতিটো কাৰ্বন পৰমাণু চাৰিটা অন্যান্য কাৰ্বন পৰমাণুৰ সৈতে বন্ধন গঠন কৰি এটা কঠিন ত্ৰি-মাত্ৰিক গঠন গঠন কৰে। গ্ৰেফাইটত, প্ৰতিটো কাৰ্বন পৰমাণু একে সমতলত থকা তিনিটা অন্যান্য কাৰ্বন পৰমাণুৰ সৈতে বন্ধন গঠন কৰি এটা ষড়ভুজীয় বিন্যাস দিয়ে। এই বন্ধনবোৰৰ ভিতৰত এটা দ্বি-বন্ধন, আৰু সেয়েহে কাৰ্বনৰ যোজ্যতা পূৰ্ণ হয়। গ্ৰেফাইটৰ গঠনটো ষড়ভুজীয় বিন্যাসবোৰ এটাতকৈ আনটোৰ ওপৰত স্তৰ হিচাপে ৰখাৰ দ্বাৰা গঠন কৰা হয়।
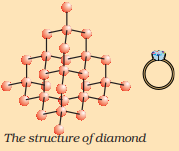
হীৰাৰ গঠন
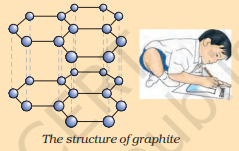
গ্ৰেফাইটৰ গঠন
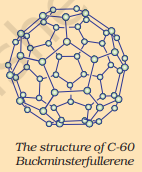
C-60 বাকমিনষ্টাৰফুলেৰিনৰ গঠন
এই দুটা ভিন্ন গঠনে হীৰা আৰু গ্ৰেফাইটৰ ভৌতিক ধৰ্ম অতি ভিন্ন হোৱাৰ সৃষ্টি কৰে যদিও ইহঁতৰ ৰাসায়নিক ধৰ্ম একে। হীৰা হৈছে জ্ঞাত আটাইতকৈ কঠিন পদাৰ্থ আনহাতে গ্ৰেফাইট মসৃণ আৰু পিছল। গ্ৰেফাইট আগৰ অধ্যায়ত তুমি অধ্যয়ন কৰা অন্যান্য অধাতুৰ দৰে নহয়, ই বিদ্যুৎৰ অতি ভাল পৰিবাহীও।
হীৰা বিশুদ্ধ কাৰ্বনক অতি উচ্চ চাপ আৰু উষ্ণতাত ৰাখি সংশ্লেষণ কৰিব পাৰি। এই সংশ্লেষিত হীৰাবোৰ সৰু কিন্তু অন্যথা প্ৰাকৃতিক হীৰাৰ পৰা পৃথক কৰিব নোৱাৰি।
ফুলেৰিনবোৰে কাৰ্বনৰ সমৰূপতাৰ আন এটা শ্ৰেণী গঠন কৰে। প্ৰথমটো চিনাক্ত কৰা হৈছিল C-60 যিটোৰ কাৰ্বন পৰমাণুবোৰ ফুটবলৰ আকৃতিৰে সজ্জিত। যিহেতু এইটো আমেৰিকান স্থপতি বাকমিনষ্টাৰ ফুলাৰে ডিজাইন কৰা জিঅ’ডেছিক গম্বুজৰ দৰে দেখা গৈছিল, সেয়েহে অণুটোৰ নাম ফুলেৰিন ৰখা হৈছিল।
4.2 কাৰ্বনৰ বহুমুখী প্ৰকৃতি
আমি বিভিন্ন মৌল আৰু যৌগত ইলেকট্ৰন ভাগ বতৰা কৰি সমযোজী বন্ধন গঠন দেখিছো। আমি এটা সৰল কাৰ্বন যৌগ, মিথেনৰ গঠনো দেখিছো। অধ্যায়ৰ আৰম্ভণিতে আমি দেখিছিলো যে আমি ব্যৱহাৰ কৰা কিমানবোৰ বস্তুৰ ভিতৰত কাৰ্বন থাকে। প্ৰকৃততে, আমি নিজেই কাৰ্বন যৌগৰে গঠিত। ৰসায়নবিদসকলৰ জনা কাৰ্বন যৌগৰ সংখ্যা সম্প্ৰতি নিযুতত গণনা কৰা হৈছিল! এইটো অন্যান্য সকলো মৌলে একেলগে গঠন কৰা যৌগৰ সংখ্যাক বহু পৰিমাণে অতিক্ৰম কৰে। কিয় এই ধৰ্মটো কাৰ্বনত দেখা যায় আৰু আন কোনো মৌলত নহয়? সমযোজী বন্ধনৰ প্ৰকৃতিয়ে কাৰ্বনক বহু সংখ্যক যৌগ গঠন কৰিবলৈ সক্ষম কৰায়। কাৰ্বনৰ ক্ষেত্ৰত লক্ষ্য কৰা দুটা কাৰক হৈছে -
(i) কাৰ্বনৰ কাৰ্বনৰ অন্যান্য পৰমাণুৰ সৈতে বন্ধন গঠন কৰাৰ অনন্য ক্ষমতা আছে, যাৰ ফলত ডাঙৰ অণুৰ সৃষ্টি হয়। এই ধৰ্মটোক শৃংখলন বোলা হয়। এই যৌগবোৰৰ কাৰ্বনৰ দীঘল শৃংখলা, কাৰ্বনৰ শাখাযুক্ত শৃংখলা বা কাৰ্বন পৰমাণুবোৰ ৰিংৰ দৰে সজ্জিত হ’ব পাৰে। ইয়াৰ উপৰি, কাৰ্বন পৰমাণুবোৰ একক, দ্বি-বন্ধন বা ত্ৰি-বন্ধনৰ দ্বাৰা সংযুক্ত হ’ব পাৰে। কাৰ্বনৰ যৌগবোৰ, যিবোৰ কাৰ্বন পৰমাণুবোৰৰ মাজত কেৱল একক বন্ধনৰ দ্বাৰা সংযুক্ত, তাক সম্পৃক্ত যৌগ বোলা হয়। কাৰ্বনৰ যৌগবোৰ যিবোৰৰ কাৰ্বন পৰমাণুবোৰৰ মাজত দ্বি-বন্ধন বা ত্ৰি-বন্ধন থাকে, তাক অসম্পৃক্ত যৌগ বোলা হয়।
কাৰ্বন যৌগত দেখা পৰিমাণৰ শৃংখলন ধৰ্ম আন কোনো মৌলে প্ৰদৰ্শন নকৰে। চিলিকনে হাইড্ৰজেনৰ সৈতে যৌগ গঠন কৰে যিবোৰত সাত বা আঠটা পৰমাণুৰ শৃংখলা থাকে, কিন্তু এই যৌগবোৰ অতি সক্ৰিয়। কাৰ্বন-কাৰ্বন বন্ধন অতি শক্তিশালী আৰু সেয়েহে স্থায়ী। এইটোৱে আমাক বহু সংখ্যক কাৰ্বন পৰমাণু ইটোৱে সিটোৰ সৈতে সংযুক্ত হৈ থকা বহু সংখ্যক যৌগ দিয়ে।
(ii) যিহেতু কাৰ্বনৰ যোজ্যতা চাৰি, ই কাৰ্বনৰ চাৰিটা অন্যান্য পৰমাণু বা আন কোনো এক-যোজী মৌলৰ পৰমাণুৰ সৈতে বন্ধন গঠন কৰিবলৈ সক্ষম। কাৰ্বনৰ যৌগবোৰ অক্সিজেন, হাইড্ৰজেন, নাইট্ৰজেন, গন্ধক, ক্ল’ৰিন আৰু বহুতো অন্য মৌলৰ সৈতে গঠন কৰা হয়, যাৰ ফলত নিৰ্দিষ্ট ধৰ্মৰ যৌগৰ সৃষ্টি হয় যিবোৰ অণুত উপস্থিত কাৰ্বনৰ বাহিৰৰ মৌলবোৰৰ ওপৰত নিৰ্ভৰ কৰে।
আকৌ, কাৰ্বনে বেছিভাগ অন্য মৌলৰ সৈতে গঠন কৰা বন্ধনবোৰ অতি শক্তিশালী, যাৰ ফলত এই যৌগবোৰ অসাধাৰণভাৱে স্থায়ী হয়। কাৰ্বনে শক্তিশালী বন্ধন গঠন কৰাৰ এটা কাৰণ হৈছে ইয়াৰ সৰু আকাৰ। এইটোৱে নিউক্লিয়াছক ভাগ বতৰা কৰা ইলেকট্ৰনৰ যোৰবোৰ দৃঢ়ভাৱে ধৰি ৰাখিবলৈ সক্ষম কৰায়। ডাঙৰ পৰমাণু থকা মৌলবোৰে গঠন কৰা বন্ধনবোৰ বহু দুৰ্বল।
তোমাৰ জনা আছে নেকি?
জৈৱ যৌগ
কাৰ্বনত দেখা দুটা বৈশিষ্ট্যপূৰ্ণ দিশ, অৰ্থাৎ, চতুৰ্যোজিতা আৰু শৃংখলন, একেলগে বহু সংখ্যক যৌগৰ সৃষ্টি কৰে। বহুতোৰ একে অধাতু পৰমাণু বা পৰমাণুৰ গোট থাকে যিবোৰ ভিন্ন কাৰ্বন শৃংখলৰ লগত সংযুক্ত। এই যৌগবোৰ প্ৰথমতে প্ৰাকৃতিক পদাৰ্থৰ পৰা নিষ্কাশন কৰা হৈছিল আৰু ভবা হৈছিল যে এই কাৰ্বন যৌগবোৰ বা জৈৱ যৌগবোৰ কেৱল জীৱিত প্ৰণালীৰ ভিতৰতহে গঠন কৰিব পাৰি। অৰ্থাৎ, এটা ‘জীৱনী শক্তি’ৰ তেওঁলোকৰ সংশ্লেষণৰ বাবে প্ৰয়োজন বুলি অনুমান কৰা হৈছিল। ফ্ৰিডৰিখ ভ’লাৰে ১৮২৮ চনত এম’নিয়াম চায়েনেটৰ পৰা ইউৰিয়া প্ৰস্তুত কৰি এইটো ভুল প্ৰমাণ কৰিছিল। কিন্তু কাৰ্বন যৌগবোৰ, কাৰ্বাইড, কাৰ্বনৰ অক্সাইড, কাৰ্বনেট আৰু হাইড্ৰজেনকাৰ্বনেট লৱণবোৰৰ বাহিৰে, জৈৱ ৰসায়নৰ অধীনত অধ্যয়ন কৰা হৈ থাকে।
4.2.1 সম্পৃক্ত আৰু অসম্পৃক্ত কাৰ্বন যৌগ
আমি ইতিমধ্যে মিথেনৰ গঠন দেখিছো। কাৰ্বন আৰু হাইড্ৰজেনৰ মাজত গঠিত আন এটা যৌগ হৈছে ইথেন যিৰ সূত্ৰ $C_2 H_6$। সৰল কাৰ্বন যৌগৰ গঠনত উপনীত হ’বলৈ, প্ৰথম পদক্ষেপটো হৈছে কাৰ্বন পৰমাণুবোৰক একক বন্ধনৰ সৈতে একেলগে সংযোগ কৰা (চিত্ৰ 4.6a) আৰু তাৰ পিছত কাৰ্বনৰ বাকী যোজ্যতাবোৰ পূৰণ কৰিবলৈ হাইড্ৰজেন পৰমাণুবোৰ ব্যৱহাৰ কৰা (চিত্ৰ 4.6b)। উদাহৰণস্বৰূপে, ইথেনৰ গঠনটো তলৰ পদক্ষেপবোৰৰ দ্বাৰা উপনীত হোৱা হয় -
$ C-C \qquad $ পদক্ষেপ 1
চিত্ৰ 4.6 (a) একক বন্ধনৰ সৈতে সংযুক্ত কাৰ্বন পৰমাণু
প্ৰতিটো কাৰ্বন পৰমাণুৰ তিনিটা যোজ্যতা অপূৰ্ণ হৈ থাকে, গতিকে প্ৰতিটো তিনিটা হাইড্ৰজেন পৰমাণুৰ সৈতে বন্ধন গঠন কৰে:
$H-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}}-\underset{H}{\underset{|}{\stackrel{H}{\stackrel{|}{C}}}} - H \qquad $ পদক্ষেপ 2
চিত্ৰ 4.6 (b) প্ৰতিটো কাৰ্বন পৰমাণু তিনিটা হাইড্ৰজেন পৰমাণুৰ সৈতে বন্ধন গঠন কৰিছে
ইথেনৰ ইলেকট্ৰন বিন্দু গঠন চিত্ৰ 4.6(c)ত দেখুওৱা হৈছে।
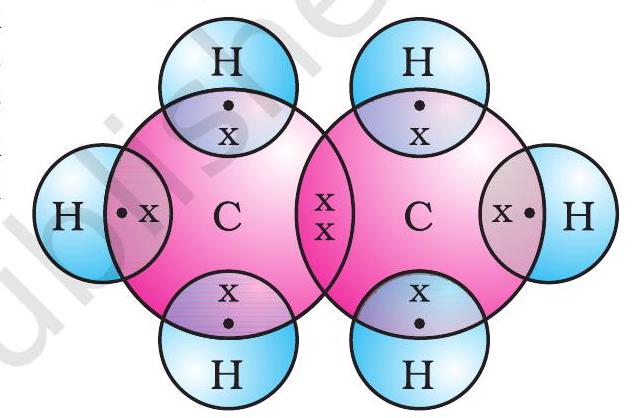
চিত্ৰ 4.6 (c) ইথেনৰ ইলেকট্ৰন বিন্দু গঠন
তুমি প্ৰ’পেনৰ গঠন আঁকিব পাৰিবানে, যাৰ আণৱিক সূত্ৰ $C_3 H_8$ একে ধৰণে? তুমি দেখিবা যে সকলো পৰমাণুৰ যোজ্যতাবোৰ ইহঁতৰ মাজৰ একক বন্ধনৰ দ্বাৰা পূৰ্ণ হয়। এই ধৰণৰ কাৰ্বন যৌগবোৰক সম্পৃক্ত যৌগ বোলা হয়। এই যৌগবোৰ সাধাৰণতে অতি সক্ৰিয় নহয়।
অৱশ্যে, কাৰ্বন আৰু হাইড্ৰজেনৰ আন এটা যৌগৰ সূত্ৰ $C_2 H_4$ আৰু ইথিন বুলি কোৱা হয়। এই অণুটো কেনেকৈ চিত্ৰিত কৰিব পাৰি? আমি ওপৰৰ দৰে একে ধাপ অনুসৰণ কৰো।
একক বন্ধনৰ সৈতে সংযুক্ত কাৰ্বন-কাৰ্বন পৰমাণু (পদক্ষেপ 1)।
আমি দেখো যে প্ৰতিটো কাৰ্বন পৰমাণুৰ এটা যোজ্যতা অপূৰ্ণ হৈ থাকে (পদক্ষেপ 2)। এইটো কেৱল যদি দুটা কাৰ্বনৰ মাজত এটা দ্বি-বন্ধন থাকে তেতিয়াহে পূৰ্ণ কৰিব পাৰি (পদক্ষেপ 3)।
ইথিনৰ বাবে ইলেকট্ৰন বিন্দু গঠন চিত্ৰ 4.7ত দিয়া হৈছে।
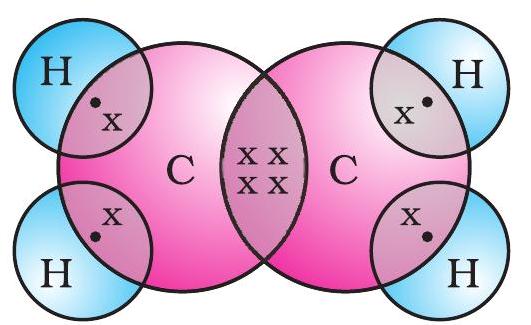
চিত্ৰ 4.7 ইথিনৰ গঠন
হাইড্ৰজেন আৰু কাৰ্বনৰ আন এটা যৌগৰ সূত্ৰ $C_2 H_2$ আৰু ইথাইন বুলি কোৱা হয়। তুমি ইথাইনৰ বাবে ইলেকট্ৰন বিন্দু গঠন আঁকিব পাৰিবানে? ইহঁতৰ যোজ্যতা পূৰ্ণ কৰিবলৈ দুটা কাৰ্বন পৰমাণুৰ মাজত কিমানটা বন্ধনৰ প্ৰয়োজন? কাৰ্বনৰ এই ধৰণৰ যৌগবোৰ যিবোৰৰ কাৰ্বন পৰমাণুবোৰৰ মাজত দ্বি-বন্ধন বা ত্ৰি-বন্ধন থাকে, তাক অসম্পৃক্ত কাৰ্বন যৌগ বুলি জনা যায় আৰু ইহঁত সম্পৃক্ত কাৰ্বন যৌগতকৈ বেছি সক্ৰিয়।
4.2.2 শৃংখলা, শাখা আৰু ৰিং
আগৰ অংশত, আমি কাৰ্বন যৌগ মিথেন, ইথেন আৰু প্ৰ’পেনৰ কথা উল্লেখ কৰিছিলো, যিবোৰত ক্ৰমে 1,2 আৰু 3টা কাৰ্বন পৰমাণু থাকে। কাৰ্বন পৰমাণুৰ এই ‘শৃংখলা’











