باب 03 دھاتیں اور غیر دھاتیں
کلاس نہم میں آپ مختلف عناصر کے بارے میں پڑھ چکے ہیں۔ آپ نے دیکھا ہے کہ عناصر کو ان کی خصوصیات کی بنیاد پر دھاتوں یا غیر دھاتوں میں درجہ بند کیا جا سکتا ہے۔
- اپنی روزمرہ زندگی میں دھاتوں اور غیر دھاتوں کے کچھ استعمالات کے بارے میں سوچیں۔
- عناصر کو دھاتوں یا غیر دھاتوں کے طور پر درجہ بند کرتے وقت آپ نے کن خصوصیات کے بارے میں سوچا؟
- یہ خصوصیات عناصر کے استعمالات سے کیسے متعلق ہیں؟
آئیے ان میں سے کچھ خصوصیات کو تفصیل سے دیکھتے ہیں۔
3.1 طبیعی خصوصیات
3.1.1 دھاتیں
مادوں کو گروپ بندی کرنے کا سب سے آسان طریقہ ان کی طبیعی خصوصیات کا موازنہ کرنا ہے۔ آئیے مندرجہ ذیل سرگرمیوں کی مدد سے اس کا مطالعہ کرتے ہیں۔ سرگرمی 3.1 سے 3.6 تک انجام دینے کے لیے، درج ذیل دھاتوں کے نمونے جمع کریں - لوہا، تانبا، ایلومینیم، میگنیشیم، سوڈیم، سیسہ، زنک اور کوئی بھی دوسری دھات جو آسانی سے دستیاب ہو۔
سرگرمی 3.1
- لوہے، تانبے، ایلومینیم اور میگنیشیم کے نمونے لیں۔ ہر نمونے کی ظاہری شکل نوٹ کریں۔
- ہر نمونے کی سطح کو سینڈ پیپر سے رگڑ کر صاف کریں اور ان کی ظاہری شکل دوبارہ نوٹ کریں۔
دھاتیں، اپنی خالص حالت میں، چمکدار سطح رکھتی ہیں۔ اس خاصیت کو دھاتی چمک (metallic lustre) کہتے ہیں۔
سرگرمی 3.2
لوہے، تانبے، ایلومینیم اور میگنیشیم کے چھوٹے ٹکڑے لیں۔ ان دھاتوں کو تیز چاقو سے کاٹنے کی کوشش کریں اور اپنے مشاہدات نوٹ کریں۔
چمٹے کی مدد سے سوڈیم دھات کا ایک ٹکڑا پکڑیں۔
احتیاط: سوڈیم دھات کو ہمیشہ احتیاط سے ہینڈل کریں۔ اسے فلٹر پیپر کی تہوں کے درمیان دبا کر خشک کریں۔
اسے واچ گلاس پر رکھیں اور چاقو سے کاٹنے کی کوشش کریں۔
آپ کیا مشاہدہ کرتے ہیں؟
آپ دیکھیں گے کہ دھاتیں عام طور پر سخت ہوتی ہیں۔ سختی دھات سے دھات مختلف ہوتی ہے۔
سرگرمی 3.3
- لوہے، زنک، سیسہ اور تانبے کے ٹکڑے لیں۔
- کسی ایک دھات کو لوہے کے بلاک پر رکھیں اور ہتھوڑے سے چار یا پانچ بار مارے۔ آپ کیا مشاہدہ کرتے ہیں؟
- دوسری دھاتوں کے ساتھ دہرائیں۔
- ان دھاتوں کی شکل میں تبدیلی ریکارڈ کریں۔
آپ دیکھیں گے کہ کچھ دھاتوں کو پتلی چادروں میں پیٹا جا سکتا ہے۔ اس خاصیت کو چکناہٹ (malleability) کہتے ہیں۔ کیا آپ جانتے ہیں کہ سونا اور چاندی سب سے زیادہ چکنی دھاتیں ہیں؟
سرگرمی 3.4
- ان دھاتوں کی فہرست بنائیں جن کے تار آپ نے روزمرہ زندگی میں دیکھے ہیں۔
دھاتوں کو پتلی تاروں میں کھینچے جانے کی صلاحیت کو تار کشی (ductility) کہتے ہیں۔ سونا سب سے زیادہ تار کش دھات ہے۔ آپ یہ جان کر حیران ہوں گے کہ ایک گرام سونے سے تقریباً $2 km$ لمبائی کی تار کھینچی جا سکتی ہے۔
ان کی چکناہٹ اور تار کشی کی وجہ سے ہی دھاتوں کو ہماری ضروریات کے مطابق مختلف شکلیں دی جا سکتی ہیں۔
کیا آپ کچھ دھاتوں کے نام بتا سکتے ہیں جو کھانا پکانے کے برتن بنانے کے لیے استعمال ہوتی ہیں؟ کیا آپ جانتے ہیں کہ یہ دھاتیں برتن بنانے کے لیے کیوں استعمال ہوتی ہیں؟ آئیے جواب تلاش کرنے کے لیے مندرجہ ذیل سرگرمی کرتے ہیں۔
سرگرمی 3.5
- ایلومینیم یا تانبے کا تار لیں۔ اس تار کو اسٹینڈ پر کلیمپ کی مدد سے جکڑیں، جیسا کہ شکل 3.1 میں دکھایا گیا ہے۔
- موم کا استعمال کرتے ہوئے تار کے آزاد سرے پر ایک پن فکس کریں۔
- اس جگہ کے قریب جہاں تار جکڑا گیا ہے، اسپرٹ لیمپ، موم بتی یا برنر سے تار کو گرم کریں۔
- کچھ دیر بعد آپ کیا مشاہدہ کرتے ہیں؟
- اپنے مشاہدات نوٹ کریں۔ کیا دھاتی تار پگھل جاتا ہے؟
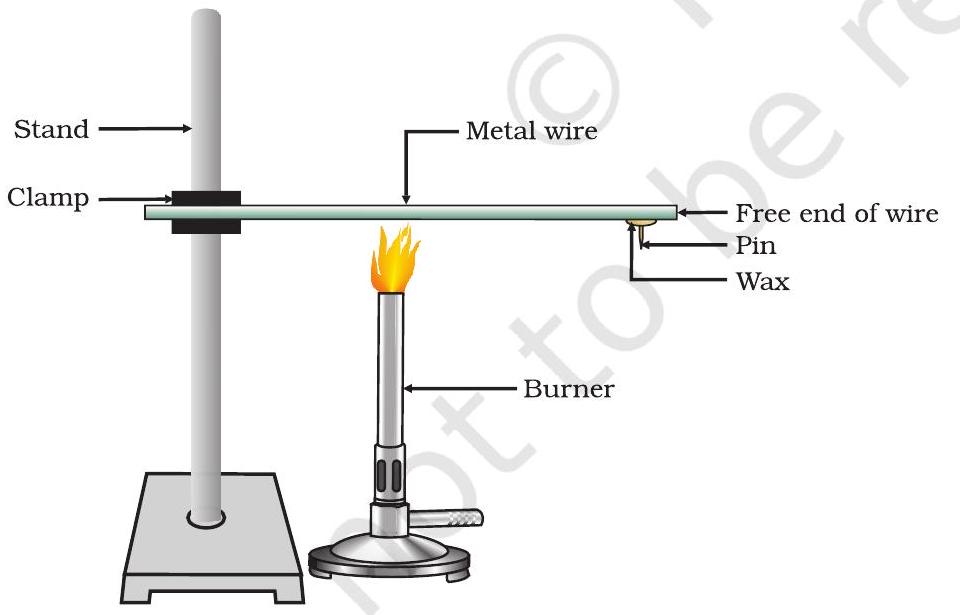
شکل 3.1 دھاتیں حرارت کی اچھی موصل (conductor) ہیں۔
مندرجہ بالا سرگرمی سے پتہ چلتا ہے کہ دھاتیں حرارت کی اچھی موصل ہوتی ہیں اور ان کے پگھلنے کے نقطے بلند ہوتے ہیں۔ حرارت کی بہترین موصل چاندی اور تانبا ہیں۔ سیسہ اور پارہ نسبتاً حرارت کے کمزور موصل ہیں۔
کیا دھاتیں بجلی بھی چلاتی ہیں؟ آئیے دیکھتے ہیں۔
سرگرمی 3.6
- برقی سرکٹ کو اس طرح ترتیب دیں جیسا کہ شکل 3.2 میں دکھایا گیا ہے۔
- جانچی جانے والی دھات کو سرکٹ میں ٹرمینلز $A$ اور $B$ کے درمیان رکھیں جیسا کہ دکھایا گیا ہے۔
- کیا بلب روشن ہوتا ہے؟ یہ کیا ظاہر کرتا ہے؟
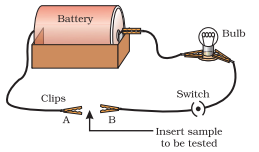
شکل 3.2 دھاتیں بجلی کی اچھی موصل ہیں۔
آپ نے ضرور دیکھا ہوگا کہ آپ کے گھروں میں کرنٹ لے جانے والے تاروں پر پولی وینائل کلورائیڈ (PVC) یا ربڑ جیسے مادے کی کوٹنگ ہوتی ہے۔ برقی تاروں کو ایسے مادوں سے کیوں ڈھانپا جاتا ہے؟
جب دھاتیں سخت سطح سے ٹکراتی ہیں تو کیا ہوتا ہے؟ کیا وہ آواز پیدا کرتی ہیں؟ جو دھاتیں سخت سطح سے ٹکرانے پر آواز پیدا کرتی ہیں انہیں صوتی (sonorous) کہا جاتا ہے۔ کیا آپ اب بتا سکتے ہیں کہ اسکول کی گھنٹیاں دھاتوں سے کیوں بنائی جاتی ہیں؟
3.1.2 غیر دھاتیں
پچھلی کلاس میں آپ نے سیکھا تھا کہ دھاتوں کے مقابلے میں بہت کم غیر دھاتیں ہیں۔ غیر دھاتوں کی کچھ مثالیں کاربن، گندھک، آیوڈین، آکسیجن، ہائیڈروجن وغیرہ ہیں۔ غیر دھاتیں یا تو ٹھوس ہیں یا گیسیں سوائے برومین کے جو ایک مائع ہے۔
کیا غیر دھاتوں میں بھی دھاتوں جیسی طبیعی خصوصیات ہوتی ہیں؟ آئیے دیکھتے ہیں۔
سرگرمی 3.7
- کاربن (کوئلہ یا گرافائٹ)، گندھک اور آیوڈین کے نمونے جمع کریں۔
- ان غیر دھاتوں کے ساتھ سرگرمی 3.1 سے 3.4 اور 3.6 انجام دیں اور اپنے مشاہدات ریکارڈ کریں۔
دھاتوں اور غیر دھاتوں سے متعلق اپنے مشاہدات کو جدول 3.1 میں مرتب کریں۔
جدول 3.1
| عنصر | علامت | سطح کی قسم | سختی | چکناہٹ | تار کشی | بجلی کی موصل | صوتی |
|---|---|---|---|---|---|---|---|
جدول 3.1 میں ریکارڈ شدہ مشاہدات کی بنیاد پر، کلاس میں دھاتوں اور غیر دھاتوں کی عمومی طبیعی خصوصیات پر بحث کریں۔ آپ اس نتیجے پر پہنچے ہوں گے کہ ہم عناصر کو صرف ان کی طبیعی خصوصیات کی بنیاد پر درجہ بند نہیں کر سکتے، کیونکہ بہت سی مستثنیات ہیں۔ مثال کے طور پر -
(i) پارہ کے علاوہ تمام دھاتیں کمرے کے درجہ حرارت پر ٹھوس حالت میں موجود ہوتی ہیں۔ سرگرمی 3.5 میں، آپ نے مشاہدہ کیا تھا کہ دھاتوں کے پگھلنے کے نقطے بلند ہوتے ہیں لیکن گیلیئم اور سیزیم کے پگھلنے کے نقطے بہت کم ہوتے ہیں۔ یہ دونوں دھاتیں پگھل جائیں گی اگر آپ انہیں اپنی ہتھیلی پر رکھیں۔
(ii) آیوڈین ایک غیر دھات ہے لیکن یہ چمکدار ہے۔
(iii) کاربن ایک غیر دھات ہے جو مختلف شکلوں میں موجود ہو سکتا ہے۔ ہر شکل کو متشکل (allotrope) کہتے ہیں۔ ہیرا، کاربن کا ایک متشکل، جانا جانے والا سب سے سخت قدرتی مادہ ہے اور اس کا پگھلنے اور ابلنے کا نقطہ بہت بلند ہے۔ گرافائٹ، کاربن کا ایک اور متشکل، بجلی کا موصل ہے۔
(iv) الکلی دھاتیں (لیتھیم، سوڈیم، پوٹاشیم) اتنی نرم ہوتی ہیں کہ انہیں چاقو سے کاٹا جا سکتا ہے۔ ان کی کثافت اور پگھلنے کے نقطے کم ہوتے ہیں۔
عناصر کو ان کی کیمیائی خصوصیات کی بنیاد پر دھاتوں اور غیر دھاتوں کے طور پر زیادہ واضح طور پر درجہ بند کیا جا سکتا ہے۔
سرگرمی 3.8
- ایک میگنیشیم ربن اور کچھ گندھک پاؤڈر لیں۔
- میگنیشیم ربن کو جلا دیں۔ بننے والی راکھ جمع کریں اور انہیں پانی میں حل کریں۔
- حاصل ہونے والے محلول کو سرخ اور نیلے لٹمس پیپر دونوں سے آزمائیں۔
- میگنیشیم جلانے پر بننے والا مصنوعہ تیزابی ہے یا بنیادی؟
- اب گندھک پاؤڈر جلا دیں۔ جلتی ہوئی گندھک پر دھواں جمع کرنے کے لیے ایک ٹیسٹ ٹیوب رکھیں۔
- اوپر والی ٹیسٹ ٹیوب میں کچھ پانی ڈالیں اور ہلائیں۔
- اس محلول کو نیلے اور سرخ لٹمس پیپر سے آزمائیں۔
- گندھک جلانے پر بننے والا مصنوعہ تیزابی ہے یا بنیادی؟
- کیا آپ ان تعاملات کے لیے مساوات لکھ سکتے ہیں؟
زیادہ تر غیر دھاتیں پانی میں حل ہونے پر تیزابی آکسائڈ بناتی ہیں۔ دوسری طرف، زیادہ تر دھاتیں، بنیادی آکسائڈ بناتی ہیں۔ آپ اگلے حصے میں ان دھاتی آکسائڈز کے بارے میں مزید سیکھیں گے۔
3.2 دھاتوں کی کیمیائی خصوصیات
ہم دھاتوں کی کیمیائی خصوصیات کے بارے میں اگلے حصوں 3.2.1 سے 3.2.4 میں سیکھیں گے۔ اس کے لیے، درج ذیل دھاتوں ایلومینیم، تانبا، لوہا، سیسہ، میگنیشیم، زنک اور سوڈیم کے نمونے جمع کریں۔
3.2.1 جب دھاتیں ہوا میں جلائی جاتی ہیں تو کیا ہوتا ہے؟
آپ نے سرگرمی 3.8 میں دیکھا کہ میگنیشیم ہوا میں چمکدار سفید شعلے کے ساتھ جلتی ہے۔ کیا تمام دھاتیں اسی طرح تعامل کرتی ہیں؟ آئیے مندرجہ ذیل سرگرمی انجام دے کر چیک کرتے ہیں۔
سرگرمی 3.9
احتیاط: مندرجہ ذیل سرگرمی کے لیے استاد کی مدد درکار ہے۔ بہتر ہوگا اگر طلباء آنکھوں کا تحفظ پہنیں۔
- اوپر لیے گئے نمونوں میں سے کسی ایک کو چمٹے سے پکڑیں اور شعلے پر جلانے کی کوشش کریں۔ دوسرے دھاتی نمونوں کے ساتھ دہرائیں۔
- اگر مصنوعہ بنے تو اسے جمع کریں۔
- مصنوعات اور دھاتی سطح کو ٹھنڈا ہونے دیں۔
- کون سی دھاتیں آسانی سے جلتی ہیں؟
- دھات جلنے پر آپ نے کس رنگ کا شعلہ مشاہدہ کیا؟
- جلنے کے بعد دھاتی سطح کیسی نظر آتی ہے؟
- دھاتوں کو آکسیجن کے ساتھ ان کی تعامل پذیری کے کم ہوتے ہوئے ترتیب میں ترتیب دیں۔
- کیا مصنوعات پانی میں حل پذیر ہیں؟
تقریباً تمام دھاتیں آکسیجن کے ساتھ مل کر دھاتی آکسائڈ بناتی ہیں۔
دھات + آکسیجن $\rightarrow$ دھاتی آکسائڈ
مثال کے طور پر، جب تانبے کو ہوا میں گرم کیا جاتا ہے، تو یہ آکسیجن کے ساتھ مل کر تانبے (II) آکسائڈ بناتا ہے، جو ایک سیاہ آکسائڈ ہے۔
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
اسی طرح، ایلومینیم ایلومینیم آکسائڈ بناتا ہے۔
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
باب 2 سے یاد کریں، تانبے کا آکسائڈ ہائیڈروکلورک ایسڈ کے ساتھ کیسے تعامل کرتا ہے۔ ہم نے سیکھا ہے کہ دھاتی آکسائڈز بنیادی نوعیت کے ہوتے ہیں۔ لیکن کچھ دھاتی آکسائڈز، جیسے ایلومینیم آکسائڈ، زنک آکسائڈ، تیزابی اور بنیادی دونوں رویے ظاہر کرتے ہیں۔ ایسے دھاتی آکسائڈز جو تیزابوں اور اساسوں دونوں کے ساتھ تعامل کر کے نمک اور پانی بناتے ہیں، انہیں دوغلی آکسائڈز (amphoteric oxides) کہا جاتا ہے۔ ایلومینیم آکسائڈ تیزابوں اور اساسوں کے ساتھ مندرجہ ذیل طریقے سے تعامل کرتا ہے -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
زیادہ تر دھاتی آکسائڈز پانی میں غیر حل پذیر ہیں لیکن ان میں سے کچھ پانی میں حل ہو کر الکلی بناتے ہیں۔ سوڈیم آکسائڈ اور پوٹاشیم آکسائڈ پانی میں حل ہو کر الکلی بناتے ہیں حسب ذیل -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
ہم نے سرگرمی 3.9 میں مشاہدہ کیا ہے کہ تمام دھاتیں آکسیجن کے ساتھ ایک ہی شرح سے تعامل نہیں کرتیں۔ مختلف دھاتیں آکسیجن کے ساتھ مختلف تعامل پذیری ظاہر کرتی ہیں۔ پوٹاشیم اور سوڈیم جیسی دھاتیں اتنی شدت سے تعامل کرتی ہیں کہ اگر کھلی جگہ پر رکھی جائیں تو آگ پکڑ لیتی ہیں۔ اس لیے، انہیں بچانے اور حادثاتی آگ کو روکنے کے لیے، انہیں مٹی کے تیل میں ڈبو کر رکھا جاتا ہے۔ عام درجہ حرارت پر، میگنیشیم، ایلومینیم، زنک، سیسہ وغیرہ جیسی دھاتوں کی سطحیں آکسائڈ کی پتلی تہہ سے ڈھکی ہوتی ہیں۔ یہ حفاظتی آکسائڈ تہہ دھات کو مزید آکسائیڈیشن سے روکتی ہے۔ لوہا گرم کرنے پر نہیں جلتا لیکن لوہے کے برادے برنر کے شعلے میں چھڑکنے پر زوردار طور پر جل جاتے ہیں۔ تانبا نہیں جلتا، لیکن گرم دھات تانبے (II) آکسائڈ کی سیاہ رنگ کی تہہ سے ڈھک جاتی ہے۔ چاندی اور سونا زیادہ درجہ حرارت پر بھی آکسیجن کے ساتھ تعامل نہیں کرتے۔
کیا آپ جانتے ہیں؟
اینوڈائزنگ (Anodising) ایلومینیم کی موٹی آکسائڈ تہہ بنانے کا عمل ہے۔ ایلومینیم ہوا کے سامنے آنے پر ایک پتلی آکسائڈ تہہ بناتا ہے۔ یہ ایلومینیم آکسائڈ کوٹ اسے مزید سنکنرن (corrosion) کے خلاف مزاحم بناتا ہے۔ آکسائڈ تہہ کو موٹا کر کے مزاحمت کو اور بہتر بنایا جا سکتا ہے۔ اینوڈائزنگ کے دوران، ایک صاف ایلومینیم مضمون کو اینوڈ بنایا جاتا ہے اور اسے ہلکی گندھک کے تیزاب کے ساتھ برق پاشیدہ (electrolysed) کیا جاتا ہے۔ اینوڈ پر پیدا ہونے والی آکسیجن گیس ایلومینیم کے ساتھ تعامل کر کے ایک موٹی حفاظتی آکسائڈ تہہ بناتی ہے۔ اس آکسائڈ تہہ کو آسانی سے رنگا جا سکتا ہے تاکہ ایلومینیم مضامین کو پرکشش خاتمہ (finish) دیا جا سکے۔
سرگرمی 3.9 انجام دینے کے بعد، آپ نے ضرور مشاہدہ کیا ہوگا کہ سوڈیم یہاں لیے گئے دھاتی نمونوں میں سب سے زیادہ تعامل پذیر ہے۔ میگنیشیم کا تعامل کم شدید ہے جس کا مطلب ہے کہ یہ سوڈیم جتنا تعامل پذیر نہیں ہے۔ لیکن آکسیجن میں جلنا ہمیں زنک، لوہے، تانبے یا سیسے کی تعامل پذیری کے بارے میں فیصلہ کرنے میں مدد نہیں دیتا۔ آئیے کچھ مزید تعاملات دیکھتے ہیں تاکہ ان دھاتوں کی تعامل پذیری کے ترتیب پر پہنچ سکیں۔
3.2.2 جب دھاتیں پانی کے ساتھ تعامل کرتی ہیں تو کیا ہوتا ہے؟
سرگرمی 3.10
احتیاط: اس سرگرمی کے لیے استاد کی مدد درکار ہے۔
- سرگرمی 3.9 کی طرح اسی دھاتوں کے نمونے جمع کریں۔
- نمونوں کے چھوٹے ٹکڑے الگ الگ بیکرز میں رکھیں جو ٹھنڈے پانی سے آدھے بھرے ہوں۔
- کون سی دھاتیں ٹھنڈے پانی کے ساتھ تعامل کرتی ہیں؟ انہیں ٹھنڈے پانی کے ساتھ ان کی تعامل پذیری کے بڑھتے ہوئے ترتیب میں ترتیب دیں۔
- کیا کوئی دھات پانی پر آگ پیدا کرتی ہے؟
- کیا کوئی دھات کچھ دیر بعد تیرنے لگتی ہے؟
- جو دھاتیں ٹھنڈے پانی کے ساتھ تعامل نہیں کرتیں، انہیں گرم پانی سے آدھے بھرے بیکرز میں رکھیں۔
- جو دھاتیں گرم پانی کے ساتھ بھی تعامل نہیں کرتیں، ان کے لیے آلات کو اس طرح ترتیب دیں جیسا کہ شکل 3.3 میں دکھایا گیا ہے اور بھاپ کے ساتھ ان کے تعامل کا مشاہدہ کریں۔
- کون سی دھاتیں بھاپ کے ساتھ بھی تعامل نہیں کرتیں؟
- دھاتوں کو پانی کے ساتھ تعامل پذیری کے کم ہوتے ہوئے ترتیب میں ترتیب دیں۔
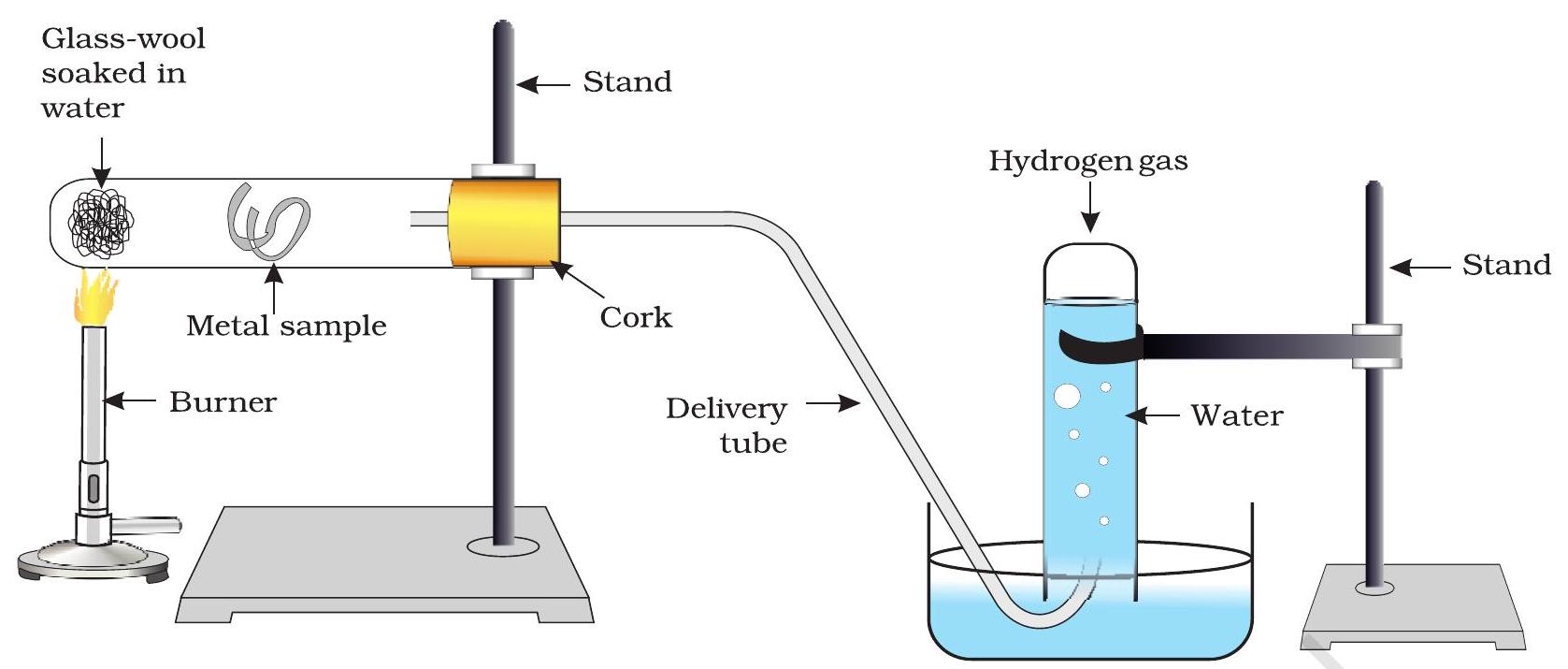
شکل 3.3 بھاپ کا دھات پر عمل
دھاتیں پانی کے ساتھ تعامل کرتی ہیں اور دھاتی آکسائڈ اور ہائیڈروجن گیس پیدا کرتی ہیں۔ دھاتی آکسائڈز جو پانی میں حل پذیر ہیں، اس میں حل ہو کر مزید دھاتی ہائیڈرو آکسائڈ بناتے ہیں۔ لیکن تمام دھاتیں پانی کے ساتھ تعامل نہیں کرتیں۔
دھات + پانی $\rightarrow$ دھاتی آکسائڈ + ہائیڈروجن
دھاتی آکسائڈ + پانی $ \rightarrow $ دھاتی ہائیڈرو آکسائڈ
پوٹاشیم اور سوڈیم جیسی دھاتیں ٹھنڈے پانی کے ساتھ شدت سے تعامل کرتی ہیں۔ سوڈیم اور پوٹاشیم کے معاملے میں، تعامل اتنا شدید اور گرمی خارج کرنے والا (exothermic) ہوتا ہے کہ پیدا ہونے والی ہائیڈروجن فوراً آگ پکڑ لیتی ہے۔
$ \begin{aligned} & 2 K(s)+2 H_2 O(l) \to 2 KOH(aq)+H_2(g)+\text{ حرارتی توانائی } \\ & 2 Na(s)+2 H_2 O(l) \to 2 NaOH(aq)+H_2(g)+\text{ حرارتی توانائی } \end{aligned} $
کیلشیم کا پانی کے ساتھ تعامل کم شدید ہوتا ہے۔ خارج ہونے والی حرارت ہائیڈروجن کے آگ پکڑنے کے لیے کافی نہیں ہوتی۔
$Ca(s)+2 H_2 O(l) \to Ca(OH)_2(aq)+H_2(g)$
کیلشیم تیرنے لگتی ہے کیونکہ بننے والے ہائیڈروجن گیس کے بلبلے دھات کی سطح سے چپک جاتے ہیں۔
میگنیشیم ٹھنڈے پانی کے ساتھ تعامل نہیں کرتا۔ یہ گرم پانی کے ساتھ تعامل کر کے میگنیشیم ہائیڈرو آکسائڈ اور ہائیڈروجن بناتا ہے۔ یہ بھی اپنی سطح سے چپکنے والے ہائیڈروجن گیس کے بلبلوں کی وجہ سے تیرنے لگتا ہے۔
ایلومینیم، لوہا اور زنک جیسی دھاتیں نہ تو ٹھنڈے اور نہ ہی گرم پانی کے ساتھ تعامل کرتی ہیں۔ لیکن یہ بھاپ کے ساتھ تعامل کر کے دھاتی آکسائڈ اور ہائیڈروجن بناتی ہیں۔
$ \begin{aligned} & 2 Al(s)+3 H_2 O(g) \to Al_2 O_3(s)+3 H_2(g) \\ & 3 Fe(s)+4 H_2 O(g) \to Fe_3 O_4(s)+4 H_2(g) \end{aligned} $
سیسہ، تانبا، چاندی اور سونا جیسی دھاتیں پانی کے ساتھ بالکل تعامل نہیں کرتیں۔
3.2.3 جب دھاتیں تیزابوں کے ساتھ تعامل کرتی ہیں تو کیا ہوتا ہے؟
آپ پہلے ہی سیکھ چکے ہیں کہ دھاتیں تیزابوں کے ساتھ تعامل کر کے نمک اور ہائیڈروجن گیس دیتی ہیں۔
دھات + ہلکا تیزاب $ \rightarrow $ نمک + ہائیڈروجن
لیکن کیا تمام دھاتیں اسی طرح تعامل کرتی ہیں؟ آئیے دیکھتے ہیں۔
سرگرمی 3.11
- سوڈیم اور پوٹاشیم کے علاوہ تمام دھاتی نمونے دوبارہ جمع کریں۔ اگر نمونے داغدار ہیں تو انہیں سینڈ پیپر سے صاف کریں۔ احتیاط: سوڈیم اور پوٹاشیم نہ لیں کیونکہ یہ ٹھنڈے پانی کے ساتھ بھی شدت سے تعامل کرتے ہیں۔
- نمونوں کو الگ الگ ٹیسٹ ٹیوبوں میں رکھیں جن میں ہلکا ہائیڈروکلورک ایسڈ ہو۔
- تھرمامیٹرز کو ٹیسٹ ٹیوبوں میں اس طرح لٹکائیں کہ ان کے بلب تیزاب میں ڈوبے رہیں۔
- بلبلوں کے بننے کی شرح کا احتیاط سے مشاہدہ کریں۔
- کون سی دھاتیں ہلکے ہائیڈروکلورک ایسڈ کے ساتھ شدت سے تعامل کرتی ہیں؟
- کس دھات کے ساتھ آپ نے سب سے زیادہ درجہ حرارت ریکارڈ کیا؟
- دھاتوں کو ہلکے تیزابوں کے ساتھ تعامل پذیری کے کم ہوتے ہوئے ترتیب میں ترتیب دیں۔
میگنیشیم، ایلومینیم، زنک اور لوہے کے ہلکے ہائیڈروکلورک ایسڈ کے ساتھ تعاملات کے لیے مساوات لکھیں۔
جب کوئی دھات نائٹرک ایسڈ کے ساتھ تعامل کرتی ہے تو ہائیڈروجن گیس پیدا نہیں ہوتی۔ اس کی وجہ یہ ہے کہ $HNO_3$ ایک طاقت ور آکسید کرنے والا عامل (oxidising agent) ہے۔ یہ پیدا ہونے والی $H_2$ کو پانی میں آکسید کر دیتا ہے اور خود نائٹروجن کے آکسائڈز ($N_2 O, NO.$, $NO_2$ ) میں کم ہو جاتا ہے۔ لیکن میگنیشیم $(Mg)$ اور میگنیز $(Mn)$ بہت ہلکے $HNO_3$ کے ساتھ تعامل کر کے $H_2$ گیس خارج کرتے ہیں۔
آپ نے سرگرمی 3.11 میں ضرور مشاہدہ کیا ہوگا کہ بلبلوں کے بننے کی شرح میگنیشیم کے معاملے میں سب سے تیز تھی۔ تعامل اس معاملے میں سب سے زیادہ گرمی خارج کرنے والا بھی تھا۔ تعامل پذیری ترتیب $Mg>Al>Zn>Fe$ میں کم ہوتی ہے۔ تانبے کے معاملے میں، کوئی بلبلے نظر نہیں آئے اور درجہ حرارت بھی تبدیل نہیں ہوا۔ یہ ظاہر کرتا ہے کہ تانبا ہلکے $HCl$ کے ساتھ تعامل نہیں کرتا۔
کیا آپ جانتے ہیں؟
ایکوا ریجیا (Aqua regia)، (لاطینی میں ‘شاہی پانی’) تیزاب شدہ ہائیڈروکلورک ایسڈ اور تیزاب شدہ نائٹرک ایسڈ کا تازہ تیار شدہ مرکب ہے جس کا تناسب 3:1 ہے۔ یہ سونا بھی حل کر سکتا ہے، حالانکہ ان میں سے کوئی بھی تیزاب اکیلے ایسا نہیں کر سکتا۔ ایکوا ریجیا ایک انتہائی کاٹنے والا، دھواں دار مائع ہے۔ یہ ان چند عاملوں میں سے ایک ہے جو سونا اور پلاٹینم کو حل کر سکتا ہے۔
3.2.4 دھاتیں دوسری دھاتی نمکیات کے محلول کے ساتھ کیسے تعامل کرتی ہیں؟
سرگرمی 3.12
- تانبے کا ایک صاف تار اور لوہے کی ایک کیل لیں۔
- تانبے کے تار کو آئرن سلفیٹ کے محلول میں اور لوہے کی کیل کو ٹیسٹ ٹیوبوں میں لیے گئے تانبے سلفیٹ کے محلول میں رکھیں (شکل 3.4)۔
- 20 منٹ بعد اپنے مشاہدات ریکارڈ کریں۔
- کس ٹیسٹ ٹیوب میں آپ نے پایا کہ تعامل ہوا ہے؟
- کس بنیاد پر آپ کہہ سکتے ہیں کہ تعامل واقعی ہوا ہے؟
- کیا آپ سرگرمی 3.9، 3.10 اور 3.11 کے لیے اپنے مشاہدات کا باہمی تعلق قائم کر سکتے ہیں؟
- ہونے والے تعامل کے لیے متوازن کیمیائی مساوات لکھیں۔
- تعامل کی قسم کا نام بتائیں۔
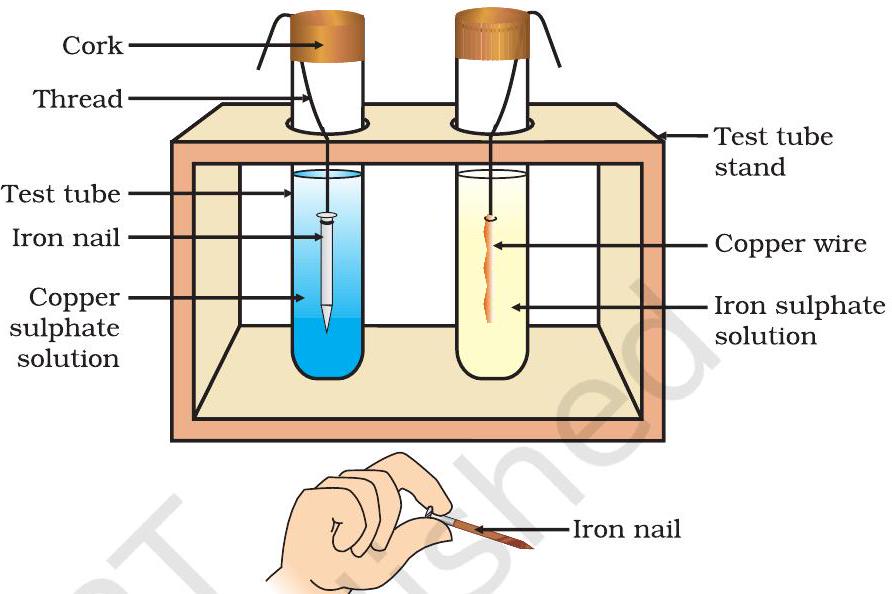
شکل 3.4 دھاتوں کا نمکیات کے محلول کے ساتھ تعامل
تعامل پذیر دھاتیں کم تعامل پذیر دھاتوں کو ان کے مرکبات سے محلول یا پگھلی ہوئی حالت میں بے گھر (dis











