अध्याय 03 धातु एवं अधातु
कक्षा IX में आपने विभिन्न तत्वों के बारे में सीखा है। आपने देखा है कि तत्वों को उनके गुणों के आधार पर धातु या अधातु के रूप में वर्गीकृत किया जा सकता है।
- अपने दैनिक जीवन में धातुओं और अधातुओं के कुछ उपयोगों के बारे में सोचें।
- तत्वों को धातु या अधातु के रूप में वर्गीकृत करते समय आपने किन गुणों के बारे में सोचा?
- ये गुण तत्वों के उपयोगों से कैसे संबंधित हैं? आइए इनमें से कुछ गुणों को विस्तार से देखें।
3.1 भौतिक गुण
3.1.1 धातु
पदार्थों को समूहित करना शुरू करने का सबसे आसान तरीका उनके भौतिक गुणों की तुलना करना है। आइए निम्नलिखित क्रियाकलापों की सहायता से इसका अध्ययन करें। क्रियाकलाप 3.1 से 3.6 तक करने के लिए, निम्नलिखित धातुओं के नमूने एकत्रित करें - लोहा, ताँबा, एल्युमीनियम, मैग्नीशियम, सोडियम, सीसा, जस्ता और कोई अन्य धातु जो आसानी से उपलब्ध हो।
क्रियाकलाप 3.1
- लोहे, ताँबे, एल्युमीनियम और मैग्नीशियम के नमूने लें। प्रत्येक नमूने की बाहरी आकृति (रंग-रूप) पर ध्यान दें।
- सैंड पेपर से रगड़कर प्रत्येक नमूने की सतह को साफ करें और उनकी बाहरी आकृति पर पुनः ध्यान दें।
धातुएँ, अपनी शुद्ध अवस्था में, चमकदार सतह वाली होती हैं। इस गुण को धात्विक चमक कहते हैं।
क्रियाकलाप 3.2
लोहे, ताँबे, एल्युमीनियम और मैग्नीशियम के छोटे-छोटे टुकड़े लें। इन धातुओं को तेज चाकू से काटने का प्रयास करें और अपने प्रेक्षण नोट करें।
सोडियम धातु के एक टुकड़े को चिमटे से पकड़ें।
सावधानी: सोडियम धातु को हमेशा सावधानी से संभालें। इसे फिल्टर पेपर की तहों के बीच दबाकर सुखाएँ।
इसे एक वॉच-ग्लास पर रखें और इसे चाकू से काटने का प्रयास करें।
आप क्या प्रेक्षण करते हैं?
आप पाएँगे कि धातुएँ सामान्यतः कठोर होती हैं। कठोरता धातु से धातु में भिन्न होती है।
क्रियाकलाप 3.3
- लोहे, जस्ता, सीसे और ताँबे के टुकड़े लें।
- किसी एक धातु को लोहे के एक गुटके पर रखें और हथौड़े से चार या पाँच बार प्रहार करें। आप क्या प्रेक्षण करते हैं?
- अन्य धातुओं के साथ दोहराएँ।
- इन धातुओं के आकार में परिवर्तन को रिकॉर्ड करें।
आप पाएँगे कि कुछ धातुओं को पीटकर पतली चादरों में बदला जा सकता है। इस गुण को आघातवर्धनीयता कहते हैं। क्या आप जानते हैं कि सोना और चाँदी सबसे अधिक आघातवर्धनीय धातुएँ हैं?
क्रियाकलाप 3.4
- उन धातुओं की सूची बनाएँ जिनके तार आपने दैनिक जीवन में देखे हैं।
धातुओं के पतले तारों में खींचे जाने की क्षमता को तन्यता कहते हैं। सोना सबसे अधिक तन्य धातु है। आपको यह जानकर आश्चर्य होगा कि एक ग्राम सोने से लगभग $2 km$ लंबाई का एक तार खींचा जा सकता है।
यह उनकी आघातवर्धनीयता और तन्यता के कारण है कि धातुओं को हमारी आवश्यकताओं के अनुसार विभिन्न आकार दिए जा सकते हैं।
क्या आप कुछ धातुओं के नाम बता सकते हैं जिनका उपयोग खाना पकाने के बर्तन बनाने के लिए किया जाता है? क्या आप जानते हैं कि इन धातुओं का उपयोग बर्तन बनाने के लिए क्यों किया जाता है? आइए उत्तर जानने के लिए निम्नलिखित क्रियाकलाप करें।
क्रियाकलाप 3.5
- एक एल्युमीनियम या ताँबे का तार लें। इस तार को एक स्टैंड पर क्लैंप की सहायता से कसें, जैसा कि चित्र 3.1 में दिखाया गया है।
- तार के मुक्त सिरे पर मोम की सहायता से एक पिन लगाएँ।
- स्पिरिट लैंप, मोमबत्ती या बर्नर से उस स्थान के निकट तार को गर्म करें जहाँ इसे क्लैंप किया गया है।
- कुछ समय बाद आप क्या प्रेक्षण करते हैं?
- अपने प्रेक्षण नोट करें। क्या धातु का तार पिघलता है?
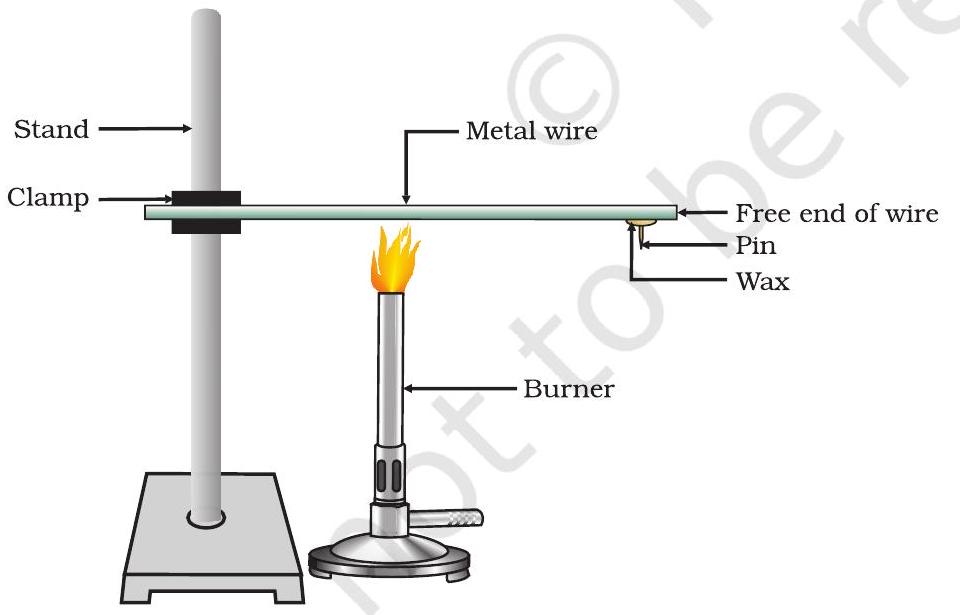
चित्र 3.1 धातुएँ ऊष्मा की सुचालक होती हैं।
उपरोक्त क्रियाकलाप दर्शाता है कि धातुएँ ऊष्मा की सुचालक होती हैं और उनके गलनांक उच्च होते हैं। ऊष्मा की सर्वोत्तम सुचालक चाँदी और ताँबा हैं। सीसा और पारा ऊष्मा की अपेक्षाकृत कुचालक हैं।
क्या धातुएँ विद्युत भी चालन करती हैं? आइए जानें।
क्रियाकलाप 3.6
- एक विद्युत परिपथ चित्र 3.2 के अनुसार स्थापित करें।
- जाँच की जाने वाली धातु को टर्मिनलों $A$ और $B$ के बीच परिपथ में रखें जैसा कि दिखाया गया है।
- क्या बल्ब जलता है? यह क्या दर्शाता है?
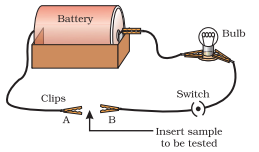
चित्र 3.2 धातुएँ विद्युत की सुचालक होती हैं।
आपने अवश्य देखा होगा कि आपके घरों में विद्युत धारा ले जाने वाले तारों पर पॉलीविनाइल क्लोराइड (PVC) या रबर जैसी सामग्री की परत चढ़ी होती है। विद्युत तारों को ऐसे पदार्थों से क्यों लेपित किया जाता है?
जब धातुएँ किसी कठोर सतह से टकराती हैं तो क्या होता है? क्या वे ध्वनि उत्पन्न करती हैं? जो धातुएँ कठोर सतह से टकराने पर ध्वनि उत्पन्न करती हैं, उन्हें ध्वनिक कहा जाता है। क्या आप अब कह सकते हैं कि स्कूल की घंटियाँ धातुओं से क्यों बनी होती हैं?
3.1.2 अधातु
पिछली कक्षा में आपने सीखा था कि धातुओं की तुलना में अधातुओं की संख्या बहुत कम है। अधातुओं के कुछ उदाहरण हैं कार्बन, सल्फर, आयोडीन, ऑक्सीजन, हाइड्रोजन, आदि। अधातुएँ या तो ठोस या गैसें होती हैं, ब्रोमीन को छोड़कर जो एक द्रव है। क्या अधातुओं में भी धातुओं के समान भौतिक गुण होते हैं? आइए जानें।
क्रियाकलाप 3.7
- कार्बन (कोयला या ग्रेफाइट), सल्फर और आयोडीन के नमूने एकत्रित करें।
- इन अधातुओं के साथ क्रियाकलाप 3.1 से 3.4 और 3.6 करें और अपने प्रेक्षण रिकॉर्ड करें।
धातुओं और अधातुओं के संबंध में अपने प्रेक्षणों को सारणी 3.1 में संकलित करें।
सारणी 3.1
| तत्व | प्रतीक | सतह का प्रकार | कठोरता | आघातवर्धनीयता | तन्यता | विद्युत चालन | ध्वनिकता |
|---|---|---|---|---|---|---|---|
सारणी 3.1 में दर्ज प्रेक्षणों के आधार पर, कक्षा में धातुओं और अधातुओं के सामान्य भौतिक गुणों पर चर्चा करें। आपने निश्चित रूप से यह निष्कर्ष निकाला होगा कि हम तत्वों को केवल उनके भौतिक गुणों के आधार पर वर्गीकृत नहीं कर सकते, क्योंकि कई अपवाद हैं। उदाहरण के लिए -
(i) पारा को छोड़कर सभी धातुएँ कमरे के तापमान पर ठोस अवस्था में होती हैं। क्रियाकलाप 3.5 में, आपने प्रेक्षण किया कि धातुओं के गलनांक उच्च होते हैं लेकिन गैलियम और सीज़ियम के गलनांक बहुत कम होते हैं। ये दोनों धातुएँ पिघल जाएँगी यदि आप उन्हें अपनी हथेली पर रखें।
(ii) आयोडीन एक अधातु है लेकिन यह चमकदार है।
(iii) कार्बन एक अधातु है जो विभिन्न रूपों में विद्यमान रह सकता है। प्रत्येक रूप को अपररूप कहा जाता है। हीरा, कार्बन का एक अपररूप, ज्ञात सबसे कठोर प्राकृतिक पदार्थ है और इसका गलनांक तथा क्वथनांक बहुत उच्च होता है। ग्रेफाइट, कार्बन का एक अन्य अपररूप, विद्युत का सुचालक है।
(iv) क्षार धातुएँ (लिथियम, सोडियम, पोटैशियम) इतनी मुलायम होती हैं कि उन्हें चाकू से काटा जा सकता है। इनका घनत्व कम होता है और गलनांक भी कम होते हैं।
तत्वों को उनके रासायनिक गुणों के आधार पर अधिक स्पष्ट रूप से धातुओं और अधातुओं के रूप में वर्गीकृत किया जा सकता है।
क्रियाकलाप 3.8
- एक मैग्नीशियम रिबन और कुछ सल्फर पाउडर लें।
- मैग्नीशियम रिबन को जलाएँ। बनी राख को एकत्रित करें और उसे पानी में घोलें।
- परिणामी विलयन को लाल और नीले दोनों लिटमस पेपर से परखें।
- मैग्नीशियम के जलने पर बना उत्पाद अम्लीय है या क्षारीय?
- अब सल्फर पाउडर जलाएँ। उत्पन्न धुएँ को एकत्रित करने के लिए जलते हुए सल्फर के ऊपर एक परखनली रखें।
- उपरोक्त परखनली में कुछ पानी मिलाएँ और हिलाएँ।
- इस विलयन को नीले और लाल लिटमस पेपर से परखें।
- सल्फर के जलने पर बना उत्पाद अम्लीय है या क्षारीय?
- क्या आप इन अभिक्रियाओं के लिए समीकरण लिख सकते हैं?
अधिकांश अधातुएँ जल में घुलने पर अम्लीय ऑक्साइड बनाती हैं। दूसरी ओर, अधिकांश धातुएँ, क्षारीय ऑक्साइड बनाती हैं। आप अगले भाग में इन धातु ऑक्साइडों के बारे में और अधिक सीखेंगे।
3.2 धातुओं के रासायनिक गुण
हम धातुओं के रासायनिक गुणों के बारे में निम्नलिखित भाग 3.2.1 से 3.2.4 में सीखेंगे। इसके लिए, निम्नलिखित धातुओं के नमूने एकत्रित करें - एल्युमीनियम, ताँबा, लोहा, सीसा, मैग्नीशियम, जस्ता और सोडियम।
3.2.1 जब धातुओं को वायु में जलाया जाता है तो क्या होता है?
आपने क्रियाकलाप 3.8 में देखा कि मैग्नीशियम वायु में एक तेज चमकदार सफेद लौ के साथ जलता है। क्या सभी धातुएँ एक ही तरीके से अभिक्रिया करती हैं? आइए निम्नलिखित क्रियाकलाप करके जाँच करें।
क्रियाकलाप 3.9
सावधानी: निम्नलिखित क्रियाकलाप के लिए शिक्षक की सहायता आवश्यक है। यह बेहतर होगा यदि छात्र आँखों की सुरक्षा करें।
- उपरोक्त में से किसी भी नमूने को चिमटे से पकड़ें और एक लौ के ऊपर जलाने का प्रयास करें। अन्य धातु नमूनों के साथ दोहराएँ।
- यदि बना तो उत्पाद एकत्रित करें।
- उत्पादों और धातु की सतह को ठंडा होने दें।
- कौन सी धातुएँ आसानी से जलती हैं?
- जब धातु जल रही थी तो आपने किस लौ का रंग देखा?
- जलने के बाद धातु की सतह कैसी दिखाई देती है?
- धातुओं को ऑक्सीजन के प्रति उनकी अभिक्रियाशीलता के घटते क्रम में व्यवस्थित करें।
- क्या उत्पाद जल में घुलनशील हैं?
लगभग सभी धातुएँ ऑक्सीजन के साथ संयोग करके धातु ऑक्साइड बनाती हैं।
धातु + ऑक्सीजन $\rightarrow$ धातु ऑक्साइड
उदाहरण के लिए, जब ताँबे को वायु में गर्म किया जाता है, तो यह ऑक्सीजन के साथ संयोग करके कॉपर(II) ऑक्साइड, एक काला ऑक्साइड बनाता है।
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
इसी प्रकार, एल्युमीनियम, एल्युमीनियम ऑक्साइड बनाता है।
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
अध्याय 2 से याद करें, कॉपर ऑक्साइड हाइड्रोक्लोरिक अम्ल के साथ कैसे अभिक्रिया करता है। हमने सीखा है कि धातु ऑक्साइड प्रकृति में क्षारीय होते हैं। लेकिन कुछ धातु ऑक्साइड, जैसे एल्युमीनियम ऑक्साइड, जिंक ऑक्साइड, अम्लीय और क्षारीय दोनों व्यवहार प्रदर्शित करते हैं। ऐसे धातु ऑक्साइड जो अम्ल और क्षार दोनों के साथ अभिक्रिया करके लवण और जल उत्पन्न करते हैं, उभयधर्मी ऑक्साइड के रूप में जाने जाते हैं। एल्युमीनियम ऑक्साइड अम्लों और क्षारों के साथ निम्न प्रकार से अभिक्रिया करता है -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
अधिकांश धातु ऑक्साइड जल में अघुलनशील होते हैं लेकिन इनमें से कुछ जल में घुलकर क्षार बनाते हैं। सोडियम ऑक्साइड और पोटैशियम ऑक्साइड जल में घुलकर क्षार निम्न प्रकार से उत्पन्न करते हैं -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
हमने क्रियाकलाप 3.9 में प्रेक्षण किया है कि सभी धातुएँ ऑक्सीजन के साथ एक ही दर से अभिक्रिया नहीं करतीं। विभिन्न धातुएँ ऑक्सीजन के प्रति भिन्न अभिक्रियाशीलता दर्शाती हैं। पोटैशियम और सोडियम जैसी धातुएँ इतनी प्रबलता से अभिक्रिया करती हैं कि यदि उन्हें खुले में रखा जाए तो वे आग पकड़ लेती हैं। इसलिए, उनकी सुरक्षा के लिए और आकस्मिक आग को रोकने के लिए, उन्हें मिट्टी के तेल में डुबोकर रखा जाता है। सामान्य तापमान पर, मैग्नीशियम, एल्युमीनियम, जस्ता, सीसा, आदि जैसी धातुओं की सतहें ऑक्साइड की एक पतली परत से ढकी रहती हैं। यह सुरक्षात्मक ऑक्साइड परत धातु को आगे ऑक्सीकरण से बचाती है। लोहा गर्म करने पर नहीं जलता लेकिन लोहे की बुरादी बर्नर की लौ में छिड़कने पर प्रबलता से जलती है। ताँबा नहीं जलता, लेकिन गर्म धातु कॉपर(II) ऑक्साइड की एक काली रंग की परत से ढक जाती है। चाँदी और सोना उच्च तापमान पर भी ऑक्सीजन के साथ अभिक्रिया नहीं करते।
क्या आप जानते हैं?
एनोडीकरण एल्युमीनियम की एक मोटी ऑक्साइड परत बनाने की एक प्रक्रिया है। एल्युमीनियम वायु के संपर्क में आने पर एक पतली ऑक्साइड परत विकसित करता है। यह एल्युमीनियम ऑक्साइड लेप इसे आगे संक्षारण के प्रति प्रतिरोधी बनाता है। ऑक्साइड परत को मोटा करके प्रतिरोध को और बेहतर बनाया जा सकता है। एनोडीकरण के दौरान, एक साफ एल्युमीनियम वस्तु को एनोड बनाया जाता है और उसे तनु सल्फ्यूरिक अम्ल के साथ विद्युत-अपघटित किया जाता है। एनोड पर मुक्त ऑक्सीजन गैस एल्युमीनियम के साथ अभिक्रिया करके एक मोटी सुरक्षात्मक ऑक्साइड परत बनाती है। इस ऑक्साइड परत को आसानी से रंगा जा सकता है जिससे एल्युमीनियम वस्तुओं को आकर्षक रूप दिया जा सकता है।
क्रियाकलाप 3.9 करने के बाद, आपने अवश्य प्रेक्षण किया होगा कि सोडियम यहाँ ली गई धातुओं के नमूनों में सबसे अधिक अभिक्रियाशील है। मैग्नीशियम की अभिक्रिया कम प्रबल है जो यह दर्शाता है कि यह सोडियम जितना अभिक्रियाशील नहीं है। लेकिन ऑक्सीजन में जलना हमें जस्ता, लोहा, ताँबा या सीसे की अभिक्रियाशीलता के बारे में निर्णय लेने में मदद नहीं करता। आइए इन धातुओं की अभिक्रियाशीलता के क्रम पर पहुँचने के लिए कुछ और अभिक्रियाएँ देखें।
3.2.2 जब धातुएँ जल के साथ अभिक्रिया करती हैं तो क्या होता है?
क्रियाकलाप 3.10
सावधानी: इस क्रियाकलाप के लिए शिक्षक की सहायता आवश्यक है।
- क्रियाकलाप 3.9 के समान धातुओं के नमूने एकत्रित करें।
- नमूनों के छोटे-छोटे टुकड़ों को अलग-अलग आधे ठंडे पानी से भरे बीकरों में डालें।
- कौन सी धातुएँ ठंडे पानी के साथ अभिक्रिया करती हैं? उन्हें ठंडे पानी के साथ उनकी अभिक्रियाशीलता के बढ़ते क्रम में व्यवस्थित करें।
- क्या कोई धातु पानी पर आग उत्पन्न करती है?
- क्या कोई धातु कुछ समय बाद तैरने लगती है?
- जो धातुएँ ठंडे पानी के साथ अभिक्रिया नहीं करतीं, उन्हें आधे गर्म पानी से भरे बीकरों में डालें।
- जो धातुएँ गर्म पानी के साथ भी अभिक्रिया नहीं करतीं, उनके लिए चित्र 3.3 के अनुसार उपकरण स्थापित करें और भाप के साथ उनकी अभिक्रिया का प्रेक्षण करें।
- कौन सी धातुएँ भाप के साथ भी अभिक्रिया नहीं करतीं?
- धातुओं को जल के साथ अभिक्रियाशीलता के घटते क्रम में व्यवस्थित करें।
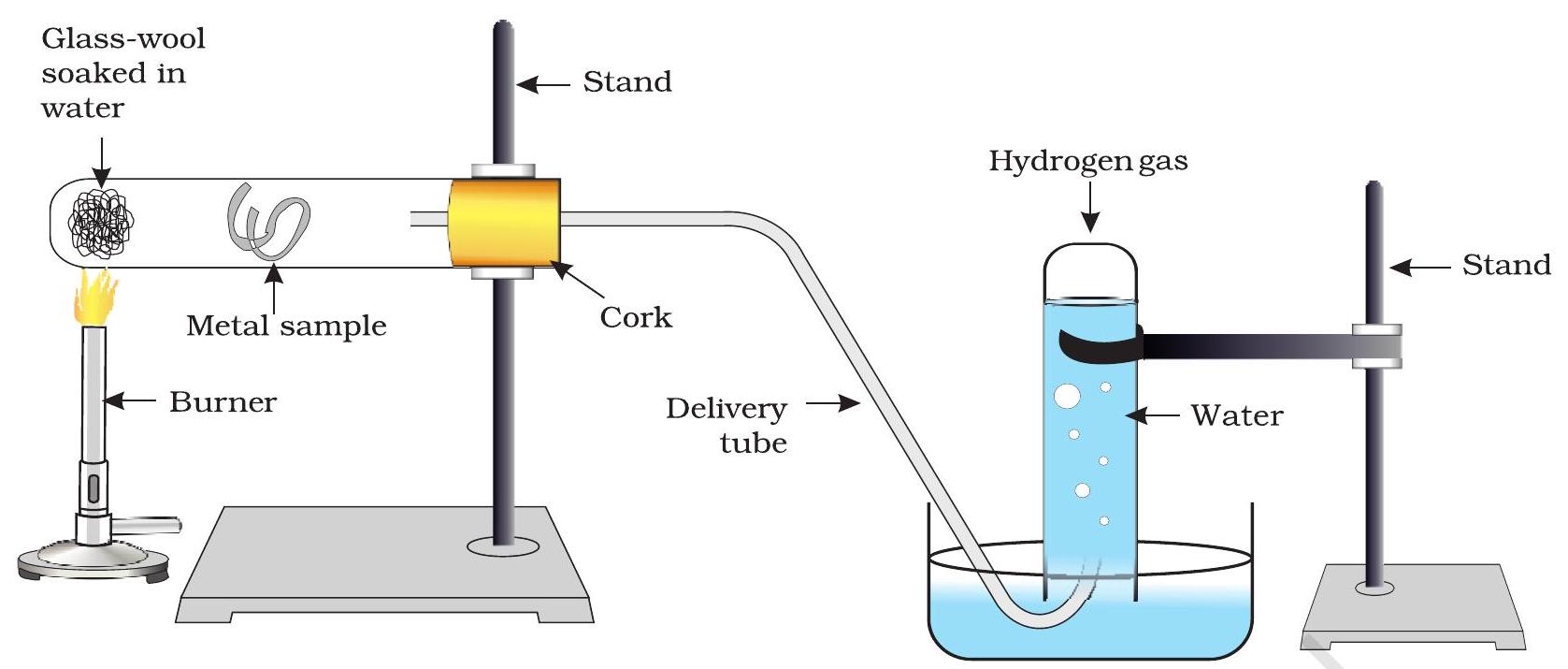
चित्र 3.3 भाप की धातु पर क्रिया
धातुएँ जल के साथ अभिक्रिया करती हैं और एक धातु ऑक्साइड और हाइड्रोजन गैस उत्पन्न करती हैं। धातु ऑक्साइड जो जल में घुलनशील होते हैं, उसमें घुलकर आगे धातु हाइड्रॉक्साइड बनाते हैं। लेकिन सभी धातुएँ जल के साथ अभिक्रिया नहीं करतीं।
धातु + जल $\rightarrow$ धातु ऑक्साइड + हाइड्रोजन
धातु ऑक्साइड + जल $ \rightarrow $ धातु हाइड्रॉक्साइड
पोटैशियम और सोडियम जैसी धातुएँ ठंडे पानी के साथ प्रबलता से अभिक्रिया करती हैं। सोडियम और पोटैशियम के मामले में, अभिक्रिया इतनी प्रबल और ऊष्माक्षेपी होती है कि मुक्त हाइड्रोजन तुरंत आग पकड़ लेती है।
$ \begin{aligned} & 2 K(s)+2 H_2 O(l) \to 2 KOH(aq)+H_2(g)+\text{ ऊष्मा ऊर्जा } \\ & 2 Na(s)+2 H_2 O(l) \to 2 NaOH(aq)+H_2(g)+\text{ ऊष्मा ऊर्जा } \end{aligned} $
कैल्शियम की जल के साथ अभिक्रिया कम प्रबल होती है। उत्पन्न ऊष्मा हाइड्रोजन के आग पकड़ने के लिए पर्याप्त नहीं होती।
$Ca(s)+2 H_2 O(l) \to Ca(OH)_2(aq)+H_2(g)$
कैल्शियम तैरने लगता है क्योंकि बने हाइड्रोजन गैस के बुलबुले धातु की सतह से चिपक जाते हैं।
मैग्नीशियम ठंडे पानी के साथ अभिक्रिया नहीं करता। यह गर्म पानी के साथ अभिक्रिया करके मैग्नीशियम हाइड्रॉक्साइड और हाइड्रोजन बनाता है। यह भी हाइड्रोजन गैस के बुलबुलों के अपनी सतह से चिपकने के कारण तैरने लगता है।
एल्युमीनियम, लोहा और जस्ता जैसी धातुएँ न तो ठंडे और न ही गर्म पानी के साथ अभिक्रिया करती हैं। लेकिन ये भाप के साथ अभिक्रिया करके धातु ऑक्साइड और हाइड्रोजन बनाती हैं।
$ \begin{aligned} & 2 Al(s)+3 H_2 O(g) \to Al_2 O_3(s)+3 H_2(g) \\ & 3 Fe(s)+4 H_2 O(g) \to Fe_3 O_4(s)+4 H_2(g) \end{aligned} $
सीसा, ताँबा, चाँदी और सोना जैसी धातुएँ जल के साथ बिल्कुल भी अभिक्रिया नहीं करतीं।
3.2.3 जब धातुएँ अम्लों के साथ अभिक्रिया करती हैं तो क्या होता है?
आप पहले ही सीख चुके हैं कि धातुएँ अम्लों के साथ अभिक्रिया करके एक लवण और हाइड्रोजन गैस देती हैं।
धातु + तनु अम्ल $ \rightarrow $ लवण + हाइड्रोजन
लेकिन क्या सभी धातुएँ एक ही तरीके से अभिक्रिया करती हैं? आइए जानें।
क्रियाकलाप 3.11
- सोडियम और पोटैशियम को छोड़कर सभी धातु नमूनों को पुनः एकत्रित करें। यदि नमूने मलिन हों, तो उन्हें सैंड पेपर से रगड़कर साफ करें। सावधानी: सोडियम और पोटैशियम न लें क्योंकि वे ठंडे पानी के साथ भी प्रबलता से अभिक्रिया करते हैं।
- नमूनों को अलग-अलग तनु हाइड्रोक्लोरिक अम्ल वाली परखनलियों में डालें।
- परखनलियों में थर्मामीटर लटकाएँ, ताकि उनके बल्ब अम्ल में डूबे रहें।
- बुलबुलों के बनने की दर का सावधानीपूर्वक प्रेक्षण करें।
- कौन सी धातुएँ तनु हाइड्रोक्लोरिक अम्ल के साथ प्रबलता से अभिक्रिया करती हैं?
- किस धातु के साथ आपने सबसे अधिक तापमान दर्ज किया?
- धातुओं को तनु अम्लों के साथ अभिक्रियाशीलता के घटते क्रम में व्यवस्थित करें











