ಅಧ್ಯಾಯ 03 ಲೋಹಗಳು ಮತ್ತು ಲೋಹೇತರಗಳು
IX ನೇ ತರಗತಿಯಲ್ಲಿ ನೀವು ವಿವಿಧ ಮೂಲಧಾತುಗಳ ಬಗ್ಗೆ ಕಲಿತಿದ್ದೀರಿ. ಮೂಲಧಾತುಗಳನ್ನು ಅವುಗಳ ಗುಣಗಳ ಆಧಾರದ ಮೇಲೆ ಲೋಹಗಳು ಅಥವಾ ಅಲೋಹಗಳಾಗಿ ವರ್ಗೀಕರಿಸಬಹುದು ಎಂದು ನೀವು ನೋಡಿದ್ದೀರಿ.
- ನಿಮ್ಮ ದೈನಂದಿನ ಜೀವನದಲ್ಲಿ ಲೋಹಗಳು ಮತ್ತು ಅಲೋಹಗಳ ಕೆಲವು ಉಪಯೋಗಗಳ ಬಗ್ಗೆ ಯೋಚಿಸಿ.
- ಮೂಲಧಾತುಗಳನ್ನು ಲೋಹಗಳು ಅಥವಾ ಅಲೋಹಗಳಾಗಿ ವರ್ಗೀಕರಿಸುವಾಗ ನೀವು ಯಾವ ಗುಣಗಳ ಬಗ್ಗೆ ಯೋಚಿಸಿದ್ದೀರಿ?
- ಈ ಗುಣಗಳು ಮೂಲಧಾತುಗಳ ಉಪಯೋಗಗಳಿಗೆ ಹೇಗೆ ಸಂಬಂಧಿಸಿವೆ?
ಈ ಗುಣಗಳಲ್ಲಿ ಕೆಲವನ್ನು ವಿವರವಾಗಿ ನೋಡೋಣ.
3.1 ಭೌತಿಕ ಗುಣಗಳು
3.1.1 ಲೋಹಗಳು
ಪದಾರ್ಥಗಳನ್ನು ಗುಂಪು ಮಾಡಲು ಪ್ರಾರಂಭಿಸುವ ಸುಲಭ ಮಾರ್ಗವೆಂದರೆ ಅವುಗಳ ಭೌತಿಕ ಗುಣಗಳನ್ನು ಹೋಲಿಸುವುದು. ಕೆಳಗಿನ ಚಟುವಟಿಕೆಗಳ ಸಹಾಯದಿಂದ ಇದನ್ನು ಅಧ್ಯಯನ ಮಾಡೋಣ. ಚಟುವಟಿಕೆಗಳು 3.1 ರಿಂದ 3.6 ರವರೆಗೆ ನಡೆಸಲು, ಕೆಳಗಿನ ಲೋಹಗಳ ಮಾದರಿಗಳನ್ನು ಸಂಗ್ರಹಿಸಿ - ಕಬ್ಬಿಣ, ತಾಮ್ರ, ಅಲ್ಯೂಮಿನಿಯಂ, ಮೆಗ್ನೀಶಿಯಂ, ಸೋಡಿಯಂ, ಸೀಸ, ಸತು ಮತ್ತು ಸುಲಭವಾಗಿ ಲಭ್ಯವಿರುವ ಯಾವುದೇ ಇತರ ಲೋಹ.
ಚಟುವಟಿಕೆ 3.1
- ಕಬ್ಬಿಣ, ತಾಮ್ರ, ಅಲ್ಯೂಮಿನಿಯಂ ಮತ್ತು ಮೆಗ್ನೀಶಿಯಂ ಮಾದರಿಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ. ಪ್ರತಿ ಮಾದರಿಯ ನೋಟವನ್ನು ಗಮನಿಸಿ.
- ಪ್ರತಿ ಮಾದರಿಯ ಮೇಲ್ಮೈಯನ್ನು ಮರಳು ಕಾಗದದಿಂದ ಉಜ್ಜಿ ಸ್ವಚ್ಛಗೊಳಿಸಿ ಮತ್ತು ಅವುಗಳ ನೋಟವನ್ನು ಮತ್ತೆ ಗಮನಿಸಿ.
ಶುದ್ಧ ಸ್ಥಿತಿಯಲ್ಲಿ, ಲೋಹಗಳು ಹೊಳೆಯುವ ಮೇಲ್ಮೈ ಹೊಂದಿರುತ್ತವೆ. ಈ ಗುಣವನ್ನು ಲೋಹೀಯ ಕಾಂತಿ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಚಟುವಟಿಕೆ 3.2
ಕಬ್ಬಿಣ, ತಾಮ್ರ, ಅಲ್ಯೂಮಿನಿಯಂ ಮತ್ತು ಮೆಗ್ನೀಶಿಯಂನ ಸಣ್ಣ ತುಂಡುಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ. ಈ ಲೋಹಗಳನ್ನು ಚೂಪಾದ ಚಾಕುವಿನಿಂದ ಕತ್ತರಿಸಲು ಪ್ರಯತ್ನಿಸಿ ಮತ್ತು ನಿಮ್ಮ ವೀಕ್ಷಣೆಗಳನ್ನು ಗಮನಿಸಿ.
ಒಂದು ಜೋಡಿ ಸೆಲಿಗೆಯಿಂದ ಸೋಡಿಯಂ ಲೋಹದ ತುಂಡನ್ನು ಹಿಡಿದುಕೊಳ್ಳಿ.
ಎಚ್ಚರಿಕೆ: ಸೋಡಿಯಂ ಲೋಹವನ್ನು ಯಾವಾಗಲೂ ಜಾಗರೂಕತೆಯಿಂದ ನಿಭಾಯಿಸಿ. ಫಿಲ್ಟರ್ ಕಾಗದದ ಮಡಿಕೆಗಳ ನಡುವೆ ಒತ್ತಿ ಅದನ್ನು ಒಣಗಿಸಿ.
ಅದನ್ನು ವಾಚ್-ಗ್ಲಾಸ್ ಮೇಲೆ ಇರಿಸಿ ಮತ್ತು ಅದನ್ನು ಚಾಕುವಿನಿಂದ ಕತ್ತರಿಸಲು ಪ್ರಯತ್ನಿಸಿ.
ನೀವು ಏನು ಗಮನಿಸುತ್ತೀರಿ?
ಲೋಹಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಗಟ್ಟಿಯಾಗಿರುತ್ತವೆ ಎಂದು ನೀವು ಕಾಣುವಿರಿ. ಗಟ್ಟಿತನವು ಲೋಹದಿಂದ ಲೋಹಕ್ಕೆ ಬದಲಾಗುತ್ತದೆ.
ಚಟುವಟಿಕೆ 3.3
- ಕಬ್ಬಿಣ, ಸತು, ಸೀಸ ಮತ್ತು ತಾಮ್ರದ ತುಂಡುಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ.
- ಯಾವುದೇ ಒಂದು ಲೋಹವನ್ನು ಕಬ್ಬಿಣದ ಬ್ಲಾಕ್ ಮೇಲೆ ಇರಿಸಿ ಮತ್ತು ಸುತ್ತಿಗೆಯಿಂದ ನಾಲ್ಕು ಅಥವಾ ಐದು ಬಾರಿ ಹೊಡೆಯಿರಿ. ನೀವು ಏನು ಗಮನಿಸುತ್ತೀರಿ?
- ಇತರ ಲೋಹಗಳೊಂದಿಗೆ ಪುನರಾವರ್ತಿಸಿ.
- ಈ ಲೋಹಗಳ ಆಕಾರದಲ್ಲಿನ ಬದಲಾವಣೆಯನ್ನು ದಾಖಲಿಸಿ.
ಕೆಲವು ಲೋಹಗಳನ್ನು ತೆಳುವಾದ ಹಾಳೆಗಳಾಗಿ ಬಡಿಯಬಹುದು ಎಂದು ನೀವು ಕಾಣುವಿರಿ. ಈ ಗುಣವನ್ನು ತಟ್ಟಬಲ್ಲಿಕೆ (ಮ್ಯಾಲಿಯಬಿಲಿಟಿ) ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಚಿನ್ನ ಮತ್ತು ಬೆಳ್ಳಿಯು ಅತ್ಯಂತ ತಟ್ಟಬಲ್ಲ ಲೋಹಗಳು ಎಂದು ನಿಮಗೆ ತಿಳಿದಿದೆಯೇ?
ಚಟುವಟಿಕೆ 3.4
- ದೈನಂದಿನ ಜೀವನದಲ್ಲಿ ನೀವು ನೋಡಿದ ತಂತಿಗಳನ್ನು ಹೊಂದಿರುವ ಲೋಹಗಳ ಪಟ್ಟಿಯನ್ನು ಮಾಡಿ.
ಲೋಹಗಳನ್ನು ತೆಳುವಾದ ತಂತಿಗಳಾಗಿ ಎಳೆಯಬಲ್ಲ ಸಾಮರ್ಥ್ಯವನ್ನು ಎಳೆತನ (ಡಕ್ಟಿಲಿಟಿ) ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಚಿನ್ನವು ಅತ್ಯಂತ ಎಳೆತನದ ಲೋಹವಾಗಿದೆ. ಒಂದು ಗ್ರಾಂ ಚಿನ್ನದಿಂದ ಸುಮಾರು $2 km$ ಉದ್ದದ ತಂತಿಯನ್ನು ಎಳೆಯಬಹುದು ಎಂದು ತಿಳಿದರೆ ನೀವು ಆಶ್ಚರ್ಯಪಡುವಿರಿ.
ಅವುಗಳ ತಟ್ಟಬಲ್ಲಿಕೆ ಮತ್ತು ಎಳೆತನದ ಕಾರಣದಿಂದಾಗಿಯೇ ಲೋಹಗಳಿಗೆ ನಮ್ಮ ಅಗತ್ಯಗಳಿಗೆ ಅನುಗುಣವಾಗಿ ವಿವಿಧ ಆಕಾರಗಳನ್ನು ನೀಡಬಹುದು.
ಅಡುಗೆ ಪಾತ್ರೆಗಳನ್ನು ತಯಾರಿಸಲು ಬಳಸುವ ಕೆಲವು ಲೋಹಗಳನ್ನು ನೀವು ಹೆಸರಿಸಬಲ್ಲಿರಾ? ಈ ಲೋಹಗಳನ್ನು ಪಾತ್ರೆಗಳನ್ನು ತಯಾರಿಸಲು ಏಕೆ ಬಳಸಲಾಗುತ್ತದೆ ಎಂದು ನಿಮಗೆ ತಿಳಿದಿದೆಯೇ? ಉತ್ತರವನ್ನು ಕಂಡುಹಿಡಿಯಲು ಕೆಳಗಿನ ಚಟುವಟಿಕೆಯನ್ನು ಮಾಡೋಣ.
ಚಟುವಟಿಕೆ 3.5
- ಅಲ್ಯೂಮಿನಿಯಂ ಅಥವಾ ತಾಮ್ರದ ತಂತಿಯನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ. ಈ ತಂತಿಯನ್ನು ಫಿಗರ್ 3.1 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ಸ್ಟ್ಯಾಂಡ್ ಮೇಲೆ ಬಿಗಿಗೊಳಿಸಿ.
- ಮೇಣದ ಸಹಾಯದಿಂದ ತಂತಿಯ ಮುಕ್ತ ತುದಿಗೆ ಪಿನ್ ಅನ್ನು ಜೋಡಿಸಿ.
- ಅದು ಬಿಗಿಗೊಳಿಸಲ್ಪಟ್ಟಿರುವ ಸ್ಥಳದ ಬಳಿ ಸ್ಪಿರಿಟ್ ದೀಪ, ಮೇಣದಬತ್ತಿ ಅಥವಾ ಬರ್ನರ್ನಿಂದ ತಂತಿಯನ್ನು ಬಿಸಿ ಮಾಡಿ.
- ಸ್ವಲ್ಪ ಸಮಯದ ನಂತರ ನೀವು ಏನು ಗಮನಿಸುತ್ತೀರಿ?
- ನಿಮ್ಮ ವೀಕ್ಷಣೆಗಳನ್ನು ಗಮನಿಸಿ. ಲೋಹದ ತಂತಿ ಕರಗುತ್ತದೆಯೇ?
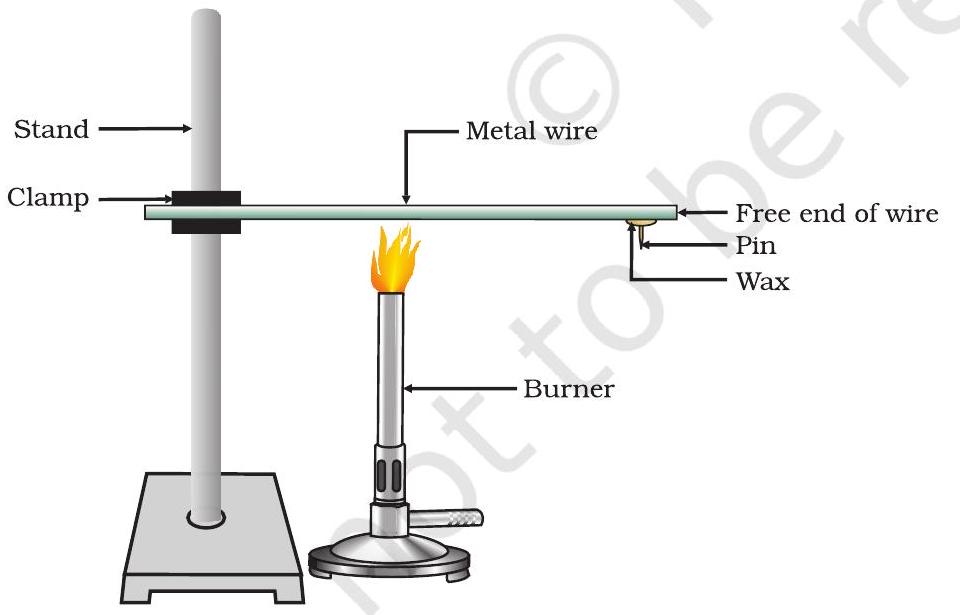
ಚಿತ್ರ 3.1 ಲೋಹಗಳು ಉಷ್ಣದ ಉತ್ತಮ ವಾಹಕಗಳಾಗಿವೆ.
ಮೇಲಿನ ಚಟುವಟಿಕೆಯು ಲೋಹಗಳು ಉಷ್ಣದ ಉತ್ತಮ ವಾಹಕಗಳಾಗಿವೆ ಮತ್ತು ಅವುಗಳು ಹೆಚ್ಚು ದ್ರವೀಕರಣ ಬಿಂದುಗಳನ್ನು ಹೊಂದಿವೆ ಎಂದು ತೋರಿಸುತ್ತದೆ. ಉಷ್ಣದ ಅತ್ಯುತ್ತಮ ವಾಹಕಗಳೆಂದರೆ ಬೆಳ್ಳಿ ಮತ್ತು ತಾಮ್ರ. ಸೀಸ ಮತ್ತು ಪಾದರಸವು ತುಲನಾತ್ಮಕವಾಗಿ ಕಳಪೆ ಉಷ್ಣ ವಾಹಕಗಳಾಗಿವೆ.
ಲೋಹಗಳು ವಿದ್ಯುತ್ ಸಹ ವಾಹಕವೇ? ಕಂಡುಹಿಡಿಯೋಣ.
ಚಟುವಟಿಕೆ 3.6
- ಫಿಗರ್ 3.2 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ವಿದ್ಯುತ್ ಸರ್ಕ್ಯೂಟ್ ಅನ್ನು ಸ್ಥಾಪಿಸಿ.
- ಪರೀಕ್ಷಿಸಬೇಕಾದ ಲೋಹವನ್ನು ಸರ್ಕ್ಯೂಟ್ನಲ್ಲಿ $A$ ಮತ್ತು $B$ ಟರ್ಮಿನಲ್ಗಳ ನಡುವೆ ತೋರಿಸಿರುವಂತೆ ಇರಿಸಿ.
- ಬಲ್ಬ್ ಹೊಳೆಯುತ್ತದೆಯೇ? ಇದು ಏನನ್ನು ಸೂಚಿಸುತ್ತದೆ?
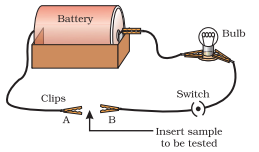
ಚಿತ್ರ 3.2 ಲೋಹಗಳು ವಿದ್ಯುತ್ನ ಉತ್ತಮ ವಾಹಕಗಳಾಗಿವೆ.
ನಿಮ್ಮ ಮನೆಗಳಲ್ಲಿ ಪ್ರವಾಹವನ್ನು ಸಾಗಿಸುವ ತಂತಿಗಳು ಪಾಲಿವಿನೈಲ್ ಕ್ಲೋರೈಡ್ (ಪಿವಿಸಿ) ಅಥವಾ ರಬ್ಬರ್ ತರಹದ ವಸ್ತುವಿನ ಲೇಪನವನ್ನು ಹೊಂದಿರುತ್ತವೆ ಎಂದು ನೀವು ನೋಡಿರಬೇಕು. ವಿದ್ಯುತ್ ತಂತಿಗಳನ್ನು ಅಂತಹ ವಸ್ತುಗಳಿಂದ ಲೇಪಿಸಲಾಗಿರುವುದು ಏಕೆ?
ಲೋಹಗಳು ಗಟ್ಟಿಯಾದ ಮೇಲ್ಮೈಯನ್ನು ಹೊಡೆದಾಗ ಏನಾಗುತ್ತದೆ? ಅವು ಶಬ್ದವನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುತ್ತವೆಯೇ? ಗಟ್ಟಿಯಾದ ಮೇಲ್ಮೈಯನ್ನು ಹೊಡೆದಾಗ ಶಬ್ದವನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುವ ಲೋಹಗಳನ್ನು ಧ್ವನಿಮುದ್ರಕ (ಸೋನೋರಸ್) ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ. ಶಾಲೆಯ ಗಂಟೆಗಳನ್ನು ಲೋಹಗಳಿಂದ ತಯಾರಿಸಲಾಗಿರುವುದು ಏಕೆ ಎಂದು ನೀವು ಈಗ ಹೇಳಬಲ್ಲಿರಾ?
3.1.2 ಅಲೋಹಗಳು
ಹಿಂದಿನ ತರಗತಿಯಲ್ಲಿ ಲೋಹಗಳಿಗೆ ಹೋಲಿಸಿದರೆ ಅಲೋಹಗಳು ಬಹಳ ಕಡಿಮೆ ಇವೆ ಎಂದು ನೀವು ಕಲಿತಿದ್ದೀರಿ. ಅಲೋಹಗಳ ಕೆಲವು ಉದಾಹರಣೆಗಳೆಂದರೆ ಇಂಗಾಲ, ಗಂಧಕ, ಅಯೊಡಿನ್, ಆಮ್ಲಜನಕ, ಜಲಜನಕ, ಇತ್ಯಾದಿ. ಅಲೋಹಗಳು ಬ್ರೋಮಿನ್ ಹೊರತುಪಡಿಸಿ ಘನ ಅಥವಾ ಅನಿಲಗಳಾಗಿವೆ, ಬ್ರೋಮಿನ್ ದ್ರವವಾಗಿದೆ.
ಅಲೋಹಗಳು ಸಹ ಲೋಹಗಳಿಗೆ ಹೋಲುವ ಭೌತಿಕ ಗುಣಗಳನ್ನು ಹೊಂದಿವೆಯೇ? ಕಂಡುಹಿಡಿಯೋಣ.
ಚಟುವಟಿಕೆ 3.7
- ಇಂಗಾಲ (ಬೆಂಕಿಕಡ್ಡಿ ಅಥವಾ ಗ್ರಾಫೈಟ್), ಗಂಧಕ ಮತ್ತು ಅಯೊಡಿನ್ ಮಾದರಿಗಳನ್ನು ಸಂಗ್ರಹಿಸಿ.
- ಈ ಅಲೋಹಗಳೊಂದಿಗೆ ಚಟುವಟಿಕೆಗಳು 3.1 ರಿಂದ 3.4 ಮತ್ತು 3.6 ಅನ್ನು ನಡೆಸಿ ಮತ್ತು ನಿಮ್ಮ ವೀಕ್ಷಣೆಗಳನ್ನು ದಾಖಲಿಸಿ.
ಲೋಹಗಳು ಮತ್ತು ಅಲೋಹಗಳ ಬಗ್ಗೆ ನಿಮ್ಮ ವೀಕ್ಷಣೆಗಳನ್ನು ಕೋಷ್ಟಕ 3.1 ರಲ್ಲಿ ಸಂಕಲಿಸಿ.
ಕೋಷ್ಟಕ 3.1
| ಮೂಲಧಾತು | ಚಿಹ್ನೆ | ಮೇಲ್ಮೈಯ ಪ್ರಕಾರ | ಗಟ್ಟಿತನ | ತಟ್ಟಬಲ್ಲಿಕೆ | ಎಳೆತನ | ವಿದ್ಯುತ್ ವಾಹಕತೆ | ಧ್ವನಿಮುದ್ರತೆ |
|---|---|---|---|---|---|---|---|
ಕೋಷ್ಟಕ 3.1 ರಲ್ಲಿ ದಾಖಲಾದ ವೀಕ್ಷಣೆಗಳ ಆಧಾರದ ಮೇಲೆ, ತರಗತಿಯಲ್ಲಿ ಲೋಹಗಳು ಮತ್ತು ಅಲೋಹಗಳ ಸಾಮಾನ್ಯ ಭೌತಿಕ ಗುಣಗಳನ್ನು ಚರ್ಚಿಸಿ. ಅನೇಕ ಅಪವಾದಗಳಿರುವುದರಿಂದ, ಮೂಲಧಾತುಗಳನ್ನು ಅವುಗಳ ಭೌತಿಕ ಗುಣಗಳ ಆಧಾರದ ಮೇಲೆ ಮಾತ್ರ ಗುಂಪು ಮಾಡಲು ಸಾಧ್ಯವಿಲ್ಲ ಎಂದು ನೀವು ತೀರ್ಮಾನಿಸಿರಬೇಕು. ಉದಾಹರಣೆಗೆ -
(i) ಪಾದರಸವನ್ನು ಹೊರತುಪಡಿಸಿ ಎಲ್ಲಾ ಲೋಹಗಳು ಕೋಣೆಯ ತಾಪಮಾನದಲ್ಲಿ ಘನಗಳಾಗಿ ಅಸ್ತಿತ್ವದಲ್ಲಿವೆ. ಚಟುವಟಿಕೆ 3.5 ರಲ್ಲಿ, ಲೋಹಗಳು ಹೆಚ್ಚು ದ್ರವೀಕರಣ ಬಿಂದುಗಳನ್ನು ಹೊಂದಿವೆ ಎಂದು ನೀವು ಗಮನಿಸಿದ್ದೀರಿ ಆದರೆ ಗ್ಯಾಲಿಯಂ ಮತ್ತು ಸೀಸಿಯಂನ ಬಹಳ ಕಡಿಮೆ ದ್ರವೀಕರಣ ಬಿಂದುಗಳಿವೆ. ನಿಮ್ಮ ಅಂಗೈಯ ಮೇಲೆ ಇಟ್ಟರೆ ಈ ಎರಡು ಲೋಹಗಳು ಕರಗುತ್ತವೆ.
(ii) ಅಯೊಡಿನ್ ಒಂದು ಅಲೋಹ ಆದರೆ ಅದು ಹೊಳೆಯುತ್ತದೆ.
(iii) ಇಂಗಾಲವು ವಿವಿಧ ರೂಪಗಳಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿರಬಲ್ಲ ಒಂದು ಅಲೋಹವಾಗಿದೆ. ಪ್ರತಿಯೊಂದು ರೂಪವನ್ನು ಅಲೋಟ್ರೋಪ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಇಂಗಾಲದ ಒಂದು ಅಲೋಟ್ರೋಪ್ ಆದ ವಜ್ರವು ತಿಳಿದಿರುವ ಅತ್ಯಂತ ಕಠಿಣ ನೈಸರ್ಗಿಕ ವಸ್ತುವಾಗಿದೆ ಮತ್ತು ಅತ್ಯಂತ ಹೆಚ್ಚು ದ್ರವೀಕರಣ ಮತ್ತು ಕುದಿಬಿಂದುಗಳನ್ನು ಹೊಂದಿದೆ. ಇಂಗಾಲದ ಇನ್ನೊಂದು ಅಲೋಟ್ರೋಪ್ ಆದ ಗ್ರಾಫೈಟ್, ವಿದ್ಯುತ್ನ ವಾಹಕವಾಗಿದೆ.
(iv) ಕ್ಷಾರ ಲೋಹಗಳು (ಲಿಥಿಯಂ, ಸೋಡಿಯಂ, ಪೊಟ್ಯಾಸಿಯಂ) ಬಹಳ ಮೃದುವಾಗಿರುತ್ತವೆ, ಅವುಗಳನ್ನು ಚಾಕುವಿನಿಂದ ಕತ್ತರಿಸಬಹುದು. ಅವುಗಳು ಕಡಿಮೆ ಸಾಂದ್ರತೆ ಮತ್ತು ಕಡಿಮೆ ದ್ರವೀಕರಣ ಬಿಂದುಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಮೂಲಧಾತುಗಳನ್ನು ಅವುಗಳ ರಾಸಾಯನಿಕ ಗುಣಗಳ ಆಧಾರದ ಮೇಲೆ ಹೆಚ್ಚು ಸ್ಪಷ್ಟವಾಗಿ ಲೋಹಗಳು ಮತ್ತು ಅಲೋಹಗಳಾಗಿ ವರ್ಗೀಕರಿಸಬಹುದು.
ಚಟುವಟಿಕೆ 3.8
- ಮೆಗ್ನೀಶಿಯಂ ರಿಬ್ಬನ್ ಮತ್ತು ಸ್ವಲ್ಪ ಗಂಧಕ ಪುಡಿಯನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ.
- ಮೆಗ್ನೀಶಿಯಂ ರಿಬ್ಬನ್ ಅನ್ನು ಸುಡಿ. ರೂಪುಗೊಂಡ ಬೂದಿಯನ್ನು ಸಂಗ್ರಹಿಸಿ ಮತ್ತು ಅದನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿ.
- ಫಲಿತಾಂಶದ ದ್ರಾವಣವನ್ನು ಕೆಂಪು ಮತ್ತು ನೀಲಿ ಲಿಟ್ಮಸ್ ಕಾಗದದಿಂದ ಪರೀಕ್ಷಿಸಿ.
- ಮೆಗ್ನೀಶಿಯಂ ಅನ್ನು ಸುಡುವಾಗ ರೂಪುಗೊಂಡ ಉತ್ಪನ್ನ ಆಮ್ಲೀಯವೇ ಅಥವಾ ಕ್ಷಾರೀಯವೇ?
- ಈಗ ಗಂಧಕ ಪುಡಿಯನ್ನು ಸುಡಿ. ಉತ್ಪತ್ತಿಯಾದ ಹೊಗೆಯನ್ನು ಸಂಗ್ರಹಿಸಲು ಜ್ವಲಿಸುತ್ತಿರುವ ಗಂಧಕದ ಮೇಲೆ ಒಂದು ಟೆಸ್ಟ್ ಟ್ಯೂಬ್ ಅನ್ನು ಇರಿಸಿ.
- ಮೇಲಿನ ಟೆಸ್ಟ್ ಟ್ಯೂಬ್ಗೆ ಸ್ವಲ್ಪ ನೀರು ಸೇರಿಸಿ ಮತ್ತು ಕುಲುಕಿ.
- ಈ ದ್ರಾವಣವನ್ನು ನೀಲಿ ಮತ್ತು ಕೆಂಪು ಲಿಟ್ಮಸ್ ಕಾಗದದಿಂದ ಪರೀಕ್ಷಿಸಿ.
- ಗಂಧಕವನ್ನು ಸುಡುವಾಗ ರೂಪುಗೊಂಡ ಉತ್ಪನ್ನ ಆಮ್ಲೀಯವೇ ಅಥವಾ ಕ್ಷಾರೀಯವೇ?
- ಈ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಸಮೀಕರಣಗಳನ್ನು ನೀವು ಬರೆಯಬಲ್ಲಿರಾ?
ಹೆಚ್ಚಿನ ಅಲೋಹಗಳು ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಆಮ್ಲೀಯ ಆಕ್ಸೈಡ್ಗಳನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುತ್ತವೆ. ಮತ್ತೊಂದೆಡೆ, ಹೆಚ್ಚಿನ ಲೋಹಗಳು, ಕ್ಷಾರೀಯ ಆಕ್ಸೈಡ್ಗಳನ್ನು ನೀಡುತ್ತವೆ. ಮುಂದಿನ ವಿಭಾಗದಲ್ಲಿ ಈ ಲೋಹ ಆಕ್ಸೈಡ್ಗಳ ಬಗ್ಗೆ ನೀವು ಇನ್ನಷ್ಟು ಕಲಿಯುವಿರಿ.
3.2 ಲೋಹಗಳ ರಾಸಾಯನಿಕ ಗುಣಗಳು
ನಾವು ಲೋಹಗಳ ರಾಸಾಯನಿಕ ಗುಣಗಳ ಬಗ್ಗೆ ಕೆಳಗಿನ ವಿಭಾಗಗಳು 3.2.1 ರಿಂದ 3.2.4 ರಲ್ಲಿ ಕಲಿಯುತ್ತೇವೆ. ಇದಕ್ಕಾಗಿ, ಕೆಳಗಿನ ಲೋಹಗಳ ಮಾದರಿಗಳನ್ನು ಸಂಗ್ರಹಿಸಿ - ಅಲ್ಯೂಮಿನಿಯಂ, ತಾಮ್ರ, ಕಬ್ಬಿಣ, ಸೀಸ, ಮೆಗ್ನೀಶಿಯಂ, ಸತು ಮತ್ತು ಸೋಡಿಯಂ.
3.2.1 ಲೋಹಗಳನ್ನು ಗಾಳಿಯಲ್ಲಿ ಸುಡುವಾಗ ಏನಾಗುತ್ತದೆ?
ಮೆಗ್ನೀಶಿಯಂ ಗಾಳಿಯಲ್ಲಿ ಪ್ರಕಾಶಮಾನವಾದ ಬಿಳಿ ಜ್ವಾಲೆಯೊಂದಿಗೆ ಉರಿಯುತ್ತದೆ ಎಂದು ನೀವು ಚಟುವಟಿಕೆ 3.8 ರಲ್ಲಿ ನೋಡಿದ್ದೀರಿ. ಎಲ್ಲಾ ಲೋಹಗಳು ಒಂದೇ ರೀತಿಯಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆಯೇ? ಕೆಳಗಿನ ಚಟುವಟಿಕೆಯನ್ನು ನಡೆಸುವ ಮೂಲಕ ಪರಿಶೀಲಿಸೋಣ.
ಚಟುವಟಿಕೆ 3.9
ಎಚ್ಚರಿಕೆ: ಕೆಳಗಿನ ಚಟುವಟಿಕೆಗೆ ಶಿಕ್ಷಕರ ಸಹಾಯ ಅಗತ್ಯವಿದೆ. ವಿದ್ಯಾರ್ಥಿಗಳು ಕಣ್ಣಿನ ರಕ್ಷಣೆ ಧರಿಸಿದರೆ ಉತ್ತಮ.
- ಮೇಲೆ ತೆಗೆದುಕೊಂಡ ಯಾವುದೇ ಮಾದರಿಯನ್ನು ಜೋಡಿ ಸೆಲಿಗೆಯಿಂದ ಹಿಡಿದುಕೊಂಡು ಜ್ವಾಲೆಯ ಮೇಲೆ ಸುಡಲು ಪ್ರಯತ್ನಿಸಿ. ಇತರ ಲೋಹ ಮಾದರಿಗಳೊಂದಿಗೆ ಪುನರಾವರ್ತಿಸಿ.
- ರೂಪುಗೊಂಡ ಉತ್ಪನ್ನವನ್ನು ಸಂಗ್ರಹಿಸಿ.
- ಉತ್ಪನ್ನಗಳು ಮತ್ತು ಲೋಹದ ಮೇಲ್ಮೈ ತಣ್ಣಗಾಗಲು ಬಿಡಿ.
- ಯಾವ ಲೋಹಗಳು ಸುಲಭವಾಗಿ ಉರಿಯುತ್ತವೆ?
- ಲೋಹವು ಉರಿದಾಗ ನೀವು ಯಾವ ಜ್ವಾಲೆಯ ಬಣ್ಣವನ್ನು ಗಮನಿಸಿದ್ದೀರಿ?
- ಸುಟ್ಟ ನಂತರ ಲೋಹದ ಮೇಲ್ಮೈ ಹೇಗೆ ಕಾಣುತ್ತದೆ?
- ಆಮ್ಲಜನಕದ ಕಡೆಗೆ ಅವುಗಳ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಯ ಇಳಿಕೆಯ ಕ್ರಮದಲ್ಲಿ ಲೋಹಗಳನ್ನು ಜೋಡಿಸಿ.
- ಉತ್ಪನ್ನಗಳು ನೀರಿನಲ್ಲಿ ಕರಗುತ್ತವೆಯೇ?
ಬಹುತೇಕ ಎಲ್ಲಾ ಲೋಹಗಳು ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಸಂಯೋಜಿಸಿ ಲೋಹ ಆಕ್ಸೈಡ್ಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ.
ಲೋಹ + ಆಮ್ಲಜನಕ $\rightarrow$ ಲೋಹ ಆಕ್ಸೈಡ್
ಉದಾಹರಣೆಗೆ, ತಾಮ್ರವನ್ನು ಗಾಳಿಯಲ್ಲಿ ಬಿಸಿ ಮಾಡಿದಾಗ, ಅದು ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಸಂಯೋಜಿಸಿ ಕಪ್ಪು ಆಕ್ಸೈಡ್ ಆದ ತಾಮ್ರ(II) ಆಕ್ಸೈಡ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ.
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
ಅಂತೆಯೇ, ಅಲ್ಯೂಮಿನಿಯಂ ಅಲ್ಯೂಮಿನಿಯಂ ಆಕ್ಸೈಡ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ.
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
ತಾಮ್ರ ಆಕ್ಸೈಡ್ ಹೈಡ್ರೋಕ್ಲೋರಿಕ್ ಆಮ್ಲದೊಂದಿಗೆ ಹೇಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ ಎಂಬುದನ್ನು ಅಧ್ಯಾಯ 2 ರಿಂದ ನೆನಪಿಸಿಕೊಳ್ಳಿ. ಲೋಹ ಆಕ್ಸೈಡ್ಗಳು ಕ್ಷಾರೀಯ ಸ್ವಭಾವದ್ದಾಗಿವೆ ಎಂದು ನಾವು ಕಲಿತಿದ್ದೇವೆ. ಆದರೆ ಅಲ್ಯೂಮಿನಿಯಂ ಆಕ್ಸೈಡ್, ಸತು ಆಕ್ಸೈಡ್ ನಂತಹ ಕೆಲವು ಲೋಹ ಆಕ್ಸೈಡ್ಗಳು ಆಮ್ಲೀಯ ಮತ್ತು ಕ್ಷಾರೀಯ ಎರಡೂ ವರ್ತನೆಯನ್ನು ತೋರಿಸುತ್ತವೆ. ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳು ಎರಡರೊಂದಿಗೂ ಪ್ರತಿಕ್ರಿಯಿಸಿ ಲವಣಗಳು ಮತ್ತು ನೀರನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುವ ಅಂತಹ ಲೋಹ ಆಕ್ಸೈಡ್ಗಳನ್ನು ದ್ವಿಮುಖ ಆಕ್ಸೈಡ್ಗಳು (ಆಂಫೋಟೆರಿಕ್ ಆಕ್ಸೈಡ್ಸ್) ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಅಲ್ಯೂಮಿನಿಯಂ ಆಕ್ಸೈಡ್ ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳೊಂದಿಗೆ ಕೆಳಗಿನ ರೀತಿಯಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
ಹೆಚ್ಚಿನ ಲೋಹ ಆಕ್ಸೈಡ್ಗಳು ನೀರಿನಲ್ಲಿ ಅದ್ರಾವ್ಯವಾಗಿರುತ್ತವೆ ಆದರೆ ಇವುಗಳಲ್ಲಿ ಕೆಲವು ಕ್ಷಾರಗಳನ್ನು ರೂಪಿಸಲು ನೀರಿನಲ್ಲಿ ಕರಗುತ್ತವೆ. ಸೋಡಿಯಂ ಆಕ್ಸೈಡ್ ಮತ್ತು ಪೊಟ್ಯಾಸಿಯಂ ಆಕ್ಸೈಡ್ ನೀರಿನಲ್ಲಿ ಕರಗಿ ಕೆಳಗಿನಂತೆ ಕ್ಷಾರಗಳನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುತ್ತವೆ -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
ಎಲ್ಲಾ ಲೋಹಗಳು ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಒಂದೇ ದರದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುವುದಿಲ್ಲ ಎಂದು ನಾವು ಚಟುವಟಿಕೆ 3.9 ರಲ್ಲಿ ಗಮನಿಸಿದ್ದೇವೆ. ವಿವಿಧ ಲೋಹಗಳು ಆಮ್ಲಜನಕದ ಕಡೆಗೆ ವಿಭಿನ್ನ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಯನ್ನು ತೋರಿಸುತ್ತವೆ. ಪೊಟ್ಯಾಸಿಯಂ ಮತ್ತು ಸೋಡಿಯಂ ನಂತಹ ಲೋಹಗಳು ತೀವ್ರವಾಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ, ಅವುಗಳನ್ನು ಮುಕ್ತವಾಗಿ ಇಟ್ಟರೆ ಬೆಂಕಿ ಹಿಡಿಯುತ್ತವೆ. ಆದ್ದರಿಂದ, ಅವುಗಳನ್ನು ರಕ್ಷಿಸಲು ಮತ್ತು ಆಕಸ್ಮಿಕ ಬೆಂಕಿಯನ್ನು ತಡೆಯಲು, ಅವುಗಳನ್ನು ಮಣ್ಣಿನ ತೈಲದಲ್ಲಿ ಮುಳುಗಿಸಿ ಇಡಲಾಗುತ್ತದೆ. ಸಾಮಾನ್ಯ ತಾಪಮಾನದಲ್ಲಿ, ಮೆಗ್ನೀಶಿಯಂ, ಅಲ್ಯೂಮಿನಿಯಂ, ಸತು, ಸೀಸ, ಇತ್ಯಾದಿ ಲೋಹಗಳ ಮೇಲ್ಮೈಗಳು ತೆಳುವಾದ ಆಕ್ಸೈಡ್ ಪದರದಿಂದ ಆವರಿಸಲ್ಪಟ್ಟಿರುತ್ತವೆ. ರಕ್ಷಣಾತ್ಮಕ ಆಕ್ಸೈಡ್ ಪದರವು ಲೋಹವನ್ನು ಮತ್ತಷ್ಟು ಉತ್ಕರ್ಷಣದಿಂದ ರಕ್ಷಿಸುತ್ತದೆ. ಕಬ್ಬಿಣವು ಬಿಸಿ ಮಾಡಿದಾಗ ಉರಿಯುವುದಿಲ್ಲ ಆದರೆ ಕಬ್ಬಿಣದ ಹುಡಿಯನ್ನು ಬರ್ನರ್ನ ಜ್ವಾಲೆಯಲ್ಲಿ ಚೆಲ್ಲಿದಾಗ ತೀವ್ರವಾಗಿ ಉರಿಯುತ್ತದೆ. ತಾಮ್ರವು ಉರಿಯುವುದಿಲ್ಲ, ಆದರೆ ಬಿಸಿ ಲೋಹವು ತಾಮ್ರ(II) ಆಕ್ಸೈಡ್ನ ಕಪ್ಪು ಬಣ್ಣದ ಪದರದಿಂದ ಲೇಪಿತವಾಗಿರುತ್ತದೆ. ಬೆಳ್ಳಿ ಮತ್ತು ಚಿನ್ನವು ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲೂ ಸಹ ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುವುದಿಲ್ಲ.
ನಿಮಗೆ ತಿಳಿದಿದೆಯೇ?
ಅಲ್ಯೂಮಿನಿಯಂನ ದಪ್ಪ ಆಕ್ಸೈಡ್ ಪದರವನ್ನು ರೂಪಿಸುವ ಪ್ರಕ್ರಿಯೆಯೇ ಅನೋಡೈಸಿಂಗ್. ಅಲ್ಯೂಮಿನಿಯಂ ಗಾಳಿಗೆ ಒಡ್ಡಿಕೊಂಡಾಗ ತೆಳುವಾದ ಆಕ್ಸೈಡ್ ಪದರವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸುತ್ತದೆ. ಈ ಅಲ್ಯೂಮಿನಿಯಂ ಆಕ್ಸೈಡ್ ಲೇಪನವು ಅದನ್ನು ಮತ್ತಷ್ಟು ತುಕ್ಕು ಹಿಡಿಯುವುದರಿಂದ ರಕ್ಷಿಸುತ್ತದೆ. ಆಕ್ಸೈಡ್ ಪದರವನ್ನು ದಪ್ಪಗಾಗಿಸುವ ಮೂಲಕ ಪ್ರತಿರೋಧವನ್ನು ಮತ್ತಷ್ಟು ಸುಧಾರಿಸಬಹುದು. ಅನೋಡೈಸಿಂಗ್ ಸಮಯದಲ್ಲಿ, ಶುದ್ಧ ಅಲ್ಯೂಮಿನಿಯಂ ವಸ್ತುವನ್ನು ಆನೋಡ್ ಆಗಿ ಮಾಡಲಾಗುತ್ತದೆ ಮತ್ತು ದುರ್ಬಲ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದೊಂದಿಗೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದನೆ ಮಾಡಲಾಗುತ್ತದೆ. ಆನೋಡ್ನಲ್ಲಿ ಬಿಡುಗಡೆಯಾದ ಆಮ್ಲಜನಕ ಅನಿಲ ಅಲ್ಯೂಮಿನಿಯಂನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಯಿಸಿ ದಪ್ಪ ರಕ್ಷಣಾತ್ಮಕ ಆಕ್ಸೈಡ್ ಪದರವನ್ನು ಮಾಡುತ್ತದೆ. ಈ ಆಕ್ಸೈಡ್ ಪದರವನ್ನು ಸುಲಭವಾಗಿ ಬಣ್ಣ ಹಾಕಬಹುದು, ಇದು ಅಲ್ಯೂಮಿನಿಯಂ ವಸ್ತುಗಳಿಗೆ ಆಕರ್ಷಕ ಮುಕ್ತಾಯವನ್ನು ನೀಡುತ್ತದೆ.
ಚಟುವಟಿಕೆ 3.9 ಅನ್ನು ನಡೆಸಿದ ನಂತರ, ಇಲ್ಲಿ ತೆಗೆದುಕೊಂಡ ಲೋಹಗಳ ಮಾದರಿಗಳಲ್ಲಿ ಸೋಡಿಯಂ ಅತ್ಯಂತ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕವಾಗಿದೆ ಎಂದು ನೀವು ಗಮನಿಸಿರಬೇಕು. ಮೆಗ್ನೀಶಿಯಂನ ಪ್ರತಿಕ್ರಿಯೆಯು ಕಡಿಮೆ ತೀವ್ರವಾಗಿರುತ್ತದೆ, ಇದು ಅದು ಸೋಡಿಯಂನಷ್ಟು ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕವಾಗಿಲ್ಲ ಎಂದು ಸೂಚಿಸುತ್ತದೆ. ಆದರೆ ಆಮ್ಲಜನಕದಲ್ಲಿ ಸುಡುವುದು ಸತು, ಕಬ್ಬಿಣ, ತಾಮ್ರ ಅಥವಾ ಸೀಸದ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಯ ಕ್ರಮದ ಬಗ್ಗೆ ನಿರ್ಧರಿಸಲು ನಮಗೆ ಸಹಾಯ ಮಾಡುವುದಿಲ್ಲ. ಈ ಲೋಹಗಳ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಯ ಕ್ರಮದ ಬಗ್ಗೆ ತೀರ್ಮಾನಕ್ಕೆ ಬರಲು ಇನ್ನೂ ಕೆಲವು ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ನೋಡೋಣ.
3.2.2 ಲೋಹಗಳು ನೀರಿನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸಿದಾಗ ಏನಾಗುತ್ತದೆ?
ಚಟುವಟಿಕೆ 3.10
ಎಚ್ಚರಿಕೆ: ಈ ಚಟುವಟಿಕೆಗೆ ಶಿಕ್ಷಕರ ಸಹಾಯ ಅಗತ್ಯವಿದೆ.
- ಚಟುವಟಿಕೆ 3.9 ರಲ್ಲಿರುವಂತೆಯೇ ಲೋಹಗಳ ಮಾದರಿಗಳನ್ನು ಸಂಗ್ರಹಿಸಿ.
- ಮಾದರಿಗಳ ಸಣ್ಣ ತುಂಡುಗಳನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ಅರ್ಧ ನೀರು ತುಂಬಿದ ಬೀಕರ್ಗಳಲ್ಲಿ ಇರಿಸಿ.
- ಯಾವ ಲೋಹಗಳು ತಣ್ಣನೆಯ ನೀರಿನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸಿದವು? ತಣ್ಣನೆಯ ನೀರಿನೊಂದಿಗೆ ಅವುಗಳ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಯ ಹೆಚ್ಚುತ್ತಿರುವ ಕ್ರ











