অধ্যায় ০৩ ধাতু আৰু অধাতু
নৱম শ্ৰেণীত তুমি বিভিন্ন মৌলৰ বিষয়ে শিকিছা। তুমি দেখিছা যে মৌলবোৰক তেওঁলোকৰ ধৰ্মৰ ওপৰত ভিত্তি কৰি ধাতু বা অধাতু হিচাপে শ্ৰেণীবিভাজন কৰিব পাৰি।
- তোমাৰ দৈনন্দিন জীৱনত ব্যৱহাৰ হোৱা কিছুমান ধাতু আৰু অধাতুৰ ব্যৱহাৰৰ কথা ভাবা।
- মৌলবোৰক ধাতু বা অধাতু হিচাপে শ্ৰেণীবিভাজন কৰোঁতে তুমি কি ধৰ্মবোৰৰ কথা ভাবিছিলা?
- এই ধৰ্মবোৰ মৌলবোৰৰ ব্যৱহাৰৰ সৈতে কেনেদৰে সম্পৰ্কিত?
আহা আমি এই ধৰ্মবোৰৰ কিছু বিস্তাৰিতভাৱে চাওঁ।
৩.১ ভৌতিক ধৰ্ম
৩.১.১ ধাতু
পদাৰ্থবোৰক শ্ৰেণীবিভাজন কৰিবলৈ আৰম্ভ কৰাৰ সবাতোকৈ সহজ উপায় হ’ল তেওঁলোকৰ ভৌতিক ধৰ্মবোৰ তুলনা কৰা। আহা আমি নিম্নলিখিত কাৰ্যকলাপবোৰৰ সহায়ত ইয়াক অধ্যয়ন কৰোঁ। ৩.১ ৰ পৰা ৩.৬ লৈ কাৰ্যকলাপবোৰ সম্পাদন কৰিবলৈ, নিম্নলিখিত ধাতুবোৰৰ নমুনা সংগ্ৰহ কৰা - লো, তাম, এলুমিনিয়াম, মেগনেছিয়াম, ছডিয়াম, সীহ, জিংক আৰু অন্যান্য সহজলভ্য ধাতু।
কাৰ্যকলাপ ৩.১
- লো, তাম, এলুমিনিয়াম আৰু মেগনেছিয়ামৰ নমুনা লোৱা। প্ৰতিটো নমুনাৰ ৰূপ লক্ষ্য কৰা।
- বালি কাগজেৰে ঘঁহি প্ৰতিটো নমুনাৰ পৃষ্ঠ পৰিষ্কাৰ কৰা আৰু আকৌ তেওঁলোকৰ ৰূপ লক্ষ্য কৰা।
ধাতুবোৰ, তেওঁলোকৰ বিশুদ্ধ অৱস্থাত, এখন উজ্জ্বল পৃষ্ঠ থাকে। এই ধৰ্মটোক ধাতৱীয় দীপ্তি বোলে।
কাৰ্যকলাপ ৩.২
লো, তাম, এলুমিনিয়াম, আৰু মেগনেছিয়ামৰ সৰু টুকুৰাবোৰ লোৱা। এই ধাতুবোৰক চোকা চাকুৰে কাটিবলৈ চেষ্টা কৰা আৰু তোমাৰ পৰ্যবেক্ষণবোৰ টোকা কৰা।
এযোৰ চিমটীৰে ছডিয়াম ধাতুৰ এটা টুকুৰা ধৰা।
সতৰ্কতা: সদায় সাৱধানতাৰে ছডিয়াম ধাতু ব্যৱহাৰ কৰিবা। ফিল্টাৰ কাগজৰ ভাঁজৰ মাজত হেঁচি শুকুৱাই ল’বাহঁক।
ইয়াক ৱাচ-গ্লাছ এখনত ৰাখি চাকুৰে কাটিবলৈ চেষ্টা কৰা।
তুমি কি লক্ষ্য কৰিলা?
তুমি দেখিবা যে ধাতুবোৰ সাধাৰণতে কঠিন। কঠিনতা ধাতু অনুসৰি ভিন্ন হয়।
কাৰ্যকলাপ ৩.৩
- লো, জিংক, সীহ আৰু তামৰ টুকুৰাবোৰ লোৱা।
- যিকোনো এটা ধাতু লোৰ এটা ব্লকৰ ওপৰত ৰাখি হাতুৰীৰে চাৰি বা পাঁচবাৰ কোবাই দিয়া। তুমি কি লক্ষ্য কৰা?
- অন্যান্য ধাতুৰ সৈতে পুনৰাবৃত্তি কৰা।
- এই ধাতুবোৰৰ আকৃতিৰ পৰিৱৰ্তনবোৰ ৰেকৰ্ড কৰা।
তুমি দেখিবা যে কিছুমান ধাতু পাতল তৰপলৈ কোবাই দিয়াৰ যোগ্য। এই ধৰ্মটোক নমনীয়তা বোলে। তুমি জানানে যে সোণ আৰু ৰূপ আটাইতকৈ নমনীয় ধাতু?
কাৰ্যকলাপ ৩.৪
- দৈনন্দিন জীৱনত তুমি দেখা ধাতুৰ তাঁৰবোৰৰ তালিকা কৰা।
ধাতুবোৰৰ পাতল তাঁৰলৈ টানি অনাৰ ক্ষমতাক নমনীয়তা বোলে। সোণ আটাইতকৈ নমনীয় ধাতু। তুমি জানি আচৰিত হ’বা যে এগ্ৰাম সোণৰ পৰা প্ৰায় $2 km$ দৈৰ্ঘ্যৰ তাঁৰ এডাল টানি উলিয়াব পাৰি।
ইয়াৰ নমনীয়তা আৰু নমনীয়তাৰ বাবেই ধাতুবোৰক আমাৰ প্ৰয়োজন অনুসৰি বিভিন্ন আকৃতি দিব পাৰি।
তুমি কিছুমান ধাতুৰ নাম কব পাৰানে যিবোৰ ৰান্ধনী পাত্ৰ তৈয়াৰ কৰিবলৈ ব্যৱহাৰ কৰা হয়? তুমি জানানে কিয় এই ধাতুবোৰ পাত্ৰ তৈয়াৰ কৰিবলৈ ব্যৱহাৰ কৰা হয়? উত্তৰটো উলিয়াবলৈ আহা আমি নিম্নলিখিত কাৰ্যকলাপটো কৰোঁ।
কাৰ্যকলাপ ৩.৫
- এডাল এলুমিনিয়াম বা তামৰ তাঁৰ লোৱা। চিত্ৰ ৩.১ ত দেখুওৱাৰ দৰে ষ্টেণ্ড এখনত এই তাঁৰডাল ক্লেম্প কৰা।
- মোমৰ সহায়ত মুক্ত মূৰটোত এটা পিন ফিক্স কৰা।
- য’ত ইয়াক ক্লেম্প কৰা হৈছে, তাত ওচৰত স্পিৰিট লেম্প, মমবাতি বা বাৰ্ণাৰৰে তাঁৰডাল তপতাওৱা।
- কিছু সময়ৰ পিছত তুমি কি লক্ষ্য কৰা?
- তোমাৰ পৰ্যবেক্ষণবোৰ টোকা কৰা। ধাতুৰ তাঁৰডাল গলেনে?
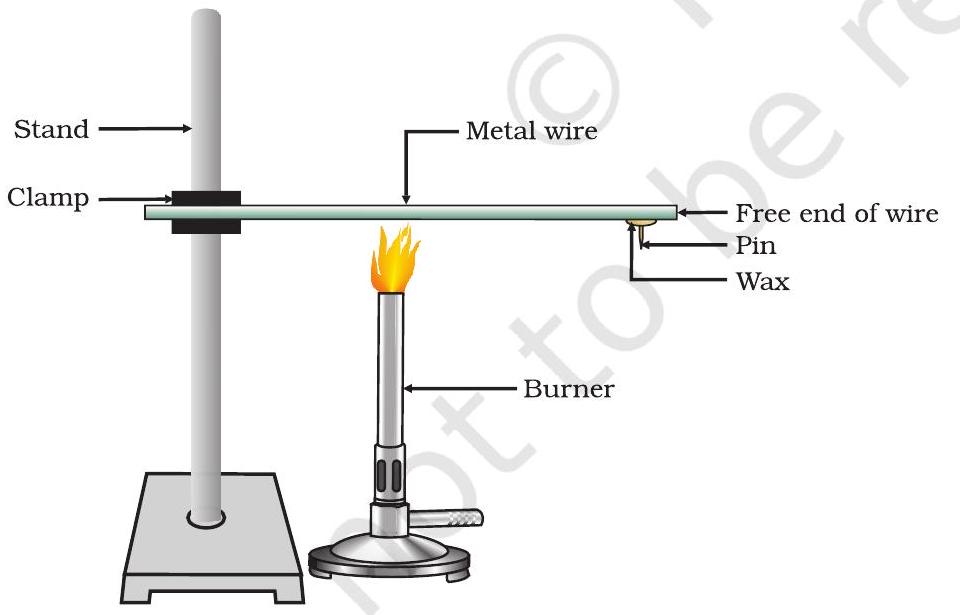
চিত্ৰ ৩.১ ধাতুবোৰ তাপৰ সুপৰিবাহী।
ওপৰৰ কাৰ্যকলাপটোৱে দেখুৱায় যে ধাতুবোৰ তাপৰ সুপৰিবাহী আৰু উচ্চ গলনাংক থাকে। তাপৰ শ্ৰেষ্ঠ পৰিবাহী হ’ল ৰূপ আৰু তাম। সীহ আৰু পাৰা তুলনামূলকভাৱে তাপৰ দুৰ্বল পৰিবাহী।
ধাতুবোৰয়ে বিদ্যুৎ পৰিবাহী নেকি? আহা আমি উলিয়াওঁ।
কাৰ্যকলাপ ৩.৬
- চিত্ৰ ৩.২ ত দেখুওৱাৰ দৰে এটা বৈদ্যুতিক বৰ্তনী স্থাপন কৰা।
- পৰীক্ষা কৰিবলগীয়া ধাতুটো $A$ আৰু $B$ ৰ মাজত বৰ্তনীত দেখুওৱাৰ দৰে ৰাখা।
- বাল্বটো জ্বলেনে? ইয়ে কি সূচায়?
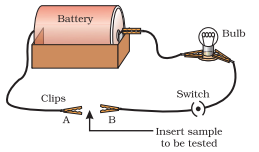
চিত্ৰ ৩.২ ধাতুবোৰ বিদ্যুৎৰ সুপৰিবাহী।
তুমি নিশ্চয় দেখিছা যে তোমাৰ ঘৰত বিদ্যুৎ পৰিবহণ কৰা তাঁৰবোৰত পলিভিনাইল ক্ল’ৰাইড (PVC) বা ৰবৰৰ দৰে পদাৰ্থৰ প্ৰলেপ থাকে। কিয় বৈদ্যুতিক তাঁৰবোৰ এনে পদাৰ্থৰে প্ৰলেপ দিয়া হয়?
ধাতুবোৰে কঠিন পৃষ্ঠত আঘাত কৰিলে কি হয়? সিহঁতে শব্দ উৎপন্ন কৰেনে? কঠিন পৃষ্ঠত আঘাত কৰিলে শব্দ উৎপন্ন কৰা ধাতুবোৰক ধ্বনিত বুলি কোৱা হয়। তুমি এতিয়া ক’ব পাৰানে কিয় স্কুলৰ ঘণ্টাবোৰ ধাতুৰে তৈয়াৰ কৰা হয়?
৩.১.২ অধাতু
পূৰ্বৰ শ্ৰেণীত তুমি শিকিছা যে ধাতুৰ তুলনাত অধাতুৰ সংখ্যা খুব কম। অধাতুৰ কিছুমান উদাহৰণ হ’ল কাৰ্বন, গন্ধক, আয়’ডিন, অক্সিজেন, হাইড্ৰজেন ইত্যাদি। অধাতুবোৰ হয় কঠিন নহয় গেছ, ব্ৰ’মিন বাদ দি যিটো এটা তৰল পদাৰ্থ।
অধাতুবোৰৰো ধাতুৰ দৰে ভৌতিক ধৰ্ম আছে নেকি? আহা আমি উলিয়াওঁ।
কাৰ্যকলাপ ৩.৭
- কাৰ্বন (কয়লা বা গ্ৰেফাইট), গন্ধক আৰু আয়’ডিনৰ নমুনা সংগ্ৰহ কৰা।
- এই অধাতুবোৰৰ সৈতে কাৰ্যকলাপ ৩.১ ৰ পৰা ৩.৪ আৰু ৩.৬ সম্পাদন কৰা আৰু তোমাৰ পৰ্যবেক্ষণবোৰ ৰেকৰ্ড কৰা।
ধাতু আৰু অধাতু সম্পৰ্কীয় তোমাৰ পৰ্যবেক্ষণবোৰ তালিকা ৩.১ ত সংকলন কৰা।
তালিকা ৩.১
| মৌল | চিহ্ন | পৃষ্ঠৰ প্ৰকাৰ | কঠিনতা | নমনীয়তা | নমনীয়তা | বিদ্যুৎ পৰিবাহীতা | ধ্বনিত |
|---|---|---|---|---|---|---|---|
তালিকা ৩.১ ত ৰেকৰ্ড কৰা পৰ্যবেক্ষণবোৰৰ ভিত্তিত, শ্ৰেণীত ধাতু আৰু অধাতুৰ সাধাৰণ ভৌতিক ধৰ্মবোৰ আলোচনা কৰা। তুমি নিশ্চয় এই সিদ্ধান্তত উপনীত হৈছা যে আমি মৌলবোৰক কেৱল তেওঁলোকৰ ভৌতিক ধৰ্মৰ ওপৰত ভিত্তি কৰি শ্ৰেণীবিভাজন কৰিব নোৱাৰোঁ, কাৰণ বহুতো ব্যতিক্ৰম আছে। উদাহৰণস্বৰূপে -
(i) পাৰা বাদ দি সকলো ধাতুৱে কোঠাৰ উষ্ণতাত কঠিন হিচাপে থাকে। কাৰ্যকলাপ ৩.৫ ত, তুমি লক্ষ্য কৰিছা যে ধাতুবোৰৰ উচ্চ গলনাংক থাকে কিন্তু গেলিয়াম আৰু ছিজিয়ামৰ খুব কম গলনাংক থাকে। এই দুটা ধাতু তোমাৰ হাতৰ তলুৱাত ৰাখিলে গলি যাব।
(ii) আয়’ডিন এটা অধাতু কিন্তু ইয়াৰ দীপ্তি আছে।
(iii) কাৰ্বন এটা অধাতু যি বিভিন্ন ৰূপত থাকিব পাৰে। প্ৰতিটো ৰূপক এটা অ্যাল’ট্ৰপ বোলে। হীৰা, কাৰ্বনৰ এটা অ্যাল’ট্ৰপ, আটাইতকৈ কঠিন প্ৰাকৃতিক পদাৰ্থ বুলি জনা যায় আৰু ইয়াৰ খুব উচ্চ গলনাংক আৰু উতলাংক থাকে। গ্ৰেফাইট, কাৰ্বনৰ আন এটা অ্যাল’ট্ৰপ, বিদ্যুৎৰ পৰিবাহী।
(iv) ক্ষাৰ ধাতুবোৰ (লিথিয়াম, ছডিয়াম, পটেছিয়াম) ইমান কোমল যে চাকুৰে কাটিব পাৰি। তেওঁলোকৰ কম ঘনত্ব আৰু কম গলনাংক থাকে।
মৌলবোৰক তেওঁলোকৰ ৰাসায়নিক ধৰ্মৰ ভিত্তিত অধিক স্পষ্টভাৱে ধাতু আৰু অধাতু হিচাপে শ্ৰেণীবিভাজন কৰিব পাৰি।
কাৰ্যকলাপ ৩.৮
- এডাল মেগনেছিয়াম ৰিবন আৰু কিছু গন্ধক গুড়ি লোৱা।
- মেগনেছিয়াম ৰিবনডাল জ্বলোৱা। গঠিত ছাইবোৰ সংগ্ৰহ কৰি পানীত দ্ৰৱীভূত কৰা।
- ফলিত দ্ৰৱটো ৰঙা আৰু নীলা লিটমাছ কাগজ দুয়োটোৰে সৈতে পৰীক্ষা কৰা।
- মেগনেছিয়াম জ্বলোৱাত গঠিত উৎপাদটো আম্লিক নে ক্ষাৰকীয়?
- এতিয়া গন্ধক গুড়ি জ্বলোৱা। উৎপন্ন হোৱা ধোঁৱা সংগ্ৰহ কৰিবলৈ জ্বলি থকা গন্ধকৰ ওপৰত এটা টেষ্ট টিউব ৰাখা।
- ওপৰৰ টেষ্ট টিউবটোত কিছু পানী যোগ কৰি জোকাৰি দিয়া।
- নীলা আৰু ৰঙা লিটমাছ কাগজৰ সৈতে এই দ্ৰৱটো পৰীক্ষা কৰা।
- গন্ধক জ্বলোৱাত গঠিত উৎপাদটো আম্লিক নে ক্ষাৰকীয়?
- তুমি এই বিক্ৰিয়াবোৰৰ সমীকৰণবোৰ লিখিব পাৰানে?
বেছিভাগ অধাতুৱে পানীত দ্ৰৱীভূত হ’লে আম্লিক অক্সাইড উৎপন্ন কৰে। আনহাতে, বেছিভাগ ধাতুৱে ক্ষাৰকীয় অক্সাইড দিয়ে। তুমি পৰৱৰ্তী অংশত এই ধাতৱীয় অক্সাইডবোৰৰ বিষয়ে অধিক শিকিবা।
৩.২ ধাতুৰ ৰাসায়নিক ধৰ্ম
আমি ধাতুৰ ৰাসায়নিক ধৰ্মবোৰ ৩.২.১ ৰ পৰা ৩.২.৪ লৈ অংশবোৰত শিকিম। ইয়াৰ বাবে, নিম্নলিখিত ধাতুবোৰৰ নমুনা সংগ্ৰহ কৰা - এলুমিনিয়াম, তাম, লো, সীহ, মেগনেছিয়াম, জিংক আৰু ছডিয়াম।
৩.২.১ ধাতুবোৰ বায়ুত দহন কৰিলে কি হয়?
তুমি কাৰ্যকলাপ ৩.৮ ত দেখিছা যে মেগনেছিয়ামে বায়ুত উজ্জ্বল বগা শিখাৰে জ্বলে। সকলো ধাতুৱে একে ধৰণে বিক্ৰিয়া কৰেনে? আহা আমি নিম্নলিখিত কাৰ্যকলাপটো সম্পাদন কৰি পৰীক্ষা কৰোঁ।
কাৰ্যকলাপ ৩.৯
সতৰ্কতা: নিম্নলিখিত কাৰ্যকলাপটো শিক্ষকৰ সহায়ৰ প্ৰয়োজন। ছাত্ৰ-ছাত্ৰীয়ে চকুৰ সুৰক্ষা ব্যৱহাৰ কৰিলে ভাল হয়।
- ওপৰত লোৱা যিকোনো নমুনা এটা চিমটীৰে ধৰি জুইৰ শিখাৰ ওপৰত জ্বলাবলৈ চেষ্টা কৰা। অন্যান্য ধাতুৰ নমুনাবোৰৰ সৈতে পুনৰাবৃত্তি কৰা।
- গঠিত হ’লে উৎপাদটো সংগ্ৰহ কৰা।
- উৎপাদবোৰ আৰু ধাতুৰ পৃষ্ঠ ঠাণ্ডা হ’বলৈ দিয়া।
- কোনবোৰ ধাতু সহজে জ্বলে?
- ধাতুটো জ্বলোঁতে তুমি কি ৰঙৰ শিখা লক্ষ্য কৰিলা?
- জ্বলোৱাৰ পিছত ধাতুৰ পৃষ্ঠ কেনে দেখা যায়?
- অক্সিজেনৰ প্ৰতি তেওঁলোকৰ সক্ৰিয়তাৰ ক্ৰমত ধাতুবোৰক ঊৰ্ধ্বক্ৰমত সজোৱা।
- উৎপাদবোৰ পানীত দ্ৰৱণীয় নেকি?
প্ৰায় সকলো ধাতুৱে অক্সিজেনৰ সৈতে সংযুক্ত হৈ ধাতৱীয় অক্সাইড গঠন কৰে।
ধাতু + অক্সিজেন $\rightarrow$ ধাতৱীয় অক্সাইড
উদাহৰণস্বৰূপে, যেতিয়া তামক বায়ুত তপতোৱা হয়, ই অক্সিজেনৰ সৈতে সংযুক্ত হৈ কপাৰ(II) অক্সাইড, এটা ক’লা অক্সাইড গঠন কৰে।
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
একেদৰে, এলুমিনিয়ামে এলুমিনিয়াম অক্সাইড গঠন কৰে।
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
অধ্যায় ২ ৰ পৰা মনত পেলোৱা, কেনেদৰে কপাৰ অক্সাইডে হাইড্ৰক্ল’ৰিক এছিডৰ সৈতে বিক্ৰিয়া কৰে। আমি শিকিছো যে ধাতৱীয় অক্সাইডবোৰ প্ৰকৃতিত ক্ষাৰকীয়। কিন্তু কিছুমান ধাতৱীয় অক্সাইড, যেনে এলুমিনিয়াম অক্সাইড, জিংক অক্সাইডে আম্লিক আৰু ক্ষাৰকীয় উভয় আচৰণ দেখুৱায়। এনে ধাতৱীয় অক্সাইডবোৰ যিবোৰে এছিড আৰু ক্ষাৰক উভয়ৰে সৈতে বিক্ৰিয়া কৰি লৱণ আৰু পানী উৎপন্ন কৰে তাক উভধৰ্মী অক্সাইড বোলে। এলুমিনিয়াম অক্সাইডে নিম্নলিখিত ধৰণে এছিড আৰু ক্ষাৰকৰ সৈতে বিক্ৰিয়া কৰে -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
বেছিভাগ ধাতৱীয় অক্সাইড পানীত অদ্ৰৱণীয় কিন্তু ইয়াৰ কিছুমান পানীত দ্ৰৱীভূত হৈ ক্ষাৰক গঠন কৰে। ছডিয়াম অক্সাইড আৰু পটেছিয়াম অক্সাইড পানীত দ্ৰৱীভূত হৈ নিম্নলিখিত ধৰণে ক্ষাৰক উৎপন্ন কৰে -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
আমি কাৰ্যকলাপ ৩.৯ ত লক্ষ্য কৰিছো যে সকলো ধাতুৱে একে হাৰত অক্সিজেনৰ সৈতে বিক্ৰিয়া নকৰে। বিভিন্ন ধাতুৱে অক্সিজেনৰ প্ৰতি বিভিন্ন সক্ৰিয়তা দেখুৱায়। পটেছিয়াম আৰু ছডিয়ামৰ দৰে ধাতুবোৰ ইমান জোৰেৰে বিক্ৰিয়া কৰে যে মুক্তভাৱে ৰাখিলে জ্বলি উঠে। সেয়েহে, তেওঁলোকক সুৰক্ষিত কৰিবলৈ আৰু আকস্মিক জুইৰ পৰা ৰক্ষা কৰিবলৈ, তেওঁলোকক কেৰাচিন তেলত ডুবাই ৰখা হয়। সাধাৰণ উষ্ণতাত, মেগনেছিয়াম, এলুমিনিয়াম, জিংক, সীহ আদি ধাতুবোৰৰ পৃষ্ঠ অক্সাইডৰ পাতল তৰপেৰে আবৃত থাকে। সুৰক্ষামূলক অক্সাইড তৰপটোৱে ধাতুটোক পৰৱৰ্তী অক্সিডেচনৰ পৰা ৰক্ষা কৰে। লোৱে তপতালে জ্বলি নাযায় কিন্তু লোৰ গুড়িবোৰ বাৰ্ণাৰৰ শিখাত ছটিয়াই দিলে জোৰেৰে জ্বলে। তাম জ্বলি নাযায়, কিন্তু তপত ধাতুটো কপাৰ(II) অক্সাইডৰ ক’লা ৰঙৰ তৰপেৰে আবৃত হয়। ৰূপ আৰু সোণে উচ্চ উষ্ণতাতো অক্সিজেনৰ সৈতে বিক্ৰিয়া নকৰে।
তুমি জানানে?
এন’ডাইজিং হ’ল এলুমিনিয়ামৰ ডাঠ অক্সাইড তৰপ গঠন কৰাৰ প্ৰক্ৰিয়া। এলুমিনিয়াম বায়ুত উন্মুক্ত হ’লে এটা পাতল অক্সাইড তৰপ গঠন কৰে। এই এলুমিনিয়াম অক্সাইডৰ প্ৰলেপে ইয়াক পৰৱৰ্তী ক্ষয়ৰ পৰা ৰোধ কৰে। অক্সাইড তৰপটো ডাঠ কৰি ইয়াৰ ৰোধকতা আৰু উন্নত কৰিব পাৰি। এন’ডাইজিং কৰোঁতে, এটা পৰিষ্কাৰ এলুমিনিয়াম বস্তুক এন’ড হিচাপে তৈয়াৰ কৰা হয় আৰু তাক পাতল গন্ধকীয় এছিডৰ সৈতে বিদ্যুৎ বিশ্লেষণ কৰা হয়। এন’ডত বিকশিত হোৱা অক্সিজেন গেছ এলুমিনিয়ামৰ সৈতে বিক্ৰিয়া কৰি এটা ডাঠ সুৰক্ষামূলক অক্সাইড তৰপ তৈয়াৰ কৰে। এই অক্সাইড তৰপটো সহজে ৰং কৰিব পাৰি যাতে এলুমিনিয়ামৰ বস্তুবোৰক আকৰ্ষণীয় সমাপ্তি দিব পাৰি।
কাৰ্যকলাপ ৩.৯ সম্পাদন কৰাৰ পিছত, তুমি নিশ্চয় লক্ষ্য কৰিছা যে ইয়াত লোৱা ধাতুৰ নমুনাবোৰৰ ভিতৰত ছডিয়াম আটাইতকৈ সক্ৰিয়। মেগনেছিয়ামৰ বিক্ৰিয়া কম জোৰদাৰ, ইয়াৰ অৰ্থ হ’ল ই ছডিয়ামৰ দৰে সক্ৰিয় নহয়। কিন্তু অক্সিজেনত দহন কৰিলে জিংক, লো, তাম বা সীহৰ সক্ৰিয়তাৰ বিষয়ে সিদ্ধান্ত ল’বলৈ আমাক সহায় নকৰে। আহা আমি এই ধাতুবোৰৰ সক্ৰিয়তাৰ ক্ৰমৰ বিষয়ে সিদ্ধান্তত উপনীত হ’বলৈ আৰু কিছুমান বিক্ৰিয়া চাওঁ।
৩.২.২ ধাতুবোৰ পানীৰ সৈতে বিক্ৰিয়া কৰিলে কি হয়?
কাৰ্যকলাপ ৩.১০
সতৰ্কতা: এই কাৰ্যকলাপটো শিক্ষকৰ সহায়ৰ প্ৰয়োজন।
- কাৰ্যকলাপ ৩.৯ ৰ দৰে একে ধাতুবোৰৰ নমুনা সংগ্ৰহ কৰা।
- নমুনাবোৰৰ সৰু টুকুৰাবোৰ পৃথককৈ ঠাণ্ডা পানীৰে আধা ভৰ্তি বীকাৰত ৰাখা।
- কোনবোৰ ধাতুৱে ঠাণ্ডা পানীৰ সৈতে বিক্ৰিয়া কৰিলে? ঠাণ্ডা পানীৰ সৈতে তেওঁলোকৰ সক্ৰিয়তাৰ ঊৰ্ধ্বক্ৰমত সজোৱা।
- কোনোবা ধাতুৱে পানীত জুই উৎপন্ন কৰিলেনে?
- কিছু সময়ৰ পিছত কোনোবা ধাতু ওপঙিবলৈ আৰম্ভ কৰেনে?
- যিবোৰ ধাতুৱে ঠাণ্ডা পানীৰ সৈতে বিক্ৰিয়া নকৰিলে, সেইবোৰ গৰম পানীৰে আধা ভৰ্তি বীকাৰত ৰাখা।
- যিবোৰ ধাতুৱে গৰম পানীৰ সৈতেও বিক্ৰিয়া নকৰিলে, চিত্ৰ ৩.৩ ত দেখুওৱাৰ দৰে সঁজুলি স্থাপন কৰি বাষ্পৰ সৈতে তেওঁলোকৰ বিক্ৰিয়া লক্ষ্য কৰা।
- কোনবোৰ ধাতুৱে বাষ্পৰ সৈতেও বিক্ৰিয়া নকৰিলে?
- পানীৰ সৈতে সক্ৰিয়তাৰ ক্ৰমত ধাতুবোৰক ঊৰ্ধ্বক্ৰমত সজোৱা।
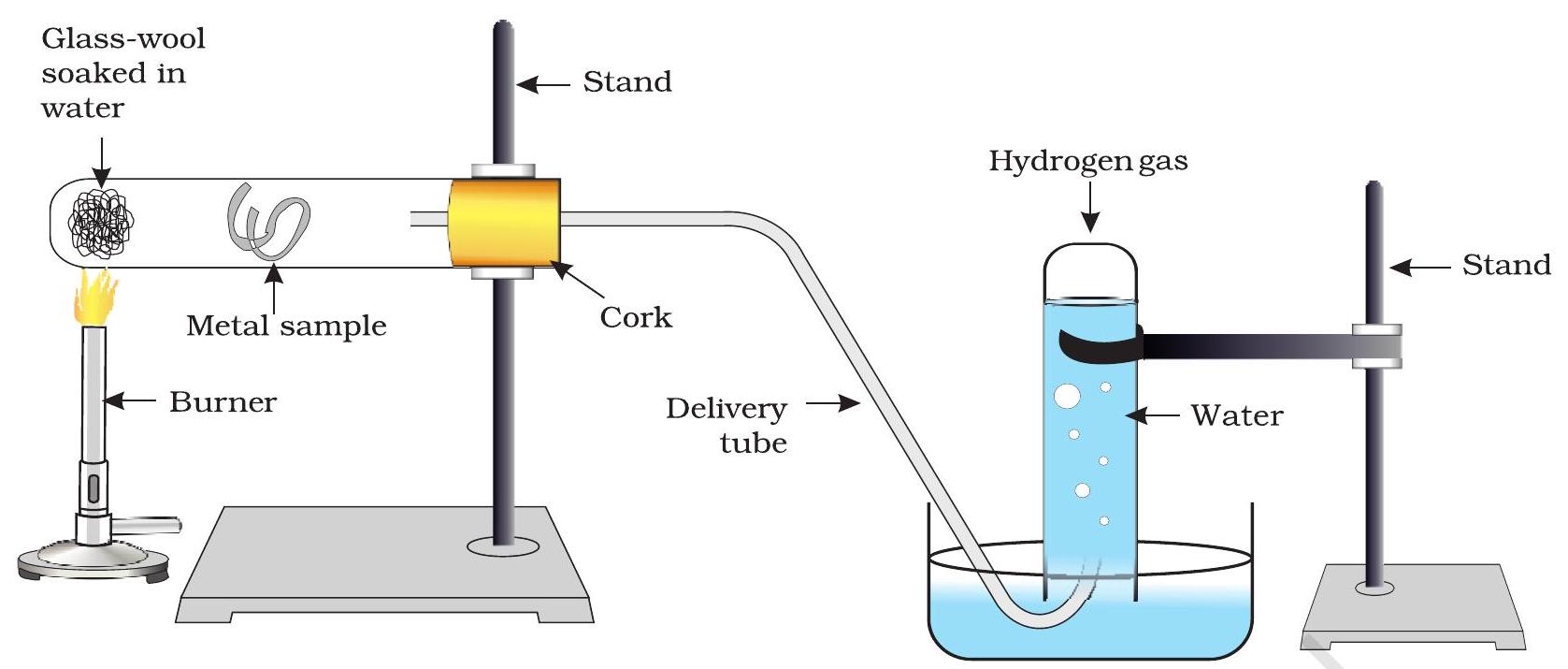
চিত্ৰ ৩.৩ ধাতু এটাত বাষ্পৰ ক্ৰিয়া
ধাতুবোৰে পানীৰ সৈতে বিক্ৰিয়া কৰি ধাতৱীয় অক্সাইড আৰু হাইড্ৰজেন গেছ উৎপন্ন কৰে। পানীত দ্ৰৱণীয় ধাতৱীয় অক্সাইডবোৰ পানীত দ্ৰৱীভূত হৈ পৰৱৰ্তী ধাতৱীয় হাইড্ৰক্সাইড গঠন কৰে। কিন্তু সকলো ধাতুৱে পানীৰ সৈতে বিক্ৰিয়া নকৰে।
ধাতু + পানী $\rightarrow$ ধাতৱীয় অক্সাইড + হাইড্ৰজেন
ধাতৱীয় অক্সাইড + পানী $ \rightarrow $ ধাতৱীয় হাইড্ৰক্সাইড
পটেছিয়াম আৰু ছডিয়ামৰ দৰে ধাতুবোৰে ঠাণ্ডা পানীৰ সৈতে জোৰেৰে বিক্ৰিয়া কৰে। ছডিয়াম আৰু পটেছিয়ামৰ ক্ষেত্ৰত, বিক্ৰিয়াটো ইমান জোৰদাৰ আৰু উষ্মাক্ষেপী যে বিকশিত হাইড্ৰজেন তৎক্ষণাত জ্বলি উঠে।
$ \begin{aligned} & 2 K(s)+2 H_2 O(l) \to 2 KOH(aq)+H_2(g)+\text{ তাপ শক্তি } \\ & 2 Na(s)+2 H_2 O(l) \to 2 NaOH(aq)+H_2(g)+\text{ তাপ শক্তি } \end{aligned} $
কেলছিয়ামৰ পানীৰ সৈতে বিক্ৰিয়া কম জোৰদাৰ। বিকশিত তাপ হাইড্ৰজেনৰ জ্বলি উঠাৰ বাবে পৰ্যাপ্ত নহয়।
$Ca(s)+2 H_2 O(l) \to Ca(OH)_2(aq)+H_2(g)$
হাইড্ৰজেন গেছৰ বুদবুদবোৰ ধাতুৰ পৃষ্ঠত লাগি ধৰাৰ বাবে কেলছিয়াম ওপঙিবলৈ আৰম্ভ কৰে।
মেগনেছিয়ামে ঠাণ্ডা পানীৰ সৈতে বিক্ৰিয়া নকৰে। ই গৰম পানীৰ সৈতে বিক্ৰিয়া কৰি মেগনেছিয়াম হাইড্ৰক্সাইড আৰু হাইড্ৰজেন গঠন কৰে। ইয়াৰ পৃষ্ঠত লাগি ধৰা হাইড্ৰজেন গেছৰ বুদবুদবোৰৰ বাবেও ই ওপঙিবলৈ আৰম্ভ কৰে।
এলুমিনিয়াম, লো আৰু জিংকৰ দৰে ধাতুবোৰে ঠাণ্ডা বা গৰম পানীৰ সৈতে বিক্ৰিয়া নকৰে। কিন্তু সিহঁতে বাষ্পৰ সৈতে বিক্ৰিয়া কৰি ধাতৱীয় অক্সাইড আৰু হাইড্ৰজেন গঠন কৰে।
$ \begin{aligned} & 2 Al(s)+3 H_2 O(g) \to Al_2 O_3(s)+3 H_2(g) \\ & 3 Fe(s)+4 H_2 O(g) \to Fe_3 O_4(s)+4 H_2(g) \end{aligned} $
সীহ, তাম, ৰূপ আৰু সোণৰ দৰে ধাতুবোৰে পানীৰ সৈতে একেবাৰে বিক্ৰিয়া নকৰে।
৩.২.৩ ধাতুবোৰ এছিডৰ সৈতে বিক্ৰিয়া কৰিলে কি হয়?
তুমি ইতিমধ্যে শিকিছা যে ধাতুবোৰে এছিডৰ সৈতে বিক্ৰিয়া কৰি লৱণ আৰু হাইড্ৰজেন গেছ দিয়ে।
ধাতু + পাতল এছিড $ \rightarrow $ লৱণ + হাইড্ৰজেন
কিন্তু সকলো ধাতুৱে একে ধৰণে বিক্ৰিয়া কৰেনে? আহা আমি উলিয়াওঁ।
কাৰ্যকলাপ ৩.১১
- ছডিয়াম আৰু পটেছিয়াম বাদ দি আকৌ সকলো ধাতুৰ নমুনা সংগ্ৰহ কৰা। যদি নমুনাবোৰ মলিন হয়, বালি কাগজেৰে ঘঁহি পৰিষ্কাৰ কৰা। সতৰ্কতা: ছডিয়াম আৰু পটেছিয়াম নল’বাহঁক কাৰণ সিহঁতে ঠাণ্ডা পানীৰ সৈতেও জোৰেৰে বিক্ৰিয়া কৰে।
- নমুনাবোৰ পৃথককৈ পাতল হাইড্ৰক্ল’ৰিক এছিড থকা টেষ্ট টিউবত ৰাখা।
- টেষ্ট টিউববোৰত থাৰ্মমিটাৰবোৰ ওলোমাই ৰাখা, যাতে তেওঁলোকৰ বাল্ববোৰ এছিডত ডুব থাকে।
- বুদবুদবোৰ গঠনৰ হাৰ সাৱধানে লক্ষ্য কৰা।
- কোনবোৰ ধাতুৱে পাতল হাইড্ৰক্ল’ৰিক এছিডৰ সৈতে জোৰেৰে বিক্ৰিয়া কৰিলে?
- কোন ধাতুৰ সৈতে তুমি সৰ্বোচ্চ উষ্ণতা ৰেকৰ্ড কৰিলা?
- পাতল এছিডৰ সৈতে সক্ৰিয়তাৰ ক্ৰমত ধাতুবোৰক ঊৰ্ধ্বক্ৰমত সজোৱা।
মেগনেছিয়াম, এলুমিনিয়াম, জিংক আৰু লোৰ পাতল হাইড্ৰক্ল’ৰিক এছিডৰ সৈতে বিক্ৰিয়াবোৰৰ সমীকৰণবোৰ লিখা।
ধাতু এটাই নাইট্ৰিক এছিডৰ সৈতে বিক্ৰিয়া কৰিলে হাইড্ৰজেন গেছ বিকশিত নহয়। ইয়াৰ কাৰণ হ’ল $HNO_3$ এটা শক্তিশালী অক্সিডাইজিং এজেণ্ট। ই উৎপন্ন $H_2$ ক পানীলৈ অক্সিডাইজ কৰে আৰু নিজে নাইট্ৰ’জেনৰ অক্সাইডবোৰৰ ($N_2 O, NO.$, $NO_2$ ) যিকোনো এটালৈ হ্ৰাস পায়। কিন্তু মেগনেছিয়াম $(Mg)$ আৰু মেংগানিজ $(Mn)$ খুব পাতল $HNO_3$ ৰ সৈতে বিক্ৰিয়া কৰি $H_2$ গেছ বিকশিত কৰে।
তুমি কাৰ্যকলাপ ৩.১১ ত নিশ্চয় লক্ষ্য কৰিছা, যে বুদবুদ গঠনৰ হাৰ মেগনেছিয়ামৰ ক্ষেত্ৰত আটাইতকৈ বেছি আছিল। এই ক্ষেত্ৰত বিক্ৰিয়াটো আটাইতকৈ বেছি উষ্মাক্ষেপীও আছিল। সক্ৰিয়তা $Mg>Al>Zn>Fe$ ক্ৰমত হ্ৰাস পায়। তামৰ ক্ষেত্ৰত, কোনো বুদবুদ দেখা নগ’ল আৰু উষ্ণতাও অপরিবৰ্তিত থাকিল। ইয়ে দেখুৱায় যে তামে পাতল $HCl$ ৰ সৈতে বিক্ৰিয়া নকৰে।
তুমি জানানে?
একৱা ৰেজিয়া, (লেটিনত ‘ৰাজকীয় পানী’) হ’ল ৩:১ অনুপাতত কেন্দ্ৰীভূত হাইড্ৰক্ল’ৰিক এছিড আৰু কেন্দ্ৰীভূত নাইট্ৰিক এছিডৰ এটা সতেজভাৱে প্ৰস্তুত কৰা মিশ্ৰণ। ই সোণ দ্ৰৱীভূত কৰিব পাৰে, যদিও এই এছিডবোৰৰ কোনোৱেই একেলগে তেনেকুৱা কৰিব নোৱাৰে। একৱা ৰেজিয়া হ’ল এটা অতি ক্ষয়কাৰী, ধোঁৱা উৎপন্ন কৰা তৰল। ইয়াৰ ভিতৰত এটা যিয়ে সোণ আৰু প্লেটিনাম দ্ৰৱীভূত কৰিব পাৰে।











