અધ્યાય 03 ધાતુઓ અને અધાતુઓ
કક્ષા IX માં તમે વિવિધ તત્વો વિશે શીખ્યા છો. તમે જોયું હશે કે તત્વોને તેમના ગુણધર્મોના આધારે ધાતુઓ અથવા અધાતુઓ તરીકે વર્ગીકૃત કરી શકાય છે.
- તમારા દૈનિક જીવનમાં ધાતુઓ અને અધાતુઓના કેટલાક ઉપયોગો વિશે વિચારો.
- તત્વોને ધાતુઓ અથવા અધાતુઓ તરીકે વર્ગીકૃત કરતી વખતે તમે કયા ગુણધર્મો વિશે વિચાર્યું?
- આ ગુણધર્મો તત્વોના ઉપયોગો સાથે કેવી રીતે સંબંધિત છે?
ચાલો આમાંના કેટલાક ગુણધર્મોને વિગતવાર જોઈએ.
3.1 ભૌતિક ગુણધર્મો
3.1.1 ધાતુઓ
પદાર્થોનું વર્ગીકરણ શરૂ કરવાની સૌથી સરળ રીત તેમના ભૌતિક ગુણધર્મોની તુલના કરવાની છે. ચાલો નીચેની પ્રવૃત્તિઓની મદદથી આનો અભ્યાસ કરીએ. પ્રવૃત્તિ 3.1 થી 3.6 કરવા માટે, નીચેની ધાતુઓના નમૂના એકત્રિત કરો - લોખંડ, તાંબુ, એલ્યુમિનિયમ, મેગ્નેશિયમ, સોડિયમ, શીસું, જસત અને કોઈપણ અન્ય ધાતુ જે સરળતાથી ઉપલબ્ધ હોય.
પ્રવૃત્તિ 3.1
- લોખંડ, તાંબુ, એલ્યુમિનિયમ અને મેગ્નેશિયમના નમૂના લો. દરેક નમૂનાની બાહ્ય રચના નોંધો.
- સેન્ડ પેપરથી ઘસીને દરેક નમૂનાની સપાટી સાફ કરો અને ફરીથી તેમની બાહ્ય રચના નોંધો.
ધાતુઓ, તેમની શુદ્ધ અવસ્થામાં, ચમકતી સપાટી ધરાવે છે. આ ગુણધર્મને ધાત્વીય ચમક (metallic lustre) કહેવામાં આવે છે.
પ્રવૃત્તિ 3.2
લોખંડ, તાંબુ, એલ્યુમિનિયમ અને મેગ્નેશિયમના નાના ટુકડા લો. આ ધાતુઓને તીક્ષ્ણ છરી વડે કાપવાનો પ્રયત્ન કરો અને તમારા અવલોકનો નોંધો.
સોડિયમ ધાતુનો ટુકડો ચીમટા વડે પકડો.
સાવધાની: સોડિયમ ધાતુનો હંમેશા સાવધાનીપૂર્વક ઉપયોગ કરો. ફિલ્ટર પેપરની તહોમાં દબાવીને તેને સૂકવો.
તેને વોચ-ગ્લાસ પર મૂકો અને છરીથી કાપવાનો પ્રયત્ન કરો.
તમે શું અવલોકન કરો છો?
તમે જોશો કે ધાતુઓ સામાન્ય રીતે સખત હોય છે. સખતપણું ધાતુથી ધાતુમાં બદલાય છે.
પ્રવૃત્તિ 3.3
- લોખંડ, જસત, શીસું અને તાંબુના ટુકડા લો.
- કોઈપણ એક ધાતુને લોખંડના ગટ્ટા પર મૂકો અને હથોડીથી ચાર અથવા પાંચ વાર પ્રહાર કરો. તમે શું અવલોકન કરો છો?
- અન્ય ધાતુઓ સાથે પુનરાવર્તન કરો.
- આ ધાતુઓની આકૃતિમાં થતા ફેરફારને રેકોર્ડ કરો.
તમે જોશો કે કેટલીક ધાતુઓને પાતળી ચાદરોમાં ઘટી શકાય છે. આ ગુણધર્મને તન્યતા (malleability) કહેવામાં આવે છે. શું તમે જાણો છો કે સોનું અને ચાંદી સૌથી વધુ તન્ય ધાતુઓ છે?
પ્રવૃત્તિ 3.4
- તે ધાતુઓની યાદી બનાવો જેના તાર તમે દૈનિક જીવનમાં જોયા છે.
ધાતુઓને પાતળા તારમાં ખેંચી શકાય તે ક્ષમતાને તન્યતા (ductility) કહેવામાં આવે છે. સોનું સૌથી વધુ તન્ય ધાતુ છે. તમે જાણીને આશ્ચર્ય થશે કે એક ગ્રામ સોનામાંથી લગભગ $2 km$ લંબાઈનો તાર ખેંચી શકાય છે.
તેમની તન્યતા અને તન્યતાને કારણે જ ધાતુઓને આપણી જરૂરિયાતો અનુસાર વિવિધ આકાર આપી શકાય છે.
શું તમે કેટલીક ધાતુઓના નામ આપી શકો છો જે રસોઈના વાસણો બનાવવા માટે વપરાય છે? શું તમે જાણો છો કે આ ધાતુઓ વાસણો બનાવવા માટે કેમ વપરાય છે? ચાલો જવાબ શોધવા માટે નીચેની પ્રવૃત્તિ કરીએ.
પ્રવૃત્તિ 3.5
- એલ્યુમિનિયમ અથવા તાંબાનો તાર લો. આ તારને સ્ટેન્ડ પર, આકૃતિ 3.1 માં બતાવ્યા પ્રમાણે, ક્લેમ્પ કરો.
- મીણનો ઉપયોગ કરીને તારના મુક્ત છેડે એક પિન લગાવો.
- જ્યાં તે ક્લેમ્પ કરેલો છે તેની નજીક સ્પિરિટ લેમ્પ, મીણબત્તી અથવા બર્નર વડે તારને ગરમ કરો.
- કેટલાક સમય પછી તમે શું અવલોકન કરો છો?
- તમારા અવલોકનો નોંધો. શું ધાતુનો તાર ઓગળે છે?
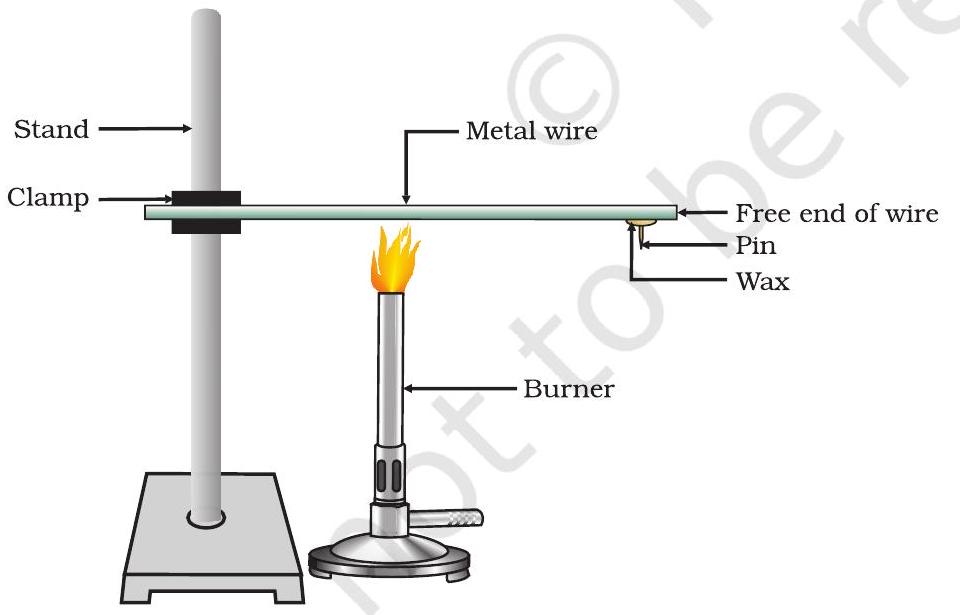
આકૃતિ 3.1 ધાતુઓ ઉષ્માના સુવાહક છે.
ઉપરોક્ત પ્રવૃત્તિ દર્શાવે છે કે ધાતુઓ ઉષ્માના સારા વાહક છે અને તેમનાં ગલનાંક ઊંચા હોય છે. ઉષ્માના શ્રેષ્ઠ વાહક ચાંદી અને તાંબુ છે. શીસું અને પારો તુલનાત્મક રીતે ઉષ્માના ખરાબ વાહક છે.
શું ધાતુઓ વિદ્યુતનું વહન પણ કરે છે? ચાલો જાણીએ.
પ્રવૃત્તિ 3.6
- આકૃતિ 3.2 માં બતાવ્યા પ્રમાણે વિદ્યુત પરિપથ સજ્જ કરો.
- પરીક્ષણ કરવાની ધાતુને ટર્મિનલ $A$ અને $B$ વચ્ચે બતાવ્યા પ્રમાણે પરિપથમાં મૂકો.
- શું બલ્બ પ્રકાશિત થાય છે? આ શું સૂચવે છે?
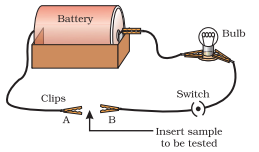
આકૃતિ 3.2 ધાતુઓ વિદ્યુતના સારા વાહક છે.
તમે જોયું હશે કે તમારા ઘરોમાં વિદ્યુતપ્રવાહ વહન કરતા તારો પર પોલીવિનાઇલ ક્લોરાઇડ (PVC) અથવા રબર જેવી સામગ્રીનું લેપન હોય છે. વિદ્યુતના તારો આવા પદાર્થોથી લેપિત કેમ હોય છે?
જ્યારે ધાતુઓ સખત સપાટી પર અથડાય છે ત્યારે શું થાય છે? શું તેઓ અવાજ ઉત્પન્ન કરે છે? જે ધાતુઓ સખત સપાટી પર અથડાય ત્યારે અવાજ ઉત્પન્ન કરે છે તેને ધ્વનિમાન (sonorous) કહેવામાં આવે છે. શું તમે હવે કહી શકો છો કે શાળાની ઘંટડીઓ ધાતુથી કેમ બનાવવામાં આવે છે?
3.1.2 અધાતુઓ
પાછલી કક્ષામાં તમે શીખ્યા છો કે ધાતુઓની તુલનામાં અધાતુઓ ખૂબ જ ઓછી છે. અધાતુઓના કેટલાક ઉદાહરણો કાર્બન, સલ્ફર, આયોડિન, ઑક્સિજન, હાઇડ્રોજન વગેરે છે. અધાતુઓ ઘન અથવા વાયુ છે, બ્રોમીન સિવાય જે પ્રવાહી છે.
શું અધાતુઓમાં પણ ધાતુઓ જેવા ભૌતિક ગુણધર્મો હોય છે? ચાલો જાણીએ.
પ્રવૃત્તિ 3.7
- કાર્બન (કોલસો અથવા ગ્રેફાઇટ), સલ્ફર અને આયોડિનના નમૂના એકત્રિત કરો.
- આ અધાતુઓ સાથે પ્રવૃત્તિ 3.1 થી 3.4 અને 3.6 કરો અને તમારા અવલોકનો રેકોર્ડ કરો.
ધાતુઓ અને અધાતુઓ સંબંધિત તમારા અવલોકનો કોષ્ટક 3.1 માં સંકલિત કરો.
કોષ્ટક 3.1
| તત્વ | પ્રતીક | સપાટીનો પ્રકાર | સખતપણું | તન્યતા | તન્યતા | વિદ્યુત વહન કરે છે | ધ્વનિમાનતા |
|---|---|---|---|---|---|---|---|
કોષ્ટક 3.1 માં રેકોર્ડ કરેલા અવલોકનોના આધારે, વર્ગમાં ધાતુઓ અને અધાતુઓના સામાન્ય ભૌતિક ગુણધર્મોની ચર્ચા કરો. તમે નિષ્કર્ષ પર આવ્યા હશો કે આપણે તત્વોને માત્ર તેમના ભૌતિક ગુણધર્મોના આધારે વર્ગીકૃત કરી શકતા નથી, કારણ કે ઘણા અપવાદો છે. ઉદાહરણ તરીકે -
(i) પારો સિવાયની બધી ધાતુઓ ઓરડાના તાપમાને ઘન અવસ્થામાં હોય છે. પ્રવૃત્તિ 3.5 માં, તમે અવલોકન કર્યું છે કે ધાતુઓના ગલનાંક ઊંચા હોય છે પરંતુ ગેલિયમ અને સીઝિયમના ગલનાંક ખૂબ જ ઓછા હોય છે. જો તમે તેમને તમારી હથેળી પર રાખશો તો આ બે ધાતુઓ ઓગળી જશે.
(ii) આયોડિન એક અધાતુ છે પરંતુ તે ચમકદાર છે.
(iii) કાર્બન એક અધાતુ છે જે વિવિધ સ્વરૂપોમાં અસ્તિત્વ ધરાવે છે. દરેક સ્વરૂપને એક અલોટ્રોપ (allotrope) કહેવામાં આવે છે. હીરો, કાર્બનનો એક અલોટ્રોપ, જાણીતો સૌથી સખત કુદરતી પદાર્થ છે અને તેનાં ગલનાંક અને ઉત્કલનાંક ખૂબ જ ઊંચા હોય છે. ગ્રેફાઇટ, કાર્બનનો બીજો અલોટ્રોપ, વિદ્યુતનો વાહક છે.
(iv) ક્ષાર ધાતુઓ (લિથિયમ, સોડિયમ, પોટેશિયમ) એટલી નરમ હોય છે કે તેમને છરીથી કાપી શકાય છે. તેમની ઘનતા ઓછી હોય છે અને ગલનાંક ઓછા હોય છે.
તત્વોને તેમના રાસાયણિક ગુણધર્મોના આધારે વધુ સ્પષ્ટ રીતે ધાતુઓ અને અધાતુઓ તરીકે વર્ગીકૃત કરી શકાય છે.
પ્રવૃત્તિ 3.8
- મેગ્નેશિયમની પટ્ટી અને થોડો સલ્ફર પાવડર લો.
- મેગ્નેશિયમની પટ્ટી સળગાવો. બનેલી રાખ એકત્રિત કરો અને તેને પાણીમાં ઓગાળો.
- પરિણામી દ્રાવણની લાલ અને વાદળી લિટમસ પેપર સાથે કસોટી કરો.
- મેગ્નેશિયમ સળગાવવાથી બનેલું ઉત્પાદન ઍસિડિક છે કે બેઝિક?
- હવે સલ્ફર પાવડર સળગાવો. ઉત્પન્ન થતા ધુમાડા એકત્રિત કરવા માટે સળગતા સલ્ફર પર એક ટેસ્ટ ટ્યુબ મૂકો.
- ઉપરોક્ત ટેસ્ટ ટ્યુબમાં થોડું પાણી ઉમેરો અને હલાવો.
- આ દ્રાવણની વાદળી અને લાલ લિટમસ પેપર સાથે કસોટી કરો.
- સલ્ફર સળગાવવાથી બનેલું ઉત્પાદન ઍસિડિક છે કે બેઝિક?
- શું તમે આ પ્રતિક્રિયાઓ માટે સમીકરણો લખી શકો છો?
બહુત અધાતુઓ પાણીમાં ઓગળવાથી ઍસિડિક ઑક્સાઇડ ઉત્પન્ન કરે છે. બીજી બાજુ, મોટાભાગની ધાતુઓ, બેઝિક ઑક્સાઇડ આપે છે. તમે આ ધાતુ ઑક્સાઇડ વિશે આગળના વિભાગમાં વધુ શીખશો.
3.2 ધાતુઓના રાસાયણિક ગુણધર્મો
આપણે ધાતુઓના રાસાયણિક ગુણધર્મો વિશે નીચેના વિભાગો 3.2.1 થી 3.2.4 માં શીખીશું. આ માટે, નીચેની ધાતુઓના નમૂના એકત્રિત કરો: એલ્યુમિનિયમ, તાંબુ, લોખંડ, શીસું, મેગ્નેશિયમ, જસત અને સોડિયમ.
3.2.1 જ્યારે ધાતુઓ હવામાં સળગાવવામાં આવે ત્યારે શું થાય છે?
તમે પ્રવૃત્તિ 3.8 માં જોયું છે કે મેગ્નેશિયમ હવામાં ચમકદાર સફેદ જ્યોત સાથે સળગે છે. શું બધી ધાતુઓ એ જ રીતે પ્રતિક્રિયા આપે છે? ચાલો નીચેની પ્રવૃત્તિ કરીને તપાસીએ.
પ્રવૃત્તિ 3.9
સાવધાની: નીચેની પ્રવૃત્તિ માટે શિક્ષકની સહાયતા જરૂરી છે. વિદ્યાર્થીઓ આંખોનું રક્ષણ કરે તો વધુ સારું.
- ઉપર લીધેલા કોઈપણ નમૂનાને ચીમટા વડે પકડો અને જ્યોત પર સળગાવવાનો પ્રયત્ન કરો. અન્ય ધાતુ નમૂનાઓ સાથે પુનરાવર્તન કરો.
- જો બને તો ઉત્પાદન એકત્રિત કરો.
- ઉત્પાદનો અને ધાતુની સપાટીને ઠંડી પડવા દો.
- કઈ ધાતુઓ સરળતાથી સળગે છે?
- ધાતુ સળગતી વખતે તમે કયો જ્યોત રંગ અવલોકન કર્યો?
- સળગાવ્યા પછી ધાતુની સપાટી કેવી દેખાય છે?
- ઑક્સિજન તરફ તેમની પ્રતિક્રિયાશીલતાના ઘટતા ક્રમમાં ધાતુઓ ગોઠવો.
- ઉત્પાદનો પાણીમાં દ્રાવ્ય છે?
લગભગ બધી ધાતુઓ ઑક્સિજન સાથે સંયોજાઈને ધાતુ ઑક્સાઇડ બનાવે છે.
ધાતુ + ઑક્સિજન $\rightarrow$ ધાતુ ઑક્સાઇડ
ઉદાહરણ તરીકે, જ્યારે તાંબાને હવામાં ગરમ કરવામાં આવે છે, ત્યારે તે ઑક્સિજન સાથે સંયોજાઈને કૉપર(II) ઑક્સાઇડ, એક કાળું ઑક્સાઇડ બનાવે છે.
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
તે જ રીતે, એલ્યુમિનિયમ એલ્યુમિનિયમ ઑક્સાઇડ બનાવે છે.
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
અધ્યાય 2 માંથી યાદ કરો, કેવી રીતે કૉપર ઑક્સાઇડ હાઇડ્રોક્લોરિક એસિડ સાથે પ્રતિક્રિયા આપે છે. આપણે શીખ્યા છો કે ધાતુ ઑક્સાઇડ પ્રકૃતિમાં બેઝિક હોય છે. પરંતુ કેટલાક ધાતુ ઑક્સાઇડ, જેમ કે એલ્યુમિનિયમ ઑક્સાઇડ, જસત ઑક્સાઇડ, ઍસિડિક તેમજ બેઝિક વર્તન બંને દર્શાવે છે. આવા ધાતુ ઑક્સાઇડ જે એસિડ તેમજ બેઝ બંને સાથે પ્રતિક્રિયા આપીને ક્ષાર અને પાણી ઉત્પન્ન કરે છે તેને ઉભયધર્મી ઑક્સાઇડ (amphoteric oxides) તરીકે ઓળખવામાં આવે છે. એલ્યુમિનિયમ ઑક્સાઇડ એસિડ અને બેઝ સાથે નીચેની રીતે પ્રતિક્રિયા આપે છે -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
મોટાભાગના ધાતુ ઑક્સાઇડ પાણીમાં અદ્રાવ્ય હોય છે પરંતુ આમાંના કેટલાક પાણીમાં ઓગળીને ક્ષાર બનાવે છે. સોડિયમ ઑક્સાઇડ અને પોટેશિયમ ઑક્સાઇડ પાણીમાં ઓગળીને નીચે પ્રમાણે ક્ષાર ઉત્પન્ન કરે છે -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
આપણે પ્રવૃત્તિ 3.9 માં અવલોકન કર્યું છે કે બધી ધાતુઓ ઑક્સિજન સાથે સમાન દરે પ્રતિક્રિયા આપતી નથી. વિવિધ ધાતુઓ ઑક્સિજન તરફ વિવિધ પ્રતિક્રિયાશીલતા દર્શાવે છે. પોટેશિયમ અને સોડિયમ જેવી ધાતુઓ એટલી જોરથી પ્રતિક્રિયા આપે છે કે જો તેમને ખુલ્લામાં રાખવામાં આવે તો તે આગ પકડે છે. તેથી, તેમને સુરક્ષિત રાખવા અને આકસ્મિક આગને રોકવા માટે, તેમને કેરોસીન તેલમાં ડુબાડીને રાખવામાં આવે છે. સામાન્ય તાપમાને, મેગ્નેશિયમ, એલ્યુમિનિયમ, જસત, શીસું વગેરે જેવી ધાતુઓની સપાટી ઑક્સાઇડની પાતળી પરતથી ઢંકાયેલી હોય છે. રક્ષણાત્મક ઑક્સાઇડ સ્તર ધાતુને આગળના ઑક્સિડેશનથી બચાવે છે. લોખંડ ગરમ કરવાથી સળગતું નથી પરંતુ લોખંડની કથરી બર્નરની જ્યોતમાં છાંટવાથી જોરથી સળગે છે. તાંબું સળગતું નથી, પરંતુ ગરમ ધાતુ કૉપર(II) ઑક્સાઇડના કાળા રંગના સ્તરથી ઢંકાયેલી હોય છે. ચાંદી અને સોનું ઊંચા તાપમાને પણ ઑક્સિજન સાથે પ્રતિક્રિયા આપતા નથી.
શું તમે જાણો છો?
એનોડાઇઝિંગ એ એલ્યુમિનિયમનો જાડો ઑક્સાઇડ સ્તર બનાવવાની પ્રક્રિયા છે. એલ્યુમિનિયમ હવાના સંપર્કમાં આવતા પાતળો ઑક્સાઇડ સ્તર વિકસાવે છે. આ એલ્યુમિનિયમ ઑક્સાઇડ લેપ તેને વધુ ક્ષય (corrosion) માટે પ્રતિરોધક બનાવે છે. ઑક્સાઇડ સ્તરને જાડો બનાવીને પ્રતિરોધકતા વધુ સુધારી શકાય છે. એનોડાઇઝિંગ દરમિયાન, સ્વચ્છ એલ્યુમિનિયમની વસ્તુને એનોડ બનાવવામાં આવે છે અને તેનું સગાળ સલ્ફ્યુરિક એસિડ સાથે વિદ્યુતવિભાજન (electrolysed) કરવામાં આવે છે. એનોડ પર ઉત્પન્ન થતો ઑક્સિજન વાયુ એલ્યુમિનિયમ સાથે પ્રતિક્રિયા આપીને જાડું રક્ષણાત્મક ઑક્સાઇડ સ્તર બનાવે છે. આ ઑક્સાઇડ સ્તરને સરળતાથી રંગી શકાય છે જેથી એલ્યુમિનિયમની વસ્તુઓને આકર્ષક સમાપ્તિ મળે છે.
પ્રવૃત્તિ 3.9 કર્યા પછી, તમે અવલોકન કર્યું હશે કે અહીં લીધેલા ધાતુના નમૂનાઓમાં સોડિયમ સૌથી વધુ પ્રતિક્રિયાશીલ છે. મેગ્નેશિયમની પ્રતિ











