অধ্যায় ০৩ ধাতু ও অধাতু
নবম শ্রেণীতে তুমি বিভিন্ন মৌল সম্পর্কে শিখেছ। তুমি দেখেছ যে, মৌলগুলিকে তাদের ধর্মের ভিত্তিতে ধাতু বা অধাতু হিসেবে শ্রেণীবদ্ধ করা যায়।
- তোমার দৈনন্দিন জীবনে ব্যবহৃত কিছু ধাতু ও অধাতুর ব্যবহার সম্পর্কে চিন্তা কর।
- মৌলগুলিকে ধাতু বা অধাতু হিসেবে শ্রেণীবদ্ধ করার সময় তুমি কোন কোন ধর্মের কথা চিন্তা করেছিলে?
- এই ধর্মগুলি কীভাবে মৌলগুলির ব্যবহারের সাথে সম্পর্কিত? আসুন আমরা এই ধর্মগুলির কিছুকে বিস্তারিতভাবে দেখি।
৩.১ ভৌত ধর্ম
৩.১.১ ধাতু
পদার্থগুলিকে শ্রেণীবদ্ধ করা শুরু করার সবচেয়ে সহজ উপায় হল তাদের ভৌত ধর্মের তুলনা করা। আসুন আমরা নিম্নলিখিত কার্যকলাপগুলির সাহায্যে এটি অধ্যয়ন করি। কার্যকলাপ ৩.১ থেকে ৩.৬ সম্পাদনের জন্য, নিম্নলিখিত ধাতুর নমুনা সংগ্রহ কর - লোহা, তামা, অ্যালুমিনিয়াম, ম্যাগনেসিয়াম, সোডিয়াম, সীসা, দস্তা এবং অন্য যে কোনও সহজলভ্য ধাতু।
কার্যকলাপ ৩.১
- লোহা, তামা, অ্যালুমিনিয়াম এবং ম্যাগনেসিয়ামের নমুনা নাও। প্রতিটি নমুনার চেহারা লক্ষ্য কর।
- প্রতিটি নমুনার পৃষ্ঠ বালির কাগজ দিয়ে ঘষে পরিষ্কার কর এবং তাদের চেহারা আবার লক্ষ্য কর।
ধাতুগুলি, তাদের বিশুদ্ধ অবস্থায়, একটি চকচকে পৃষ্ঠ থাকে। এই ধর্মকে ধাতব মরিচা বলে।
কার্যকলাপ ৩.২
লোহা, তামা, অ্যালুমিনিয়াম এবং ম্যাগনেসিয়ামের ছোট টুকরো নাও। এই ধাতুগুলিকে একটি ধারালো ছুরি দিয়ে কাটার চেষ্টা কর এবং তোমার পর্যবেক্ষণগুলি নোট কর।
এক জোড়া চিমটা দিয়ে সোডিয়াম ধাতুর একটি টুকরো ধরে রাখো।
সতর্কতা: সর্বদা সোডিয়াম ধাতু সাবধানে হ্যান্ডেল কর। একটি ফিল্টার পেপারের ভাঁজের মধ্যে চেপে শুকিয়ে নাও।
এটিকে একটি ওয়াচ-গ্লাসের উপর রাখ এবং ছুরি দিয়ে কাটার চেষ্টা কর।
তুমি কী পর্যবেক্ষণ কর?
তুমি দেখবে যে ধাতুগুলি সাধারণত কঠিন। কঠিনতা ধাতুভেদে ভিন্ন হয়।
কার্যকলাপ ৩.৩
- লোহা, দস্তা, সীসা এবং তামার টুকরো নাও।
- যে কোনও একটি ধাতু লোহার একটি ব্লকের উপর রাখ এবং হাতুড়ি দিয়ে চার বা পাঁচবার আঘাত কর। তুমি কী পর্যবেক্ষণ কর?
- অন্যান্য ধাতু দিয়ে পুনরাবৃত্তি কর।
- এই ধাতুগুলির আকৃতির পরিবর্তন রেকর্ড কর।
তুমি দেখবে যে কিছু ধাতুকে পাতলা চাদরে পিটানো যায়। এই ধর্মকে নমনীয়তা বলে। তুমি কি জান যে সোনা ও রূপা সবচেয়ে নমনীয় ধাতু?
কার্যকলাপ ৩.৪
- দৈনন্দিন জীবনে তুমি যে ধাতুর তারগুলি দেখেছ সেগুলির তালিকা কর।
ধাতুগুলিকে পাতলা তারে টানা যাওয়ার ক্ষমতাকে নমনীয়তা বলে। সোনা সবচেয়ে নমনীয় ধাতু। তুমি জেনে অবাক হবে যে এক গ্রাম সোনা থেকে প্রায় $2 km$ দৈর্ঘ্যের একটি তার টানা যেতে পারে।
এটি তাদের নমনীয়তা এবং নমনীয়তার কারণেই ধাতুগুলিকে আমাদের প্রয়োজনে বিভিন্ন আকার দেওয়া যায়।
তুমি কি কিছু ধাতুর নাম বলতে পার যা রান্নার পাত্র তৈরিতে ব্যবহৃত হয়? তুমি কি জানো কেন এই ধাতুগুলি পাত্র তৈরিতে ব্যবহৃত হয়? আসুন উত্তর খুঁজে বের করতে নিম্নলিখিত কার্যকলাপটি করি।
কার্যকলাপ ৩.৫
- একটি অ্যালুমিনিয়াম বা তামার তার নাও। চিত্র ৩.১-এ দেখানো হিসাবে এই তারটিকে একটি স্ট্যান্ডে ক্ল্যাম্প কর।
- মোম ব্যবহার করে তারটির মুক্ত প্রান্তে একটি পিন স্থির কর।
- যেখানে এটি ক্ল্যাম্প করা হয়েছে তার কাছাকাছি একটি স্পিরিট ল্যাম্প, মোমবাতি বা বার্নার দিয়ে তারটিকে গরম কর।
- কিছু সময় পরে তুমি কী পর্যবেক্ষণ কর?
- তোমার পর্যবেক্ষণগুলি নোট কর। ধাতুর তারটি গলে যায় কি?
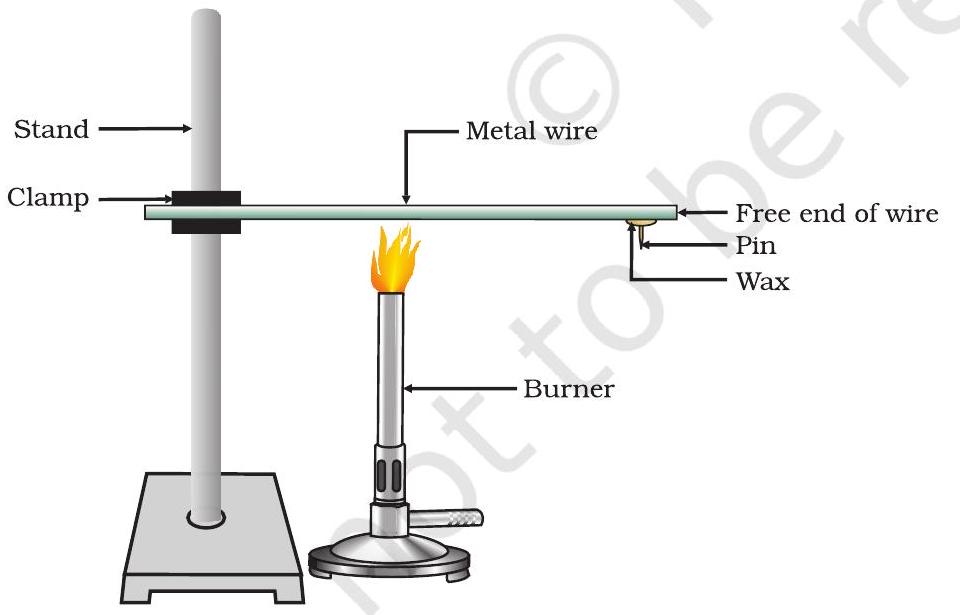
চিত্র ৩.১ ধাতুগুলি তাপের ভাল পরিবাহী।
উপরের কার্যকলাপটি দেখায় যে ধাতুগুলি তাপের ভাল পরিবাহী এবং এদের গলনাঙ্ক উচ্চ। তাপের সেরা পরিবাহী হল রূপা ও তামা। সীসা ও পারদ তুলনামূলকভাবে তাপের দুর্বল পরিবাহী।
ধাতুগুলি কি বিদ্যুৎও পরিবহন করে? আসুন জেনে নেওয়া যাক।
কার্যকলাপ ৩.৬
- চিত্র ৩.২-এ দেখানো হিসাবে একটি বৈদ্যুতিক বর্তনী সেট আপ কর।
- পরীক্ষা করা ধাতুটিকে $A$ এবং $B$ টার্মিনালের মধ্যে বর্তনীতে রাখ, যেমন দেখানো হয়েছে।
- বাল্বটি জ্বলে কি? এটি কী নির্দেশ করে?
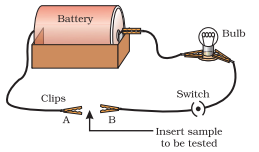
চিত্র ৩.২ ধাতুগুলি বিদ্যুতের ভাল পরিবাহী।
তুমি নিশ্চয়ই দেখেছ যে তোমার বাড়িতে যে তারগুলি বিদ্যুৎ বহন করে সেগুলির উপর পলিভিনাইল ক্লোরাইড (পিভিসি) বা রাবারের মতো পদার্থের প্রলেপ থাকে। বৈদ্যুতিক তারগুলি কেন এমন পদার্থ দিয়ে প্রলেপিত করা হয়?
ধাতুগুলি একটি কঠিন পৃষ্ঠে আঘাত করলে কী হয়? তারা কি শব্দ উৎপন্ন করে? যে ধাতুগুলি একটি কঠিন পৃষ্ঠে আঘাত করলে শব্দ উৎপন্ন করে তাদেরকে ধ্বনিবাহী বলে। তুমি কি এখন বলতে পারো কেন স্কুলের ঘণ্টাগুলি ধাতু দিয়ে তৈরি?
৩.১.২ অধাতু
পূর্ববর্তী শ্রেণীতে তুমি শিখেছ যে ধাতুর তুলনায় খুব কম অধাতু আছে। অধাতুর কিছু উদাহরণ হল কার্বন, সালফার, আয়োডিন, অক্সিজেন, হাইড্রোজেন ইত্যাদি। অধাতুগুলি হয় কঠিন বা গ্যাস, ব্রোমিন ব্যতীত যা একটি তরল। অধাতুগুলির কি ধাতুর মতোই ভৌত ধর্ম আছে? আসুন জেনে নেওয়া যাক।
কার্যকলাপ ৩.৭
- কার্বন (কয়লা বা গ্রাফাইট), সালফার এবং আয়োডিনের নমুনা সংগ্রহ কর।
- এই অধাতুগুলির সাথে কার্যকলাপ ৩.১ থেকে ৩.৪ এবং ৩.৬ সম্পাদন কর এবং তোমার পর্যবেক্ষণগুলি রেকর্ড কর।
ধাতু ও অধাতু সম্পর্কে তোমার পর্যবেক্ষণগুলি সারণী ৩.১-এ সংকলন কর।
সারণী ৩.১
| মৌল | প্রতীক | পৃষ্ঠের প্রকৃতি | কঠিনতা | নমনীয়তা | নমনীয়তা | বিদ্যুৎ পরিবহন করে | ধ্বনিবাহিতা |
|---|---|---|---|---|---|---|---|
সারণী ৩.১-এ রেকর্ড করা পর্যবেক্ষণের ভিত্তিতে, শ্রেণীতে ধাতু ও অধাতুর সাধারণ ভৌত ধর্ম নিয়ে আলোচনা কর। তুমি নিশ্চয়ই এই সিদ্ধান্তে পৌঁছেছ যে আমরা শুধুমাত্র ভৌত ধর্মের ভিত্তিতে মৌলগুলিকে শ্রেণীবদ্ধ করতে পারি না, কারণ অনেক ব্যতিক্রম আছে। উদাহরণস্বরূপ -
(i) পারদ ব্যতীত সমস্ত ধাতু ঘরের তাপমাত্রায় কঠিন হিসেবে থাকে। কার্যকলাপ ৩.৫-এ, তুমি পর্যবেক্ষণ করেছ যে ধাতুগুলির গলনাঙ্ক উচ্চ কিন্তু গ্যালিয়াম এবং সিজিয়ামের গলনাঙ্ক খুব কম। এই দুটি ধাতু তোমার হাতের তালুতে রাখলে গলে যাবে।
(ii) আয়োডিন একটি অধাতু কিন্তু এটি চকচকে।
(iii) কার্বন একটি অধাতু যা বিভিন্ন রূপে থাকতে পারে। প্রতিটি রূপকে একটি সমরূপ বলে। কার্বনের একটি সমরূপ হীরা, যা পরিচিত hardest প্রাকৃতিক পদার্থ এবং এর গলনাঙ্ক ও স্ফুটনাঙ্ক খুব উচ্চ। কার্বনের আরেকটি সমরূপ গ্রাফাইট, বিদ্যুতের পরিবাহী।
(iv) ক্ষার ধাতুগুলি (লিথিয়াম, সোডিয়াম, পটাসিয়াম) এত নরম যে এগুলি ছুরি দিয়ে কাটা যায়। এদের ঘনত্ব কম এবং গলনাঙ্ক কম।
মৌলগুলিকে তাদের রাসায়নিক ধর্মের ভিত্তিতে আরও স্পষ্টভাবে ধাতু ও অধাতু হিসেবে শ্রেণীবদ্ধ করা যায়।
কার্যকলাপ ৩.৮
- একটি ম্যাগনেসিয়াম ফিতে এবং কিছু সালফার গুঁড়ো নাও।
- ম্যাগনেসিয়াম ফিতেটি জ্বালাও। গঠিত ছাই সংগ্রহ কর এবং সেগুলি জলে দ্রবীভূত কর।
- উৎপন্ন দ্রবণটি লাল ও নীল লিটমাস কাগজ উভয় দিয়ে পরীক্ষা কর।
- ম্যাগনেসিয়াম জ্বালানোর ফলে গঠিত উৎপাদনটি অম্লীয় নাকি ক্ষারকীয়?
- এখন সালফার গুঁড়ো জ্বালাও। উৎপন্ন ধোঁয়া সংগ্রহ করার জন্য জ্বলন্ত সালফারের উপর একটি টেস্ট টিউব রাখ।
- উপরের টেস্ট টিউবে কিছু জল যোগ কর এবং ঝাঁকাও।
- নীল ও লাল লিটমাস কাগজ দিয়ে এই দ্রবণটি পরীক্ষা কর।
- সালফার জ্বালানোর ফলে গঠিত উৎপাদনটি অম্লীয় নাকি ক্ষারকীয়?
- তুমি কি এই বিক্রিয়াগুলির জন্য সমীকরণ লিখতে পার?
বেশিরভাগ অধাতু জলে দ্রবীভূত হলে অম্লীয় অক্সাইড উৎপন্ন করে। অন্যদিকে, বেশিরভাগ ধাতু, ক্ষারকীয় অক্সাইড দেয়। তুমি পরবর্তী বিভাগে এই ধাতব অক্সাইডগুলি সম্পর্কে আরও শিখবে।
৩.২ ধাতুর রাসায়নিক ধর্ম
আমরা ধাতুর রাসায়নিক ধর্ম সম্পর্কে নিম্নলিখিত বিভাগ ৩.২.১ থেকে ৩.২.৪-এ শিখব। এর জন্য, নিম্নলিখিত ধাতুর নমুনা সংগ্রহ কর অ্যালুমিনিয়াম, তামা, লোহা, সীসা, ম্যাগনেসিয়াম, দস্তা এবং সোডিয়াম।
৩.২.১ ধাতুগুলি বাতাসে পোড়ালে কী হয়?
তুমি কার্যকলাপ ৩.৮-এ দেখেছ যে ম্যাগনেসিয়াম বাতাসে একটি ঝলমলে সাদা শিখা নিয়ে জ্বলে। সব ধাতু কি একইভাবে বিক্রিয়া করে? আসুন নিম্নলিখিত কার্যকলাপটি সম্পাদন করে পরীক্ষা করি।
কার্যকলাপ ৩.৯
সতর্কতা: নিম্নলিখিত কার্যকলাপটির জন্য শিক্ষকের সহায়তা প্রয়োজন। শিক্ষার্থীরা চোখের সুরক্ষা পরলে ভাল হবে।
- উপরে নেওয়া যে কোনও নমুনা একটি জোড়া চিমটা দিয়ে ধরে একটি শিখার উপর জ্বালানোর চেষ্টা কর। অন্যান্য ধাতুর নমুনা দিয়ে পুনরাবৃত্তি কর।
- গঠিত হলে উৎপাদন সংগ্রহ কর।
- উৎপাদন এবং ধাতুর পৃষ্ঠকে ঠান্ডা হতে দাও।
- কোন ধাতুগুলি সহজে জ্বলে?
- ধাতুটি জ্বললে তুমি কী রঙের শিখা পর্যবেক্ষণ করেছ?
- জ্বালানোর পর ধাতুর পৃষ্ঠটি কেমন দেখায়?
- অক্সিজেনের প্রতি তাদের বিক্রিয়াশীলতার ক্রম অনুসারে ধাতুগুলিকে সাজাও।
- উৎপাদনগুলি জলে দ্রবণীয় কি?
প্রায় সব ধাতু অক্সিজেনের সাথে মিলিত হয়ে ধাতব অক্সাইড গঠন করে।
ধাতু + অক্সিজেন $\rightarrow$ ধাতব অক্সাইড
উদাহরণস্বরূপ, যখন তামাকে বাতাসে গরম করা হয়, এটি অক্সিজেনের সাথে মিলিত হয়ে তামা(II) অক্সাইড গঠন করে, একটি কালো অক্সাইড।
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
একইভাবে, অ্যালুমিনিয়াম অ্যালুমিনিয়াম অক্সাইড গঠন করে।
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
অধ্যায় ২ থেকে স্মরণ কর, কিভাবে কপার অক্সাইড হাইড্রোক্লোরিক অ্যাসিডের সাথে বিক্রিয়া করে। আমরা শিখেছি যে ধাতব অক্সাইডগুলি প্রকৃতিতে ক্ষারকীয়। কিন্তু কিছু ধাতব অক্সাইড, যেমন অ্যালুমিনিয়াম অক্সাইড, জিঙ্ক অক্সাইড অম্লীয় এবং ক্ষারকীয় উভয় আচরণ দেখায়। এমন ধাতব অক্সাইড যা অ্যাসিড এবং ক্ষারক উভয়ের সাথেই বিক্রিয়া করে লবণ ও জল উৎপন্ন করে তাদের উভধর্মী অক্সাইড বলে। অ্যালুমিনিয়াম অক্সাইড নিম্নলিখিতভাবে অ্যাসিড এবং ক্ষারকের সাথে বিক্রিয়া করে -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
বেশিরভাগ ধাতব অক্সাইড জলে অদ্রবণীয় কিন্তু এগুলির কিছু জল দ্রবীভূত হয়ে ক্ষারক গঠন করে। সোডিয়াম অক্সাইড এবং পটাসিয়াম অক্সাইড জলে দ্রবীভূত হয়ে নিম্নরূপ ক্ষারক উৎপন্ন করে -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
আমরা কার্যকলাপ ৩.৯-এ পর্যবেক্ষণ করেছি যে সব ধাতু একই হারে অক্সিজেনের সাথে বিক্রিয়া করে না। বিভিন্ন ধাতু অক্সিজেনের প্রতি বিভিন্ন বিক্রিয়াশীলতা দেখায়। পটাসিয়াম এবং সোডিয়ামের মতো ধাতুগুলি এত জোরালোভাবে বিক্রিয়া করে যে খোলা অবস্থায় রাখলে তারা আগুন ধরে ফেলে। তাই, এগুলিকে রক্ষা করতে এবং আকস্মিক আগুন প্রতিরোধ করতে, এগুলিকে কেরোসিন তেলে ডুবিয়ে রাখা হয়। সাধারণ তাপমাত্রায়, ম্যাগনেসিয়াম, অ্যালুমিনিয়াম, দস্তা, সীসা ইত্যাদি ধাতুর পৃষ্ঠ একটি পাতলা অক্সাইড স্তর দ্বারা আবৃত থাকে। প্রতিরক্ষামূলক অক্সাইড স্তরটি ধাতুটিকে আরও অক্সিডেশন থেকে রক্ষা করে। লোহা গরম করলে জ্বলে না কিন্তু লোহার গুঁড়ো বার্নারের শিখায় ছিটালে জোরালোভাবে জ্বলে। তামা জ্বলে না, কিন্তু গরম ধাতুটির উপর তামা(II) অক্সাইডের একটি কালো রঙের স্তর জমে। রূপা ও সোনা উচ্চ তাপমাত্রায়ও অক্সিজেনের সাথে বিক্রিয়া করে না।
তুমি কি জান?
অ্যানোডাইজিং হল অ্যালুমিনিয়ামের একটি পুরু অক্সাইড স্তর গঠনের একটি প্রক্রিয়া। অ্যালুমিনিয়াম বাতাসের সংস্পর্শে এলে একটি পাতলা অক্সাইড স্তর তৈরি করে। এই অ্যালুমিনিয়াম অক্সাইড আবরণ এটিকে আরও ক্ষয় প্রতিরোধী করে তোলে। অক্সাইড স্তরটিকে পুরু করে প্রতিরোধ ক্ষমতা আরও উন্নত করা যেতে পারে। অ্যানোডাইজিংয়ের সময়, একটি পরিষ্কার অ্যালুমিনিয়াম বস্তুকে অ্যানোড বানানো হয় এবং এটি পাতলা সালফিউরিক অ্যাসিড দিয়ে তড়িৎ বিশ্লেষিত হয়। অ্যানোডে উৎপন্ন অক্সিজেন গ্যাস অ্যালুমিনিয়ামের সাথে বিক্রিয়া করে একটি পুরু প্রতিরক্ষামূলক অক্সাইড স্তর তৈরি করে। এই অক্সাইড স্তরটি সহজেই রঞ্জিত করা যেতে পারে যা অ্যালুমিনিয়াম বস্তুগুলিকে একটি আকর্ষণীয় ফিনিশ দেয়।
কার্যকলাপ ৩.৯ সম্পাদনের পর, তুমি নিশ্চয়ই পর্যবেক্ষণ করেছ যে এখানে নেওয়া ধাতুর নমুনাগুলির মধ্যে সোডিয়াম সবচেয়ে বিক্রিয়াশীল। ম্যাগনেসিয়ামের বিক্রিয়া কম জোরালো যা বোঝায় যে এটি সোডিয়ামের মতো বিক্রিয়াশীল নয়। কিন্তু অক্সিজেনে জ্বলন আমাদের দস্তা, লোহা, তামা বা সীসার বিক্রিয়াশীলতা সম্পর্কে সিদ্ধান্ত নিতে সাহায্য করে না। আসুন এই ধাতুগুলির বিক্রিয়াশীলতার ক্রম সম্পর্কে একটি সিদ্ধান্তে পৌঁছাতে আরও কিছু বিক্রিয়া দেখি।
৩.২.২ ধাতুগুলি জলের সাথে বিক্রিয়া করলে কী হয়?
কার্যকলাপ ৩.১০
সতর্কতা: এই কার্যকলাপটির জন্য শিক্ষকের সহায়তা প্রয়োজন।
- কার্যকলাপ ৩.৯-এর মতো একই ধাতুর নমুনা সংগ্রহ কর।
- নমুনাগুলির ছোট টুকরোগুলি আলাদাভাবে অর্ধেক ঠান্ডা জল দিয়ে ভরা বিকারগুলিতে রাখ।
- কোন ধাতুগুলি ঠান্ডা জলের সাথে বিক্রিয়া করল? ঠান্ডা জলের সাথে তাদের বিক্রিয়াশীলতার ক্রম অনুসারে সাজাও।
- কোন ধাতু কি জলের উপর আগুন উৎপন্ন করল?
- কিছু সময় পরে কোন ধাতু কি ভাসতে শুরু করে?
- যে ধাতুগুলি ঠান্ডা জলের সাথে বিক্রিয়া করে নি সেগুলিকে অর্ধেক গরম জল দিয়ে ভরা বিকারগুলিতে রাখ।
- যে ধাতুগুলি গরম জলের সাথেও বিক্রিয়া করে নি, চিত্র ৩.৩-এ দেখানো হিসাবে যন্ত্রপাতি সেট আপ কর এবং বাষ্পের সাথে তাদের বিক্রিয়া পর্যবেক্ষণ কর।
- কোন ধাতুগুলি বাষ্পের সাথেও বিক্রিয়া করে নি?
- জলের সাথে বিক্রিয়াশীলতার ক্রম অনুসারে ধাতুগুলিকে সাজাও।
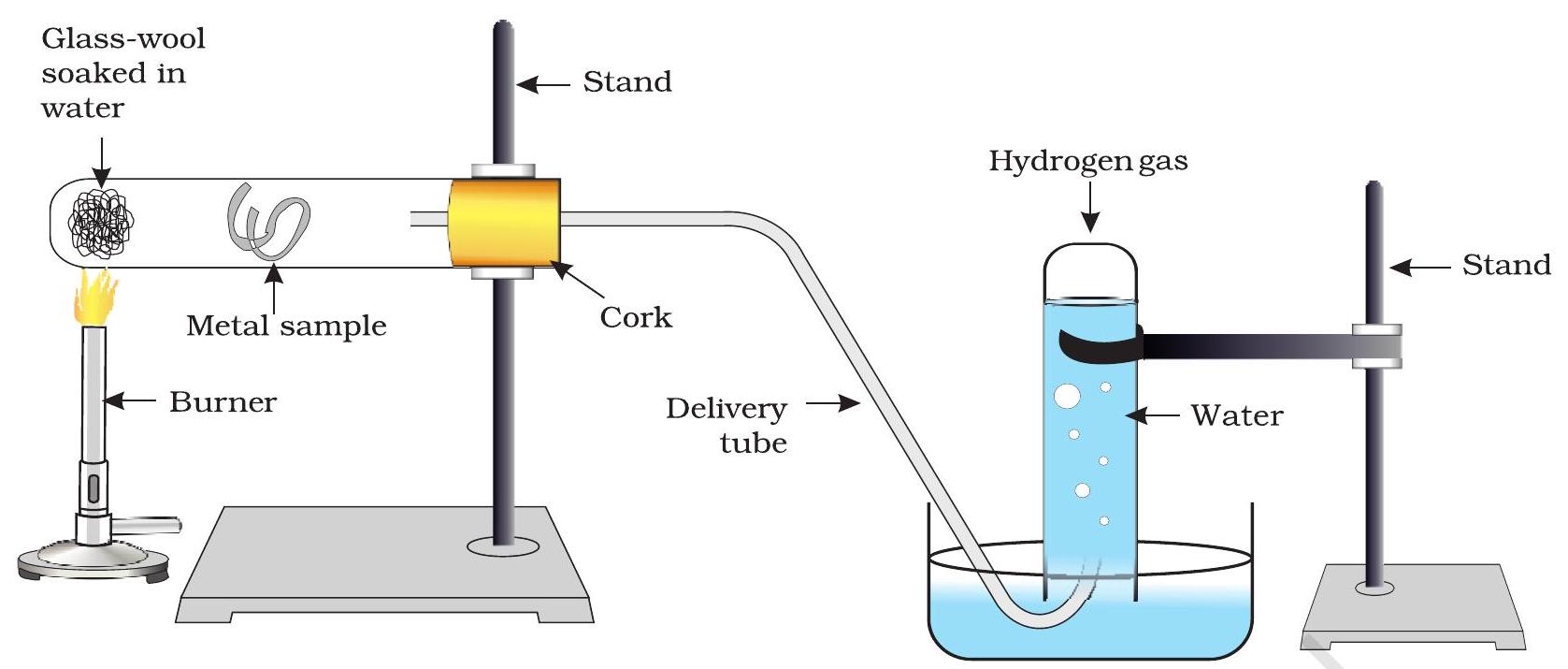
চিত্র ৩.৩ একটি ধাতুর উপর বাষ্পের ক্রিয়া
ধাতুগুলি জলের সাথে বিক্রিয়া করে একটি ধাতব অক্সাইড এবং হাইড্রোজেন গ্যাস উৎপন্ন করে। ধাতব অক্সাইডগুলি যা জলে দ্রবণীয় সেগুলি আরও ধাতব হাইড্রোক্সাইড গঠন করতে তাতে দ্রবীভূত হয়। কিন্তু সব ধাতু জলের সাথে বিক্রিয়া করে না।
ধাতু + জল $\rightarrow$ ধাতব অক্সাইড + হাইড্রোজেন
ধাতব অক্সাইড + জল $ \rightarrow $ ধাতব হাইড্রোক্সাইড
পটাসিয়াম এবং সোডিয়ামের মতো ধাতুগুলি ঠান্ডা জলের সাথে সহিংসভাবে বিক্রিয়া করে। সোডিয়াম এবং পটাসিয়ামের ক্ষেত্রে, বিক্রিয়াটি এত সহিংস এবং উষ্ণতাপীয় যে উৎপন্ন হাইড্রোজেন তৎক্ষণাৎ আগুন ধরে ফেলে।
$ \begin{aligned} & 2 K(s)+2 H_2 O(l) \to 2 KOH(aq)+H_2(g)+\text{ heat energy } \\ & 2 Na(s)+2 H_2 O(l) \to 2 NaOH(aq)+H_2(g)+\text{ heat energy } \end{aligned} $
ক্যালসিয়ামের জলের সাথে বিক্রিয়া কম সহিংস। উৎপন্ন তাপ হাইড্রোজেনের জন্য আগুন ধরানোর জন্য পর্যাপ্ত নয়।
$Ca(s)+2 H_2 O(l) \to Ca(OH)_2(aq)+H_2(g)$
হাইড্রোজেন গ্যাসের বুদবুদগুলি ধাতুর পৃষ্ঠে আটকে থাকার কারণে ক্যালসিয়াম ভাসতে শুরু করে।
ম্যাগনেসিয়াম ঠান্ডা জলের সাথে বিক্রিয়া করে না। এটি গরম জলের সাথে বিক্রিয়া করে ম্যাগনেসিয়াম হাইড্রোক্সাইড এবং হাইড্রোজেন গঠন করে। হাইড্রোজেন গ্যাসের বুদবুদগুলি এর পৃষ্ঠে আটকে থাকার কারণে এটিও ভাসতে শুরু করে।
অ্যালুমিনিয়াম, লোহা এবং দস্তার মতো ধাতুগুলি ঠান্ডা বা গরম জলের কোনোটির সাথেই বিক্রিয়া করে না। কিন্তু তারা বাষ্পের সাথে বিক্রিয়া করে ধাতব অক্সাইড এবং হাইড্রোজেন গঠন করে।
$ \begin{aligned} & 2 Al(s)+3 H_2 O(g) \to Al_2 O_3(s)+3 H_2(g) \\ & 3 Fe(s)+4 H_2 O(g) \to Fe_3 O_4(s)+4 H_2(g) \end{aligned} $
সীসা, তামা, রূপা এবং সোনার মতো ধাতুগুলি জলের সাথে মোটেও বিক্রিয়া করে না।
৩.২.৩ ধাতুগুলি অ্যাসিডের সাথে বিক্রিয়া করলে কী হয়?
তুমি ইতিমধ্যেই শিখেছ যে ধাতুগুলি অ্যাসিডের সাথে বিক্রিয়া করে একটি লবণ এবং হাইড্রোজেন গ্যাস দেয়।
ধাতু + তরল অ্যাসিড $ \rightarrow $ লবণ + হাইড্রোজেন
কিন্তু সব ধাতু কি একইভাবে বিক্রিয়া করে? আসুন জেনে নেওয়া যাক।
কার্যকলাপ ৩.১১
- সোডিয়াম এবং পটাসিয়াম ব্যতীত আবার সমস্ত ধাতুর নমুনা সংগ্রহ কর। যদি নমুনাগুলি মলিন হয়, বালির কাগজ দিয়ে ঘষে পরিষ্কার কর। সতর্কতা: সোডিয়াম এবং পটাসিয়াম নিও না কারণ তারা ঠান্ডা জলের সাথেও জোরালোভাবে বিক্রিয়া করে।
- নমুনাগুলিকে আলাদাভাবে তরল হাইড্রোক্লোরিক অ্যাসিড ধারণকারী টেস্ট টিউবগুলিতে রাখ।
- থার্মোমিটারগুলি টেস্ট টিউবগুলিতে ঝুলিয়ে দাও, যাতে তাদের বাল্বগুলি অ্যাসিডে ডুবে থাকে।
- বুদবুদ গঠনের হার সাবধানে পর্যবেক্ষণ কর।
- কোন ধাতুগুলি তরল হাইড্রোক্লোরিক অ্যাসিডের সাথে জোরালোভাবে বিক্রিয়া করল?
- কোন ধাতুর সাথে তুমি সর্বোচ্চ তাপমাত্রা রেকর্ড করেছ?
- তরল অ্যাসিডের সাথে বিক্রিয়াশীলতার ক্রম অনুসারে ধাতুগুলিকে সাজাও।
ম্যাগনেসিয়াম, অ্যালুমিনিয়াম, দস্তা এবং লোহার তরল হাইড্রোক্লোরিক অ্যাসিডের সাথে বিক্রিয়ার সমীকরণ লিখ।
একটি ধাতু নাইট্রিক অ্যাসিডের সাথে বিক্রিয়া করলে হাইড্রোজেন গ্যাস উৎপন্ন হয় না। এটি কারণ $HNO_3$ একটি শক্তিশালী জারক। এটি উৎপন্ন $H_2$ কে জলে জারিত করে এবং নিজে নাইট্রোজেন অক্সাইডে ($N_2 O, NO.$, $NO_2$ ) বিজারিত হয়। কিন্তু ম্যাগনেসিয়াম $(Mg)$ এবং ম্যাঙ্গানিজ $(Mn)$ খুব তরল $HNO_3$ এর সাথে বিক্রিয়া করে $H_2$ গ্যাস উৎপন্ন করে।
তুমি নিশ্চয়ই কার্যকলাপ ৩.১১-এ পর্যবেক্ষণ করেছ যে, বুদবুদ গঠনের হার ম্যাগনেসিয়ামের ক্ষেত্রে সবচেয়ে দ্রুত ছিল। এই ক্ষেত্রে বিক্রিয়াটিও সবচেয়ে উষ্ণতাপীয় ছিল। বিক্রিয়াশীলতা $Mg>Al>Zn>Fe$ ক্রমে হ্রাস পায়। তামার ক্ষেত্রে, কোন বুদবুদ দেখা যায়নি এবং তাপমাত্রাও অপরিবর্তিত থাকে। এটি দেখায় যে তামা তরল $HCl$ এর সাথে বিক্রিয়া করে না।
তুমি কি জান?
অ্যাকোয়া রেজিয়া, (ল্যাটিনে ‘রাজকীয় জল’) হল ঘন হাইড্রোক্লোরিক অ্যাসিড এবং ঘন নাইট্রিক অ্যাসিডের ৩:১ অনুপাতে তাজা প্রস্তুত মিশ্রণ। এটি সোনা দ্রবীভূত করতে পারে, যদিও এই অ্যাসিডগুলির কোনোটিই একা তা করতে পারে না। অ্যাকোয়া রেজিয়া একটি অত্যন্ত ক্ষয়কারী, ধূমায়িত তরল। এটি সেই কয়েকটি বিকারকগুলির মধ্যে একটি যা সোনা এবং প্লাটিনাম দ্রবীভূত করতে সক্ষম।
৩.২.৪ ধাতুগুলি অন্যান্য ধাতব লবণের দ্রবণের সাথে কীভাবে বিক্রিয়া করে?
কার্যকলাপ ৩.১২
- একটি পরিষ্কার তামার তার এবং একটি লোহার পেরেক নাও।
- তামার তারটিকে আয়রন সালফেটের দ্রবণে এবং লোহার পেরেকটিকে টেস্ট টিউবগুলিতে নেওয়া কপার সালফেটের দ্রবণে রাখ (চিত্র ৩.৪)।
- ২০ মিনিট পর তোমার পর্যবেক্ষণগুলি রেকর্ড কর।
- কোন টেস্ট টিউবে তুমি দেখেছ যে একটি বিক্রিয়া ঘটেছে?
- কোন ভিত্তিতে তুমি বলতে পার যে একটি বিক্রিয়া আসলেই ঘটেছে?
- তুমি কি কার্যকলাপ ৩.৯, ৩.১০ এবং ৩.১১-এর জন্য তোমার পর্যবেক্ষণগুলির মধ্যে সম্পর্ক স্থাপন করতে পার?
- যে বিক্রিয়া ঘটেছে তার জন্য একটি সুষম রাসায়নিক সমীকরণ লিখ।
- বিক্রিয়াটির ধরনের নাম কর।
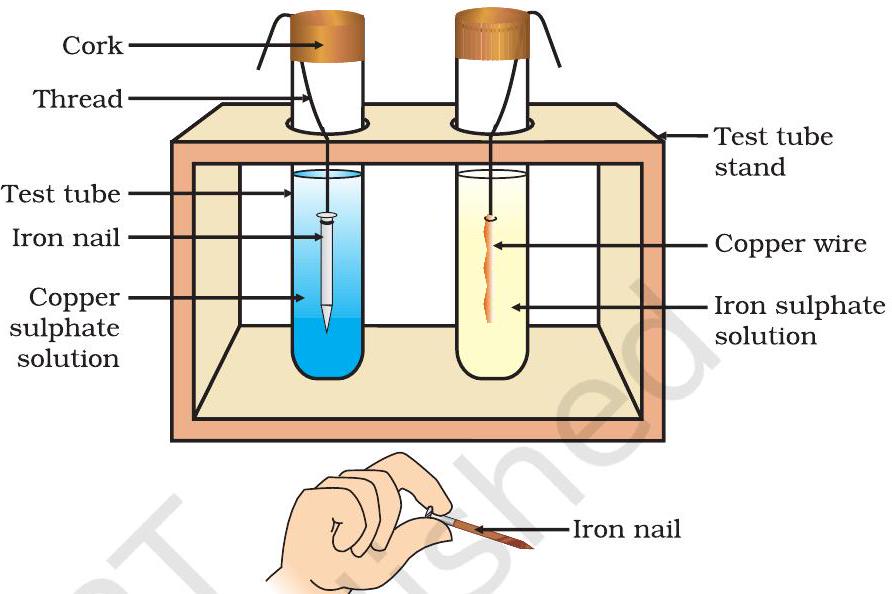
চিত্র ৩.৪ ধাতুগুলির লবণের দ্রবণের সাথে বিক্রিয়া
সক্রিয় ধাতুগুলি কম সক্রিয় ধাতুগুলিকে তাদের যৌগের দ্রবণ বা গলিত অবস্থা থেকে স্থানচ্যুত করতে পারে।
আমরা পূর্ববর্তী বিভাগগুলিতে দেখেছি যে সব ধাতু সমানভাবে সক্রিয় নয়। আমরা বিভিন্ন ধাতুর অক্সিজেন, জল এবং অ্যাসিডের সাথে বিক্রিয়াশীলতা পরীক্ষা করেছি। কিন্তু সব ধাতু এই বিকারকগুলির সাথে বিক্রিয়া করে না। তাই আমরা আমাদের সংগ্রহ করা সমস্ত ধাতুর নমুনাকে তাদের বিক্রিয়াশীলতার ক্রম অনুসারে সাজাতে পারিনি। অধ্যায় ১-এ অধ্যয়ন করা স্থানচ্যুতি বিক্রিয়া ধাতুগুলির বিক্রিয়াশীলতা সম্পর্কে ভাল প্রমাণ দেয়। এটি সহজ এবং সহজ যদি ধাতু A ধাতু $B$ কে তার দ্রবণ থেকে স্থানচ্যুত করে, এটি $B$ এর চেয়ে বেশি সক্রিয়।
$ \text{ ধাতু A }+ \text{ B এর লবণ দ্রবণ } \to \text{ A এর লবণ দ্রবণ }+ \text{ ধাতু B } $
কার্যকলাপ ৩.১২-এ তোমার পর্যবেক্ষণ অনুসারে কোন ধাতু, তামা নাকি লোহা, বেশি সক্রিয়?
৩.২.৫ সক্রিয়তা শ্রেণী
সক্রিয়তা শ্রেণী হল ধাতুগুলির একটি তালিকা যা তাদের ক্রমহ্রাসমান সক্রিয়তার ক্রমে সাজানো। স্থানচ্যুতি পরীক্ষা (কার্যকলাপ ১.৯ এবং ৩.১২) সম্পাদনের পর, নিম্নলিখিত শ্রেণী, (সারণী ৩.২) যা সক্রিয়তা শ্রেণী নামে পরিচিত, তৈরি করা হয়েছে।
সারণী ৩.২ সক্রিয়তা শ্রেণী: ধাতুগুলির আপেক্ষিক সক্রিয়তা
| K | পটাসিয়াম | $\downarrow$ সবচেয়ে সক্রিয় |
| $Na$ | সোডিয়াম | |
| $Ca$ | ক্যালসিয়াম | |
| Mg | ম্যাগনেসিয়াম | |
| Al | অ্যালুমিনিয়াম | |
| $Zn$ | দস্তা | $\downarrow$ সক্রিয়তা হ্রাস পায় |
| $Fe$ | লোহা | |
| $Pb$ | সীসা | |
| $[H]$ | [হাইড্রোজেন] | |
| $Cu$ | তামা | |
| $Hg$ | পারদ | |
| $Ag$ | রূপা | |
| $Au$ | সোনা | $\downarrow$ সবচেয়ে কম সক্রিয় |
৩.৩ ধাতু ও অধাতু কীভাবে বিক্রিয়া করে?
উপরের কার্যকলাপগুলিতে, তুমি অনেকগুলি বিকারকের সাথে ধাতুর বিক্রিয়া দেখেছ। ধাতুগুলি কেন এইভাবে বিক্রিয়া করে? আসুন আমরা নবম শ্রেণীতে মৌলগুলির ইলেকট্রন বিন্যাস সম্পর্কে যা শিখেছি তা স্মরণ করি। আমরা শিখেছি যে মহৎ গ্যাসগুলি, যাদের সম্পূর্ণরূপে পূর্ণ যোজ্যতা শেল আছে, খুব কম রাসায়নিক ক্রিয়াকলাপ দেখায়। তাই, আমরা মৌলগুলির সক্রিয়তাকে সম্পূর্ণরূপে পূর্ণ যোজ্যতা শেল অর্জনের প্রবণতা হিসেবে ব্যাখ্যা করি।
আসুন মহৎ গ্যাস এবং কিছু ধাতু ও অধাতুর ইলেকট্রন বিন্যাস দেখি।
সারণী ৩.৩ থেকে আমরা দেখতে পাই যে একটি সোডিয়াম পরমাণুর তার সর্ববহিঃস্থ শেলে একটি ইলেকট্রন আছে। যদি এটি তার $M$ শেল থেকে ইলেকট্রন হারায় তবে তার $L$ শেল এখন সর্ববহিঃস্থ শেল হয়ে যায় এবং যার একটি স্থিত অষ্টক আছে। এই পরমাণুর নিউক্লিয়াসে এখনও ১১টি প্রোটন আছে কিন্তু ইলেকট্রনের সংখ্যা ১০ হয়ে গেছে, তাই একটি নেট ধনাত্মক আধান আছে যা আমাদের একটি সোডিয়াম ক্যাটায়ন $Na^{+}$ দেয়। অন্যদিকে ক্লোরিনের তার সর্ববহিঃস্থ শেলে সাতটি ইলেকট্রন আছে এবং এর অষ্টক সম্পূর্ণ করতে আরও একটি ইলেকট্রনের প্রয়োজন। যদি সোডিয়াম এবং ক্লোরিন বিক্রিয়া করে, সোডিয়াম দ্বারা হারানো ইলেকট্রনটি ক্লোরিন দ্বারা গ্রহণ করা যেতে পারে। একটি ইলেকট্রন লাভ করার পর, ক্লোরিন পরমাণু একটি একক ঋণাত্মক আধান পায়, কারণ এর নিউক্লিয়াসে ১৭টি প্রোটন আছে এবং এর $K, L$ এবং $M$ শেলগুলিতে ১৮টি ইলেকট্রন আছে। এটি আমাদের একটি ক্লোরাইড অ্যানায়ন $Cl^{-}$ দেয়। তাই এই দুটি মৌলের মধ্যে একটি দেওয়া-নেওয়ার সম্পর্ক থাকতে পারে নিম্নরূপ (চিত্র ৩.৫)।
সারণী ৩.৩ কিছু মৌলের ইলেকট











