അദ്ധ്യായം 03 ലോഹങ്ങളും അലോഹങ്ങളും
ഒൻപതാം ക്ലാസ്സിൽ നിങ്ങൾ വിവിധ മൂലകങ്ങളെക്കുറിച്ച് പഠിച്ചിട്ടുണ്ട്. മൂലകങ്ങളെ അവയുടെ ഗുണങ്ങളുടെ അടിസ്ഥാനത്തിൽ ലോഹങ്ങളോ അലോഹങ്ങളോ ആയി തരംതിരിക്കാമെന്ന് നിങ്ങൾ കണ്ടിട്ടുണ്ട്.
- നിങ്ങളുടെ ദൈനംദിന ജീവിതത്തിൽ ലോഹങ്ങളുടെയും അലോഹങ്ങളുടെയും ചില ഉപയോഗങ്ങളെക്കുറിച്ച് ചിന്തിക്കുക.
- മൂലകങ്ങളെ ലോഹങ്ങളോ അലോഹങ്ങളോ ആയി തരംതിരിക്കുമ്പോൾ നിങ്ങൾ ഏത് ഗുണങ്ങളെക്കുറിച്ചാണ് ചിന്തിച്ചത്?
- ഈ ഗുണങ്ങൾ മൂലകങ്ങളുടെ ഉപയോഗങ്ങളുമായി എങ്ങനെ ബന്ധപ്പെട്ടിരിക്കുന്നു?
ഈ ഗുണങ്ങളിൽ ചിലത് നമുക്ക് വിശദമായി പരിശോധിക്കാം.
3.1 ഭൗതിക ഗുണങ്ങൾ
3.1.1 ലോഹങ്ങൾ
പദാർത്ഥങ്ങളെ തരംതിരിക്കാൻ ഏറ്റവും എളുപ്പമുള്ള വഴി അവയുടെ ഭൗതിക ഗുണങ്ങൾ താരതമ്യം ചെയ്യുക എന്നതാണ്. താഴെ കൊടുത്തിരിക്കുന്ന പ്രവർത്തനങ്ങളുടെ സഹായത്തോടെ ഇത് നമുക്ക് പഠിക്കാം. 3.1 മുതൽ 3.6 വരെയുള്ള പ്രവർത്തനങ്ങൾ നടത്തുന്നതിന്, ഇനിപ്പറയുന്ന ലോഹങ്ങളുടെ സാമ്പിളുകൾ - ഇരുമ്പ്, ചെമ്പ്, അലുമിനിയം, മഗ്നീഷ്യം, സോഡിയം, ഈയം, നാകം, മറ്റേതെങ്കിലും എളുപ്പത്തിൽ ലഭ്യമാകുന്ന ലോഹം എന്നിവ ശേഖരിക്കുക.
പ്രവർത്തനം 3.1
- ഇരുമ്പ്, ചെമ്പ്, അലുമിനിയം, മഗ്നീഷ്യം എന്നിവയുടെ സാമ്പിളുകൾ എടുക്കുക. ഓരോ സാമ്പിളിന്റെയും രൂപം ശ്രദ്ധിക്കുക.
- ഓരോ സാമ്പിളിന്റെയും ഉപരിതലം സാൻഡ് പേപ്പർ ഉപയോഗിച്ച് തടവി വൃത്തിയാക്കി അവയുടെ രൂപം വീണ്ടും ശ്രദ്ധിക്കുക.
ലോഹങ്ങൾ, അവയുടെ ശുദ്ധാവസ്ഥയിൽ, മിനുസമാർന്ന ഉപരിതലം ഉള്ളതാണ്. ഈ ഗുണത്തെ ലോഹീയ തിളക്കം എന്ന് വിളിക്കുന്നു.
പ്രവർത്തനം 3.2
ഇരുമ്പ്, ചെമ്പ്, അലുമിനിയം, മഗ്നീഷ്യം എന്നിവയുടെ ചെറിയ കഷണങ്ങൾ എടുക്കുക. ഈ ലോഹങ്ങൾ ഒരു മൂർച്ചയുള്ള കത്തിയുപയോഗിച്ച് മുറിക്കാൻ ശ്രമിച്ച് നിങ്ങളുടെ നിരീക്ഷണങ്ങൾ രേഖപ്പെടുത്തുക.
ഒരു ജോടി ടോങ്ങുകൾ ഉപയോഗിച്ച് സോഡിയം ലോഹത്തിന്റെ ഒരു കഷണം പിടിക്കുക.
മുന്നറിയിപ്പ്: സോഡിയം ലോഹം എപ്പോഴും ശ്രദ്ധയോടെ കൈകാര്യം ചെയ്യുക. ഒരു ഫിൽട്ടർ പേപ്പറിന്റെ മടക്കുകൾക്കിടയിൽ അമർത്തി വരണ്ടതാക്കുക.
അത് ഒരു വാച്ച് ഗ്ലാസിൽ വെച്ച് ഒരു കത്തി ഉപയോഗിച്ച് മുറിക്കാൻ ശ്രമിക്കുക.
നിങ്ങൾ എന്താണ് നിരീക്ഷിക്കുന്നത്?
ലോഹങ്ങൾ പൊതുവേ കഠിനമാണെന്ന് നിങ്ങൾ കാണും. കാഠിന്യം ലോഹം തോറും വ്യത്യാസപ്പെട്ടിരിക്കുന്നു.
പ്രവർത്തനം 3.3
- ഇരുമ്പ്, നാകം, ഈയം, ചെമ്പ് എന്നിവയുടെ കഷണങ്ങൾ എടുക്കുക.
- ഏതെങ്കിലും ഒരു ലോഹം ഒരു ഇരുമ്പ് ബ്ലോക്കിൽ വെച്ച് ഒരു ചുറ്റിക ഉപയോഗിച്ച് നാലോ അഞ്ചോ തവണ അടിക്കുക. നിങ്ങൾ എന്താണ് നിരീക്ഷിക്കുന്നത്?
- മറ്റ് ലോഹങ്ങൾ ഉപയോഗിച്ച് ആവർത്തിക്കുക.
- ഈ ലോഹങ്ങളുടെ ആകൃതിയിലുണ്ടാകുന്ന മാറ്റം രേഖപ്പെടുത്തുക.
ചില ലോഹങ്ങളെ നേർത്ത തകിടുകളാക്കി അടിക്കാമെന്ന് നിങ്ങൾ കാണും. ഈ ഗുണത്തെ വ്യാപനശേഷി (Malleability) എന്ന് വിളിക്കുന്നു. സ്വർണ്ണവും വെള്ളിയും ഏറ്റവും കൂടുതൽ വ്യാപനശേഷിയുള്ള ലോഹങ്ങളാണെന്ന് നിങ്ങൾക്കറിയാമോ?
പ്രവർത്തനം 3.4
- നിങ്ങൾ ദൈനംദിന ജീവിതത്തിൽ കണ്ടിട്ടുള്ള കമ്പികൾ ഉണ്ടാക്കുന്ന ലോഹങ്ങളുടെ പട്ടിക തയ്യാറാക്കുക.
ലോഹങ്ങളെ നേർത്ത കമ്പികളാക്കി വലിക്കാനുള്ള കഴിവിനെ വലിച്ചുനീട്ടാനുള്ള ശേഷി (Ductility) എന്ന് വിളിക്കുന്നു. സ്വർണ്ണം ഏറ്റവും കൂടുതൽ വലിച്ചുനീട്ടാനുള്ള ശേഷിയുള്ള ലോഹമാണ്. ഒരു ഗ്രാം സ്വർണ്ണത്തിൽ നിന്ന് ഏകദേശം $2 km$ നീളമുള്ള ഒരു കമ്പി വലിക്കാമെന്ന് അറിയുമ്പോൾ നിങ്ങൾ അത്ഭുതപ്പെടും.
അവയുടെ വ്യാപനശേഷിയും വലിച്ചുനീട്ടാനുള്ള ശേഷിയും കാരണം തന്നെയാണ് ലോഹങ്ങൾക്ക് നമ്മുടെ ആവശ്യങ്ങൾക്കനുസരിച്ച് വ്യത്യസ്ത ആകൃതികൾ നൽകാൻ കഴിയുന്നത്.
പാചക പാത്രങ്ങൾ നിർമ്മിക്കാൻ ഉപയോഗിക്കുന്ന ചില ലോഹങ്ങളുടെ പേര് നിങ്ങൾക്ക് പറയാമോ? ഈ ലോഹങ്ങൾ പാത്രങ്ങൾ നിർമ്മിക്കാൻ എന്തുകൊണ്ടാണ് ഉപയോഗിക്കുന്നതെന്ന് നിങ്ങൾക്കറിയാമോ? ഉത്തരം കണ്ടെത്താൻ നമുക്ക് ഇനിപ്പറയുന്ന പ്രവർത്തനം ചെയ്യാം.
പ്രവർത്തനം 3.5
- ഒരു അലുമിനിയം അല്ലെങ്കിൽ ചെമ്പ് കമ്പി എടുക്കുക. ചിത്രം 3.1-ൽ കാണിച്ചിരിക്കുന്നതുപോലെ ഈ കമ്പി ഒരു സ്റ്റാൻഡിൽ ഘടിപ്പിക്കുക.
- മെഴുക് ഉപയോഗിച്ച് കമ്പിയുടെ സ്വതന്ത്ര അറ്റത്ത് ഒരു പിൻ ഘടിപ്പിക്കുക.
- അത് ഘടിപ്പിച്ചിരിക്കുന്ന സ്ഥലത്തിനടുത്ത് ഒരു സ്പിരിറ്റ് ലാമ്പ്, മെഴുകുതിരി അല്ലെങ്കിൽ ബർണർ ഉപയോഗിച്ച് കമ്പി ചൂടാക്കുക.
- കുറച്ച് സമയത്തിന് ശേഷം നിങ്ങൾ എന്താണ് നിരീക്ഷിക്കുന്നത്?
- നിങ്ങളുടെ നിരീക്ഷണങ്ങൾ രേഖപ്പെടുത്തുക. ലോഹ കമ്പി ഉരുകുന്നുണ്ടോ?
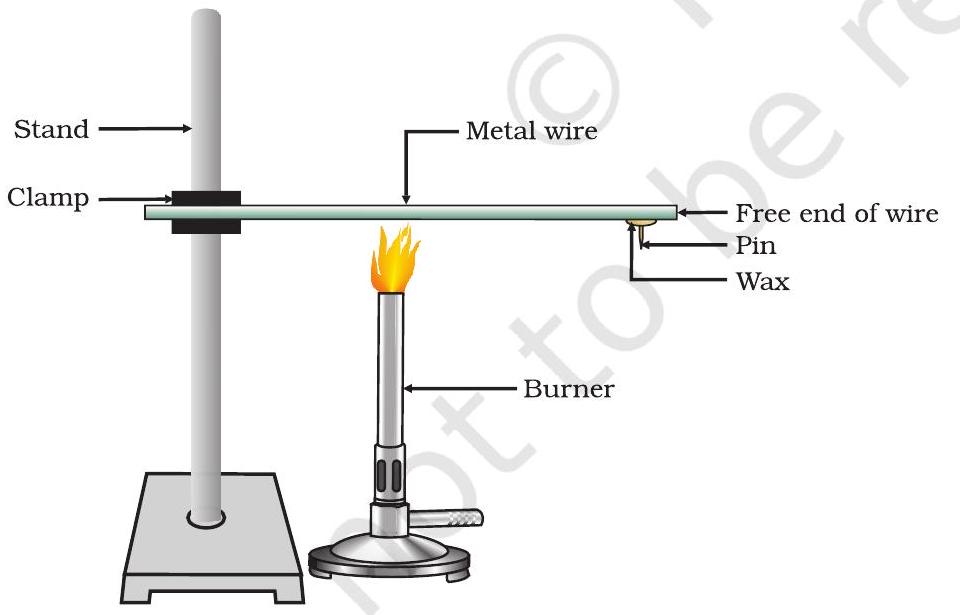
ചിത്രം 3.1 ലോഹങ്ങൾ താപത്തിന്റെ നല്ല ചാലകങ്ങളാണ്.
മുകളിലെ പ്രവർത്തനം കാണിക്കുന്നത് ലോഹങ്ങൾ താപത്തിന്റെ നല്ല ചാലകങ്ങളാണെന്നും അവയ്ക്ക് ഉയർന്ന ദ്രവണാങ്കങ്ങളുണ്ടെന്നുമാണ്. താപത്തിന്റെ ഏറ്റവും നല്ല ചാലകങ്ങൾ വെള്ളിയും ചെമ്പുമാണ്. ഈയവും പാരദവും താരതമ്യേന മോശം താപ ചാലകങ്ങളാണ്.
ലോഹങ്ങൾ വൈദ്യുതിയും ചാലകം ആണോ? നമുക്ക് അറിയാം.
പ്രവർത്തനം 3.6
- ചിത്രം 3.2-ൽ കാണിച്ചിരിക്കുന്നതുപോലെ ഒരു വൈദ്യുത സർക്യൂട്ട് സജ്ജമാക്കുക.
- പരീക്ഷിക്കേണ്ട ലോഹം $A$, $B$ എന്നീ ടെർമിനലുകൾക്കിടയിലുള്ള സർക്യൂട്ടിൽ കാണിച്ചിരിക്കുന്നതുപോലെ വയ്ക്കുക.
- ബൾബ് പ്രകാശിക്കുന്നുണ്ടോ? ഇത് എന്താണ് സൂചിപ്പിക്കുന്നത്?
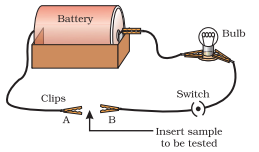
ചിത്രം 3.2 ലോഹങ്ങൾ വൈദ്യുതിയുടെ നല്ല ചാലകങ്ങളാണ്.
നിങ്ങളുടെ വീടുകളിൽ കറന്റ് വഹിക്കുന്ന വയറുകൾക്ക് പോളിവിനൈൽ ക്ലോറൈഡ് (PVC) അല്ലെങ്കിൽ റബ്ബർ പോലുള്ള വസ്തുവിന്റെ ഒരു പാളി ഉണ്ടെന്ന് നിങ്ങൾ കണ്ടിട്ടുണ്ടാകും. വൈദ്യുത വയറുകൾ അത്തരം പദാർത്ഥങ്ങൾ കൊണ്ട് പൂശിയിരിക്കുന്നത് എന്തുകൊണ്ടാണ്?
ലോഹങ്ങൾ ഒരു കഠിനമായ ഉപരിതലത്തിൽ അടിക്കുമ്പോൾ എന്ത് സംഭവിക്കും? അവ ഒരു ശബ്ദം ഉണ്ടാക്കുമോ? ഒരു കഠിനമായ ഉപരിതലത്തിൽ അടിക്കുമ്പോൾ ശബ്ദം ഉണ്ടാക്കുന്ന ലോഹങ്ങളെ ശബ്ദോത്പാദകം (Sonorous) എന്ന് പറയുന്നു. സ്കൂൾ മണികൾ ലോഹങ്ങൾ കൊണ്ടാണ് നിർമ്മിക്കുന്നതെന്ന് ഇപ്പോൾ നിങ്ങൾക്ക് പറയാമോ?
3.1.2 അലോഹങ്ങൾ
മുമ്പത്തെ ക്ലാസ്സിൽ ലോഹങ്ങളുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ വളരെ കുറച്ച് അലോഹങ്ങൾ മാത്രമേ ഉള്ളൂ എന്ന് നിങ്ങൾ പഠിച്ചിട്ടുണ്ട്. അലോഹങ്ങളുടെ ചില ഉദാഹരണങ്ങൾ കാർബൺ, സൾഫർ, അയോഡിൻ, ഓക്സിജൻ, ഹൈഡ്രജൻ മുതലായവയാണ്. ദ്രാവകമായ ബ്രോമിൻ ഒഴികെയുള്ള അലോഹങ്ങൾ ഖരങ്ങളോ വാതകങ്ങളോ ആണ്.
അലോഹങ്ങൾക്കും ലോഹങ്ങളുടെ ഭൗതിക ഗുണങ്ങൾക്ക് സമാനമായ ഭൗതിക ഗുണങ്ങൾ ഉണ്ടോ? നമുക്ക് അറിയാം.
പ്രവർത്തനം 3.7
- കാർബൺ (കൽക്കരി അല്ലെങ്കിൽ ഗ്രാഫൈറ്റ്), സൾഫർ, അയോഡിൻ എന്നിവയുടെ സാമ്പിളുകൾ ശേഖരിക്കുക.
- ഈ അലോഹങ്ങൾ ഉപയോഗിച്ച് 3.1 മുതൽ 3.4 വരെയും 3.6 ഉം പ്രവർത്തനങ്ങൾ നടത്തി നിങ്ങളുടെ നിരീക്ഷണങ്ങൾ രേഖപ്പെടുത്തുക.
ലോഹങ്ങളെയും അലോഹങ്ങളെയും കുറിച്ചുള്ള നിങ്ങളുടെ നിരീക്ഷണങ്ങൾ പട്ടിക 3.1-ൽ സമാഹരിക്കുക.
പട്ടിക 3.1
| മൂലകം | ചിഹ്നം | ഉപരിതലത്തിന്റെ തരം | കാഠിന്യം | വ്യാപനശേഷി | വലിച്ചുനീട്ടാനുള്ള ശേഷി | വൈദ്യുതി ചാലകം | ശബ്ദോത്പാദകം |
|---|---|---|---|---|---|---|---|
പട്ടിക 3.1-ൽ രേഖപ്പെടുത്തിയ നിരീക്ഷണങ്ങളുടെ അടിസ്ഥാനത്തിൽ, ക്ലാസ്സിൽ ലോഹങ്ങളുടെയും അലോഹങ്ങളുടെയും പൊതുവായ ഭൗതിക ഗുണങ്ങളെക്കുറിച്ച് ചർച്ച ചെയ്യുക. അവയുടെ ഭൗതിക ഗുണങ്ങൾ മാത്രം അടിസ്ഥാനമാക്കി മൂലകങ്ങളെ തരംതിരിക്കാൻ കഴിയില്ലെന്ന് നിങ്ങൾ നിഗമനത്തിലെത്തിയിരിക്കണം, കാരണം പല ഒഴിവാക്കലുകളും ഉണ്ട്. ഉദാഹരണത്തിന് -
(i) പാരദം ഒഴികെയുള്ള എല്ലാ ലോഹങ്ങളും മുറിയുടെ താപനിലയിൽ ഖരാവസ്ഥയിലാണ് കാണപ്പെടുന്നത്. പ്രവർത്തനം 3.5-ൽ, ലോഹങ്ങൾക്ക് ഉയർന്ന ദ്രവണാങ്കങ്ങളുണ്ടെന്ന് നിങ്ങൾ നിരീക്ഷിച്ചിട്ടുണ്ട്, പക്ഷേ ഗാലിയത്തിനും സീസിയത്തിനും വളരെ കുറഞ്ഞ ദ്രവണാങ്കങ്ങളുണ്ട്. നിങ്ങളുടെ ഉള്ളങ്കയ്യിൽ വെച്ചാൽ ഈ രണ്ട് ലോഹങ്ങളും ഉരുകും.
(ii) അയോഡിൻ ഒരു അലോഹമാണ്, പക്ഷേ അതിന് തിളക്കമുണ്ട്.
(iii) കാർബൺ വ്യത്യസ്ത രൂപങ്ങളിൽ നിലനിൽക്കാൻ കഴിയുന്ന ഒരു അലോഹമാണ്. ഓരോ രൂപത്തെയും അലോട്രോപ്പ് എന്ന് വിളിക്കുന്നു. കാർബണിന്റെ ഒരു അലോട്രോപ്പായ വജ്രം, അറിയപ്പെടുന്ന ഏറ്റവും കഠിനമായ പ്രകൃതിദത്ത പദാർത്ഥമാണ്, കൂടാതെ വളരെ ഉയർന്ന ദ്രവണാങ്കവും തിളനിലയും ഉണ്ട്. കാർബണിന്റെ മറ്റൊരു അലോട്രോപ്പായ ഗ്രാഫൈറ്റ്, വൈദ്യുതിയുടെ ഒരു ചാലകമാണ്.
(iv) ആൽക്കലി ലോഹങ്ങൾ (ലിഥിയം, സോഡിയം, പൊട്ടാസ്യം) വളരെ മൃദുവായതിനാൽ ഒരു കത്തി ഉപയോഗിച്ച് മുറിക്കാൻ കഴിയും. അവയ്ക്ക് കുറഞ്ഞ സാന്ദ്രതയും കുറഞ്ഞ ദ്രവണാങ്കങ്ങളും ഉണ്ട്.
മൂലകങ്ങളെ അവയുടെ രാസ ഗുണങ്ങളുടെ അടിസ്ഥാനത്തിൽ കൂടുതൽ വ്യക്തമായി ലോഹങ്ങളായും അലോഹങ്ങളായും തരംതിരിക്കാം.
പ്രവർത്തനം 3.8
- ഒരു മഗ്നീഷ്യം റിബ്ബണും കുറച്ച് സൾഫർ പൊടിയും എടുക്കുക.
- മഗ്നീഷ്യം റിബ്ബൺ കത്തിക്കുക. രൂപപ്പെടുന്ന ചാരം ശേഖരിച്ച് വെള്ളത്തിൽ ലയിപ്പിക്കുക.
- ഫലമായുണ്ടാകുന്ന ലായനി ചുവപ്പും നീലയുമുള്ള ലിറ്റ്മസ് പേപ്പർ ഉപയോഗിച്ച് പരീക്ഷിക്കുക.
- മഗ്നീഷ്യം കത്തിക്കുമ്പോൾ രൂപപ്പെടുന്ന ഉൽപ്പന്നം അമ്ലീയമാണോ അല്ലെങ്കിൽ ക്ഷാരമാണോ?
- ഇപ്പോൾ സൾഫർ പൊടി കത്തിക്കുക. ഉത്പാദിപ്പിക്കുന്ന പുക ശേഖരിക്കാൻ കത്തിക്കുന്ന സൾഫറിന് മുകളിൽ ഒരു ടെസ്റ്റ് ട്യൂബ് വയ്ക്കുക.
- മുകളിലുള്ള ടെസ്റ്റ് ട്യൂബിലേക്ക് കുറച്ച് വെള്ളം ചേർത്ത് കുലുക്കുക.
- ഈ ലായനി നീലയും ചുവപ്പുമുള്ള ലിറ്റ്മസ് പേപ്പർ ഉപയോഗിച്ച് പരീക്ഷിക്കുക.
- സൾഫർ കത്തിക്കുമ്പോൾ രൂപപ്പെടുന്ന ഉൽപ്പന്നം അമ്ലീയമാണോ അല്ലെങ്കിൽ ക്ഷാരമാണോ?
- ഈ പ്രതികരണങ്ങൾക്കായി നിങ്ങൾക്ക് സമവാക്യങ്ങൾ എഴുതാമോ?
മിക്ക അലോഹങ്ങളും വെള്ളത്തിൽ ലയിക്കുമ്പോൾ അമ്ലീയ ഓക്സൈഡുകൾ ഉത്പാദിപ്പിക്കുന്നു. മറുവശത്ത്, മിക്ക ലോഹങ്ങളും, ക്ഷാര ഓക്സൈഡുകൾ നൽകുന്നു. ഈ ലോഹ ഓക്സൈഡുകളെക്കുറിച്ച് അടുത്ത ഭാഗത്ത് നിങ്ങൾ കൂടുതൽ പഠിക്കും.
3.2 ലോഹങ്ങളുടെ രാസ ഗുണങ്ങൾ
ലോഹങ്ങളുടെ രാസ ഗുണങ്ങളെക്കുറിച്ച് ഇനിപ്പറയുന്ന 3.2.1 മുതൽ 3.2.4 വരെയുള്ള ഭാഗങ്ങളിൽ നിന്ന് നമുക്ക് പഠിക്കാം. ഇതിനായി, ഇനിപ്പറയുന്ന ലോഹങ്ങളുടെ സാമ്പിളുകൾ ശേഖരിക്കുക: അലുമിനിയം, ചെമ്പ്, ഇരുമ്പ്, ഈയം, മഗ്നീഷ്യം, നാകം, സോഡിയം.
3.2.1 ലോഹങ്ങൾ വായുവിൽ കത്തിക്കുമ്പോൾ എന്ത് സംഭവിക്കും?
പ്രവർത്തനം 3.8-ൽ മഗ്നീഷ്യം വായുവിൽ ഒരു തിളക്കമുള്ള വെളുത്ത ജ്വാലയോടെ കത്തുന്നത് നിങ്ങൾ കണ്ടിട്ടുണ്ട്. എല്ലാ ലോഹങ്ങളും ഒരേ രീതിയിൽ പ്രതികരിക്കുമോ? ഇനിപ്പറയുന്ന പ്രവർത്തനം നടത്തി നമുക്ക് പരിശോധിക്കാം.
പ്രവർത്തനം 3.9
മുന്നറിയിപ്പ്: ഇനിപ്പറയുന്ന പ്രവർത്തനത്തിന് അധ്യാപകന്റെ സഹായം ആവശ്യമാണ്. വിദ്യാർത്ഥികൾ കണ്ണ് സംരക്ഷണം ധരിക്കുന്നത് നല്ലതാണ്.
- മുകളിൽ എടുത്ത സാമ്പിളുകളിൽ ഏതെങ്കിലും ഒന്ന് ഒരു ജോടി ടോങ്ങുകൾ ഉപയോഗിച്ച് പിടിച്ച് ഒരു ജ്വാലയ്ക്ക് മുകളിൽ കത്തിക്കാൻ ശ്രമിക്കുക. മറ്റ് ലോഹ സാമ്പിളുകൾ ഉപയോഗിച്ച് ആവർത്തിക്കുക.
- രൂപപ്പെട്ടാൽ ഉൽപ്പന്നം ശേഖരിക്കുക.
- ഉൽപ്പന്നങ്ങളും ലോഹ ഉപരിതലവും തണുപ്പിക്കട്ടെ.
- ഏത് ലോഹങ്ങളാണ് എളുപ്പത്തിൽ കത്തുന്നത്?
- ലോഹം കത്തുമ്പോൾ നിങ്ങൾ ഏത് ജ്വാലാ നിറം നിരീക്ഷിച്ചു?
- കത്തിച്ചതിന് ശേഷം ലോഹ ഉപരിതലം എങ്ങനെ കാണപ്പെടുന്നു?
- ഓക്സിജനോടുള്ള അവയുടെ പ്രതിപ്രവർത്തനശേഷിയുടെ കുറയുന്ന ക്രമത്തിൽ ലോഹങ്ങൾ ക്രമീകരിക്കുക.
- ഉൽപ്പന്നങ്ങൾ വെള്ളത്തിൽ ലയിക്കുന്നുണ്ടോ?
ഏകദേശം എല്ലാ ലോഹങ്ങളും ഓക്സിജനുമായി സംയോജിച്ച് ലോഹ ഓക്സൈഡുകൾ രൂപപ്പെടുത്തുന്നു.
ലോഹം + ഓക്സിജൻ $\rightarrow$ ലോഹ ഓക്സൈഡ്
ഉദാഹരണത്തിന്, ചെമ്പ് വായുവിൽ ചൂടാക്കുമ്പോൾ, അത് ഓക്സിജനുമായി സംയോജിച്ച് കറുത്ത ഓക്സൈഡായ ചെമ്പ്(II) ഓക്സൈഡ് രൂപപ്പെടുത്തുന്നു.
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
അതുപോലെ, അലുമിനിയം അലുമിനിയം ഓക്സൈഡ് രൂപപ്പെടുത്തുന്നു.
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
അദ്ധ്യായം 2-ൽ നിന്ന് ഓർക്കുക, ചെമ്പ് ഓക്സൈഡ് ഹൈഡ്രോക്ലോറിക് ആസിഡുമായി എങ്ങനെ പ്രതിപ്രവർത്തിക്കുന്നു. ലോഹ ഓക്സൈഡുകൾ അടിസ്ഥാനപരമായ സ്വഭാവമുള്ളതാണെന്ന് നമ്മൾ പഠിച്ചിട്ടുണ്ട്. എന്നാൽ അലുമിനിയം ഓക്സൈഡ്, നാക ഓക്സൈഡ് തുടങ്ങിയ ചില ലോഹ ഓക്സൈഡുകൾ അമ്ലീയവും അടിസ്ഥാനപരവുമായ സ്വഭാവം കാണിക്കുന്നു. അമ്ലങ്ങളുമായും ക്ഷാരങ്ങളുമായും പ്രതിപ്രവർത്തിച്ച് ലവണങ്ങളും വെള്ളവും ഉത്പാദിപ്പിക്കുന്ന അത്തരം ലോഹ ഓക്സൈഡുകളെ ഉഭയസ്വഭാവ ഓക്സൈഡുകൾ (Amphoteric oxides) എന്ന് അറിയപ്പെടുന്നു. അലുമിനിയം ഓക്സൈഡ് ഇനിപ്പറയുന്ന രീതിയിൽ അമ്ലങ്ങളുമായും ക്ഷാരങ്ങളുമായും പ്രതിപ്രവർത്തിക്കുന്നു -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
മിക്ക ലോഹ ഓക്സൈഡുകളും വെള്ളത്തിൽ അലിയില്ല, പക്ഷേ ഇവയിൽ ചിലത് വെള്ളത്തിൽ ലയിച്ച് ആൽക്കലികൾ രൂപപ്പെടുത്തുന്നു. സോഡിയം ഓക്സൈഡും പൊട്ടാസ്യം ഓക്സൈഡും വെള്ളത്തിൽ ലയിച്ച് ഇനിപ്പറയുന്ന രീതിയിൽ ആൽക്കലികൾ ഉത്പാദിപ്പിക്കുന്നു -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
എല്ലാ ലോഹങ്ങളും ഓക്സിജനുമായി ഒരേ നിരക്കിൽ പ്രതിപ്രവർത്തിക്കുന്നില്ലെന്ന് പ്രവർത്തനം 3.9-ൽ നമ്മൾ നിരീക്ഷിച്ചിട്ടുണ്ട്. വ്യത്യസ്ത ലോഹങ്ങൾ ഓക്സിജനോട് വ











