அத்தியாயம் 03 உலோகங்களும் அலோகங்களும்
IX ஆம் வகுப்பில் நீங்கள் பல்வேறு தனிமங்களைப் பற்றி கற்றுக்கொண்டீர்கள். தனிமங்களை அவற்றின் பண்புகளின் அடிப்படையில் உலோகங்கள் அல்லது அலோகங்கள் என வகைப்படுத்தலாம் என்பதை நீங்கள் கண்டிருக்கிறீர்கள்.
- உங்கள் அன்றாட வாழ்வில் உலோகங்கள் மற்றும் அலோகங்களின் சில பயன்பாடுகளைப் பற்றி சிந்தியுங்கள்.
- தனிமங்களை உலோகங்கள் அல்லது அலோகங்களாக வகைப்படுத்தும் போது நீங்கள் எந்தப் பண்புகளைப் பற்றி சிந்தித்தீர்கள்?
- இந்தப் பண்புகள் தனிமங்களின் பயன்பாடுகளுடன் எவ்வாறு தொடர்புடையவை?
இந்தப் பண்புகளில் சிலவற்றை விரிவாகப் பார்ப்போம்.
3.1 இயற்பியல் பண்புகள்
3.1.1 உலோகங்கள்
பொருட்களை தொகுக்கத் தொடங்க எளிதான வழி, அவற்றின் இயற்பியல் பண்புகளை ஒப்பிடுவதாகும். பின்வரும் செயல்பாடுகளின் உதவியுடன் இதைப் படிப்போம். 3.1 முதல் 3.6 வரையிலான செயல்பாடுகளைச் செய்வதற்கு, பின்வரும் உலோகங்களின் மாதிரிகளைச் சேகரிக்கவும் - இரும்பு, தாமிரம், அலுமினியம், மெக்னீசியம், சோடியம், ஈயம், துத்தநாகம் மற்றும் எளிதில் கிடைக்கும் வேறு எந்த உலோகமும்.
செயல்பாடு 3.1
- இரும்பு, தாமிரம், அலுமினியம் மற்றும் மெக்னீசியம் ஆகியவற்றின் மாதிரிகளை எடுத்துக் கொள்ளுங்கள். ஒவ்வொரு மாதிரியின் தோற்றத்தையும் கவனிக்கவும்.
- ஒவ்வொரு மாதிரியின் மேற்பரப்பையும் மணல் தாளால் தேய்த்து சுத்தம் செய்து, அவற்றின் தோற்றத்தை மீண்டும் கவனிக்கவும்.
உலோகங்கள், தூய நிலையில், பளபளப்பான மேற்பரப்பைக் கொண்டிருக்கும். இந்தப் பண்பு உலோகப் பிரகாசம் என்று அழைக்கப்படுகிறது.
செயல்பாடு 3.2
இரும்பு, தாமிரம், அலுமினியம் மற்றும் மெக்னீசியம் ஆகியவற்றின் சிறிய துண்டுகளை எடுத்துக் கொள்ளுங்கள். இந்த உலோகங்களைக் கூர்மையான கத்தியால் வெட்ட முயற்சித்து உங்கள் கணிப்புகளைக் குறிக்கவும்.
சோடியம் உலோகத்தின் ஒரு துண்டை இடுக்கிக் குறடு கொண்டு பிடித்துக் கொள்ளுங்கள்.
எச்சரிக்கை: சோடியம் உலோகத்தை எப்போதும் கவனத்துடன் கையாளவும். வடிகட்டித் தாளின் மடிப்புகளுக்கு இடையே அழுத்தி உலர்த்தவும்.
அதை ஒரு வாட்ச் கண்ணாடியில் வைத்து, கத்தியால் வெட்ட முயற்சிக்கவும்.
நீங்கள் என்ன கவனிக்கிறீர்கள்?
உலோகங்கள் பொதுவாக கடினமானவை என்பதை நீங்கள் காண்பீர்கள். கடினத்தன்மை உலோகத்திற்கு உலோகம் மாறுபடும்.
செயல்பாடு 3.3
- இரும்பு, துத்தநாகம், ஈயம் மற்றும் தாமிரம் ஆகியவற்றின் துண்டுகளை எடுத்துக் கொள்ளுங்கள்.
- எந்த ஒரு உலோகத்தையும் இரும்புத் துண்டின் மீது வைத்து, சுத்தியலால் நான்கு அல்லது ஐந்து முறை அடிக்கவும். நீங்கள் என்ன கவனிக்கிறீர்கள்?
- மற்ற உலோகங்களுடன் மீண்டும் செய்யவும்.
- இந்த உலோகங்களின் வடிவத்தில் ஏற்படும் மாற்றத்தைப் பதிவு செய்யவும்.
சில உலோகங்களை மெல்லிய தகடுகளாக அடிக்க முடியும் என்பதை நீங்கள் காண்பீர்கள். இந்தப் பண்பு நீர்த்தன்மை (Malleability) என்று அழைக்கப்படுகிறது. தங்கமும் வெள்ளியும் மிகவும் நீர்த்தன்மை கொண்ட உலோகங்கள் என்பது உங்களுக்குத் தெரியுமா?
செயல்பாடு 3.4
- உங்கள் அன்றாட வாழ்வில் நீங்கள் பார்த்திருக்கும் கம்பிகள் எந்த எந்த உலோகங்களால் ஆனவை என பட்டியலிடுங்கள்.
உலோகங்கள் மெல்லிய கம்பிகளாக இழுக்கப்படும் திறன் இழுவைத்தன்மை (Ductility) என்று அழைக்கப்படுகிறது. தங்கம் மிகவும் இழுவைத்தன்மை கொண்ட உலோகமாகும். ஒரு கிராம் தங்கத்திலிருந்து சுமார் $2 km$ நீளமுள்ள கம்பி இழுக்கப்பட முடியும் என்பதை அறிந்து நீங்கள் ஆச்சரியப்படுவீர்கள்.
அவற்றின் நீர்த்தன்மை மற்றும் இழுவைத்தன்மை காரணமாகவே, உலோகங்களுக்கு நமது தேவைகளுக்கேற்ப வெவ்வேறு வடிவங்களைக் கொடுக்க முடியும்.
சமையல் பாத்திரங்கள் தயாரிக்கப் பயன்படும் சில உலோகங்களின் பெயர்களைச் சொல்ல முடியுமா? இந்த உலோகங்கள் பாத்திரங்கள் தயாரிக்கப் பயன்படுவதற்கான காரணம் உங்களுக்குத் தெரியுமா? விடையைக் கண்டறிய பின்வரும் செயல்பாட்டைச் செய்வோம்.
செயல்பாடு 3.5
- ஒரு அலுமினியம் அல்லது தாமிரக் கம்பியை எடுத்துக் கொள்ளுங்கள். படம் 3.1 இல் காட்டப்பட்டுள்ளபடி, இந்தக் கம்பியை ஒரு நிலைப்பாட்டில் இறுக்கவும்.
- கம்பியின் கட்டற்ற முனையில் மெழுகு பயன்படுத்தி ஒரு ஊசியைப் பொருத்தவும்.
- அது இறுக்கப்பட்ட இடத்திற்கு அருகில், ஒரு ஆவிவிளக்கு, மெழுகுவர்த்தி அல்லது பர்னர் மூலம் கம்பியை சூடாக்கவும்.
- சிறிது நேரம் கழித்து நீங்கள் என்ன கவனிக்கிறீர்கள்?
- உங்கள் கணிப்புகளைக் குறிக்கவும். உலோகக் கம்பி உருகுகிறதா?
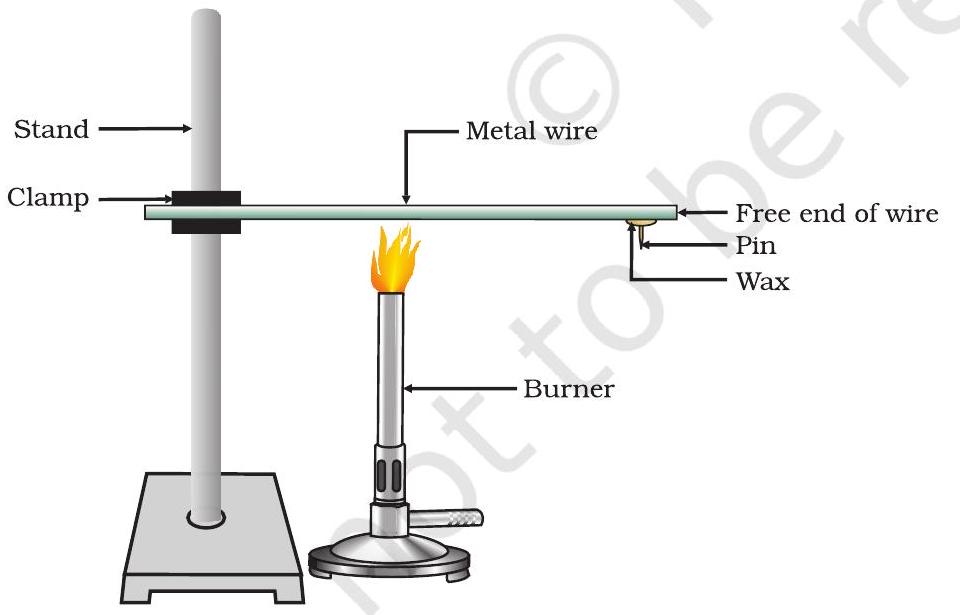
படம் 3.1 உலோகங்கள் வெப்பத்தின் நல்ல கடத்திகள்.
மேலே உள்ள செயல்பாடு, உலோகங்கள் வெப்பத்தின் நல்ல கடத்திகள் மற்றும் அதிக உருகு நிலைகளைக் கொண்டுள்ளன என்பதைக் காட்டுகிறது. வெப்பத்தின் சிறந்த கடத்திகள் வெள்ளி மற்றும் தாமிரம் ஆகும். ஈயம் மற்றும் பாதரசம் ஒப்பீட்டளவில் மோசமான வெப்பக் கடத்திகள் ஆகும்.
உலோகங்களும் மின்சாரத்தைக் கடத்துமா? கண்டுபிடிப்போம்.
செயல்பாடு 3.6
- படம் 3.2 இல் காட்டப்பட்டுள்ளபடி ஒரு மின்சுற்றை அமைக்கவும்.
- சோதிக்க வேண்டிய உலோகத்தை $A$ மற்றும் $B$ முனையங்களுக்கு இடையே சுற்றில் காட்டப்பட்டுள்ளபடி வைக்கவும்.
- பல்பு ஒளிர்கிறதா? இது எதைக் குறிக்கிறது?
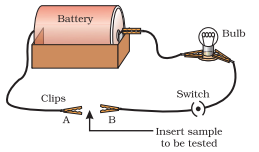
படம் 3.2 உலோகங்கள் மின்சாரத்தின் நல்ல கடத்திகள்.
உங்கள் வீடுகளில் மின்னோட்டத்தைச் சுமந்து செல்லும் கம்பிகள் பாலிவினைல் குளோரைடு (PVC) அல்லது ரப்பர் போன்ற பொருளால் பூசப்பட்டிருக்கும் என்பதை நீங்கள் கண்டிருக்கலாம். மின்சார கம்பிகள் ஏன் அத்தகைய பொருட்களால் பூசப்படுகின்றன?
உலோகங்கள் கடினமான மேற்பரப்பைத் தாக்கும் போது என்ன நடக்கும்? அவை ஒலியை உருவாக்குமா? கடினமான மேற்பரப்பைத் தாக்கும் போது ஒலியை உருவாக்கும் உலோகங்கள் ஒலிக்கும் பண்பு (Sonorous) உடையவை என்று கூறப்படுகிறது. பள்ளி மணிகள் ஏன் உலோகங்களால் செய்யப்படுகின்றன என்று இப்போது நீங்கள் சொல்ல முடியுமா?
3.1.2 அலோகங்கள்
முந்தைய வகுப்பில், உலோகங்களுடன் ஒப்பிடும்போது மிகச் சில அலோகங்கள் மட்டுமே உள்ளன என்பதை நீங்கள் கற்றுக்கொண்டீர்கள். அலோகங்களின் சில எடுத்துக்காட்டுகள் கார்பன், கந்தகம், அயோடின், ஆக்ஸிஜன், ஹைட்ரஜன் போன்றவை. அலோகங்கள் திண்மங்களாகவோ அல்லது வாயுக்களாகவோ உள்ளன, திரவமான புரோமின் தவிர.
அலோகங்களுக்கும் உலோகங்களைப் போன்ற இயற்பியல் பண்புகள் உள்ளதா? கண்டுபிடிப்போம்.
செயல்பாடு 3.7
- கார்பன் (நிலக்கரி அல்லது கிராஃபைட்), கந்தகம் மற்றும் அயோடின் ஆகியவற்றின் மாதிரிகளைச் சேகரிக்கவும்.
- இந்த அலோகங்களுடன் 3.1 முதல் 3.4 மற்றும் 3.6 செயல்பாடுகளை மேற்கொண்டு உங்கள் கணிப்புகளைப் பதிவு செய்யவும்.
உலோகங்கள் மற்றும் அலோகங்கள் தொடர்பான உங்கள் கணிப்புகளை அட்டவணை 3.1 இல் தொகுக்கவும்.
அட்டவணை 3.1
| தனிமம் | குறியீடு | மேற்பரப்பின் வகை | கடினத்தன்மை | நீர்த்தன்மை | இழுவைத்தன்மை | மின்சாரத்தைக் கடத்துதல் | ஒலிக்கும் பண்பு |
|---|---|---|---|---|---|---|---|
அட்டவணை 3.1 இல் பதிவு செய்யப்பட்ட கணிப்புகளின் அடிப்படையில், வகுப்பில் உலோகங்கள் மற்றும் அலோகங்களின் பொதுவான இயற்பியல் பண்புகளைப் பற்றி விவாதிக்கவும். பல விதிவிலக்குகள் இருப்பதால், தனிமங்களை அவற்றின் இயற்பியல் பண்புகளை மட்டுமே கொண்டு தொகுக்க முடியாது என்று நீங்கள் முடிவு செய்திருக்க வேண்டும். எடுத்துக்காட்டாக -
(i) பாதரசம் தவிர அனைத்து உலோகங்களும் அறை வெப்பநிலையில் திண்மங்களாக உள்ளன. செயல்பாடு 3.5 இல், உலோகங்கள் அதிக உருகு நிலைகளைக் கொண்டுள்ளன, ஆனால் காலியம் மற்றும் சீசியம் மிகக் குறைந்த உருகு நிலைகளைக் கொண்டுள்ளன என்பதை நீங்கள் கவனித்தீர்கள். இந்த இரண்டு உலோகங்களையும் உங்கள் உள்ளங்கையில் வைத்திருந்தால் உருகிவிடும்.
(ii) அயோடின் ஒரு அலோகம் ஆனால் அது பளபளப்பானது.
(iii) கார்பன் என்பது வெவ்வேறு வடிவங்களில் இருக்கக்கூடிய ஒரு அலோகமாகும். ஒவ்வொரு வடிவமும் அலோட்ரோப் என்று அழைக்கப்படுகிறது. கார்பனின் ஒரு அலோட்ரோப்பான வைரம், அறியப்பட்ட மிகக் கடினமான இயற்கைப் பொருள் மற்றும் மிக அதிக உருகு மற்றும் கொதி நிலைகளைக் கொண்டுள்ளது. கார்பனின் மற்றொரு அலோட்ரோப்பான கிராஃபைட், மின்சாரத்தின் கடத்தியாகும்.
(iv) கார உலோகங்கள் (லித்தியம், சோடியம், பொட்டாசியம்) மிகவும் மென்மையானவை, கத்தியால் வெட்டப்படக்கூடியவை. அவை குறைந்த அடர்த்தி மற்றும் குறைந்த உருகு நிலைகளைக் கொண்டுள்ளன.
தனிமங்களை அவற்றின் வேதிப் பண்புகளின் அடிப்படையில் உலோகங்கள் மற்றும் அலோகங்களாக மிகத் தெளிவாக வகைப்படுத்தலாம்.
செயல்பாடு 3.8
- ஒரு மெக்னீசியம் நாடாவையும் சிறிது கந்தகத் தூளையும் எடுத்துக் கொள்ளுங்கள்.
- மெக்னீசியம் நாடாவை எரிக்கவும். உருவாகும் சாம்பலைச் சேகரித்து நீரில் கரையச் செய்யவும்.
- விளைந்த கரைசலை சிவப்பு மற்றும் நீல லிட்மஸ் தாள்களால் சோதிக்கவும்.
- மெக்னீசியத்தை எரிப்பதால் உருவாகும் பொருள் அமிலமானதா அல்லது காரமானதா?
- இப்போது கந்தகத் தூளை எரிக்கவும். உருவாகும் புகையைச் சேகரிக்க எரியும் கந்தகத்தின் மேல் ஒரு சோதனைக் குழாயை வைக்கவும்.
- மேலே உள்ள சோதனைக் குழாயில் சிறிது நீர் சேர்த்து குலுக்கவும்.
- இந்தக் கரைசலை நீல மற்றும் சிவப்பு லிட்மஸ் தாள்களால் சோதிக்கவும்.
- கந்தகத்தை எரிப்பதால் உருவாகும் பொருள் அமிலமானதா அல்லது காரமானதா?
- இந்த வினைகளுக்கான சமன்பாடுகளை நீங்கள் எழுத முடியுமா?
பெரும்பாலான அலோகங்கள் நீரில் கரையும் போது அமில ஆக்சைடுகளைத் தருகின்றன. மறுபுறம், பெரும்பாலான உலோகங்கள், கார ஆக்சைடுகளைத் தருகின்றன. இந்த உலோக ஆக்சைடுகளைப் பற்றி அடுத்த பகுதியில் நீங்கள் மேலும் அறிவீர்கள்.
3.2 உலோகங்களின் வேதிப் பண்புகள்
3.2.1 முதல் 3.2.4 வரையிலான பின்வரும் பகுதிகளில் உலோகங்களின் வேதிப் பண்புகளைப் பற்றி கற்றுக்கொள்வோம். இதற்காக, பின்வரும் உலோகங்களின் மாதிரிகளைச் சேகரிக்கவும் - அலுமினியம், தாமிரம், இரும்பு, ஈயம், மெக்னீசியம், துத்தநாகம் மற்றும் சோடியம்.
3.2.1 உலோகங்கள் காற்றில் எரிக்கப்படும் போது என்ன நடக்கும்?
செயல்பாடு 3.8 இல் மெக்னீசியம் காற்றில் ஒரு கண்கூசும் வெள்ளை சுடருடன் எரிவதை நீங்கள் பார்த்தீர்கள். அனைத்து உலோகங்களும் ஒரே மாதிரியாக வினைபுரிகின்றனவா? பின்வரும் செயல்பாட்டைச் செய்வதன் மூலம் சரிபார்ப்போம்.
செயல்பாடு 3.9
எச்சரிக்கை: பின்வரும் செயல்பாட்டிற்கு ஆசிரியரின் உதவி தேவைப்படும். மாணவர்கள் கண் பாதுகாப்பு அணிவது நல்லது.
- மேலே எடுத்துக் கொள்ளப்பட்ட மாதிரிகளில் ஏதேனும் ஒன்றை இடுக்கிக் குறடு கொண்டு பிடித்து, ஒரு சுடரின் மேல் எரிக்க முயற்சிக்கவும். மற்ற உலோக மாதிரிகளுடன் மீண்டும் செய்யவும்.
- பொருள் உருவானால் அதைச் சேகரிக்கவும்.
- பொருட்களையும் உலோக மேற்பரப்பையும் குளிர்விக்கவும்.
- எந்த உலோகங்கள் எளிதில் எரிகின்றன?
- உலோகம் எரிந்தபோது நீங்கள் எந்த சுடர் நிறத்தைக் கவனித்தீர்கள்?
- எரிந்த பிறகு உலோக மேற்பரப்பு எவ்வாறு தோன்றுகிறது?
- ஆக்ஸிஜனுடனான அவற்றின் வினைத்திறன் குறைந்து வரும் வரிசையில் உலோகங்களை அமைக்கவும்.
- பொருட்கள் நீரில் கரையக்கூடியவையா?
கிட்டத்தட்ட அனைத்து உலோகங்களும் ஆக்ஸிஜனுடன் சேர்ந்து உலோக ஆக்சைடுகளை உருவாக்குகின்றன.
உலோகம் + ஆக்ஸிஜன் $\rightarrow$ உலோக ஆக்சைடு
எடுத்துக்காட்டாக, தாமிரம் காற்றில் சூடாக்கப்படும் போது, அது ஆக்ஸிஜனுடன் சேர்ந்து கருப்பு நிற ஆக்சைடான தாமிர(II) ஆக்சைடை உருவாக்குகிறது.
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
இதேபோல், அலுமினியம் அலுமினிய ஆக்சைடை உருவாக்குகிறது.
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
அத்தியாயம் 2 இலிருந்து நினைவுகூருங்கள், தாமிர ஆக்சைடு ஹைட்ரோகுளோரிக் அமிலத்துடன் எவ்வாறு வினைபுரிகிறது. உலோக ஆக்சைடுகள் கார இயல்புடையவை என்பதை நாம் கற்றுக்கொண்டோம். ஆனால் அலுமினிய ஆக்சைடு, துத்தநாக ஆக்சைடு போன்ற சில உலோக ஆக்சைடுகள் அமில மற்றும் கார இயல்புகளைக் காட்டுகின்றன. அமிலங்கள் மற்றும் காரங்கள் இரண்டுடனும் வினைபுரிந்து உப்புகள் மற்றும் நீரை உருவாக்கும் இத்தகைய உலோக ஆக்சைடுகள் இருமுனை ஆக்சைடுகள் (Amphoteric oxides) என்று அழைக்கப்படுகின்றன. அலுமினிய ஆக்சைடு பின்வரும் முறையில் அமிலங்கள் மற்றும் காரங்களுடன் வினைபுரிகிறது -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
பெரும்பாலான உலோக ஆக்சைடுகள் நீரில் கரையாதவை, ஆனால் இவற்றில் சில நீரில் கரைந்து காரங்களை உருவாக்குகின்றன. சோடியம் ஆக்சைடு மற்றும் பொட்டாசியம் ஆக்சைடு நீரில் கரைந்து பின்வருமாறு காரங்களை உருவாக்குகின்றன -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
செயல்பாடு 3.9 இல் நாம் கவனித்தபடி, அனைத்து உலோகங்களும் ஆக்ஸிஜனுடன் ஒரே விகிதத்தில் வினைபுரிவதில்லை. வெவ்வேறு உலோகங்கள் ஆக்ஸிஜனுடன் வெவ்வேறு வினைத்திறனைக் காட்டுகின்றன. பொட்டாசியம் மற்றும் சோடியம் போன்ற உலோகங்கள் மிகவும் கடுமையாக வினைபுரிந்து, திறந்தவெளியில் வைத்திருந்தால் தீப்பிடித்துக் கொள்ளும். எனவே, அவற்றைப் பாதுகாக்கவும் தற்செயல் தீயைத் தடுக்கவும், அவை மண்ணெண்ணெயில் மூழ்க வைக்கப்படுகின்றன. சாதாரண வெப்பநிலையில், மெக்னீசியம், அலுமினியம், துத்தநாகம், ஈயம் போன்ற உலோகங்களின் மேற்பரப்புகள் மெல்லிய ஆக்சைடு அடுக்கால் மூடப்பட்டிருக்கும். இந்தப் பாதுகாப்பு ஆக்சைடு அடுக்கு உலோகத்தை மேலும் ஆக்சிஜனேற்றத்திலிருந்து தடுக்கிறது. இரும்பு சூடாக்கப்படும் போது எரிவதில்லை, ஆனால் இரும்பு தூள் பர்னரின் சுடரில் தூவப்படும் போது கடுமையாக எரியும். தாமிரம் எரிவதில்லை, ஆனால் சூடான உலோகம் கருப்பு நிற தாமிர(II) ஆக்சைடு அடுக்கால் பூசப்பட்டிருக்கும். வெள்ளி மற்றும் தங்கம் அதிக வெப்பநிலையிலும் கூட ஆக்ஸிஜனுடன் வினைபுரிவதில்லை.
உங்களுக்குத் தெரியுமா?
அனோடைசிங் என்பது அலுமினியத்தின் தடிமனான ஆக்சைடு அடுக்கை உருவாக்கும் ஒரு செயல்முறையாகும். அலுமினியம் காற்றைச் சந்திக்கும் போது ஒரு மெல்லிய ஆக்சைடு அடுக்கை உருவாக்குகிறது. இந்த அலுமினிய ஆக்சைடு பூச்சு அதை மேலும் அரிப்பிலிருந்து எதிர்க்கும் தன்மையுடையதாக ஆக்குகிறது. ஆக்சைடு அடுக்கை தடிமனாக்குவதன் மூலம் எதிர்ப்புத் தன்மையை மேலும் மேம்படுத்தலாம். அனோடைசிங் செயல்பாட்டின் போது, ஒரு சுத்தமான அலுமினியப் பொருள் அனோடாக ஆக்கப்பட்டு நீர்த்த கந்தக அமிலத்துடன் மின்னாற்பகுப்பு செய்யப்படுகிறது. அனோடில் உருவாகும் ஆக்ஸிஜன் வாயு அலுமினியத்துடன் வினைபுரிந்து தடிமனான பாதுகாப்பு ஆக்சைடு அடுக்கை உருவாக்குகிறது. இந்த ஆக்சைடு அடுக்கு எளிதில் சாயமேற்றப்பட்டு அலுமினியப் பொருட்களுக்கு கவர்ச்சிகரமான முடிப்பைக் கொடுக்க முடியும்.
செயல்பாடு 3.9 ஐச் செய்த பிறகு, இங்கு எடுத்துக் கொள்ளப்பட்ட உலோக மாதிரிகளில் சோடியமே மிகவும் வினைத்திறன் மிக்கது என்பதை நீங்கள் கவனித்திருக்க வேண்டும். மெக்னீசியத்தின் வினை குறைவான கடுமையானது, அது சோடியம் போல் வினைத்திறன் மிக்கதல்ல என்பதைக் குறிக்கிறது. ஆனால் ஆக்ஸிஜனில் எரிவது துத்தநாகம், இரும்பு, தாமிரம் அல்லது ஈயத்தின் வினைத்திறனைப் பற்றி முடிவு செய்ய நமக்கு உதவாது. இந்த உலோகங்களின் வினைத்திறன் வரிசையைப் பற்றி ஒரு முடிவுக்கு வர இன்னும் சில வினைகளைப் பார்ப்போம்.
3.2.2 உலோகங்கள் நீருடன் வினைபுரியும் போது என்ன நடக்கும்?
செயல்பாடு 3.10
எச்சரிக்கை: இந்தச் செயல்பாட்டிற்கு ஆசிரியரின் உதவி தேவைப்படுகிறது.
- செயல்பாடு 3.9 இல் உள்ள அதே உலோகங்களின் மாதிரிகளைச் சேகரிக்கவும்.
- மாதிரிகளின் சிறிய துண்டுகளை தனித்தனியே பாதி நீர் நிரப்பப்பட்ட குடுவைகளில் வைக்கவும்.
- எந்த உலோகங்கள் குளிர்ந்த நீருடன் வினைபுரிந்தன? குளிர்ந்த நீருடன் அவற்றின் வினைத்திறன் அதிகரிக்கும் வரிசையில் அவற்றை அமைக்கவும்.
- எந்த உலோகமும் நீரில் தீப்பிடித்ததா?
- சிறிது நேரம் கழித்து எந்த உலோகமும் மிதக்கத் தொடங்குகிறதா?
- குளிர்ந்த நீருடன் வினைபுரியாத உலோகங்களை பாதி நீர் நிரப்பப்பட்ட வெந்நீர் கொண்ட குடுவைகளில் வைக்கவும்.
- வெந்நீருடன் கூட வினைபுரியாத உலோகங்களுக்கு, படம் 3.3 இல் காட்டப்பட்டுள்ளபடி கருவியமைப்பை அமைத்து நீராவியுடனான அவற்றின் வினையைக் கவனிக்கவும்.
- எந்த உலோகங்கள் நீராவியுடன் கூட வினைபுரியவில்லை?
- நீருடனான வினைத்திறன் குறைந்து வரும் வரிசையில் உலோகங்களை அமைக்கவும்.
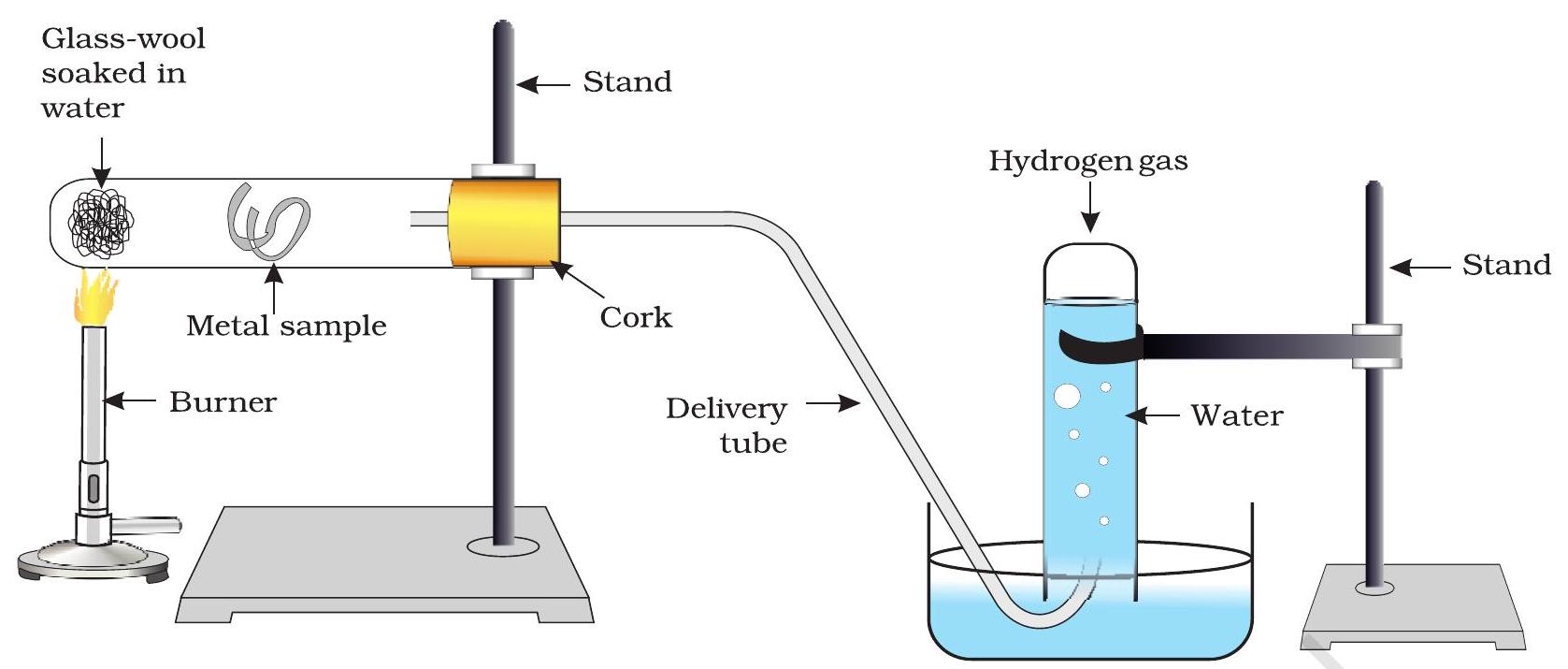
படம் 3.3 ஒரு உலோகத்தின் மீது நீராவியின் வினை
உலோகங்கள் நீருடன் வினைபுரிந்து ஒரு உலோக ஆக்சைடு மற்றும் ஹைட்ரஜன் வாயுவை உருவாக்குகின்றன. நீரில் கரையக்கூடிய உலோக ஆக்சைடுகள் அதில் கரைந்து மேலும் உலோக ஹைட்ராக்சைடை உருவாக்குகின்றன. ஆனால் அனைத்து உலோகங்களும் நீருடன் வினைபுரிவதில்லை.
உலோகம் + நீர் $\rightarrow$ உலோக ஆக்சைடு + ஹைட்ரஜன்
உலோக ஆக்சைடு + நீர் $ \rightarrow $ உலோக ஹைட்ராக்சைடு
பொட்டாசியம் மற்றும் சோடியம் போன்ற உலோகங்கள் குளிர்ந்த நீருடன் கடுமையாக வினைபுரிகின்றன. சோடியம் மற்றும் பொட்டாசியம் விஷயத்தில், வினை மிகவும் கடுமையானது மற்றும் வெப்பம் வெளியிடும் தன்மையுடையதாக இருப்பதால், உருவாகும் ஹைட்ரஜன் உடனடியாக தீப்பிடித்துக் கொள்ளும்.
$ \begin{aligned} & 2 K(s)+2 H_2 O(l) \to 2 KOH(aq)+H_2(g)+\text{ heat energy } \\ & 2 Na(s)+2 H_2 O(l) \to 2 NaOH(aq)+H_2(g)+\text{ heat energy } \end{aligned} $
கால்சியத்தின் நீருடனான வினை குறைவான கடுமையானது. வெளியிடப்படும் வெப்பம் ஹைட்ரஜன் தீப்பிடிப்பதற்கு போதுமானதாக இல்லை.
$Ca(s)+2 H_2 O(l) \to Ca(OH)_2(aq)+H_2(g)$
உருவாகும் ஹைட்ரஜன் வாயுவின் குமிழிகள் உலோகத்தின் மேற்பரப்பில் ஒட்டிக்கொள்வதால் கால்சியம் மிதக்கத் தொடங்குகிறது.
மெக்னீசியம் குளிர்ந்த நீருடன் வினைபுரிவதில்லை. இது வெந்நீருடன் வினைபுரிந்து மெக்னீசியம் ஹைட்ராக்சைடு மற்றும் ஹைட்ரஜனை உருவாக்குகிறது. அதன் மேற்பரப்பில் ஒட்டிக்கொள்ளும் ஹைட்ரஜன் வாயுவின் குமிழிகள் காரணமாக இதுவும் மிதக்கத் தொடங்குகிறது.
அலுமினியம், இரும்பு மற்றும் துத்தநாகம் போன்ற உலோகங்கள் குளிர்ந்த அல்லது வெந்நீருடன் வினைபுரிவதில்லை. ஆனால் அவை நீராவியுடன் வினைபுரிந்து உலோக ஆக்சைடு மற்றும் ஹைட்ரஜனை உருவாக்குகின்றன.
$ \begin{aligned} & 2 Al(s)+3 H_2 O(g) \to Al_2 O_3(s)+3











