ਅਧਿਆਇ 03 ਧਾਤੂ ਅਤੇ ਅਧਾਤੂ
ਕਲਾਸ ਨੌਵੀਂ ਵਿੱਚ ਤੁਸੀਂ ਵੱਖ-ਵੱਖ ਤੱਤਾਂ ਬਾਰੇ ਸਿੱਖਿਆ ਹੈ। ਤੁਸੀਂ ਦੇਖਿਆ ਹੈ ਕਿ ਤੱਤਾਂ ਨੂੰ ਉਨ੍ਹਾਂ ਦੇ ਗੁਣਾਂ ਦੇ ਆਧਾਰ ‘ਤੇ ਧਾਤੂ ਜਾਂ ਅਧਾਤੂ ਵਜੋਂ ਵਰਗੀਕ੍ਰਿਤ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ।
- ਆਪਣੇ ਰੋਜ਼ਾਨਾ ਜੀਵਨ ਵਿੱਚ ਧਾਤੂਆਂ ਅਤੇ ਅਧਾਤੂਆਂ ਦੇ ਕੁਝ ਉਪਯੋਗਾਂ ਬਾਰੇ ਸੋਚੋ।
- ਤੱਤਾਂ ਨੂੰ ਧਾਤੂ ਜਾਂ ਅਧਾਤੂ ਵਜੋਂ ਵਰਗੀਕ੍ਰਿਤ ਕਰਦੇ ਸਮੇਂ ਤੁਸੀਂ ਕਿਹੜੇ ਗੁਣਾਂ ਬਾਰੇ ਸੋਚਿਆ?
- ਇਹ ਗੁਣ ਤੱਤਾਂ ਦੇ ਉਪਯੋਗਾਂ ਨਾਲ ਕਿਵੇਂ ਸੰਬੰਧਿਤ ਹਨ?
ਆਓ ਇਨ੍ਹਾਂ ਵਿੱਚੋਂ ਕੁਝ ਗੁਣਾਂ ਨੂੰ ਵਿਸਤਾਰ ਨਾਲ ਦੇਖੀਏ।
3.1 ਭੌਤਿਕ ਗੁਣ
3.1.1 ਧਾਤੂ
ਪਦਾਰਥਾਂ ਨੂੰ ਸਮੂਹਿਤ ਕਰਨ ਦਾ ਸਭ ਤੋਂ ਆਸਾਨ ਤਰੀਕਾ ਉਨ੍ਹਾਂ ਦੇ ਭੌਤਿਕ ਗੁਣਾਂ ਦੀ ਤੁਲਨਾ ਕਰਨਾ ਹੈ। ਆਓ ਹੇਠਾਂ ਦਿੱਤੀਆਂ ਕਿਰਿਆਵਾਂ ਦੀ ਮਦਦ ਨਾਲ ਇਸ ਦਾ ਅਧਿਐਨ ਕਰੀਏ। ਕਿਰਿਆਵਾਂ 3.1 ਤੋਂ 3.6 ਕਰਨ ਲਈ, ਹੇਠ ਲਿਖੀਆਂ ਧਾਤੂਆਂ ਦੇ ਨਮੂਨੇ ਇਕੱਠੇ ਕਰੋ - ਲੋਹਾ, ਤਾਂਬਾ, ਐਲੂਮੀਨੀਅਮ, ਮੈਗਨੀਸ਼ੀਅਮ, ਸੋਡੀਅਮ, ਸਿੱਕਾ, ਜ਼ਿੰਕ ਅਤੇ ਕੋਈ ਵੀ ਹੋਰ ਧਾਤੂ ਜੋ ਆਸਾਨੀ ਨਾਲ ਉਪਲਬਧ ਹੋਵੇ।
ਕਿਰਿਆ 3.1
- ਲੋਹੇ, ਤਾਂਬੇ, ਐਲੂਮੀਨੀਅਮ ਅਤੇ ਮੈਗਨੀਸ਼ੀਅਮ ਦੇ ਨਮੂਨੇ ਲਓ। ਹਰੇਕ ਨਮੂਨੇ ਦੀ ਦਿੱਖ ਨੋਟ ਕਰੋ।
- ਹਰੇਕ ਨਮੂਨੇ ਦੀ ਸਤਹ ਨੂੰ ਸੈਂਡ ਪੇਪਰ ਨਾਲ ਰਗੜ ਕੇ ਸਾਫ਼ ਕਰੋ ਅਤੇ ਫਿਰ ਉਨ੍ਹਾਂ ਦੀ ਦਿੱਖ ਨੋਟ ਕਰੋ।
ਧਾਤੂਆਂ ਦੀ, ਆਪਣੀ ਸ਼ੁੱਧ ਅਵਸਥਾ ਵਿੱਚ, ਚਮਕਦਾਰ ਸਤਹ ਹੁੰਦੀ ਹੈ। ਇਸ ਗੁਣ ਨੂੰ ਧਾਤਵੀ ਚਮਕ (metallic lustre) ਕਿਹਾ ਜਾਂਦਾ ਹੈ।
ਕਿਰਿਆ 3.2
ਲੋਹੇ, ਤਾਂਬੇ, ਐਲੂਮੀਨੀਅਮ, ਅਤੇ ਮੈਗਨੀਸ਼ੀਅਮ ਦੇ ਛੋਟੇ ਟੁਕੜੇ ਲਓ। ਇਨ੍ਹਾਂ ਧਾਤੂਆਂ ਨੂੰ ਤੇਜ਼ ਚਾਕੂ ਨਾਲ ਕੱਟਣ ਦੀ ਕੋਸ਼ਿਸ਼ ਕਰੋ ਅਤੇ ਆਪਣੇ ਨਿਰੀਖਣ ਨੋਟ ਕਰੋ।
ਸੋਡੀਅਮ ਧਾਤੂ ਦਾ ਇੱਕ ਟੁਕੜਾ ਚਿਮਟੀ ਨਾਲ ਫੜੋ।
ਸਾਵਧਾਨੀ: ਸੋਡੀਅਮ ਧਾਤੂ ਨੂੰ ਹਮੇਸ਼ਾ ਸਾਵਧਾਨੀ ਨਾਲ ਹੈਂਡਲ ਕਰੋ। ਇਸਨੂੰ ਫਿਲਟਰ ਪੇਪਰ ਦੀਆਂ ਤਹਿਆਂ ਵਿਚਕਾਰ ਦਬਾ ਕੇ ਸੁਕਾਓ।
ਇਸਨੂੰ ਵਾਚ-ਗਲਾਸ ‘ਤੇ ਰੱਖੋ ਅਤੇ ਇਸਨੂੰ ਚਾਕੂ ਨਾਲ ਕੱਟਣ ਦੀ ਕੋਸ਼ਿਸ਼ ਕਰੋ।
ਤੁਸੀਂ ਕੀ ਦੇਖਦੇ ਹੋ?
ਤੁਸੀਂ ਦੇਖੋਗੇ ਕਿ ਧਾਤੂਆਂ ਆਮ ਤੌਰ ‘ਤੇ ਸਖ਼ਤ ਹੁੰਦੀਆਂ ਹਨ। ਸਖ਼ਤਾਈ ਧਾਤੂ ਤੋਂ ਧਾਤੂ ਵੱਖਰੀ ਹੁੰਦੀ ਹੈ।
ਕਿਰਿਆ 3.3
- ਲੋਹੇ, ਜ਼ਿੰਕ, ਸਿੱਕੇ ਅਤੇ ਤਾਂਬੇ ਦੇ ਟੁਕੜੇ ਲਓ।
- ਕਿਸੇ ਇੱਕ ਧਾਤੂ ਨੂੰ ਲੋਹੇ ਦੇ ਬਲਾਕ ‘ਤੇ ਰੱਖੋ ਅਤੇ ਹਥੌੜੇ ਨਾਲ ਚਾਰ ਜਾਂ ਪੰਜ ਵਾਰ ਮਾਰੋ। ਤੁਸੀਂ ਕੀ ਦੇਖਦੇ ਹੋ?
- ਹੋਰ ਧਾਤੂਆਂ ਨਾਲ ਦੁਹਰਾਓ।
- ਇਨ੍ਹਾਂ ਧਾਤੂਆਂ ਦੇ ਆਕਾਰ ਵਿੱਚ ਹੋਏ ਪਰਿਵਰਤਨ ਨੂੰ ਰਿਕਾਰਡ ਕਰੋ।
ਤੁਸੀਂ ਦੇਖੋਗੇ ਕਿ ਕੁਝ ਧਾਤੂਆਂ ਨੂੰ ਪਤਲੀਆਂ ਚਾਦਰਾਂ ਵਿੱਚ ਠੋਕਿਆ ਜਾ ਸਕਦਾ ਹੈ। ਇਸ ਗੁਣ ਨੂੰ ਤਨਯਤਾ (malleability) ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਕੀ ਤੁਸੀਂ ਜਾਣਦੇ ਹੋ ਕਿ ਸੋਨਾ ਅਤੇ ਚਾਂਦੀ ਸਭ ਤੋਂ ਵੱਧ ਤਨਯ (malleable) ਧਾਤੂਆਂ ਹਨ?
ਕਿਰਿਆ 3.4
- ਉਨ੍ਹਾਂ ਧਾਤੂਆਂ ਦੀ ਸੂਚੀ ਬਣਾਓ ਜਿਨ੍ਹਾਂ ਦੇ ਤਾਰ ਤੁਸੀਂ ਰੋਜ਼ਾਨਾ ਜੀਵਨ ਵਿੱਚ ਦੇਖੇ ਹਨ।
ਧਾਤੂਆਂ ਦੀ ਪਤਲੇ ਤਾਰਾਂ ਵਿੱਚ ਖਿੱਚੇ ਜਾਣ ਦੀ ਯੋਗਤਾ ਨੂੰ ਤਨ੍ਯਤਾ (ductility) ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਸੋਨਾ ਸਭ ਤੋਂ ਵੱਧ ਤਨ੍ਯ (ductile) ਧਾਤੂ ਹੈ। ਤੁਹਾਨੂੰ ਇਹ ਜਾਣ ਕੇ ਹੈਰਾਨੀ ਹੋਵੇਗੀ ਕਿ ਇੱਕ ਗ੍ਰਾਮ ਸੋਨੇ ਤੋਂ ਲਗਭਗ $2 km$ ਲੰਬਾਈ ਦਾ ਤਾਰ ਖਿੱਚਿਆ ਜਾ ਸਕਦਾ ਹੈ।
ਇਹ ਉਨ੍ਹਾਂ ਦੀ ਤਨਯਤਾ ਅਤੇ ਤਨ੍ਯਤਾ ਦੇ ਕਾਰਨ ਹੈ ਕਿ ਧਾਤੂਆਂ ਨੂੰ ਸਾਡੀਆਂ ਲੋੜਾਂ ਅਨੁਸਾਰ ਵੱਖ-ਵੱਖ ਆਕਾਰ ਦਿੱਤੇ ਜਾ ਸਕਦੇ ਹਨ।
ਕੀ ਤੁਸੀਂ ਕੁਝ ਧਾਤੂਆਂ ਦੇ ਨਾਮ ਦੱਸ ਸਕਦੇ ਹੋ ਜੋ ਖਾਣਾ ਪਕਾਉਣ ਵਾਲੇ ਬਰਤਨ ਬਣਾਉਣ ਲਈ ਵਰਤੀਆਂ ਜਾਂਦੀਆਂ ਹਨ? ਕੀ ਤੁਸੀਂ ਜਾਣਦੇ ਹੋ ਕਿ ਇਹ ਧਾਤੂਆਂ ਬਰਤਨ ਬਣਾਉਣ ਲਈ ਕਿਉਂ ਵਰਤੀਆਂ ਜਾਂਦੀਆਂ ਹਨ? ਆਓ ਜਵਾਬ ਲੱਭਣ ਲਈ ਹੇਠਾਂ ਦਿੱਤੀ ਕਿਰਿਆ ਕਰੀਏ।
ਕਿਰਿਆ 3.5
- ਇੱਕ ਐਲੂਮੀਨੀਅਮ ਜਾਂ ਤਾਂਬੇ ਦਾ ਤਾਰ ਲਓ। ਇਸ ਤਾਰ ਨੂੰ ਇੱਕ ਸਟੈਂਡ ‘ਤੇ ਕਲੈਂਪ ਕਰੋ, ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 3.1 ਵਿੱਚ ਦਿਖਾਇਆ ਗਿਆ ਹੈ।
- ਤਾਰ ਦੇ ਮੁਫਤ ਸਿਰੇ ਨੂੰ ਮੋਮ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਇੱਕ ਪਿੰਨ ਨਾਲ ਫਿਕਸ ਕਰੋ।
- ਜਿਸ ਜਗ੍ਹਾ ‘ਤੇ ਇਹ ਕਲੈਂਪ ਕੀਤਾ ਗਿਆ ਹੈ, ਉਸ ਦੇ ਨੇੜੇ ਸਪਿਰਿਟ ਲੈਂਪ, ਮੋਮਬੱਤੀ ਜਾਂ ਬਰਨਰ ਨਾਲ ਤਾਰ ਨੂੰ ਗਰਮ ਕਰੋ।
- ਕੁਝ ਸਮੇਂ ਬਾਅਦ ਤੁਸੀਂ ਕੀ ਦੇਖਦੇ ਹੋ?
- ਆਪਣੇ ਨਿਰੀਖਣ ਨੋਟ ਕਰੋ। ਕੀ ਧਾਤੂ ਦਾ ਤਾਰ ਪਿਘਲਦਾ ਹੈ?
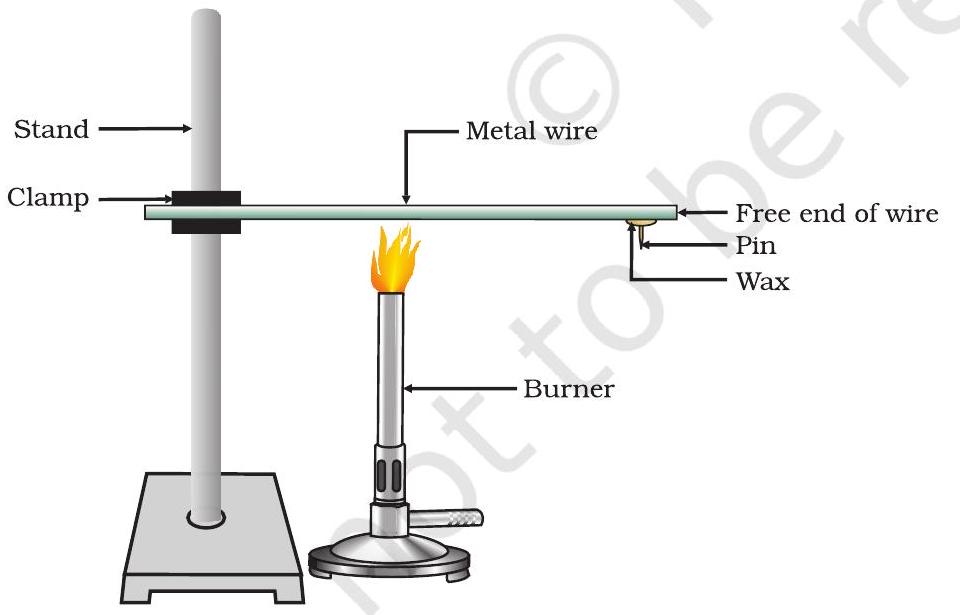
ਚਿੱਤਰ 3.1 ਧਾਤੂਆਂ ਗਰਮੀ ਦੇ ਚੰਗੇ ਸੁਚਾਲਕ ਹਨ।
ਉਪਰੋਕਤ ਕਿਰਿਆ ਦਰਸਾਉਂਦੀ ਹੈ ਕਿ ਧਾਤੂਆਂ ਗਰਮੀ ਦੇ ਚੰਗੇ ਸੁਚਾਲਕ ਹਨ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਉੱਚ ਗਲਨਾਕ ਹੁੰਦੇ ਹਨ। ਗਰਮੀ ਦੇ ਸਭ ਤੋਂ ਚੰਗੇ ਸੁਚਾਲਕ ਚਾਂਦੀ ਅਤੇ ਤਾਂਬਾ ਹਨ। ਸਿੱਕਾ ਅਤੇ ਪਾਰਾ ਗਰਮੀ ਦੇ ਤੁਲਨਾਤਮਕ ਰੂਪ ਵਿੱਚ ਮਾੜੇ ਸੁਚਾਲਕ ਹਨ।
ਕੀ ਧਾਤੂਆਂ ਬਿਜਲੀ ਦੀ ਵੀ ਚਾਲਕਤਾ ਕਰਦੀਆਂ ਹਨ? ਆਓ ਪਤਾ ਕਰੀਏ।
ਕਿਰਿਆ 3.6
- ਇੱਕ ਬਿਜਲੀ ਸਰਕਟ ਸੈੱਟ ਅਪ ਕਰੋ ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 3.2 ਵਿੱਚ ਦਿਖਾਇਆ ਗਿਆ ਹੈ।
- ਜਾਂਚ ਕੀਤੀ ਜਾਣ ਵਾਲੀ ਧਾਤੂ ਨੂੰ ਸਰਕਟ ਵਿੱਚ ਟਰਮੀਨਲਾਂ $A$ ਅਤੇ $B$ ਦੇ ਵਿਚਕਾਰ ਰੱਖੋ ਜਿਵੇਂ ਕਿ ਦਿਖਾਇਆ ਗਿਆ ਹੈ।
- ਕੀ ਬਲਬ ਚਮਕਦਾ ਹੈ? ਇਹ ਕੀ ਦਰਸਾਉਂਦਾ ਹੈ?
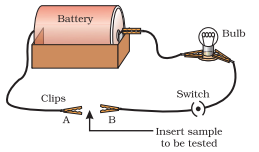
ਚਿੱਤਰ 3.2 ਧਾਤੂਆਂ ਬਿਜਲੀ ਦੇ ਚੰਗੇ ਸੁਚਾਲਕ ਹਨ।
ਤੁਸੀਂ ਜ਼ਰੂਰ ਦੇਖਿਆ ਹੋਵੇਗਾ ਕਿ ਤੁਹਾਡੇ ਘਰਾਂ ਵਿੱਚ ਕਰੰਟ ਲੈ ਜਾਣ ਵਾਲੇ ਤਾਰਾਂ ‘ਤੇ ਪੋਲੀਵਿਨਾਈਲ ਕਲੋਰਾਈਡ (PVC) ਜਾਂ ਰਬੜ ਵਰਗੀ ਸਮੱਗਰੀ ਦੀ ਲੇਪ ਹੁੰਦੀ ਹੈ। ਬਿਜਲੀ ਦੇ ਤਾਰਾਂ ਨੂੰ ਅਜਿਹੇ ਪਦਾਰਥਾਂ ਨਾਲ ਕਿਉਂ ਲੇਪਿਆ ਜਾਂਦਾ ਹੈ?
ਜਦੋਂ ਧਾਤੂਆਂ ਕਿਸੇ ਸਖ਼ਤ ਸਤਹ ‘ਤੇ ਟਕਰਾਉਂਦੀਆਂ ਹਨ ਤਾਂ ਕੀ ਹੁੰਦਾ ਹੈ? ਕੀ ਉਹ ਆਵਾਜ਼ ਪੈਦਾ ਕਰਦੀਆਂ ਹਨ? ਜੋ ਧਾਤੂਆਂ ਸਖ਼ਤ ਸਤਹ ‘ਤੇ ਟਕਰਾਉਣ ‘ਤੇ ਆਵਾਜ਼ ਪੈਦਾ ਕਰਦੀਆਂ ਹਨ, ਉਨ੍ਹਾਂ ਨੂੰ ਧੁਨਿਆਤਮਕ (sonorous) ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਕੀ ਤੁਸੀਂ ਹੁਣ ਦੱਸ ਸਕਦੇ ਹੋ ਕਿ ਸਕੂਲ ਦੀਆਂ ਘੰਟੀਆਂ ਧਾਤੂਆਂ ਤੋਂ ਕਿਉਂ ਬਣੀਆਂ ਹੁੰਦੀਆਂ ਹਨ?
3.1.2 ਅਧਾਤੂ
ਪਿਛਲੀ ਕਲਾਸ ਵਿੱਚ ਤੁਸੀਂ ਸਿੱਖਿਆ ਹੈ ਕਿ ਧਾਤੂਆਂ ਦੀ ਤੁਲਨਾ ਵਿੱਚ ਬਹੁਤ ਘੱਟ ਅਧਾਤੂ ਹਨ। ਅਧਾਤੂਆਂ ਦੀਆਂ ਕੁਝ ਉਦਾਹਰਨਾਂ ਕਾਰਬਨ, ਸਲਫਰ, ਆਇਓਡੀਨ, ਆਕਸੀਜਨ, ਹਾਈਡ੍ਰੋਜਨ, ਆਦਿ ਹਨ। ਅਧਾਤੂਆਂ ਜਾਂ ਤਾਂ ਠੋਸ ਹੁੰਦੀਆਂ ਹਨ ਜਾਂ ਗੈਸਾਂ ਹੁੰਦੀਆਂ ਹਨ, ਬਰੋਮੀਨ ਨੂੰ ਛੱਡ ਕੇ ਜੋ ਇੱਕ ਤਰਲ ਹੈ।
ਕੀ ਅਧਾਤੂਆਂ ਵਿੱਚ ਵੀ ਧਾਤੂਆਂ ਵਰਗੇ ਭੌਤਿਕ ਗੁਣ ਹੁੰਦੇ ਹਨ? ਆਓ ਪਤਾ ਕਰੀਏ।
ਕਿਰਿਆ 3.7
- ਕਾਰਬਨ (ਕੋਲਾ ਜਾਂ ਗ੍ਰਾਫਾਈਟ), ਸਲਫਰ ਅਤੇ ਆਇਓਡੀਨ ਦੇ ਨਮੂਨੇ ਇਕੱਠੇ ਕਰੋ।
- ਇਨ੍ਹਾਂ ਅਧਾਤੂਆਂ ਨਾਲ ਕਿਰਿਆਵਾਂ 3.1 ਤੋਂ 3.4 ਅਤੇ 3.6 ਕਰੋ ਅਤੇ ਆਪਣੇ ਨਿਰੀਖਣ ਰਿਕਾਰਡ ਕਰੋ।
ਧਾਤੂਆਂ ਅਤੇ ਅਧਾਤੂਆਂ ਬਾਰੇ ਆਪਣੇ ਨਿਰੀਖਣਾਂ ਨੂੰ ਸਾਰਣੀ 3.1 ਵਿੱਚ ਸੰਕਲਿਤ ਕਰੋ।
ਸਾਰਣੀ 3.1
| ਤੱਤ | ਚਿੰਨ੍ਹ | ਸਤਹ ਦੀ ਕਿਸਮ | ਸਖ਼ਤਾਈ | ਤਨਯਤਾ | ਤਨ੍ਯਤਾ | ਬਿਜਲੀ ਦੀ ਚਾਲਕਤਾ | ਧੁਨਿਆਤਮਕਤਾ |
|---|---|---|---|---|---|---|---|
ਸਾਰਣੀ 3.1 ਵਿੱਚ ਰਿਕਾਰਡ ਕੀਤੇ ਗਏ ਨਿਰੀਖਣਾਂ ਦੇ ਆਧਾਰ ‘ਤੇ, ਕਲਾਸ ਵਿੱਚ ਧਾਤੂਆਂ ਅਤੇ ਅਧਾਤੂਆਂ ਦੇ ਸਧਾਰਨ ਭੌਤਿਕ ਗੁਣਾਂ ਬਾਰੇ ਚਰਚਾ ਕਰੋ। ਤੁਸੀਂ ਇਹ ਨਿਸ਼ਕਰਸ਼ ਕੱਢਿਆ ਹੋਵੇਗਾ ਕਿ ਅਸੀਂ ਤੱਤਾਂ ਨੂੰ ਸਿਰਫ਼ ਉਨ੍ਹਾਂ ਦੇ ਭੌਤਿਕ ਗੁਣਾਂ ਦੇ ਆਧਾਰ ‘ਤੇ ਸਮੂਹਿਤ ਨਹੀਂ ਕਰ ਸਕਦੇ, ਕਿਉਂਕਿ ਬਹੁਤ ਸਾਰੀਆਂ ਅਪਵਾਦਾਂ ਹਨ। ਉਦਾਹਰਨ ਲਈ -
(i) ਪਾਰੇ ਨੂੰ ਛੱਡ ਕੇ ਸਾਰੀਆਂ ਧਾਤੂਆਂ ਕਮਰੇ ਦੇ ਤਾਪਮਾਨ ‘ਤੇ ਠੋਸਾਂ ਦੇ ਰੂਪ ਵਿੱਚ ਮੌਜੂਦ ਹੁੰਦੀਆਂ ਹਨ। ਕਿਰਿਆ 3.5 ਵਿੱਚ, ਤੁਸੀਂ ਦੇਖਿਆ ਹੈ ਕਿ ਧਾਤੂਆਂ ਦੇ ਉੱਚ ਗਲਨਾਕ ਹੁੰਦੇ ਹਨ ਪਰ ਗੈਲੀਅਮ ਅਤੇ ਸੀਜ਼ੀਅਮ ਦੇ ਬਹੁਤ ਘੱਟ ਗਲਨਾਕ ਹੁੰਦੇ ਹਨ। ਇਹ ਦੋਵੇਂ ਧਾਤੂਆਂ ਪਿਘਲ ਜਾਣਗੀਆਂ ਜੇਕਰ ਤੁਸੀਂ ਉਨ੍ਹਾਂ ਨੂੰ ਆਪਣੀ ਹਥੇਲੀ ‘ਤੇ ਰੱਖੋਗੇ।
(ii) ਆਇਓਡੀਨ ਇੱਕ ਅਧਾਤੂ ਹੈ ਪਰ ਇਹ ਚਮਕਦਾਰ ਹੈ।
(iii) ਕਾਰਬਨ ਇੱਕ ਅਧਾਤੂ ਹੈ ਜੋ ਵੱਖ-ਵੱਖ ਰੂਪਾਂ ਵਿੱਚ ਮੌਜੂਦ ਹੋ ਸਕਦਾ ਹੈ। ਹਰੇਕ ਰੂਪ ਨੂੰ ਇੱਕ ਅਲੋਟ੍ਰੋਪ (allotrope) ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਹੀਰਾ, ਕਾਰਬਨ ਦਾ ਇੱਕ ਅਲੋਟ੍ਰੋਪ, ਜਾਣਿਆ ਜਾਂਦਾ ਸਭ ਤੋਂ ਸਖ਼ਤ ਕੁਦਰਤੀ ਪਦਾਰਥ ਹੈ ਅਤੇ ਇਸਦਾ ਬਹੁਤ ਉੱਚ ਗਲਨਾਕ ਅਤੇ ਉਬਾਲ ਦਰਜਾ ਹੁੰਦਾ ਹੈ। ਗ੍ਰਾਫਾਈਟ, ਕਾਰਬਨ ਦਾ ਇੱਕ ਹੋਰ ਅਲੋਟ੍ਰੋਪ, ਬਿਜਲੀ ਦਾ ਇੱਕ ਸੁਚਾਲਕ ਹੈ।
(iv) ਖਾਰੀ ਧਾਤੂਆਂ (ਲਿਥੀਅਮ, ਸੋਡੀਅਮ, ਪੋਟਾਸ਼ੀਅਮ) ਇੰਨੀਆਂ ਨਰਮ ਹੁੰਦੀਆਂ ਹਨ ਕਿ ਉਨ੍ਹਾਂ ਨੂੰ ਚਾਕੂ ਨਾਲ ਕੱਟਿਆ ਜਾ ਸਕਦਾ ਹੈ। ਉਨ੍ਹਾਂ ਦੀ ਘਣਤਾ ਘੱਟ ਹੁੰਦੀ ਹੈ ਅਤੇ ਗਲਨਾਕ ਘੱਟ ਹੁੰਦੇ ਹਨ।
ਤੱਤਾਂ ਨੂੰ ਉਨ੍ਹਾਂ ਦੇ ਰਸਾਇਣਕ ਗੁਣਾਂ ਦੇ ਆਧਾਰ ‘ਤੇ ਵਧੇਰੇ ਸਪਸ਼ਟ ਰੂਪ ਵਿੱਚ ਧਾਤੂਆਂ ਅਤੇ ਅਧਾਤੂਆਂ ਵਜੋਂ ਵਰਗੀਕ੍ਰਿਤ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ।
ਕਿਰਿਆ 3.8
- ਇੱਕ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਅਤੇ ਕੁਝ ਸਲਫਰ ਪਾਊਡਰ ਲਓ।
- ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਸਾੜੋ। ਬਣੇ ਰਾਖ ਨੂੰ ਇਕੱਠਾ ਕਰੋ ਅਤੇ ਉਨ੍ਹਾਂ ਨੂੰ ਪਾਣੀ ਵਿੱਚ ਘੋਲੋ।
- ਨਤੀਜੇ ਵਜੋਂ ਬਣੇ ਘੋਲ ਨੂੰ ਲਾਲ ਅਤੇ ਨੀਲੇ ਲਿਟਮਸ ਪੇਪਰ ਨਾਲ ਟੈਸਟ ਕਰੋ।
- ਮੈਗਨੀਸ਼ੀਅਮ ਨੂੰ ਸਾੜਨ ‘ਤੇ ਬਣਿਆ ਉਤਪਾਦ ਤੇਜ਼ਾਬੀ ਹੈ ਜਾਂ ਖਾਰੀ?
- ਹੁਣ ਸਲਫਰ ਪਾਊਡਰ ਨੂੰ ਸਾੜੋ। ਬਣੀ ਧੂੰਆਂ ਨੂੰ ਇਕੱਠਾ ਕਰਨ ਲਈ ਸਾੜਦੇ ਸਲਫਰ ‘ਤੇ ਇੱਕ ਟੈਸਟ ਟਿਊਬ ਰੱਖੋ।
- ਉਪਰੋਕਤ ਟੈਸਟ ਟਿਊਬ ਵਿੱਚ ਕੁਝ ਪਾਣੀ ਮਿਲਾਓ ਅਤੇ ਹਿਲਾਓ।
- ਇਸ ਘੋਲ ਨੂੰ ਨੀਲੇ ਅਤੇ ਲਾਲ ਲਿਟਮਸ ਪੇਪਰ ਨਾਲ ਟੈਸਟ ਕਰੋ।
- ਸਲਫਰ ਨੂੰ ਸਾੜਨ ‘ਤੇ ਬਣਿਆ ਉਤਪਾਦ ਤੇਜ਼ਾਬੀ ਹੈ ਜਾਂ ਖਾਰੀ?
- ਕੀ ਤੁਸੀਂ ਇਨ੍ਹਾਂ ਕਿਰਿਆਵਾਂ ਲਈ ਸਮੀਕਰਨ ਲਿਖ ਸਕਦੇ ਹੋ?
ਬਹੁਤੇ ਅਧਾਤੂ ਪਾਣੀ ਵਿੱਚ ਘੁਲਣ ‘ਤੇ ਤੇਜ਼ਾਬੀ ਆਕਸਾਈਡ ਬਣਾਉਂਦੇ ਹਨ। ਦੂਜੇ ਪਾਸੇ, ਬਹੁਤੀਆਂ ਧਾਤੂਆਂ, ਖਾਰੀ ਆਕਸਾਈਡ ਬਣਾਉਂਦੀਆਂ ਹਨ। ਤੁਸੀਂ ਅਗਲੇ ਭਾਗ ਵਿੱਚ ਇਨ੍ਹਾਂ ਧਾਤੂ ਆਕਸਾਈਡਾਂ ਬਾਰੇ ਹੋਰ ਸਿੱਖੋਗੇ।
3.2 ਧਾਤੂਆਂ ਦੇ ਰਸਾਇਣਕ ਗੁਣ
ਅਸੀਂ ਧਾਤੂਆਂ ਦੇ ਰਸਾਇਣਕ ਗੁਣਾਂ ਬਾਰੇ ਹੇਠ ਲਿਖੇ ਭਾਗਾਂ 3.2.1 ਤੋਂ 3.2.4 ਵਿੱਚ ਸਿੱਖਾਂਗੇ। ਇਸ ਲਈ, ਹੇਠ ਲਿਖੀਆਂ ਧਾਤੂਆਂ ਦੇ ਨਮੂਨੇ ਇਕੱਠੇ ਕਰੋ: ਐਲੂਮੀਨੀਅਮ, ਤਾਂਬਾ, ਲੋਹਾ, ਸਿੱਕਾ, ਮੈਗਨੀਸ਼ੀਅਮ, ਜ਼ਿੰਕ ਅਤੇ ਸੋਡੀਅਮ।
3.2.1 ਜਦੋਂ ਧਾਤੂਆਂ ਨੂੰ ਹਵਾ ਵਿੱਚ ਸਾੜਿਆ ਜਾਂਦਾ ਹੈ ਤਾਂ ਕੀ ਹੁੰਦਾ ਹੈ?
ਤੁਸੀਂ ਕਿਰਿਆ 3.8 ਵਿੱਚ ਦੇਖਿਆ ਹੈ ਕਿ ਮੈਗਨੀਸ਼ੀਅਮ ਹਵਾ ਵਿੱਚ ਇੱਕ ਚਮਕਦਾਰ ਚਿੱਟੀ ਲਾਟ ਨਾਲ ਸੜਦਾ ਹੈ। ਕੀ ਸਾਰੀਆਂ ਧਾਤੂਆਂ ਇਸੇ ਤਰ੍ਹਾਂ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਦੀਆਂ ਹਨ? ਆਓ ਹੇਠਾਂ ਦਿੱਤੀ ਕਿਰਿਆ ਕਰਕੇ ਜਾਂਚ ਕਰੀਏ।
ਕਿਰਿਆ 3.9
ਸਾਵਧਾਨੀ: ਹੇਠ ਲਿਖੀ ਕਿਰਿਆ ਲਈ ਅਧਿਆਪਕ ਦੀ ਸਹਾਇਤਾ ਦੀ ਲੋੜ ਹੈ। ਇਹ ਬਿਹਤਰ ਹੋਵੇਗਾ ਜੇਕਰ ਵਿਦਿਆਰਥੀ ਅੱਖਾਂ ਦੀ ਸੁਰੱਖਿਆ ਪਹਿਨਣ।
- ਉਪਰੋਕਤ ਲਏ ਗਏ ਨਮੂਨਿਆਂ ਵਿੱਚੋਂ ਕਿਸੇ ਨੂੰ ਚਿਮਟੀ ਨਾਲ ਫੜੋ ਅਤੇ ਇੱਕ ਲਾਟ ‘ਤੇ ਸਾੜਨ ਦੀ ਕੋਸ਼ਿਸ਼ ਕਰੋ। ਹੋਰ ਧਾਤੂ ਨਮੂਨਿਆਂ ਨਾਲ ਦੁਹਰਾਓ।
- ਜੇਕਰ ਬਣਿਆ ਤਾਂ ਉਤਪਾਦ ਇਕੱਠਾ ਕਰੋ।
- ਉਤਪਾਦਾਂ ਅਤੇ ਧਾਤੂ ਸਤਹ ਨੂੰ ਠੰਡਾ ਹੋਣ ਦਿਓ।
- ਕਿਹੜੀਆਂ ਧਾਤੂਆਂ ਆਸਾਨੀ ਨਾਲ ਸੜਦੀਆਂ ਹਨ?
- ਜਦੋਂ ਧਾਤੂ ਸੜਦੀ ਸੀ ਤਾਂ ਤੁਸੀਂ ਕਿਹੜਾ ਲਾਟ ਰੰਗ ਦੇਖਿਆ?
- ਸਾੜਨ ਤੋਂ ਬਾਅਦ ਧਾਤੂ ਸਤਹ ਕਿਵੇਂ ਦਿਖਾਈ ਦਿੰਦੀ ਹੈ?
- ਆਕਸੀਜਨ ਪ੍ਰਤੀ ਉਨ੍ਹਾਂ ਦੀ ਪ੍ਰਤੀਕਿਰਿਆਸ਼ੀਲਤਾ ਦੇ ਘਟਦੇ ਕ੍ਰਮ ਵਿੱਚ ਧਾਤੂਆਂ ਨੂੰ ਕ੍ਰਮਬੱਧ ਕਰੋ।
- ਕੀ ਉਤਪਾਦ ਪਾਣੀ ਵਿੱਚ ਘੁਲਣਸ਼ੀਲ ਹਨ?
ਲਗਭਗ ਸਾਰੀਆਂ ਧਾਤੂਆਂ ਆਕਸੀਜਨ ਨਾਲ ਮਿਲ ਕੇ ਧਾਤੂ ਆਕਸਾਈਡ ਬਣਾਉਂਦੀਆਂ ਹਨ।
ਧਾਤੂ + ਆਕਸੀਜਨ $\rightarrow$ ਧਾਤੂ ਆਕਸਾਈਡ
ਉਦਾਹਰਨ ਲਈ, ਜਦੋਂ ਤਾਂਬੇ ਨੂੰ ਹਵਾ ਵਿੱਚ ਗਰਮ ਕੀਤਾ ਜਾਂਦਾ ਹੈ, ਤਾਂ ਇਹ ਆਕਸੀਜਨ ਨਾਲ ਮਿਲ ਕੇ ਤਾਂਬਾ(II) ਆਕਸਾਈਡ, ਇੱਕ ਕਾਲਾ ਆਕਸਾਈਡ ਬਣਾਉਂਦਾ ਹੈ।
$\underset{\text{ (Copper) }}{2 Cu+O_2} \to \underset{\text{ (Copper(II) oxide) }}{2 CuO}$
ਇਸੇ ਤਰ੍ਹਾਂ, ਐਲੂਮੀਨੀਅਮ ਐਲੂਮੀਨੀਅਮ ਆਕਸਾਈਡ ਬਣਾਉਂਦਾ ਹੈ।
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$
ਅਧਿਆਇ 2 ਤੋਂ ਯਾਦ ਕਰੋ, ਕਿਵੇਂ ਤਾਂਬਾ ਆਕਸਾਈਡ ਹਾਈਡ੍ਰੋਕਲੋਰਿਕ ਐਸਿਡ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਦਾ ਹੈ। ਅਸੀਂ ਸਿੱਖਿਆ ਹੈ ਕਿ ਧਾਤੂ ਆਕਸਾਈਡ ਕੁਦਰਤ ਵਿੱਚ ਖਾਰੀ ਹੁੰਦੇ ਹਨ। ਪਰ ਕੁਝ ਧਾਤੂ ਆਕਸਾਈਡ, ਜਿਵੇਂ ਕਿ ਐਲੂਮੀਨੀਅਮ ਆਕਸਾਈਡ, ਜ਼ਿੰਕ ਆਕਸਾਈਡ ਤੇਜ਼ਾਬੀ ਅਤੇ ਖਾਰੀ ਦੋਵਾਂ ਵਰਤਾਰੇ ਦਿਖਾਉਂਦੇ ਹਨ। ਅਜਿਹੇ ਧਾਤੂ ਆਕਸਾਈਡ ਜੋ ਤੇਜ਼ਾਬਾਂ ਅਤੇ ਖਾਰਾਂ ਦੋਵਾਂ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਕੇ ਲੂਣ ਅਤੇ ਪਾਣੀ ਬਣਾਉਂਦੇ ਹਨ, ਉਨ੍ਹਾਂ ਨੂੰ ਉਭਯਧਰਮੀ ਆਕਸਾਈਡ (amphoteric oxides) ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਐਲੂਮੀਨੀਅਮ ਆਕਸਾਈਡ ਤੇਜ਼ਾਬਾਂ ਅਤੇ ਖਾਰਾਂ ਨਾਲ ਹੇਠ ਲਿਖੇ ਢੰਗ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਦਾ ਹੈ -
$ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $
$ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $
ਬਹੁਤੇ ਧਾਤੂ ਆਕਸਾਈਡ ਪਾਣੀ ਵਿੱਚ ਅਘੁਲਣਸ਼ੀਲ ਹੁੰਦੇ ਹਨ ਪਰ ਇਨ੍ਹਾਂ ਵਿੱਚੋਂ ਕੁਝ ਪਾਣੀ ਵਿੱਚ ਘੁਲ ਕੇ ਖਾਰ ਬਣਾਉਂਦੇ ਹਨ। ਸੋਡੀਅਮ ਆਕਸਾਈਡ ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ ਆਕਸਾਈਡ ਪਾਣੀ ਵਿੱਚ ਘੁਲ ਕੇ ਹੇਠ ਲਿਖੇ ਅਨੁਸਾਰ ਖਾਰ ਬਣਾਉਂਦੇ ਹਨ -
$ \begin{aligned} & Na_2 O(s)+H_2 O(l) \to 2 NaOH(aq) \\ & K_2 O(s)+H_2 O(l) \to 2 KOH(aq) \end{aligned} $
ਅਸੀਂ ਕਿਰਿਆ 3.9 ਵਿੱਚ ਦੇਖਿਆ ਹੈ ਕਿ ਸਾਰੀਆਂ ਧਾਤੂਆਂ ਆਕਸੀਜਨ ਨਾਲ ਇੱਕੋ ਦਰ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਨਹੀਂ ਕਰਦੀਆਂ। ਵੱਖ-ਵੱਖ ਧਾਤੂਆਂ ਆਕਸੀਜਨ ਪ੍ਰਤੀ ਵੱਖ-ਵੱਖ ਪ੍ਰਤੀਕਿਰਿਆਸ਼ੀਲਤਾ ਦਿਖਾਉਂਦੀਆਂ ਹਨ। ਪੋਟਾਸ਼ੀਅਮ ਅਤੇ ਸੋਡੀਅਮ ਵਰਗੀਆਂ ਧਾਤੂਆਂ ਇੰਨੀ ਜ਼ੋਰਦਾਰ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਦੀਆਂ ਹਨ ਕਿ ਜੇਕਰ ਉਨ੍ਹਾਂ ਨੂੰ ਖੁੱਲ੍ਹੇ ਵਿੱਚ ਰੱਖਿਆ ਜਾਵੇ ਤਾਂ ਉਹ ਅੱਗ ਫੜ ਲੈਂਦੀਆਂ ਹਨ। ਇਸ ਲਈ, ਉਨ੍ਹਾਂ ਨੂੰ ਬਚਾਉਣ ਅਤੇ ਅਚਾਨਕ ਅੱਗ ਲੱਗਣ ਤੋਂ ਰੋਕਣ ਲਈ, ਉਨ੍ਹਾਂ ਨੂੰ ਮਿੱਟੀ ਦੇ ਤੇਲ ਵਿੱਚ ਡੁਬੋ ਕੇ ਰੱਖਿਆ ਜਾਂਦਾ ਹੈ। ਆਮ ਤਾਪਮਾਨ ‘ਤੇ, ਮੈਗਨੀਸ਼ੀਅਮ, ਐਲੂਮੀਨੀਅਮ, ਜ਼ਿੰਕ, ਸਿੱਕਾ, ਆਦਿ ਵਰਗੀਆ











